文档内容
重难点 04 元素推断与元素周期律
元素周期律是江苏高考的必考内容,属于热点题型,本题考查元素周期律的应用,进行元素推断,判断元
素及其化合物的性质,如第一电离能、电负性、微粒半径、化学键、酸碱性等。高考对本讲内容的考查空
间很大,知识面很广,主要考查原子结构中各种微粒关系,结合原子结构图式进行分析判断和简单计算,
对1~20号元素原子结构的考查是重点,注意规律和结论的应用。其次以元素化合物为载体,综合应用元
素周期表和元素周期律。另外高考对化学键的考查主要是围绕电子式正误判断、化学键与物质类别和性质
的关系两方面进行、题目基础性强,一般不独立命题。通常为选择题的一个选项和基础填空。预测2024年
高考仍然以短周期元素原子或离子结构特征及核外电子排布规律为背景,考查原子结构、元素周期律和常
见物质的相关性质;或者以“残缺的”元素周期表或元素性质的递变规律为切入点,考查元素的“位-构-
性”关系;结合元素化合物和化学反应原理等基础知识,采用框图或文字叙述形式,考查元素推断、元素
周期律的综合运用。
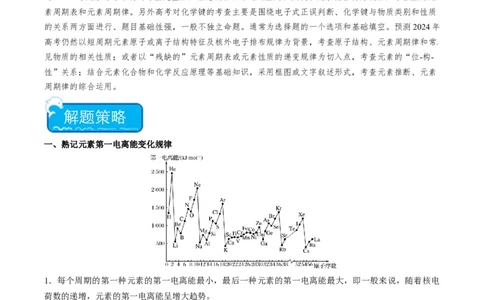
一、熟记元素第一电离能变化规律
1.每个周期的第一种元素的第一电离能最小,最后一种元素的第一电离能最大,即一般来说,随着核电
荷数的递增,元素的第一电离能呈增大趋势。
2.同一族,从上到下第一电离能逐渐减小。
3.电离能的应用
(1)根据电离能数据,确定元素原子核外电子的排布及元素的化合价。如 Li:I≪IⅢA,ⅤA>ⅥA。
二、熟记元素电负性变化规律
1.同周期,自左到右,元素的电负性逐渐增大,元素的非金属性逐渐增强、金属性逐渐减弱。
同主族,自上到下,元素的电负性逐渐减小,元素的金属性逐渐增强、非金属性逐渐减弱。
2.电负性的应用
(1)判断元素的金属性和非金属性强弱
①金属的电负性一般小于1.8,非金属的电负性一般大于1.8,而位于非金属三角区边界的“类金属”(如锗、
锑等)的电负性则在1.8左右,它们既有金属性,又有非金属性。
②金属元素的电负性越小,金属元素越活泼;非金属元素的电负性越大,非金属元素越活泼。
(2)判断元素的化合价
①电负性数值小的元素在化合物中吸引电子的能力弱,元素的化合价为正值。
②电负性数值大的元素在化合物中吸引电子的能力强,元素的化合价为负值。
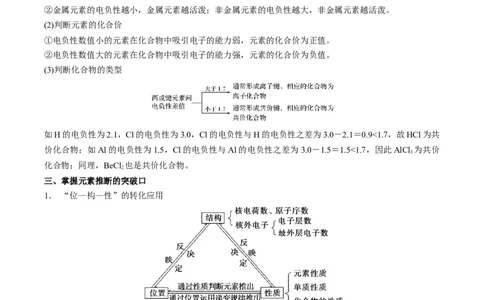
(3)判断化合物的类型
如H的电负性为2.1,Cl的电负性为3.0,Cl的电负性与H的电负性之差为3.0-2.1=0.9<1.7,故HCl为共
价化合物;如Al的电负性为1.5,Cl的电负性与Al的电负性之差为3.0-1.5=1.5<1.7,因此AlCl 为共价
3
化合物;同理,BeCl 也是共价化合物。
2
三、掌握元素推断的突破口
1. “位—构—性”的转化应用
2.(1)性质与位置的互推
①根据元素的性质可以推知元素在周期表中的位置,如同周期主族元素A、B、C的金属性逐渐增强,则
可知A、B、C在同周期中按C、B、A的顺序从左向右排列。
②根据元素在周期表中的位置关系可以推断元素的性质,如A、B、C三元素在同一主族中从上往下排列,
则A、B、C的单质氧化性依次减弱或还原性依次增强。
(2)结构与性质的互推
①若某主族元素的最外层电子数小于4,则该元素容易失电子;若该元素的最外层电子数大于4,则该元素容易得电子。
②若某主族元素容易得电子,则可推知该元素的最外层电子数大于4;若该元素容易失电子,则可推知该
元素的最外层电子数小于4。
(3)结构与位置的互推
由原子序数确定主族元素位置方法:只要记住了稀有气体元素的原子序数
(He-2、Ne-10、Ar-18、Kr-36、Xe-54、Rn-86),就可确定主族元素的位置。
①若比相应的稀有气体元素多1或2,则应处在下周期的第ⅠA族或第ⅡA族,如88号元素:88-86=
2,则应在第七周期ⅡA族;
②若比相应的稀有气体元素少1~5时,则应处在同周期的ⅢA族~ⅦA族,如84号元素应在第六周期
ⅥA族。
1. (2023江苏卷)元素C、Si、Ge位于周期表中ⅣA族。下列说法正确的是
A. 原子半径: B. 第一电离能:
C. 碳单质、晶体硅、SiC均为共价晶体 D. 可在周期表中元素Si附近寻找新半导体材料
2. (2022江苏卷)工业上电解熔融 和冰晶石 的混合物可制得铝。下列说法正确的是
A. 半径大小: B. 电负性大小:
C. 电离能大小: D. 碱性强弱:
3. (2021江苏卷)前4周期主族元素X、Y、Z、W的原子序数依次增大,X是空气中含量最多的元素,Y
的周期序数与族序数相等,基态时Z原子3p原子轨道上有5个电子,W与Z处于同个主族。下列说法正
确的是
A. 原子半径:r(X)X
C.Z、W的简单离子的半径:
D.简单气态氢化物的热稳定性:Z>Y
13.W、X、Y、Z为原子序数依次增大的短周期主族元素,W在所有元素中原子半径最小,X的最外层电
子数是Z的最外层电子数的一半,Y与Z同主族。 中含有32mol电子。下列说法正确的是
A.原子半径:Y>X B.简单氢化物的沸点: Yr(As) B.电负性:x(P)>x(S)
C.第一电离能:I(S)KOH
C.电负性大小:χ(Li)<χ(Na) D.可在IA族找到制造光电材料的元素
20.M、W、X、Y、Z是五种原子序数依次增大的短周期主族元素,其原子序数之和为31;其中Y的最外
层电子数等于 X 的核外电子总数;五种主族元素组成的化合物Q的结构如图所示。下列说法错误的是
A.原子半径:
B.X 的氧化物属于酸性氧化物
C.Y 元素组成的最常见单质和M的单质,在加热条件下生成的化合物中只含离子键
D.在Q 的结构中,除M外,其余原子最外层均满足8 电子稳定结构