文档内容
高频考点 34 难溶电解质的沉淀溶解平衡
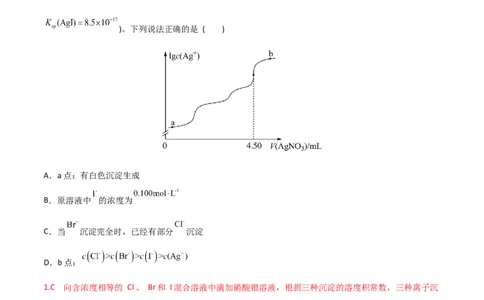
1.(2022·湖南卷)室温时,用 的标准 溶液滴定 浓度相等的 、 和 混合
溶液,通过电位滴定法获得 与 的关系曲线如图所示(忽略沉淀对离子的吸附作用。若溶
液中离子浓度小于 时,认为该离子沉淀完全。 , ,
)。下列说法正确的是 ( )
A.a点:有白色沉淀生成
B.原溶液中 的浓度为
C.当 沉淀完全时,已经有部分 沉淀
D.b点:
1.C 向含浓度相等的 Cl-、 Br-和 I-混合溶液中滴加硝酸银溶液,根据三种沉淀的溶度积常数,三种离子沉
淀的先后顺序为I-、Br-、Cl-,根据滴定图示,当滴入4.50mL硝酸银溶液时,Cl-恰好沉淀完全,此时共消耗
硝酸银的物质的量为4.50mL×10-3L/mL×0.1000mol/L=4.5×10-4mol,所以Cl-、 Br-和 I-均为1.5×10-4mol。A.I-
先沉淀,AgI是黄色的,所以a点有黄色沉淀AgI生成,故A错误;B.原溶液中I-的物质的量为1.5×10-
4mol,则I-的浓度为 =0.0100mol⋅L-1,故B错误;C.当Br-沉淀完全时(Br-浓度为1.0×10-5mol/L),溶液中的c(Ag+)= =5.4×10-8mol/L,若Cl-已经开始沉淀,则此时溶液中的c(Cl-)=
=3.3×10-3mol/L,原溶液中的c(Cl-)= c(I-)=0.0100mol⋅L-1,则已经有部分Cl-沉淀,故C
正确;D.b点加入了过量的硝酸银溶液,Ag+浓度最大,则b点各离子浓度为:
,故D错误;故选C。
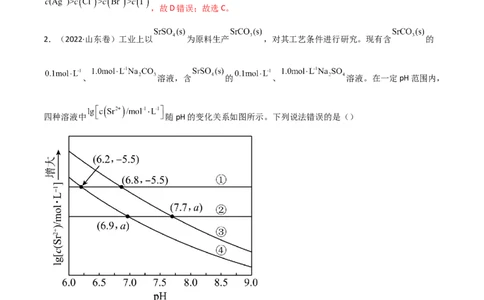
2.(2022·山东卷)工业上以 为原料生产 ,对其工艺条件进行研究。现有含 的
、 溶液,含 的 、 溶液。在一定pH范围内,
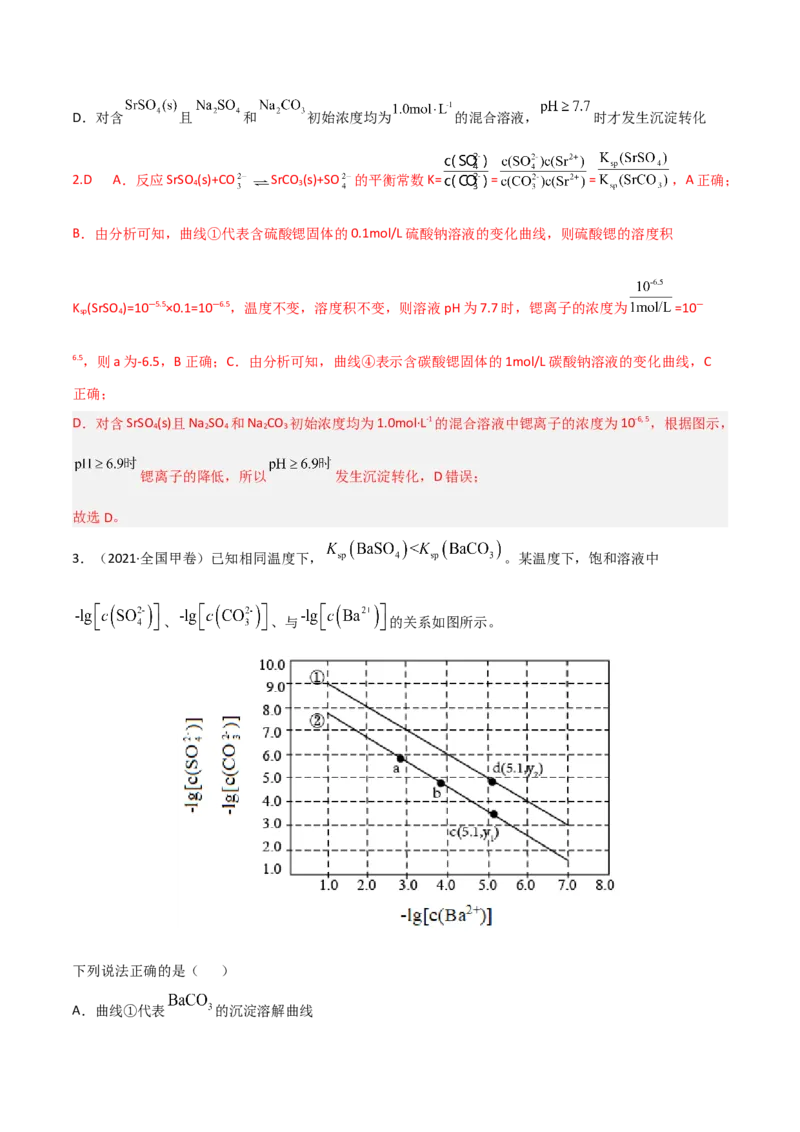
四种溶液中 随pH的变化关系如图所示。下列说法错误的是()
A.反应 的平衡常数
B.
C.曲线④代表含 的 溶液的变化曲线D.对含 且 和 初始浓度均为 的混合溶液, 时才发生沉淀转化
2.D A.反应SrSO (s)+CO SrCO (s)+SO 的平衡常数K= = = ,A正确;
4 3
B.由分析可知,曲线①代表含硫酸锶固体的0.1mol/L硫酸钠溶液的变化曲线,则硫酸锶的溶度积
K (SrSO )=10—5.5×0.1=10—6.5,温度不变,溶度积不变,则溶液pH为7.7时,锶离子的浓度为 =10—
sp 4
6.5,则a为-6.5,B正确;C.由分析可知,曲线④表示含碳酸锶固体的1mol/L碳酸钠溶液的变化曲线,C
正确;
D.对含SrSO (s)且Na SO 和Na CO 初始浓度均为1.0mol·L-1的混合溶液中锶离子的浓度为10-6, 5,根据图示,
4 2 4 2 3
锶离子的降低,所以 发生沉淀转化,D错误;
故选D。
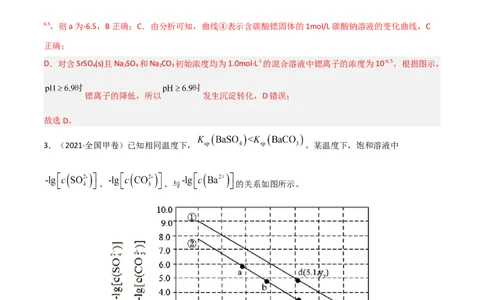
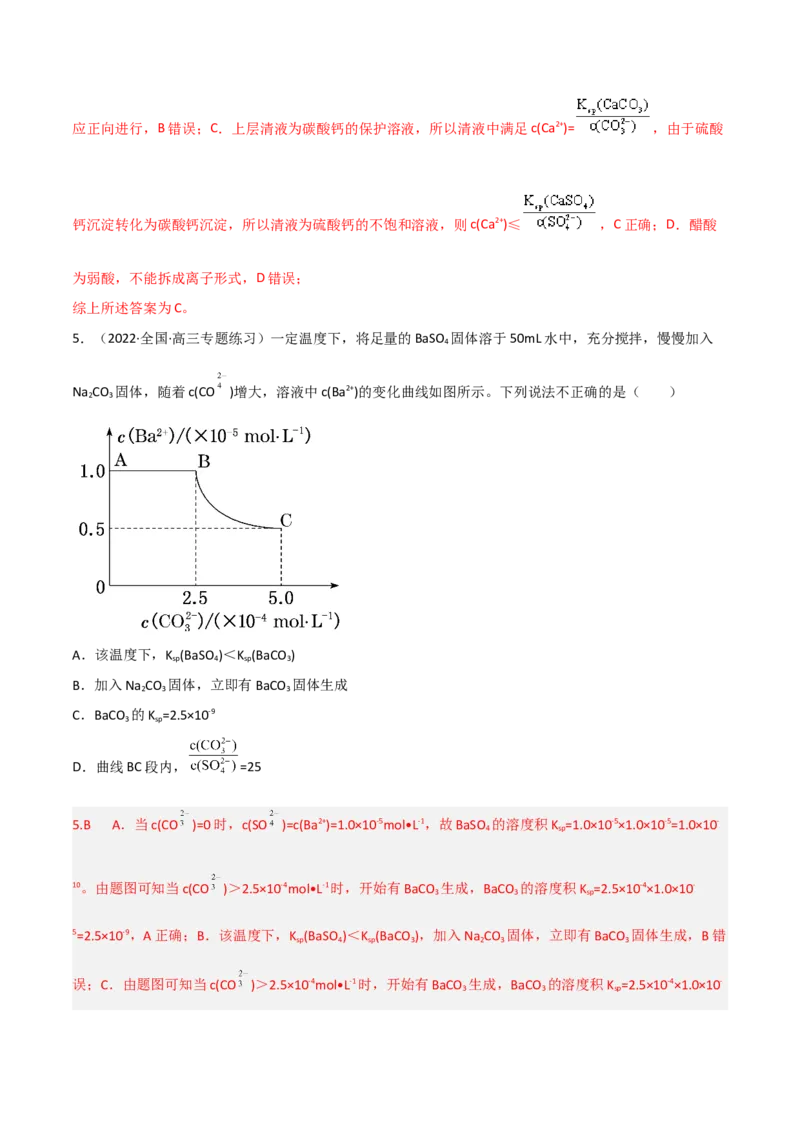
3.(2021·全国甲卷)已知相同温度下, 。某温度下,饱和溶液中
、 、与 的关系如图所示。
下列说法正确的是( )
A.曲线①代表 的沉淀溶解曲线B.该温度下 的 值为
C.加适量 固体可使溶液由a点变到b点
D. 时两溶液中
3.B A.由题可知,曲线上的点均为饱和溶液中微粒浓度关系,由上述分析可知,曲线①为BaSO 的沉淀
4
溶解曲线,选项A错误;B.曲线①为BaSO 溶液中-lg[c(Ba2+)]与-lg[c( )]的关系,由图可知,当溶液
4
中-lg[c(Ba2+)]=3时,-lg[c( )=7,则-lg[K (BaSO )]=7+3=10,因此K (BaSO )=1.0×10-10,选项B
sp 4 sp 4
正确;C.向饱和BaSO 溶液中加入适量BaCl 固体后,溶液中c(Ba2+)增大,根据温度不变则K (BaSO )不变
4 2 sp 4
可知,溶液中c( )将减小,因此a点将沿曲线①向左上方移动,选项C错误;D.由图可知,当溶液中
c(Ba2+)=10-5.1时,两溶液中 = = ,选项D错误;答案选B。
4.(2021·江苏卷)室温下,用0.5mol·L-1Na CO 溶液浸泡CaSO 粉末,一段时间后过滤,向滤渣中加稀醋
2 3 4
酸,产生气泡。已知K (CaSO )=5×10-5,K (CaCO )=3×10-9。下列说法正确的是( )
sp 4 sp 3
A.0.5mol·L-1Na CO 溶液中存在:c(OH-)=c(H+)+c(HCO )+c(H CO )
2 3 2 3
B.反应CaSO +CO CaCO +SO 正向进行,需满足 > ×104
4 3
C.过滤后所得清液中一定存在:c(Ca2+)= 且c(Ca2+)≤
D.滤渣中加入醋酸发生反应的离子方程式:CaCO +2H+=Ca2++CO ↑+H O
3 2 2
4.C A.0.5mol·L-1Na CO 溶液中存在质子守恒:c(OH-)=c(H+)+c(HCO )+2c(H CO ),A错误;
2 3 2 3
B.该反应的平衡常数K= = = = = ×104,当浓度商 <K时,反应正向进行,B错误;C.上层清液为碳酸钙的保护溶液,所以清液中满足c(Ca2+)= ,由于硫酸
钙沉淀转化为碳酸钙沉淀,所以清液为硫酸钙的不饱和溶液,则c(Ca2+)≤ ,C正确;D.醋酸
为弱酸,不能拆成离子形式,D错误;
综上所述答案为C。
5.(2022·全国·高三专题练习)一定温度下,将足量的BaSO 固体溶于50mL水中,充分搅拌,慢慢加入
4
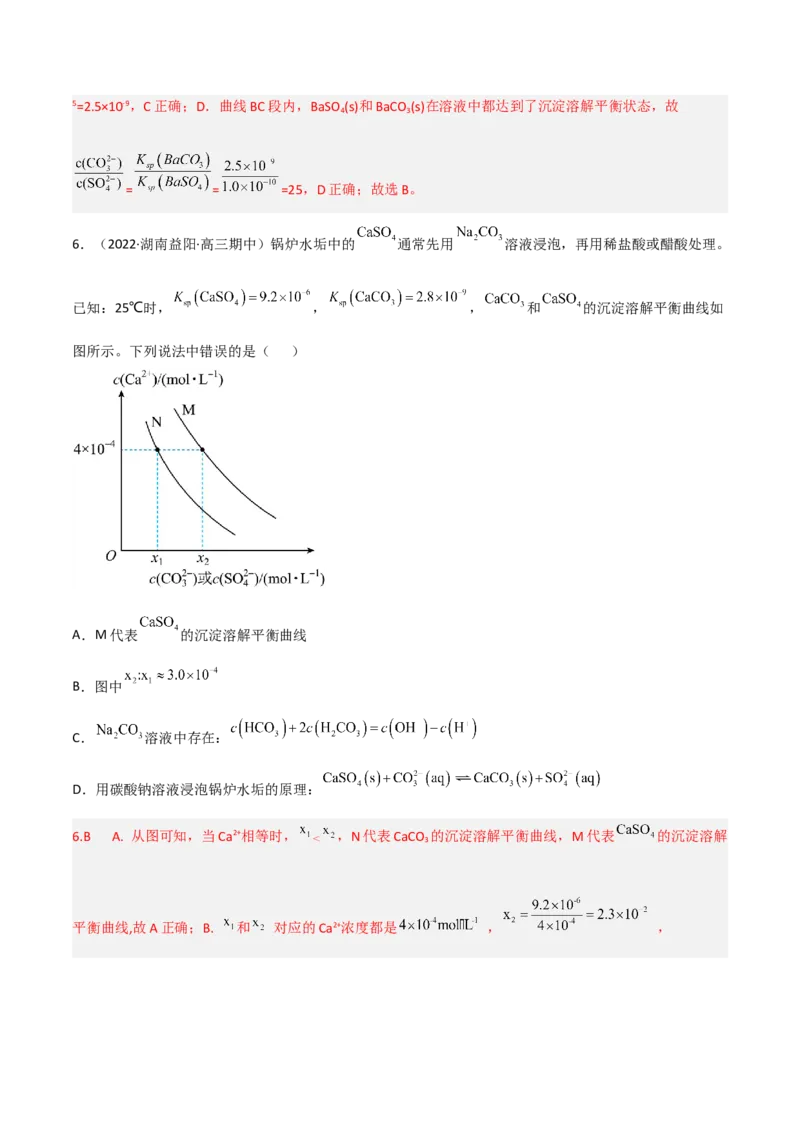
Na CO 固体,随着c(CO )增大,溶液中c(Ba2+)的变化曲线如图所示。下列说法不正确的是( )
2 3
A.该温度下,K (BaSO )<K (BaCO )
sp 4 sp 3
B.加入Na CO 固体,立即有BaCO 固体生成
2 3 3
C.BaCO 的K =2.5×10-9
3 sp
D.曲线BC段内, =25
5.B A.当c(CO )=0时,c(SO )=c(Ba2+)=1.0×10-5mol•L-1,故BaSO 的溶度积K =1.0×10-5×1.0×10-5=1.0×10-
4 sp
10。由题图可知当c(CO )>2.5×10-4mol•L-1时,开始有BaCO 生成,BaCO 的溶度积K =2.5×10-4×1.0×10-
3 3 sp
5=2.5×10-9,A正确;B.该温度下,K (BaSO )<K (BaCO ),加入Na CO 固体,立即有BaCO 固体生成,B错
sp 4 sp 3 2 3 3
误;C.由题图可知当c(CO )>2.5×10-4mol•L-1时,开始有BaCO 生成,BaCO 的溶度积K =2.5×10-4×1.0×10-
3 3 sp5=2.5×10-9,C正确;D.曲线BC段内,BaSO (s)和BaCO (s)在溶液中都达到了沉淀溶解平衡状态,故
4 3
= = =25,D正确;故选B。
6.(2022·湖南益阳·高三期中)锅炉水垢中的 通常先用 溶液浸泡,再用稀盐酸或醋酸处理。
已知:25℃时, , , 和 的沉淀溶解平衡曲线如
图所示。下列说法中错误的是( )
A.M代表 的沉淀溶解平衡曲线
B.图中
C. 溶液中存在:
D.用碳酸钠溶液浸泡锅炉水垢的原理:
6.B A. 从图可知,当Ca2+相等时, ,N代表CaCO 的沉淀溶解平衡曲线,M代表 的沉淀溶解
< 3
平衡曲线,故A正确;B. 和 对应的Ca2+浓度都是 , ,, ,故B错误;C. Na CO 溶液中,根据电荷守恒可得
2 3
c(OH−)+c( )+2c( )=c(H+)+c(Na+),又根据物料守恒可得c(Na+)=2[c( )+c( )+
c(H CO )],两式联立可得c(OH−)=c(H+)+2c(H CO )+c( ),故C正确;D. 碳酸钠溶液浸泡锅炉水垢的
2 3 2 3
原理: ,故D正确;故选B。
7.(2022·湖北武汉·高三期末)常温下,用0.12 mol/L的Na SO 溶液滴定50.00 mL未知浓度的BaCl 溶液。
2 4 2
溶液中电导率k、-lgc(Ba2+)随滴入Na SO 溶液体积V(Na SO )的变化关系如下图所示。
2 4 2 4
下列叙述错误的是( )
A.当 时,溶液中的溶质为NaCl
B.该BaCl 溶液的物质的量浓度是6.0×10-3 mol/L
2
C.该温度下BaSO 的溶度积常数
4
D.当V(Na SO )=3.00 mL时,溶液中
2 4
7.D A.根据图示可知:当 时,Na SO 与BaCl 恰好反应完全,溶液的电导率最小,
2 4 2则此时溶液中的溶质为NaCl,A正确;B.根据反应Na SO +BaCl =BaSO ↓+2NaCl,n(BaCl )=n(Na SO )=0.12
2 4 2 4 2 2 4
mol/L×2.5 mL=3.0×10-4 mol,而BaCl 溶液体积是50 mL,故c(BaCl )= = 6.0×10-3 mol/L,B正确;
2 2
C.根据图示可知当V(Na SO )=2.5 mL时恰好发生反应Na SO +BaCl =BaSO ↓+2NaCl,此时-lgc(Ba2+)=5.0,
2 4 2 4 2 4
c(Ba2+)=10-5.0 mol/L,溶液中的Ba2+为BaSO 电离产生,则c( )=c(Ba2+)=10-5.0 mol/L,由于K (BaSO )=c(
4 sp 4
)·c(Ba2+)=10-5.0 mol/L×10-5.0 mol/L=10-10(mol/L)2,C正确;D.根据上述分析可知:当V(Na SO )=2.5 mL时
2 4
恰好发生反应Na SO +BaCl =BaSO ↓+2NaCl,此时溶液中溶质为NaCl,n(NaCl)=6.0×10-4 mol。当
2 4 2 4
V(Na SO )=3.00 mL时,n(Na SO )=0.12 mol/L×(3.0-2.5) ×10-3 L=6.0×10-5 mol,所以c(Cl-)>c( ),D错误;
2 4 2 4
故合理选项是D。
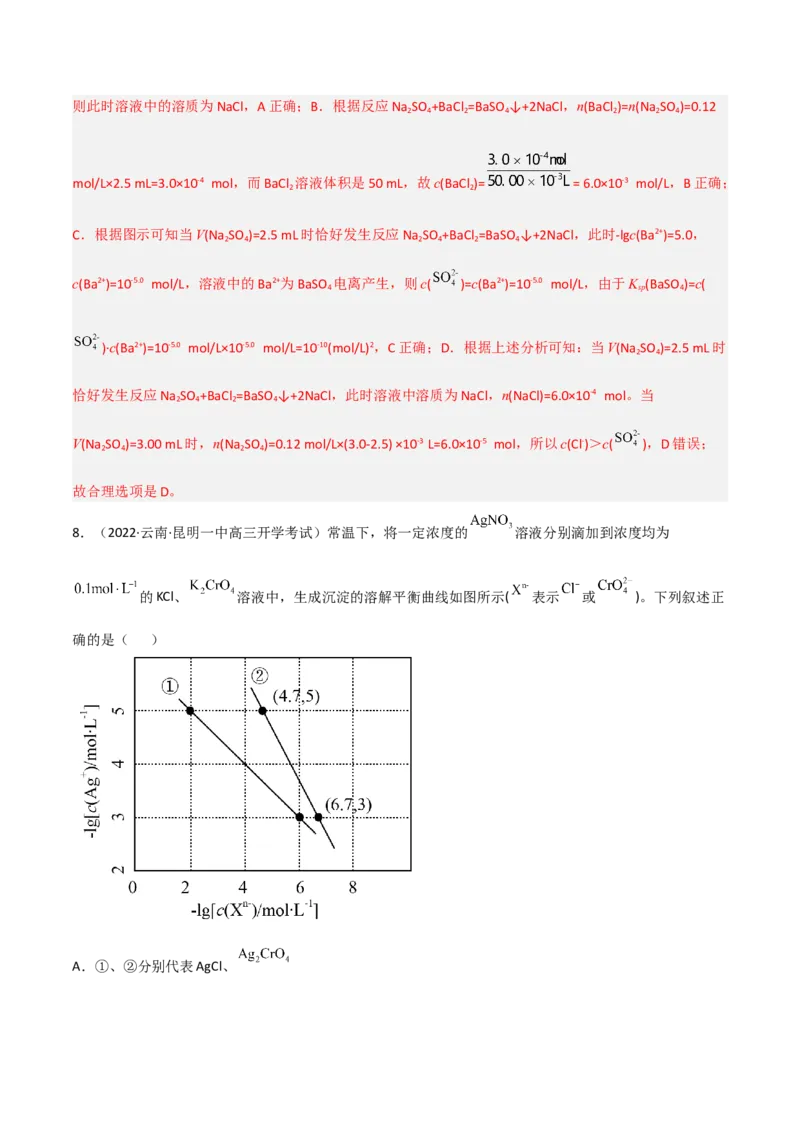
8.(2022·云南·昆明一中高三开学考试)常温下,将一定浓度的 溶液分别滴加到浓度均为
的KCl、 溶液中,生成沉淀的溶解平衡曲线如图所示( 表示 或 )。下列叙述正
确的是( )
A.①、②分别代表AgCl、B.
C. ,说明 的溶解度更小
D. 的
8.D 氯离子、 和银离子反应分别为Cl-+Ag+=AgCl↓, +2Ag+=Ag CrO ↓,则
2 4
、 ,K值只受温度影响,则结合图像可知,②
上点(4.7,5)、(6.7,3)的 符合 的表达形式,则②代表AgCl、
①代表 ;A.由分析可知,①代表 、②代表AgCl;A错误;B.①代表 ,由点
(5,2)可知, ,B错误;C.②代表AgCl,由点
(4.7,5)可知, ;设AgCl溶解的浓度为xmol/L,则溶液中的
银离子浓度为xmol/L,氯离子也为xmol/L,则根据溶度积为10﹣9.7=x×x,解得x=10﹣4.85mol/L;同理设
Ag CrO 溶解的浓度为ymol/L,则溶液中的银离子浓度为2ymol/L, 也为ymol/L,再根据溶度积为10﹣
2 4
12=(2y)2×y,解得y 1.59×10﹣4mol/L;由此可知AgCl的溶解度反而小,而 的溶解度反而大,所以K
sp
≈
的大小与溶解能力没有一定的关系,如由K 的大小直接判断溶解能力的大小,则需两种难溶电解质类型应
sp
相同;故 ,不能说明 的溶解度更小,C错误;
D. 的
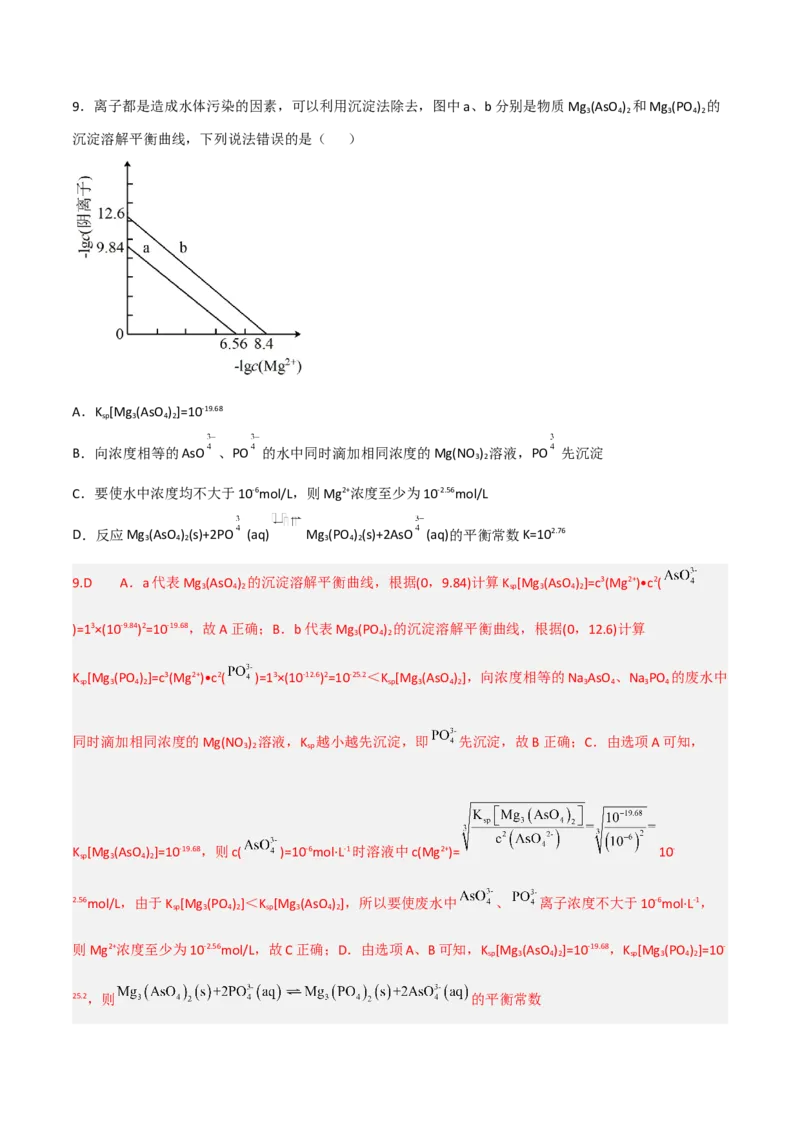
,D正确;故选D。9.离子都是造成水体污染的因素,可以利用沉淀法除去,图中a、b分别是物质Mg (AsO ) 和Mg (PO ) 的
3 4 2 3 4 2
沉淀溶解平衡曲线,下列说法错误的是( )
A.K [Mg (AsO ) ]=10-19.68
sp 3 4 2
B.向浓度相等的AsO 、PO 的水中同时滴加相同浓度的Mg(NO ) 溶液,PO 先沉淀
3 2
C.要使水中浓度均不大于10-6mol/L,则Mg2+浓度至少为10-2.56mol/L
D.反应Mg (AsO ) (s)+2PO (aq) Mg (PO ) (s)+2AsO (aq)的平衡常数K=102.76
3 4 2 3 4 2
9.D A.a代表Mg (AsO ) 的沉淀溶解平衡曲线,根据(0,9.84)计算K [Mg (AsO ) ]=c3(Mg2+)•c2(
3 4 2 sp 3 4 2
)=13×(10-9.84)2=10-19.68,故A正确;B.b代表Mg (PO ) 的沉淀溶解平衡曲线,根据(0,12.6)计算
3 4 2
K [Mg (PO ) ]=c3(Mg2+)•c2( )=13×(10-12.6)2=10-25.2<K [Mg (AsO ) ],向浓度相等的Na AsO 、Na PO 的废水中
sp 3 4 2 sp 3 4 2 3 4 3 4
同时滴加相同浓度的Mg(NO ) 溶液,K 越小越先沉淀,即 先沉淀,故B正确;C.由选项A可知,
3 2 sp
K [Mg (AsO ) ]=10-19.68,则c( )=10-6molL-1时溶液中c(Mg2+)= 10-
sp 3 4 2
⋅
2.56mol/L,由于K [Mg (PO ) ]<K [Mg (AsO ) ],所以要使废水中 、 离子浓度不大于10-6molL-1,
sp 3 4 2 sp 3 4 2
⋅
则Mg2+浓度至少为10-2.56mol/L,故C正确;D.由选项A、B可知,K [Mg (AsO ) ]=10-19.68,K [Mg (PO ) ]=10-
sp 3 4 2 sp 3 4 2
25.2,则 的平衡常数,故D错误;
故选:D。
10.室温下,向 溶液和 溶液中分别滴加 的
溶液, [ 或 ]与 溶液体积的关系如图所示。下列说法错误的是()
A.室温下,
B.A、C、D点对应溶液中,C点对应的 最大
C.若用 的 溶液滴定,则A点向B点移动
D.室温下,
10.B A.由分析可知,室温下,氯化银的溶度积为10—4.9×10—4.9=10—9.8,故A正确;
B.由分析可知,A点溶液中银离子浓度为10—4.9mol/L,D点溶液中银离子浓度为2×10—1.8mol/L,C点硫酸
钠溶液为完全反应,溶液中硫酸根离子浓度大于D点,由温度不变,溶度积不变可知,溶液中银离子浓度
小于D点,则A、C、D点对应溶液中银离子浓度最大的是D点,故B错误;C.若用0.05mol/L硝酸银溶液
滴定10mL0.1mol/L氯化钠溶液,硝酸银溶液体积为20mL时氯化钠溶液和硝酸银溶液恰好完全反应,由温
度不变,溶度积不变可知,溶液中氯离子浓度为10—4.9mol/L,则图中A点移向B点,故C正确;D.由分析
可知,室温下,氯化银的溶度积为10—4.9×10—4.9=10—9.8,硫酸银的溶度积为10—1.8×(2×10—1.8)2=4×10—5.4,由方程式可知,反应的平衡常数K= = = = =4×1014.2,故D正确;故
选B。
11.(2021·福建节选)四钼酸铵是钼深加工的重要中间产品具有广泛的用途。一种以钼精矿(主要含 ,
还有 、 的化合物及 等)为原料制备四钼酸铵的工艺流程如下图所示。
回答下列问题:
(3)“净化”时,浸出液中残留的 、 转化为沉淀除去。研究表明,该溶液中 和pH的关系为:
。为了使溶液中的杂质离子浓度小于 ,应控制溶液的pH不小于_______。
(已知: ; 和 的 分别为35.2和17.2)
11. 3.9
解析: 和 的 分别为35.2和17.2,则K (CuS)=10-35.2,K (FeS)=10-17.2,要使Cu2+浓度小于
sp sp
,则S2-浓度大于 mol/L=10-29.2mol/L,要使Fe2+浓度小于 ,则S2-浓度大
于 mol/L=10-11.2mol/L,综述:c(S2-)>10-11.2mol/L,c(S2-)=10-11.2mol/L时,lg(10-11.2)=pH-15.1,pH=15.1-
11.2=3.9,综上所述,为了使溶液中的杂质离子浓度小于 ,应控制溶液的pH不小于3.9;