文档内容
高频考点 4 配制一定物质的量浓度的溶液
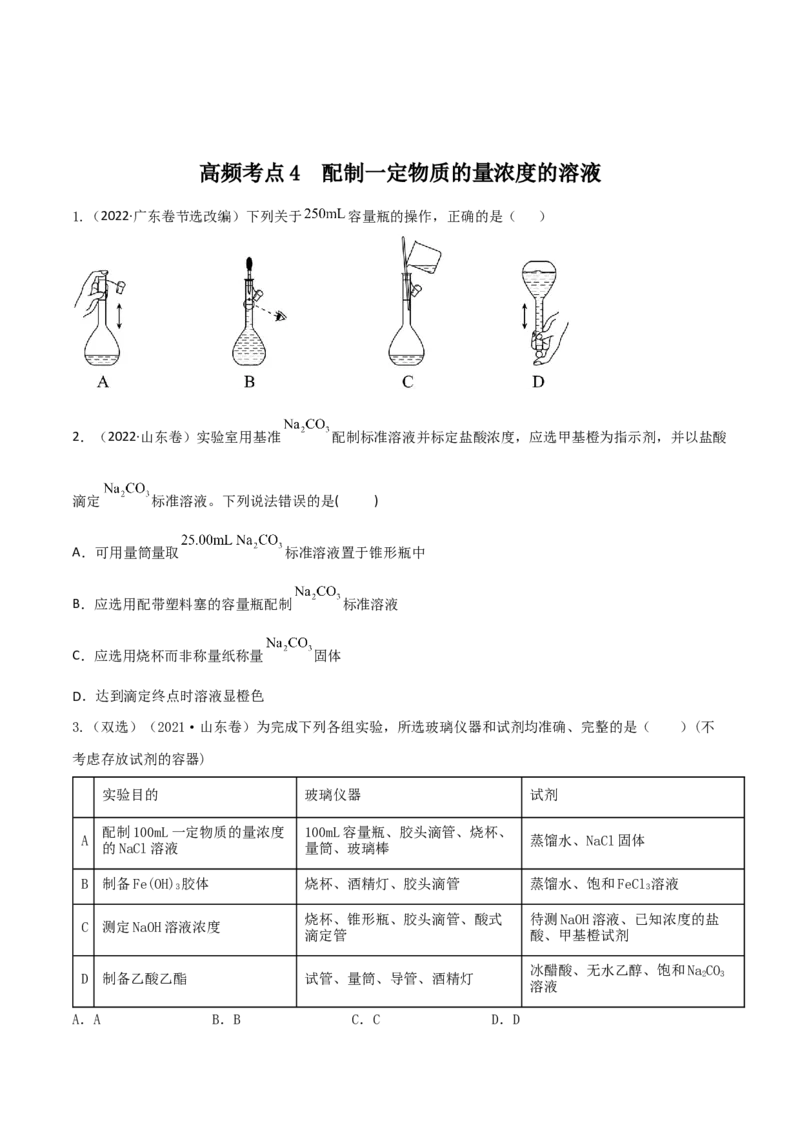
1.(2022·广东卷节选改编)下列关于 容量瓶的操作,正确的是( )
2.(2022·山东卷)实验室用基准 配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,并以盐酸
滴定 标准溶液。下列说法错误的是( )
A.可用量筒量取 标准溶液置于锥形瓶中
B.应选用配带塑料塞的容量瓶配制 标准溶液
C.应选用烧杯而非称量纸称量 固体
D.达到滴定终点时溶液显橙色
3.(双选)(2021·山东卷)为完成下列各组实验,所选玻璃仪器和试剂均准确、完整的是( )(不
考虑存放试剂的容器)
实验目的 玻璃仪器 试剂
配制100mL一定物质的量浓度 100mL容量瓶、胶头滴管、烧杯、
A 蒸馏水、NaCl固体
的NaCl溶液 量筒、玻璃棒
B 制备Fe(OH) 胶体 烧杯、酒精灯、胶头滴管 蒸馏水、饱和FeCl 溶液
3 3
烧杯、锥形瓶、胶头滴管、酸式 待测NaOH溶液、已知浓度的盐
C 测定NaOH溶液浓度
滴定管 酸、甲基橙试剂
冰醋酸、无水乙醇、饱和NaCO
D 制备乙酸乙酯 试管、量筒、导管、酒精灯 2 3
溶液
A.A B.B C.C D.D4.下列实验操作规范且能达到目的的是( )
目的 操作
在50 mL酸式滴定管中装入盐酸,调整初始读数为30.00
A 取20.00 mL盐酸
mL后,将剩余盐酸放入锥形瓶
B 清洗碘升华实验所用试管 先用酒精清洗,再用水清洗
C 测定醋酸钠溶液pH 用玻璃棒蘸取溶液,点在湿润的pH试纸上
配制浓度为0.010 mol·L-1的KMnO 称取KMnO 固体0.158 g,放入100 mL容量瓶中,加水溶
D 4 4
溶液 解并稀释至刻度
5.(双选)(2022·青岛高三模拟)(某同学购买了一瓶“84”消毒液,包装说明如下:
主要成分:25%NaClO、1 000 mL、密度1.19 g·cm-3
使用方法:稀释100倍(体积比)后使用
注意事项:密封保存,易吸收空气中的CO 变质
2
请根据以上信息和相关知识判断,下列分析不正确的是( )
A.该“84”消毒液的物质的量浓度为40.0 mol·L-1
B.一瓶该“84”消毒液敞口放置一段时间后浓度会变小
C.取100 mL该“84”消毒液稀释100倍后用于消毒,稀释后的溶液中c(Na+)约为0.04 mol·L-1
D.参阅该“84”消毒液的配方,欲用NaClO固体配制含25%NaClO的消毒液480 mL,需要称量的NaClO固
体质量为143 g
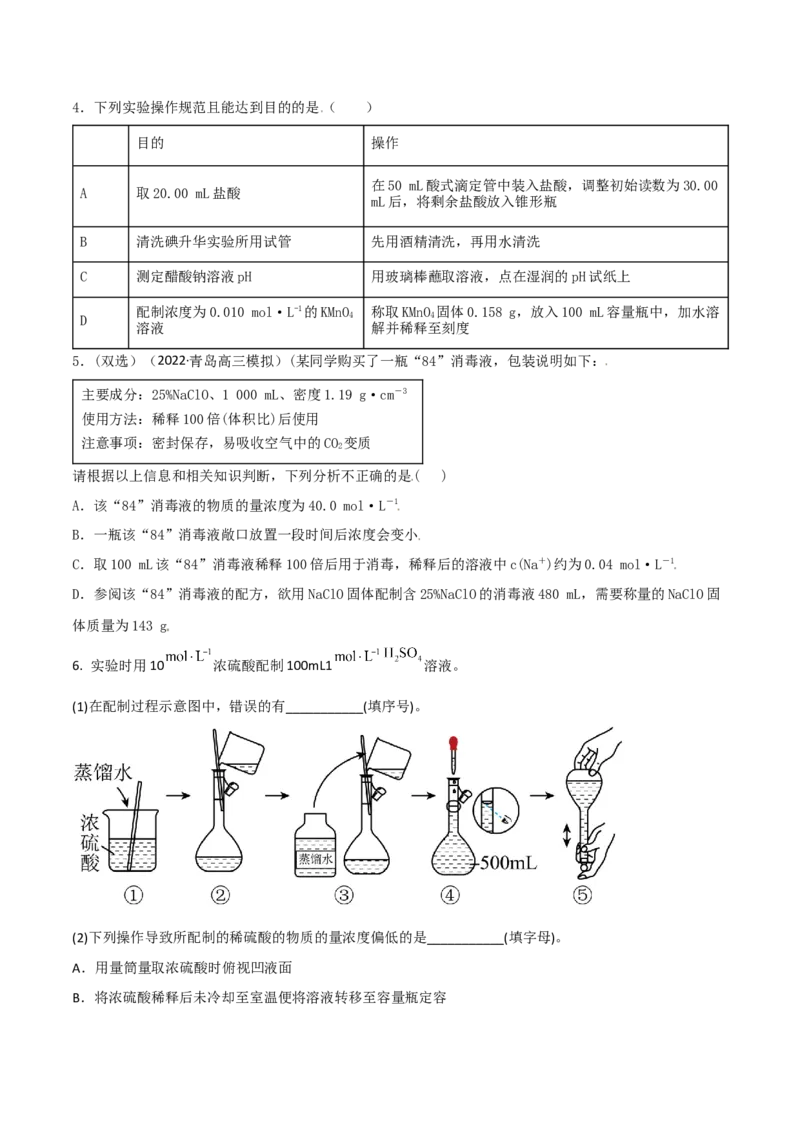
6. 实验时用10 浓硫酸配制100mL1 溶液。
(1)在配制过程示意图中,错误的有___________(填序号)。
(2)下列操作导致所配制的稀硫酸的物质的量浓度偏低的是___________(填字母)。
A.用量筒量取浓硫酸时俯视凹液面
B.将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶定容C.容量瓶用蒸馏水洗后未干燥
D.定容时仰视液面
E.未洗涤烧杯和玻璃棒
F.转移到容量瓶的过程中,有少量的溶液溅出
G.用量筒量取浓硫酸倒入小烧杯后,用蒸馏水洗涤量筒并将洗涤液转移至小烧杯中
H.用不干燥的量筒量取浓硫酸
7.(2022·北京平谷高三期末)学习小组探究碳酸钠和碳酸氢钠性质
(1)分别取 和
如图:Ⅰ中浅红色褪去,且立即产生大量气泡;Ⅱ中开始无气泡,溶液颜色由红色变为浅红色,最后出现
大量气泡.
①浓度相同时,碱性 ________ (填“>”或“<”)。
②Ⅱ的反应过程出现 的证据是___________,其离子反应的方程式________________。
(2)用 固体配制 溶液。
①用到的玻璃仪器有:量筒、烧杯、玻璃棒、胶头滴管和_____________。
②计算需要 固体的质量是_________g。
③下列情况中,会使所配溶液浓度偏高的是___________(填字母)。
a.转移时,没有洗涤烧杯和玻璃棒
b.定容时,眼睛俯视刻度线
c.摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
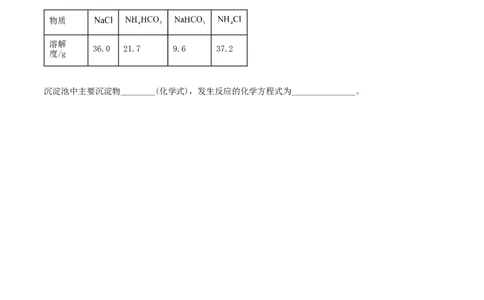
(3)我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献.下图为联合制碱法的主要
过程(部分物质已略去)。已知:ⅰ. 极易溶于水并生成碱,与酸反应生成盐,如 。
ⅱ.有关物质的溶解度
物质
溶解
36.0 21.7 9.6 37.2
度/g
沉淀池中主要沉淀物________(化学式),发生反应的化学方程式为_______________。