文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(浙江专用)
黄金卷01
(考试时间:90分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 Li 7 N 14 O 16 Na 23 Mg 24 Al 27 Si 28 P 31 S 32
Cl 35.5 K 39 Ca 40 Mn 55 Fe 56 Cu 64 Zn 65 Ga 70 Br 80 Ag 108 Ba 137
第Ⅰ卷
一、单项选择题:共16题,每题3分,共48分。每题只有一个选项最符合题意。
1.下列材料主要成分属于新型无机非金属材料的是( )
A.聚酰胺纤维 B.金刚砂陶瓷轴承 C.硬铝 D.酚醛树脂
2.下列化学用语表示正确的是( )
A.Ca2+的结构示意图:
B.锌原子的价层电子的轨道表示式:
C.SO 的VSEPR模型:V形
2
D.HO 的电子式:
2 2
3.铁及其化合物应用广泛,下列说法正确的是( )
A.Fe元素位于周期表VIIIB族 B.Fe(SCN) 属于弱电解质
3
C.Fe (SO ) 可用作补血剂 D.Fe元素位于周期表 区
2 4 3
4.下列物质的性质与用途的对应关系正确的是( )
A.NaClO溶液呈碱性,可用作消毒剂
B.稀硝酸具有强氧化性,常温下可清洗附着在试管内壁的银镜
C.石墨晶体内含大 键,可用作润滑剂
D.非金属性C>Si,工业上用焦碳与SiO 反应制备粗Si
2
5.下列实验能达到实验目的的是( )A.图①操作可除去溴水中的溴单质
B.图②操作用于分离饱和碳酸钠溶液和乙酸乙酯,将分层的液体依次从下口放出
C.图③装置进行铁与水蒸气的反应,点燃肥皂泡检验氢气
D.图④装置用于蒸馏、收集低沸点成分,冷凝水应该从 a口进b口出
6.某原电池总反应为Li+SOCl =SO↑+4 LiCl+S↓,设N 为阿伏伽德罗常数的值,下列有关说法不正
2 2 A
确的是( )
A.SO 不是还原产物
2
B.每生成 ,电子转移是4N
A
C.其正极反应式是2SOCl +4e-=SO↑+4Cl-+S↓
2 2
D.单质锂是还原剂,该电池可用水作溶剂
7.设N 为阿伏伽德罗常数的值,下列说法正确的是( )
A
A. 中含有的中子数为10N
A
B.42g环己烷( )中含有 键的数目为9N
A
C.标准状况下,22.4L CHCl 中含有的分子数为N
3 A
D.6.0 gSiO 与足量NaOH溶液反应,所得溶液中SiO2-的个数为0.1N
2 3 A
8.下列说法不正确的是( )
A.发蓝处理后的钢铁耐腐蚀性较强,是因为发蓝过程改变了钢铁的晶体结构
B.硫化橡胶具有较高强度,是因为二硫键将线型结构转变为网状结构
C.低密度聚乙烯的软化温度较低,是因为高分子链之间有较多长短不一的支链
D.石墨具有导电性,是因为碳原子的p轨道相互重叠,使p电子可在层内自由移动
9.下列过程中对应的离子方程式正确的是( )
A.向苯酚钠溶液中通入少量CO:2C HO-+CO +H O→2C HOH+CO 2-
2 6 5 2 2 6 5 3
B.酚酞滴入碳酸钠溶液中变红:CO2-+H O HCO+2OH-
3 2 2 3
C.同浓度同体积明矾[K Al(SO )·12H O]溶液与Ba(OH) 溶液混合:2Al3++3SO2-+3Ba2++6OH-
4 2 2 2 4
=3BaSO ↓+2 Al(OH) ↓
4 3D.用醋酸和淀粉-KI溶液检验加碘盐中的IO -:IO -+5I-+6H+=3I +3H O
3 3 2 2
10.2-丁炔可发生如下转化,下列说法不正确的是( )
A.2-丁炔分子中最多有6个原子共面
B.X与酸性KMnO 溶液反应可生成CHCOOH
4 3
C.Y可以发生银镜反应
D.高分子Z可能存在顺式结构和反式结构
11.W、X、Y、Z是短周期主族元素,W与其他元素不在同一周期,X元素的电负性仅次于氟元素,
Y的基态原子中单电子与成对电子个数比为3∶4,Z原子电子总数与X原子的最外层电子数相同。下列说法
不正确的是( )
A.键角:YX +<YX -
2 2
B.第一电离能:Y>X>Z
C.基态Z原子核外电子有4种空间运动状态
D.W、X可形成离子化合物,也可形成共价化合物
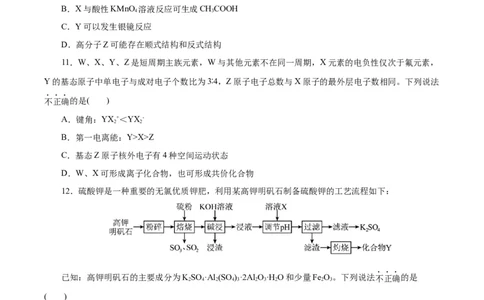
12.硫酸钾是一种重要的无氯优质钾肥,利用某高钾明矾石制备硫酸钾的工艺流程如下:
已知:高钾明矾石的主要成分为KSO ·Al(SO )·2AlO·H O和少量Fe O。下列说法不正确的是
2 4 2 4 3 2 3 2 2 3
( )
A.焙烧时Al (SO ) 反应的化学方程式为2Al (SO )+4S+6O 2Al O+10SO
2 4 3 2 4 3 2 2 3 3
B.溶液X可能是NH ·H O
3 2
C.工业上通过电解化合物Y制成铝单质
D.SO 可回收利用后应用于本流程
3
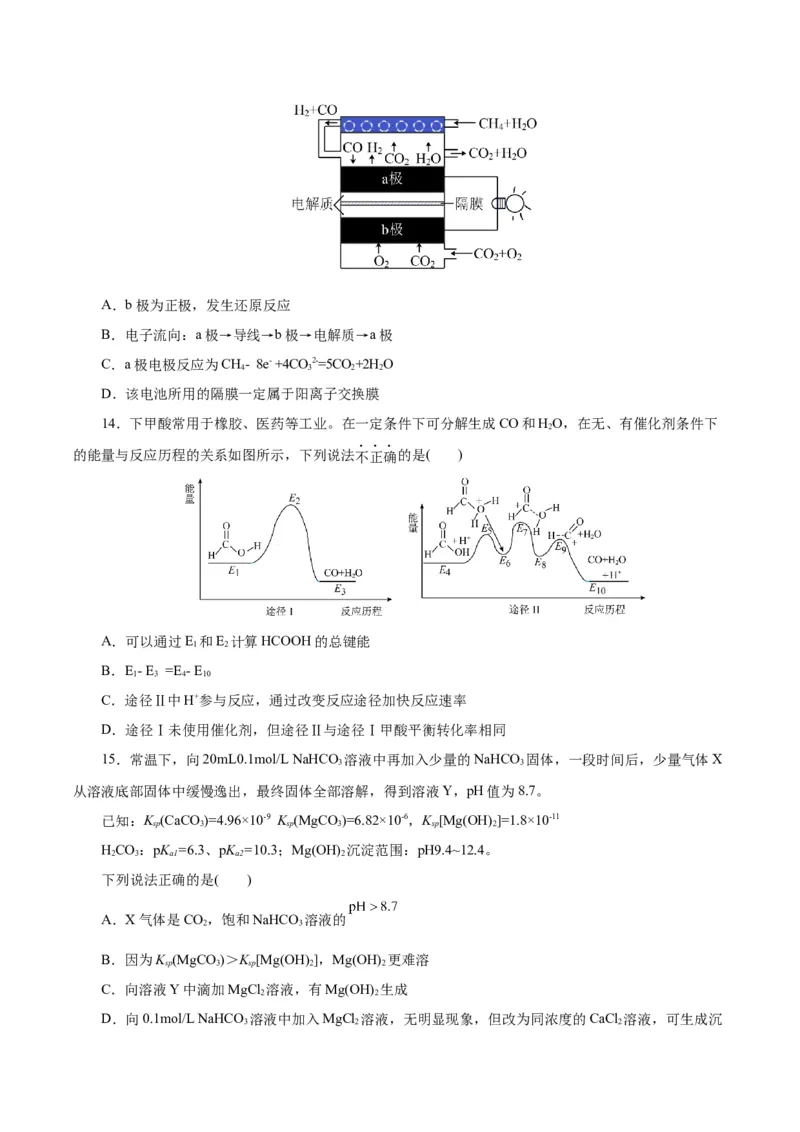
13.内部重整式高温燃料电池具有良好的商业化前景,其基本工作原理(以CH 为原料,熔融碳酸盐为
4
电解质)如图所示。下列说法正确的是( )A.b极为正极,发生还原反应
B.电子流向:a极→导线→b极→电解质→a极
C.a极电极反应为CH- 8e- +4CO 2-=5CO +2H O
4 3 2 2
D.该电池所用的隔膜一定属于阳离子交换膜
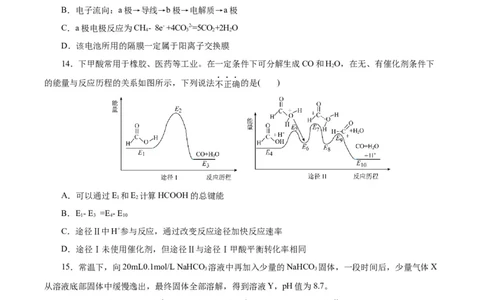
14.下甲酸常用于橡胶、医药等工业。在一定条件下可分解生成CO和HO,在无、有催化剂条件下
2
的能量与反应历程的关系如图所示,下列说法不正确的是( )
A.可以通过E 和E 计算HCOOH的总键能
1 2
B.E- E =E - E
1 3 4 10
C.途径Ⅱ中H+参与反应,通过改变反应途径加快反应速率
D.途径Ⅰ未使用催化剂,但途径Ⅱ与途径Ⅰ甲酸平衡转化率相同
15.常温下,向20mL0.1mol/LNaHCO 溶液中再加入少量的NaHCO 固体,一段时间后,少量气体X
3 3
从溶液底部固体中缓慢逸出,最终固体全部溶解,得到溶液Y,pH值为8.7。
已知:K (CaCO)=4.96×10-9 K (MgCO )=6.82×10-6,K [Mg(OH) ]=1.8×10-11
sp 3 sp 3 sp 2
HCO:pK =6.3、pK =10.3;Mg(OH) 沉淀范围:pH9.4~12.4。
2 3 a1 a2 2
下列说法正确的是( )
A.X气体是CO,饱和NaHCO 溶液的
2 3
B.因为K (MgCO )>K [Mg(OH) ],Mg(OH) 更难溶
sp 3 sp 2 2
C.向溶液Y中滴加MgCl 溶液,有Mg(OH) 生成
2 2
D.向0.1mol/L NaHCO 溶液中加入MgCl 溶液,无明显现象,但改为同浓度的CaCl 溶液,可生成沉
3 2 2淀。
16.探究铜及其化合物的性质,下列实验方案设计、现象和结论都正确的是( )
实验方案 现象 结论
铜片不断溶解,而
铁片与铜片用导线相连,放入盛有
A 铁片表面无明显变 该情况下,铜单质的还原性强于铁单质
浓硝酸的烧杯中
化
向铜丝与浓硫酸反应后的溶液中加
B 溶液变为蓝色 该反应的产物中有CuSO 产生
蒸馏水稀释 4
在试管中加入2mL 10% NaOH溶
乙醛能将新制氢氧化铜悬浊液还原为
C 液,再加入5滴5% CuSO 溶液,振 有砖红色沉淀产生
4 Cu O
荡后加入0.5mL乙醛溶液,加热 2
向10mL 0.1mol/L Na S溶液中滴入 开始有白色沉淀产
2
D 2mL 0.1mol/L ZnSO 溶液,再加入 生,后产生黑色沉 Ksp(CuS)<Ksp(ZnS)
4
2mL 0.1mol/L CuSO 溶液 淀
4
第Ⅱ卷
二、非选择题:共5题,共52分。
17.(10分)2023年8月1日起,我国对镓(Ga)等相关物项实施出口管制。Ga与B、Al处于同一主族。
请回答:
(1)基态Ga原子的价电子排布图: ;
(2)①硼的氢化物叫硼烷(B H )。如B H (乙硼烷-6)、B H (丁硼烷-10)等。下列说法不正确的是
n m 2 6 4 10
;
A.B原子由 需吸收能量
B.B H 的结构式:
2 6
C.同周期相邻元素的电负性大小:Be<B<C
D.B H 与C≡O反应生成HBCO,HBCO分子中 键与 键数目之比为:5:2
2 6 3 3
②氮和硼形成的化合的BN,与C 互为等电子体,通常存在石墨型与金刚石型两种结构,可发生如下
2
转化: 。两类化合物中B原子的杂化方式分别为:
;金刚石型的BN的硬度大于金刚石,原因是 ;③B H 极易发生水解生成HBO 和H,请写出反应的化学方程式: ;
n m 3 3 2
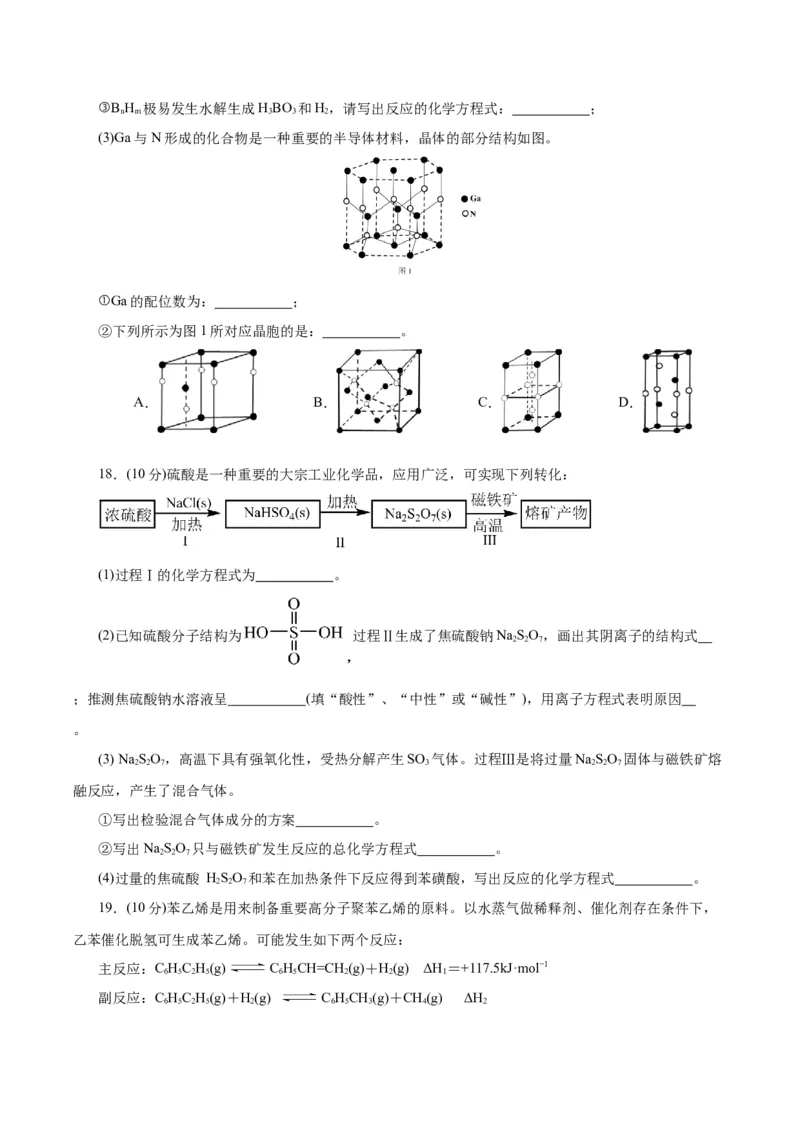
(3)Ga与N形成的化合物是一种重要的半导体材料,晶体的部分结构如图。
①Ga的配位数为: ;
②下列所示为图1所对应晶胞的是: 。
A. B. C. D.
18.(10分)硫酸是一种重要的大宗工业化学品,应用广泛,可实现下列转化:
(1)过程Ⅰ的化学方程式为 。
(2)已知硫酸分子结构为 过程Ⅱ生成了焦硫酸钠NaSO,画出其阴离子的结构式
2 2 7
;推测焦硫酸钠水溶液呈 (填“酸性”、“中性”或“碱性”),用离子方程式表明原因
。
(3) Na SO,高温下具有强氧化性,受热分解产生SO 气体。过程Ⅲ是将过量NaSO 固体与磁铁矿熔
2 2 7 3 2 2 7
融反应,产生了混合气体。
①写出检验混合气体成分的方案 。
②写出NaSO 只与磁铁矿发生反应的总化学方程式 。
2 2 7
(4)过量的焦硫酸 HSO 和苯在加热条件下反应得到苯磺酸,写出反应的化学方程式 。
2 2 7
19.(10分)苯乙烯是用来制备重要高分子聚苯乙烯的原料。以水蒸气做稀释剂、催化剂存在条件下,
乙苯催化脱氢可生成苯乙烯。可能发生如下两个反应:
主反应:C HC H(g) C HCH=CH(g)+H(g) ΔH =+117.5kJ·mol−1
6 5 2 5 6 5 2 2 1
副反应:C HC H(g)+H(g) C HCH(g)+CH(g) ΔH
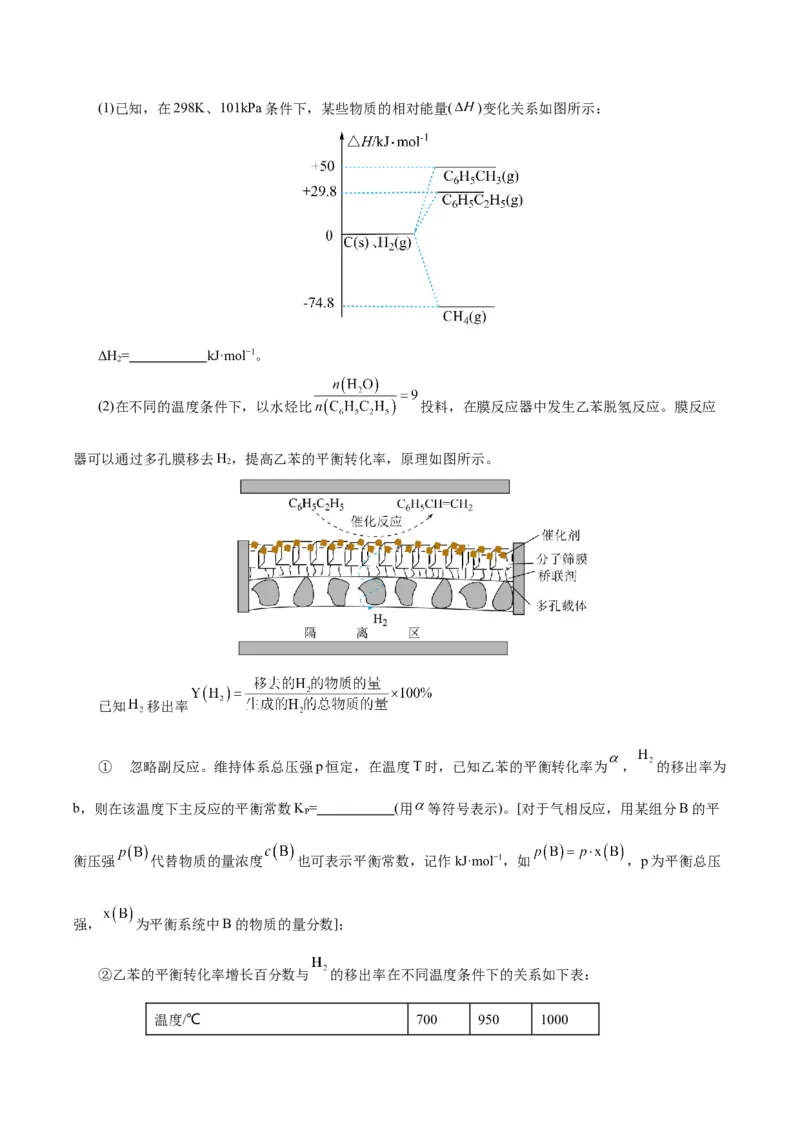
6 5 2 5 2 6 5 3 4 2(1)已知,在298K、101kPa条件下,某些物质的相对能量( )变化关系如图所示:
ΔH= kJ·mol−1。
2
(2)在不同的温度条件下,以水烃比 投料,在膜反应器中发生乙苯脱氢反应。膜反应
器可以通过多孔膜移去H,提高乙苯的平衡转化率,原理如图所示。
2
已知 移出率
① 忽略副反应。维持体系总压强p恒定,在温度T时,已知乙苯的平衡转化率为 , 的移出率为
b,则在该温度下主反应的平衡常数K = (用 等符号表示)。[对于气相反应,用某组分B的平
P
衡压强 代替物质的量浓度 也可表示平衡常数,记作kJ·mol−1,如 ,p为平衡总压
强, 为平衡系统中B的物质的量分数];
②乙苯的平衡转化率增长百分数与 的移出率在不同温度条件下的关系如下表:
温度/℃ 700 950 1000增长百分数/%
移出率/%
60 8.43 4.38 2.77
80 16.8 6.1 3.8
90 27 7.1 4.39
高温下副反应程度极小。试说明当温度高于950℃时,乙苯的平衡转化率随 的移去率的变化改变程
度不大的原因: ;
③下列说法正确的是 。
A.生成H 的总物质的量与苯乙烯相等
2
B.因为H 被分离至隔离区,故反应器中不发生副反应
2
C.在恒容的膜反应器中,其他条件不变,增大水烃比,可提高乙苯的转化率
D.膜反应器可降低反应温度,减少副反应的影响
(3)不同催化剂效能与水烃比有关。保持体系总压为常压的条件下,水烃比为9(曲线Ⅰ)时乙苯的平衡
转化率与温度的关系的示意图如下:
①请在图中画出水烃比为1时乙苯的平衡转化率与温度的关系曲线(曲线Ⅱ) ;
②工业上,减小水烃比是降低苯乙烯脱氢装置能耗的一个重要方向。若其他条件不变,减少水烃比,
为使反应从起始到平衡均达到或接近原有的反应速率、限度,则可相应的改变的条件: 。
A.升温 B.降温 C.增压 D.减压 E.催化剂
20.(10分)明矾[Kal(SO )·12H O]在工业上用作净水剂,医药上用作收敛剂。实验小组采用废弃的铝
4 2 2
制易拉罐按如下流程制备明矾大晶体。
已知:晶体结晶需要晶核,外加成核剂、杂质、残余晶体(易附在器壁上)均可作晶核。请回答:
(1)废铝制易拉罐溶于KOH溶液发生的主要反应为 (用离子方程式表示)。(2)下列说法不正确的是___________。
A.可采取将废易拉罐剪碎、酒精灯加热等方式加快溶解速率
B.加入KOH溶液至不再产生气泡后,趁热过滤,除去不溶物
C.“系列操作I”有:蒸发浓缩、冷却结晶、过滤洗涤灼烧
D.制备明矾大晶体时,小晶体应悬挂在靠近烧杯底部的位置
(3)“系列操作II”的装置如图所示,烧杯上方所盖的纸片的作用是 。
(4) 是一种慢性神经毒素,长期积累会导致神经结节。实验室可采用置换滴定法测定天然水体样品
中的 浓度。简要过程如下:
有关反应如下(试剂EDTA用 表示):
步骤①:Al3++Y- =AlY-
步骤②:Zn2++Y4-= ZnY2-
步骤③:AlY-+6F- =AlF3-+ Y4-
6
①下列有关说法不正确的是 。
A.碱式滴定管有气泡时,将橡皮塞向上弯曲,两手指挤压橡皮管中玻璃珠的下方(图所示位置),将气
泡从管尖排出
B.天然水体样品中的Ca2+( CaY2-不与F反应)不影响 含量的测定
C.步骤①所加试剂EDTA,实验前不需要标定其浓度
D.如果步骤②所加 标准溶液偏少,会导致 浓度的测定值小于真实值
②根据检测过程,请给出配合离子ZnY2-、AlY-、AlF3-的稳定性由弱到强的顺序: 。
6
③要准确计算水样中 浓度,须利用水样1的体积以及步骤 的实验数据(选填:①、②、③、④)
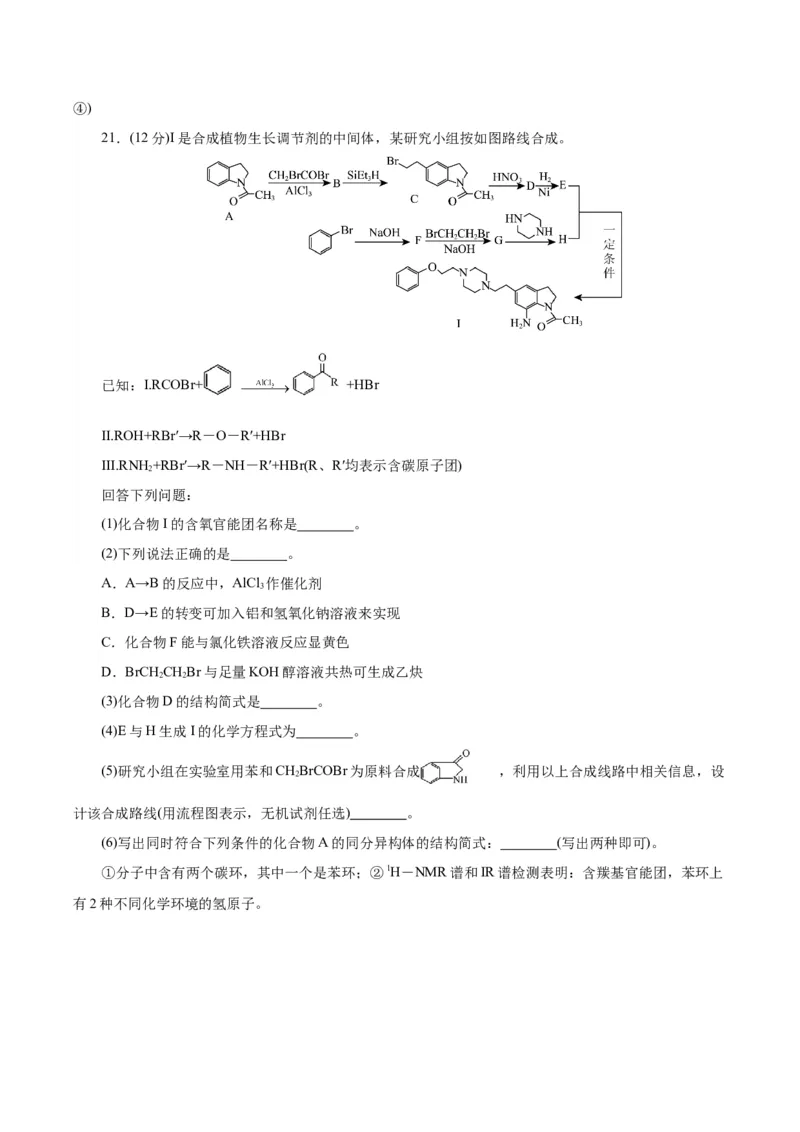
21.(12分)I是合成植物生长调节剂的中间体,某研究小组按如图路线合成。
已知:I.RCOBr+ +HBr
II.ROH+RBr′→R-O-R′+HBr
III.RNH +RBr′→R-NH-R′+HBr(R、R′均表示含碳原子团)
2
回答下列问题:
(1)化合物I的含氧官能团名称是 。
(2)下列说法正确的是 。
A.A→B的反应中,AlCl 作催化剂
3
B.D→E的转变可加入铝和氢氧化钠溶液来实现
C.化合物F能与氯化铁溶液反应显黄色
D.BrCHCHBr与足量KOH醇溶液共热可生成乙炔
2 2
(3)化合物D的结构简式是 。
(4)E与H生成I的化学方程式为 。
(5)研究小组在实验室用苯和CHBrCOBr为原料合成 ,利用以上合成线路中相关信息,设
2
计该合成路线(用流程图表示,无机试剂任选) 。
(6)写出同时符合下列条件的化合物A的同分异构体的结构简式: (写出两种即可)。
①分子中含有两个碳环,其中一个是苯环;②1H-NMR谱和IR谱检测表明:含羰基官能团,苯环上
有2种不同化学环境的氢原子。