文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(辽宁专用)
黄金卷02
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64
第Ⅰ卷
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项符合题目要
求。
1.2023年10月8日第19届亚运会在杭州圆满闭幕,本届亚运会秉持“绿色、智能、节俭、文明”的办会
理念。下列说法正确的是
A.零碳甲醇作为本届亚运会的火炬燃料,甲醇燃烧属于吸热反应
B.吉祥物“江南忆”机器人所采用芯片的主要成分为硅单质
C.亚运会纪念章“琮琮”是由锌合金镀金制成的,锌合金镀金属于合成材料
D.场馆全部使用绿色能源,打造首届碳中和亚运会,碳中和就是不排放二氧化碳
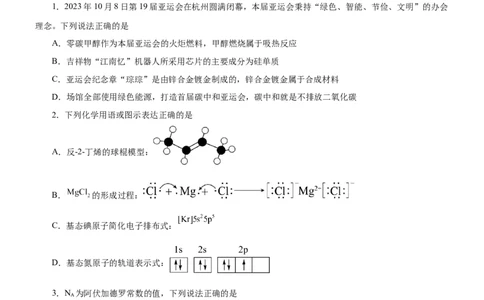
2.下列化学用语或图示表达正确的是
A.反-2-丁烯的球棍模型:
B. 的形成过程:
C.基态碘原子简化电子排布式:
D.基态氮原子的轨道表示式:
3.N 为阿伏加德罗常数的值,下列说法正确的是
A
A.密闭容器中2molNO 与1molO 充分反应,产物的分子数为:2N
2 A
B.5.8g正丁烷和异丁烷的混合物中含有σ键数目为1.3N
A
C.1L 0.1 mol∙L−1的 NaHCO 溶液中 数目为0.1N
3 A
D.2L 0.5mol/LFeCl 溶液水解生成氢氧化铁胶粒的数目为N
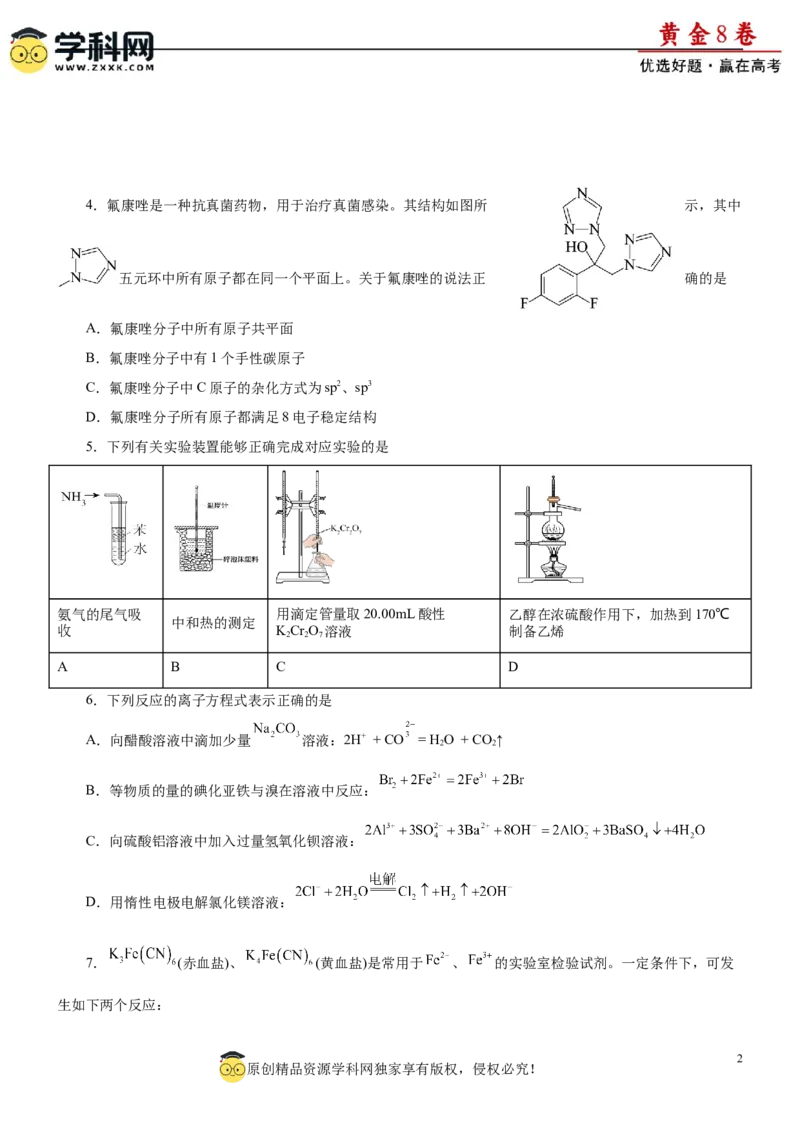
3 A4.氟康唑是一种抗真菌药物,用于治疗真菌感染。其结构如图所 示,其中
五元环中所有原子都在同一个平面上。关于氟康唑的说法正 确的是
A.氟康唑分子中所有原子共平面
B.氟康唑分子中有1个手性碳原子
C.氟康唑分子中C原子的杂化方式为sp2、sp3
D.氟康唑分子所有原子都满足8电子稳定结构
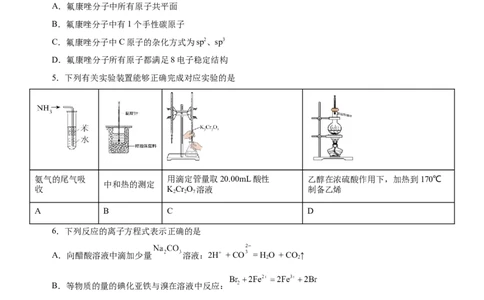
5.下列有关实验装置能够正确完成对应实验的是
氨气的尾气吸 用滴定管量取20.00mL酸性 乙醇在浓硫酸作用下,加热到170℃
中和热的测定
收 KCr O 溶液 制备乙烯
2 2 7
A B C D
6.下列反应的离子方程式表示正确的是
A.向醋酸溶液中滴加少量 溶液:2H+ + CO = H O + CO↑
2 2
B.等物质的量的碘化亚铁与溴在溶液中反应:
C.向硫酸铝溶液中加入过量氢氧化钡溶液:
D.用惰性电极电解氯化镁溶液:
7. (赤血盐)、 (黄血盐)是常用于 、 的实验室检验试剂。一定条件下,可发
生如下两个反应:
2
原创精品资源学科网独家享有版权,侵权必究!① ,固态混合,释放 ;
② ,溶液混合,消耗 。
下列有关说法不正确的是
A. 检验: (蓝色)
B. 含有离子键、极性键、配位键
C. 氧化性强于
D.两个反应方向不一致,原因可能是溶液中 与 的配位能力强于
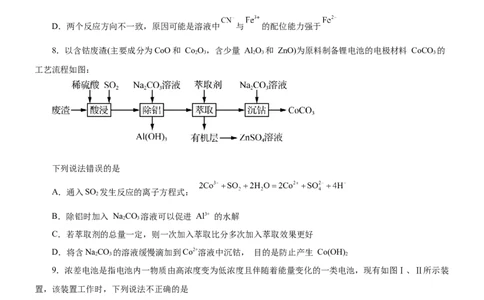
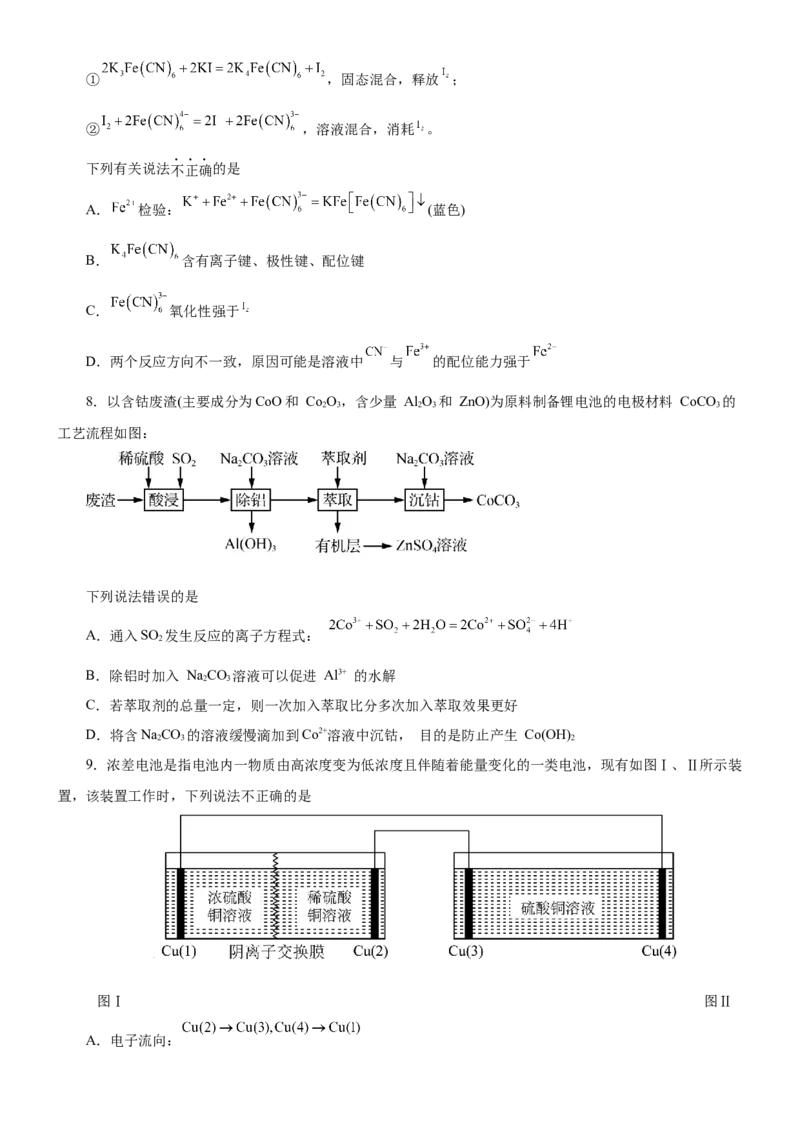
8.以含钴废渣(主要成分为CoO和 Co O,含少量 Al O 和 ZnO)为原料制备锂电池的电极材料 CoCO 的
2 3 2 3 3
工艺流程如图:
下列说法错误的是
A.通入SO 发生反应的离子方程式:
2
B.除铝时加入 NaCO 溶液可以促进 Al3+ 的水解
2 3
C.若萃取剂的总量一定,则一次加入萃取比分多次加入萃取效果更好
D.将含NaCO 的溶液缓慢滴加到Co2+溶液中沉钴, 目的是防止产生 Co(OH)
2 3 2
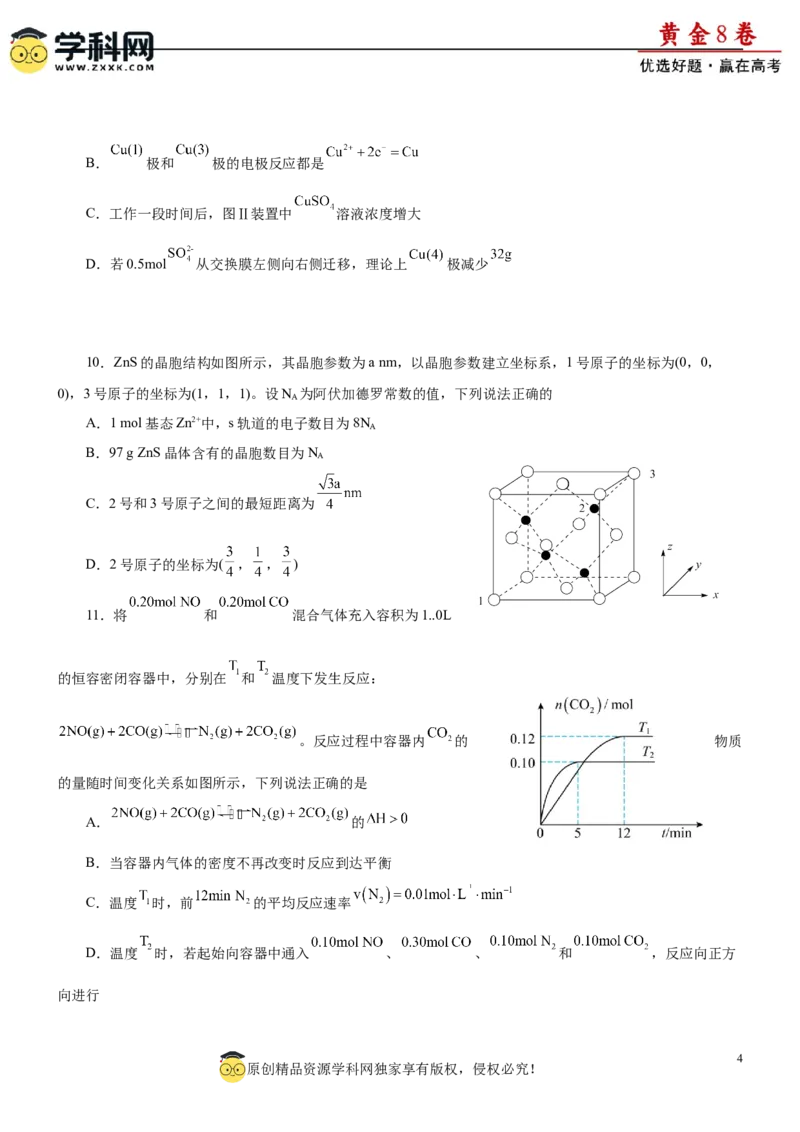
9.浓差电池是指电池内一物质由高浓度变为低浓度且伴随着能量变化的一类电池,现有如图Ⅰ、Ⅱ所示装
置,该装置工作时,下列说法不正确的是
图Ⅰ 图Ⅱ
A.电子流向:B. 极和 极的电极反应都是
C.工作一段时间后,图Ⅱ装置中 溶液浓度增大
D.若0.5mol 从交换膜左侧向右侧迁移,理论上 极减少
10.ZnS的晶胞结构如图所示,其晶胞参数为a nm,以晶胞参数建立坐标系,1号原子的坐标为(0,0,
0),3号原子的坐标为(1,1,1)。设N 为阿伏加德罗常数的值,下列说法正确的
A
A.1 mol基态Zn2+中,s轨道的电子数目为8N
A
B.97 g ZnS晶体含有的晶胞数目为N
A
C.2号和3号原子之间的最短距离为
D.2号原子的坐标为( , , )
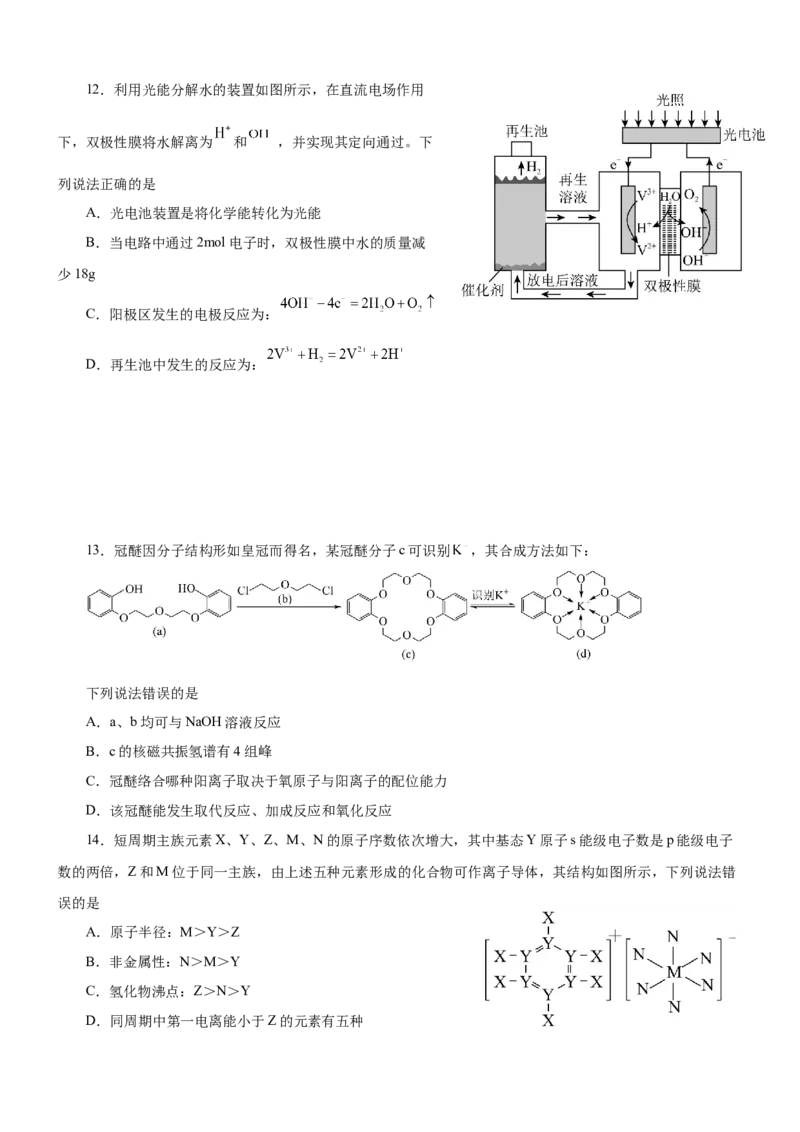
11.将 和 混合气体充入容积为1..0L
的恒容密闭容器中,分别在 和 温度下发生反应:
。反应过程中容器内 的 物质
的量随时间变化关系如图所示,下列说法正确的是
A. 的
B.当容器内气体的密度不再改变时反应到达平衡
C.温度 时,前 的平均反应速率
D.温度 时,若起始向容器中通入 、 、 和 ,反应向正方
向进行
4
原创精品资源学科网独家享有版权,侵权必究!12.利用光能分解水的装置如图所示,在直流电场作用
下,双极性膜将水解离为 和 ,并实现其定向通过。下
列说法正确的是
A.光电池装置是将化学能转化为光能
B.当电路中通过2mol电子时,双极性膜中水的质量减
少18g
C.阳极区发生的电极反应为:
D.再生池中发生的反应为:
13.冠醚因分子结构形如皇冠而得名,某冠醚分子c可识别 ,其合成方法如下:
下列说法错误的是
A.a、b均可与NaOH溶液反应
B.c的核磁共振氢谱有4组峰
C.冠醚络合哪种阳离子取决于氧原子与阳离子的配位能力
D.该冠醚能发生取代反应、加成反应和氧化反应
14.短周期主族元素X、Y、Z、M、N的原子序数依次增大,其中基态Y原子s能级电子数是p能级电子
数的两倍,Z和M位于同一主族,由上述五种元素形成的化合物可作离子导体,其结构如图所示,下列说法错
误的是
A.原子半径:M>Y>Z
B.非金属性:N>M>Y
C.氢化物沸点:Z>N>Y
D.同周期中第一电离能小于Z的元素有五种15.常温下,向20.00mL 0.10 MOH溶液中滴入0.10
的稀盐酸,溶液中pX[ ]与加入稀盐酸的体积
关系如图所示。下列说法正确的是
A.常温下,MOH电离常数的数量级为
B.a点对应的溶液中:
C.b点对应的溶液中水的电离程度最大,且溶液中:
D.c点溶液中:
第Ⅱ卷
二、非选择题:本题共4小题,共55分。
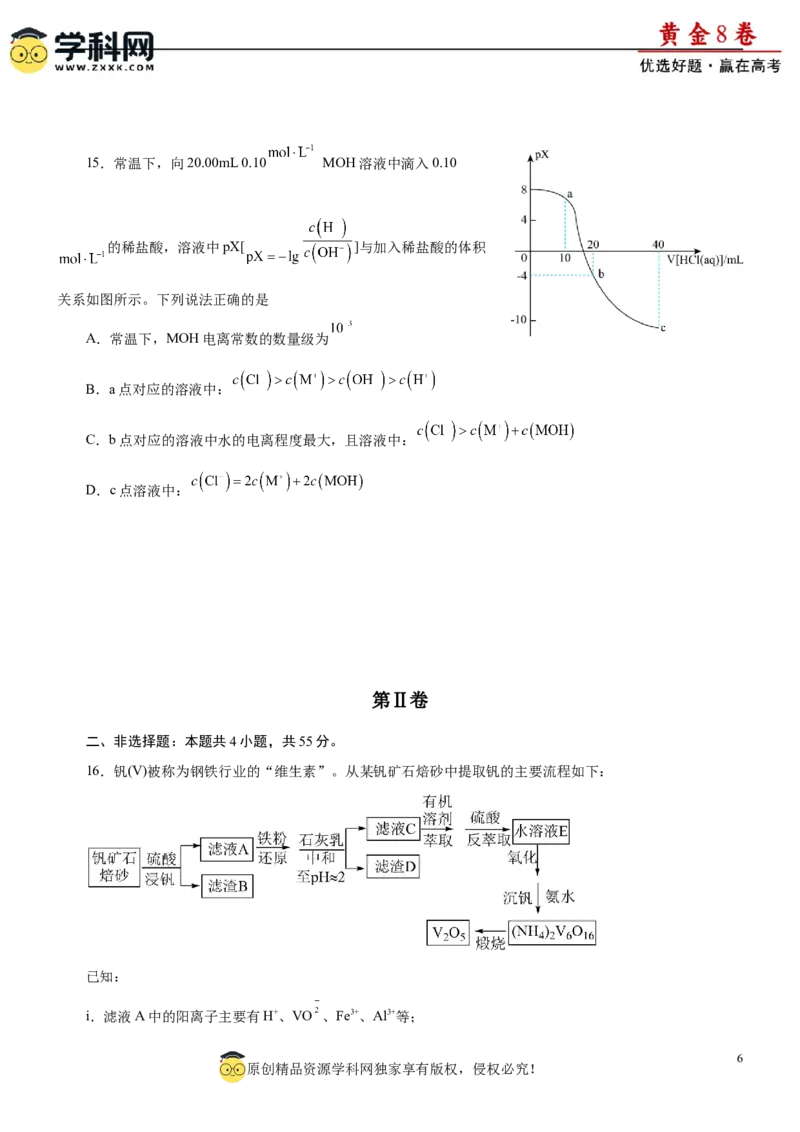
16.钒(V)被称为钢铁行业的“维生素”。从某钒矿石焙砂中提取钒的主要流程如下:
已知:
i.滤液A中的阳离子主要有H+、VO 、Fe3+、Al3+等;
6
原创精品资源学科网独家享有版权,侵权必究!ii.“萃取”过程可表示为VO2++2HA(有机相) VOA(有机相)+2H+。
2
(1)“浸钒”时,为加快浸出速率可采取的措施有 (写出1条即可)。
(2)“浸钒”过程中,焙砂中的VO 与硫酸反应的离子方程式为 。
2 5
(3)“还原”过程中,铁粉发生的反应有Fe+2H+=Fe2++H ↑、2Fe3++Fe=3Fe2+和如下反应,补全该反应的离子方
2
程式 。
VO + Fe+ ___________= VO2++ Fe2++ ___________
(4)“萃取”前,若不用石灰乳先中和,萃取效果不好,原因是 。
(5)写出“煅烧”过程发生反应的化学方程式 。
(6)用以下方法测量“浸钒”过程中钒的浸出率。从滤液A中取出1mL,用蒸馏水稀释至
10mL,加入适量过硫酸铵,加热,将滤液A中可能存在的VO2+氧化为VO ,继续加热煮沸,除去过量的
过硫酸铵。冷却后加入3滴指示剂,用cmol·L-1的(NH )Fe(SO ) 标准溶液将VO 滴定为VO2+,共消耗
4 2 4 2
vmL(NH)Fe(SO ) 溶液。
1 4 2 4 2
已知:a.所取钒矿石焙砂中钒元素的质量为ag;所得滤液A的总体积为bmL;
b.3滴指示剂消耗vmL(NH)Fe(SO ) 溶液。
2 4 2 4 2
①用上述方法测得“浸钒”过程中钒的浸出率为 。
②若不除去过量的过硫酸铵,钒浸出率的测定结果将 (填“偏高”“不变”或“偏低”)。
17.汽车尾气的污染是现代研究的重要课题。一定条件下对汽车尾气有效治理的反应要经历以下三个基元
反应阶段,反应历程如图甲所示(TS表示过渡态,图示涉及的物质均是气体)。
请回答下列问题:
(1)写出有效治理汽车尾气的三个基元反应中反应②的热化学方程式为 ;上述该过程的总反应热化
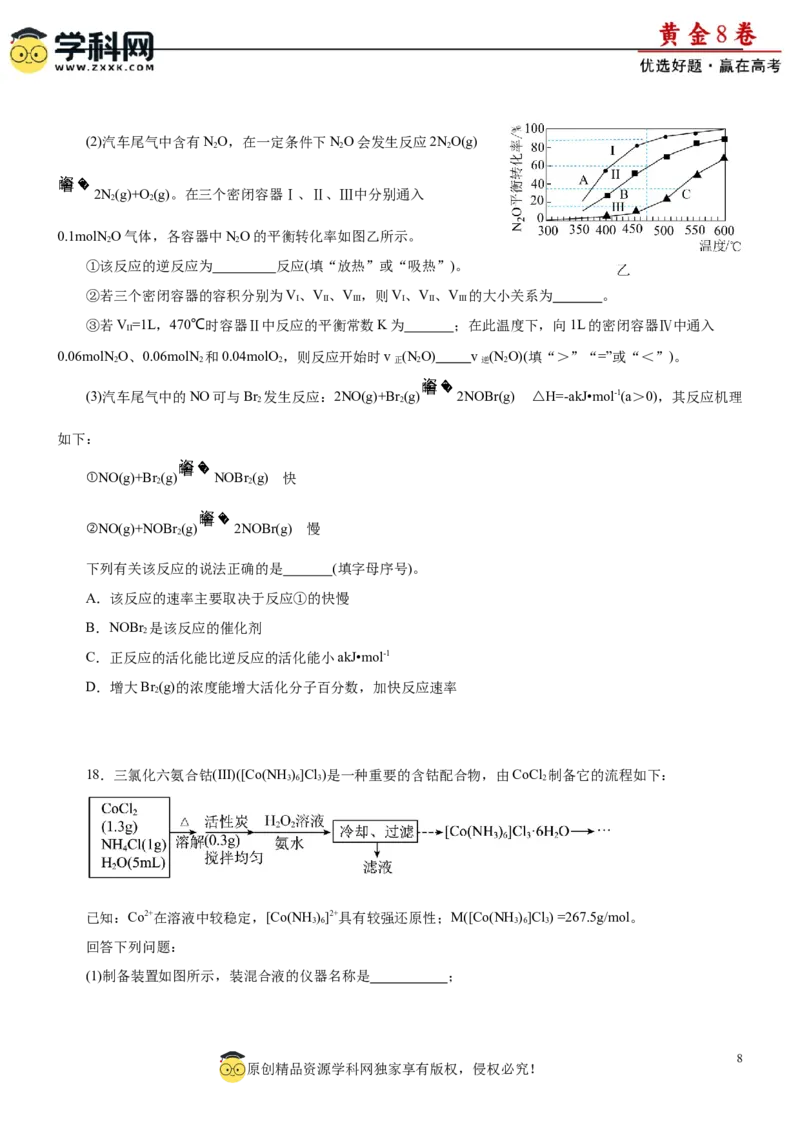
学方程式为 。(2)汽车尾气中含有NO,在一定条件下NO会发生反应2NO(g)
2 2 2
2N(g)+O(g)。在三个密闭容器Ⅰ、Ⅱ、Ⅲ中分别通入
2 2
0.1molNO气体,各容器中NO的平衡转化率如图乙所示。
2 2
①该反应的逆反应为 反应(填“放热”或“吸热”)。
②若三个密闭容器的容积分别为V、V 、V ,则V、V 、V 的大小关系为 。
I II III I II III
③若V =1L,470℃时容器Ⅱ中反应的平衡常数K为 ;在此温度下,向1L的密闭容器Ⅳ中通入
II
0.06molNO、0.06molN 和0.04molO,则反应开始时v (N O) v (N O)(填“>”“=”或“<”)。
2 2 2 正 2 逆 2
(3)汽车尾气中的NO可与Br 发生反应:2NO(g)+Br (g) 2NOBr(g) △H=-akJ•mol-1(a>0),其反应机理
2 2
如下:
①NO(g)+Br (g) NOBr (g) 快
2 2
②NO(g)+NOBr (g) 2NOBr(g) 慢
2
下列有关该反应的说法正确的是 (填字母序号)。
A.该反应的速率主要取决于反应①的快慢
B.NOBr 是该反应的催化剂
2
C.正反应的活化能比逆反应的活化能小akJ•mol-1
D.增大Br (g)的浓度能增大活化分子百分数,加快反应速率
2
18.三氯化六氨合钴(III)([Co(NH )]Cl )是一种重要的含钴配合物,由CoCl 制备它的流程如下:
3 6 3 2
已知:Co2+在溶液中较稳定,[Co(NH )]2+具有较强还原性;M([Co(NH)]Cl ) =267.5g/mol。
3 6 3 6 3
回答下列问题:
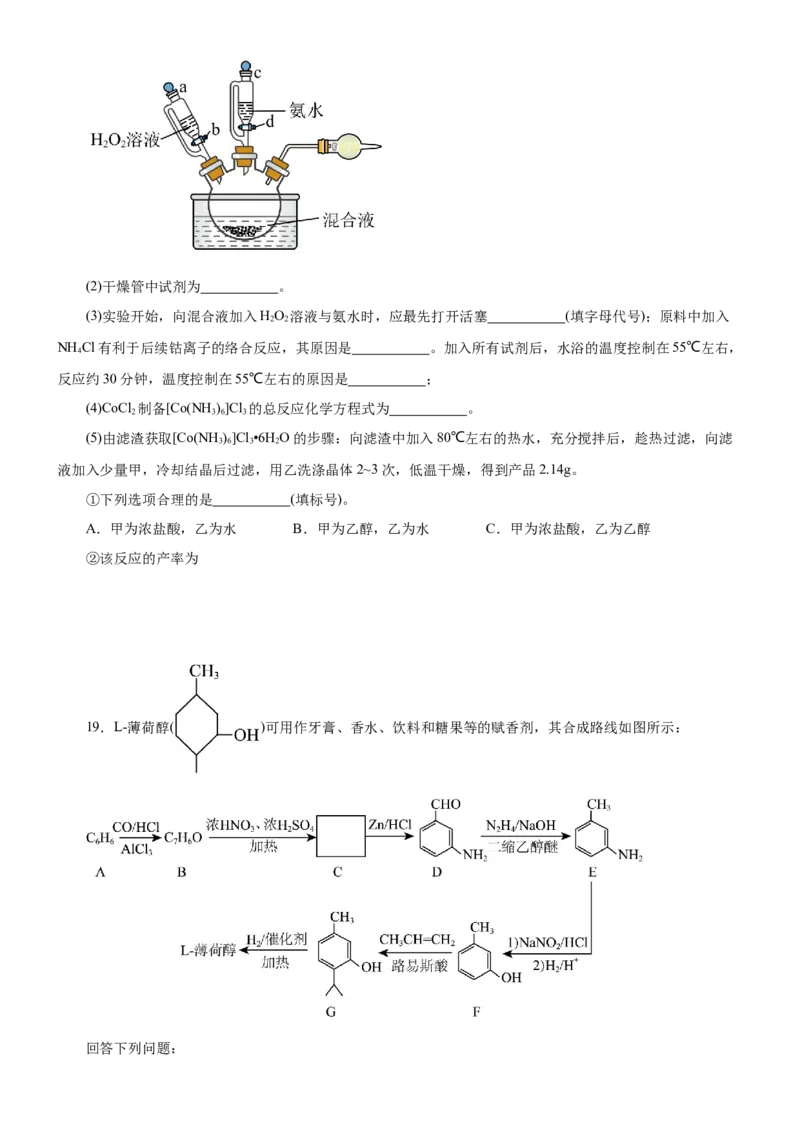
(1)制备装置如图所示,装混合液的仪器名称是 ;
8
原创精品资源学科网独家享有版权,侵权必究!(2)干燥管中试剂为 。
(3)实验开始,向混合液加入HO 溶液与氨水时,应最先打开活塞 (填字母代号);原料中加入
2 2
NH Cl有利于后续钴离子的络合反应,其原因是 。加入所有试剂后,水浴的温度控制在55℃左右,
4
反应约30分钟,温度控制在55℃左右的原因是 ;
(4)CoCl 制备[Co(NH )]Cl 的总反应化学方程式为 。
2 3 6 3
(5)由滤渣获取[Co(NH )]Cl •6H O的步骤:向滤渣中加入80℃左右的热水,充分搅拌后,趁热过滤,向滤
3 6 3 2
液加入少量甲,冷却结晶后过滤,用乙洗涤晶体2~3次,低温干燥,得到产品2.14g。
①下列选项合理的是 (填标号)。
A.甲为浓盐酸,乙为水 B.甲为乙醇,乙为水 C.甲为浓盐酸,乙为乙醇
②该反应的产率为
19.L-薄荷醇( )可用作牙膏、香水、饮料和糖果等的赋香剂,其合成路线如图所示:
回答下列问题:(1)下列说法错误的是___________(填选项字母)。
A. 中所有原子处于同一平面上 B.D中官能团为醛基、氨基
C.L-薄荷醇的分子式为 D.G与L-薄荷醇均能与 反应
(2)B的化学名称为 ,C的结构简式为 。
(3)B→C的化学方程式是 ,反应类型为 ;F→G的化学方程式是 ,反
应类型为 。
(4)G的一种同分异构体Y同时满足下列条件,写出Y的结构简式: 。
①Y能与 溶液发生显色反应。
②Y分子中有4种不同化学环境的氢,且氢原子数目比为1∶2∶2∶9。
10
原创精品资源学科网独家享有版权,侵权必究!