文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(河北专用)
黄金卷03
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64 Ce 140
第Ⅰ卷
一、单项选择题:共14题,每题3分,共42分。每题只有一个选项最符合题意。
1.化学与社会发展和人类进步息息相关。下列说法错误的是
A.华为Mate60pro系列“争气机”的芯片材料主要为晶体硅
B.用机械剥离法从石墨中分离出的石墨烯能导电,石墨烯与金刚石互为同素异形体
C.国产飞机C919用到的氮化硅陶瓷是新型无机非金属材料
D.维生素C可用作水果罐头的抗氧化剂是由于其难以被氧化
【答案】D
【解析】A.单晶硅可用于制作计算机芯片,华为Mate60pro系列“争气机”的芯片材料主要为晶体硅,A
项正确;
B.石墨烯与金刚石均为碳的单质,它们互为同素异形体,B项正确:
C.氮化硅陶瓷是新型无机非金属材料,C项正确;
D.维生素C可用作水果罐头的抗氧化剂,是由于其具有强还原性,易于被氧化,D项错误;
故选D。
2.下列化学用语或图示表达正确的是
A.金刚石的晶体结构:
B.基态溴原子电子占据最高能级的电子云轮廓图:
C. 的空间填充模型:
D. 的电子式:【答案】A
【解析】A.金刚石的晶胞中一个碳原子与其他四个碳原子构成正四面体,选项A正确;
B.基态溴原子电子占据的最高能级是p能级,电子云轮廓图是哑铃形,选项B错误;
C. 的空间结构是正四面体,不是平面结构,选项C错误;
D. 的电子式中碳原子周围是6个电子,选项D错误;
故选A。
3.N 表示阿伏加德罗常数的值。下列说法正确的是
A
A.11.2LCH 和44.8LCl (均为标准状况)在光照下充分反应后的分子数为2.5N
4 2 A
B.28g乙烯和丙烯的混合气体充分燃烧,消耗的O 分子数为4N
2 A
C.1mol14C16O(一氧化碳)中含有15N 个中子
A
D.1molNaHSO 固体中含离子总数为3N
4 A
【答案】A
【解析】A.标准状况下11.2L 和44.8L 的物质的量分别为0.5mol和2mol,光照下发生取代反应,
反应前后气体分子数不变,因此反应后的分子的物质的量为2.5mol,分子数为2.5 ,A正确;
B.乙烯和丙烯的最简式均为 ,28g乙烯和丙烯的混合气体含2mol ,1mol 消耗1.5mol氧气,
因此28g混合气体消耗3mol ,分子数为3 ,B错误;
C.一个 所含的中子数为14-6+16-8=16,所以1mol (一氧化碳)中含有16 个中子,C错
误;
D. 固体由 和 构成,则1mol 固体含有离子总数为2 ,D错误;
故选A。
4.下列反应的离子方程式正确的是
A.向NaHSO 中滴加少量Ba(HCO ) 溶液:
4 3 2
B.向有AgCl沉淀的溶液中滴加氨水,沉淀消失:C.向FeI 溶液中通入一定量氯气,测得有50%的Fe2+被氧化:
2
D.NaHCO 的水解:
3
【答案】C
【解析】A.向NaHSO 中滴加少量Ba(HCO ) 溶液:
4 3 2
,选项A错误;
B.向有AgCl沉淀的溶液中滴加氨水,沉淀消失: ,选项B错误;
C.离子还原性:I->Fe2+,通入氯气后按照还原性强弱依次反应,由题意可知两种离子的物质的量之比为
1:4,选项C正确;
D.水解是可逆的,正确的离子方程式为 ,选项D错误;
故选C。
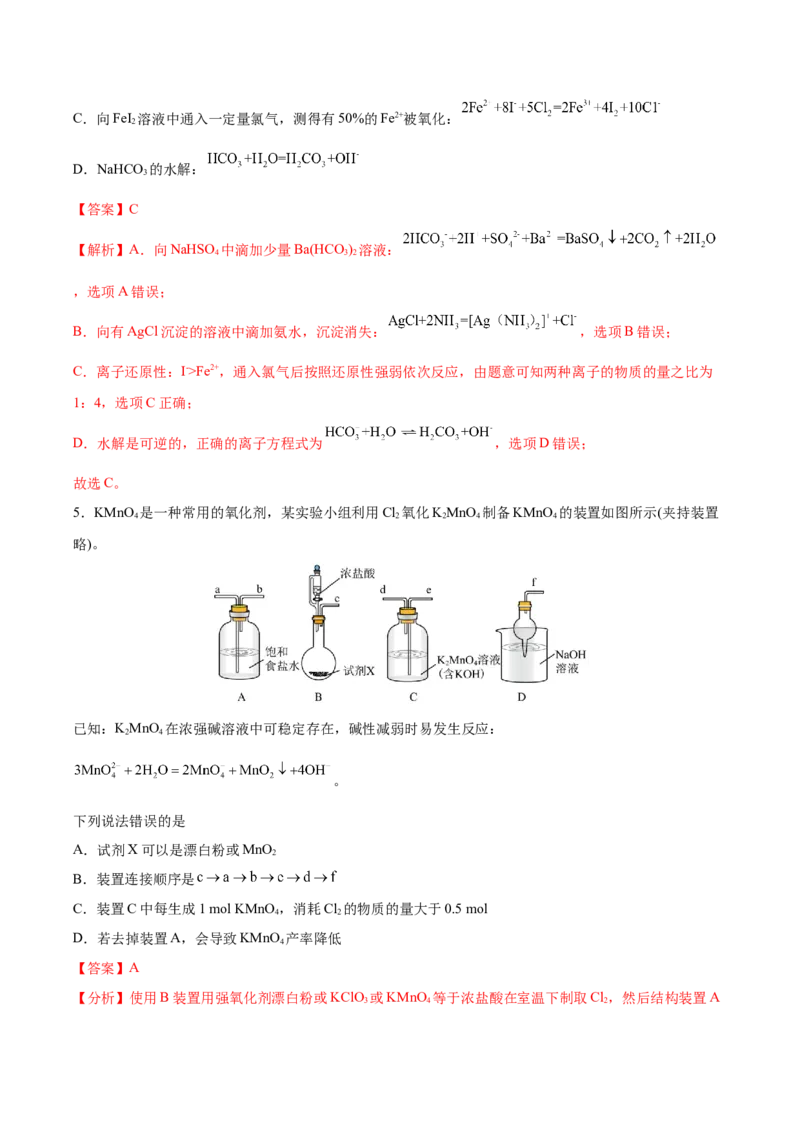
5.KMnO 是一种常用的氧化剂,某实验小组利用Cl 氧化KMnO 制备KMnO 的装置如图所示(夹持装置
4 2 2 4 4
略)。
已知:KMnO 在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
2 4
。
下列说法错误的是
A.试剂X可以是漂白粉或MnO
2
B.装置连接顺序是
C.装置C中每生成1 mol KMnO,消耗Cl 的物质的量大于0.5 mol
4 2
D.若去掉装置A,会导致KMnO 产率降低
4
【答案】A
【分析】使用B装置用强氧化剂漂白粉或KClO 或KMnO 等于浓盐酸在室温下制取Cl,然后结构装置A
3 4 2除去Cl 中的杂质HCl,再将Cl 通入装置C中与KMnO 制备KMnO ,导气管应该长进短出,最后通入装
2 2 2 4 4
置D进行尾气处理,防止多余Cl 污染环境。
2
【解析】A.在装置B中与与浓盐酸在室温下反应制取Cl,试剂X可以是漂白粉或KClO 或KMnO ,试
2 3 4
剂X不可以是MnO ,因为MnO 和浓盐酸反应需要加热,图中无加热装置,因此MnO 不能与浓盐酸反应
2 2 2
制取得到Cl,A错误;
2
B.根据上述分析可知装置连接顺序是BACD,则装置导气管连接顺序是 ,B正
确;
C.因氯气会与溶液中的KOH也会发生反应,故根据反应过程中电子转移数目相等可知:装置C中每生成
1 mol KMnO,反应消耗Cl 的物质的量大于0.5 mol,C正确;
4 2
D.若去掉装置A,挥发的氯化氢会与溶液中的KOH中和,导致溶液碱性减弱,反应生成MnO ,从而导
2
致KMnO 产率降低,D正确;
4
故选A。
6.实验探究是化学学习的方法之一、根据下列实验设计的现象所得实验结论正确的是
选
实验设计 现象 实验结论
项
在坩埚中加入16.4g ,加热一段时 加热后坩埚内固体为
A 质量为12.8g
和 混合物
间,在干燥器中冷却,称量剩余固体质量
产生白色沉淀,加
B 向鸡蛋清溶液中滴入几滴硫酸铜溶液 蛋白质发生了变性
水后沉淀不溶解
分别用蒸馏水、 溶液喷洒甲、乙两 喷洒 溶液的纸
C 能促进纸张的老化
张白纸,静置、干燥 张老化明显
烧瓶中有红棕色气 木炭具有还原性,能还
D 在烧瓶中加入木炭颗粒与浓硝酸,然后加热
体产生 原
【答案】B
【解析】A.116.4g 中含结晶水为 ,则坩埚中剩余物质质量为
12.8g时,坩埚内固体为CaC O,A项错误;
2 4
B.Cu是重金属元素,向鸡蛋清溶液中滴入几滴硫酸铜溶液,蛋白质会发生变性,产生白色沉淀,且变性
不可逆,故B正确;
C.氯化铝溶液中含铝离子和氯离子,由实验操作和现象不能证明Cl-能促进纸张的老化,铝离子也可能使
纸张老化,C项错误;D.红棕色气体也可能是由浓硝酸受热分解生成,故由实验操作和现象不能证明木炭具有还原性,D项错
误;
故选B。
7.X、Y、Z、W为原子序数依次增大的短周期主族元素,X、Y、Z位于同周期且相邻,X与W同族,W
的核外电子总数等于X和Z的核外电子总数之和。下列说法正确的是
A.元素的第一电离能:
B.简单氢化物的稳定性:
C. 中有 键
D. 的空间结构为V形,属于含有极性键的极性分子
【答案】B
【分析】X、Y、Z、W为原子序数依次增大的短周期主族元素,X、Y、Z位于同周期且相邻,则X、Y、
Z位于第二周期,W位于第三周期, X与W同族,设X的原子序数为a,则Y、Z、W的原子序数分别为
a+1,a+2,a+8,W的核外电子总数等于X和Z的核外电子总数之和,则a=6.由题意可推知,X为C,Y
为N,Z为O,W为 。
【解析】A.元素的第一电离能: ,A错误;
B.简单氢化物的稳定性: ,B正确;
C. 中含有 键,C错误;
D. 的空间结构为直线形,属于含有极性键的非极性分子,D错误。
故选B。
8.一种由Cu、In、Te组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,晶体中Te原
子填充在Cu、In围成的四面体空隙中,A点、B点原子的分数坐标分别为 、 ,下列说法
错误的是A.该晶体的化学式为
B.C点原子的分数坐标为
C.晶胞中四面体空隙的占有率为50%
D.晶胞中C、D间距离
【答案】D
【解析】A.晶胞中位于顶点、面上、和体内的Cu原子个数= ,位于面上、棱上的In原
子个数= ,位于体内的Te原子个数=8×1=8,则Cu、In、Te的原子个数比为4:4:8=1:1:2,晶
体的化学式为CuInTe ,A正确;
2
B.由位于顶点A点和体心B点原子的分数坐标分别为(0,0,0)、 可知,晶胞边长为1,则位于体
对角线 处,面对角线 处的C原子的分数坐标分别为 ,B正确;
C.由晶胞结构可知,In原子形成的四面体空隙有8个,形成的八面体空隙也有8个,则四面体空隙的占
有率为 ,C正确;
D.由晶胞中C、D形成的直角三角形的边长为 pm、 pm可知,C、D间距离d=,D错误;
故选D。
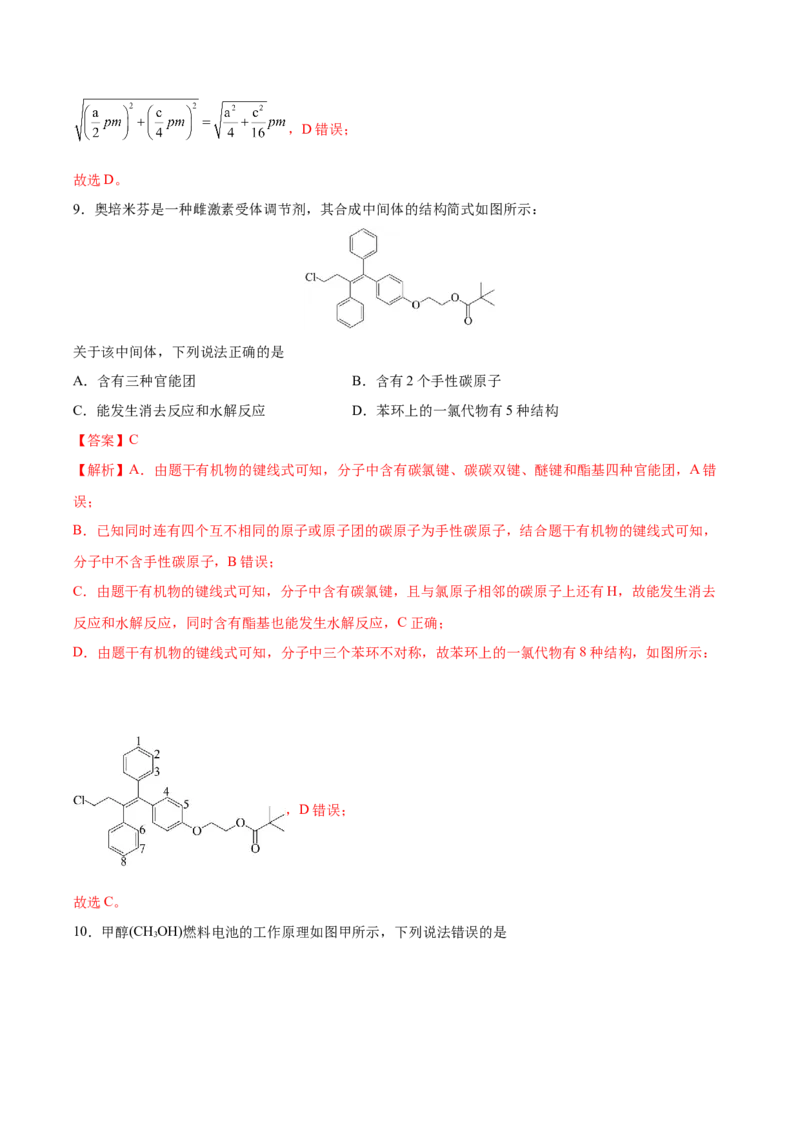
9.奥培米芬是一种雌激素受体调节剂,其合成中间体的结构简式如图所示:
关于该中间体,下列说法正确的是
A.含有三种官能团 B.含有2个手性碳原子
C.能发生消去反应和水解反应 D.苯环上的一氯代物有5种结构
【答案】C
【解析】A.由题干有机物的键线式可知,分子中含有碳氯键、碳碳双键、醚键和酯基四种官能团,A错
误;
B.已知同时连有四个互不相同的原子或原子团的碳原子为手性碳原子,结合题干有机物的键线式可知,
分子中不含手性碳原子,B错误;
C.由题干有机物的键线式可知,分子中含有碳氯键,且与氯原子相邻的碳原子上还有H,故能发生消去
反应和水解反应,同时含有酯基也能发生水解反应,C正确;
D.由题干有机物的键线式可知,分子中三个苯环不对称,故苯环上的一氯代物有8种结构,如图所示:
,D错误;
故选C。
10.甲醇(CHOH)燃料电池的工作原理如图甲所示,下列说法错误的是
3A.该电池工作时,b口通入的物质为CHOH,c口通入的物质为O
3 2
B.该电池负极的电极反应式为
C.精炼铜时,粗铜应与甲醇燃料电池的正极相连,阴极的电极反应式为 ,电解质溶液为
CuSO 溶液
4
D.用该燃料电池作电源,在实验室中模拟铝制品表面“钝化”处理的过程(如图乙),阳极电极反应为
【答案】D
【分析】通过电子的移动方向知,左半极为负极,右半极为正极;燃料电池中,负极上投放燃料,燃料在
负极上失电子发生氧化反应;正极上投放氧化剂,氧化剂在正极上得电子发生还原反应,据此分析解题。
【解析】A.根据氢离子的流向可知左侧电极为负极,右侧电极为正极,甲醇燃料电池中,甲醇被氧化作
负极,氧气被还原作正极,所以b口通入CHOH,c口通入O,故A正确;
3 2
B.甲醇被氧化作负极,据图可知负极产生氢离子,根据电子守恒、元素守恒可得电极反应为
CHOH+H O-6e-=CO ↑+6H+,故B正确;
3 2 2
C.精炼铜时,粗铜应在阳极被氧化,所以与甲醇燃料电池的正极相连;阴极上铜离子得电子被还原为铜
单质,电极反应为Cu2++2e-=Cu;电解质溶液应选用铜盐溶液,如CuSO 溶液,故C正确;
4
D.铝失电子生成铝离子,铝离子和碳酸氢根离子发生双水解反应生成氢氧化铝沉淀和二氧化碳,所以溶
液逐渐变浑浊,电极反应式为 ,故D错误;
故选D。
11.A、B、C、D、E是原子序数依次增大的五种短周期元素且B、C元素相邻,D元素原子的最外层电子
数与核外电子层数相等;A元素可以与B、C、E元素分别形成甲、乙、丙三种物质且甲、乙均为10电子
化合物,丙为18电子化合物。已知:甲+E=丙+B ,甲+丙=丁。下列说法一定正确的是
2 2
A.离子半径:E>D>C>B
B.常温下,含D元素的盐溶液pH<7C.丁物质均由非金属元素组成,只含共价键
D.一元弱酸AEC,其结构式为A-C-E
【答案】D
【分析】由题意A元素可以与B、C、E元素分别形成甲、乙、丙三种物质且甲、乙均为10电子化合物,
可推测甲、乙、丙均为氢化物,故A为H,B、C是第二周期的元素,丙为18电子氢化物,故E为Cl,丙
为HCl;又因为甲+E=丙+B ,故甲是NH ,B为N;且B、C元素相邻,故C为O,乙为HO;甲+丙=
2 2 3 2
丁,即NH +HCl=NH Cl;D元素原子的最外层电子数与核外电子层数相等且在氧元素之后,故D位于第
3 4
三周期,为Al。
【解析】A.据分析离子半径排序为:D>E>B>C,故A项错误;
B.含D元素的盐溶液可分为铝盐和偏铝酸盐,常温下,前者的溶液中铝离子水解导致溶液pH<7,后者
的溶液中偏铝酸根水解导致溶液显碱性故pH>7,故B项错误;
C.丁是NH Cl,均右非金属元素组成,但氯化铵中既含有离子键又含有共价键,故C项错误;
4
D.据分析故一元弱酸AEC为HClO,中心原子为氧原子,杂化方式为sp3,有两个孤电子对,故该分子为
直线形分子,其结构为:H-O-Cl,既A-C-E,故D项正确。
故选D。
12.锌是重要的金属材料。以硫化锌精矿(主要含有FeS、CuS等杂质)为原料制备单质锌的工业流程如图所
示,下列说法不正确的是
已知:金属阳离子在阴极的放电顺序和离子浓度有关
A.HO 反应后生成HO
2 2 2
B.烟气主要含 可用钙基固硫法处理
C.电解 溶液时,阴极发生还原反应的是锌离子
D.进一步净化过程可投入铁粉去除Cu
【答案】D
【解析】A.HO 做氧化剂,得电子化合价降低,反应后生成HO,A正确;
2 2 2
B.烟气主要含 可用钙基固硫法处理生成硫酸钙,B正确;C.电解 溶液制取锌,所以阴极发生还原反应的是锌离子,C正确;
D.进一步净化过程投入铁粉会引入新杂质Fe2+,D错误。
故选D。
13.汽车尾气中CO与NO转化的三段反应历程及各物质的相对能量如图所示,其中TS代表过渡态,IM
表示反应过程中的复杂中间产物,每段历程的反应物相对总能量定义为0.下列说法不正确的是
A.反应①决定尾气转化的快慢
B.反应①为吸热反应,反应②、③为放热反应
C.由上图可判断过渡态的相对能量:TS1>TS3>TS2
D.采用对反应③选择性高的催化剂可以避免尾气中出现
【答案】D
【解析】A.由图可知,反应①的活化能最高,为298.4 -42.6 =255.8 ,反应②、③
的活化能分别为108.4 、226.1 ,活化能越高反应速率越慢,慢反应决定整个反应的速
率,故反应①决定尾气转化的快慢,A正确;
B.由图可知,反应①为吸热反应,反应②、③为放热反应,B正确;
C.图中可知三个过渡态的能量分别为298.4 、130.0 、248.3 ,故过渡态的相对
能量:TS1>TS3>TS2,C正确;
D.采用对反应③选择性高的催化剂不代表反应②的产物 会完全消耗,无法避免尾气中不出现 ,
D错误;
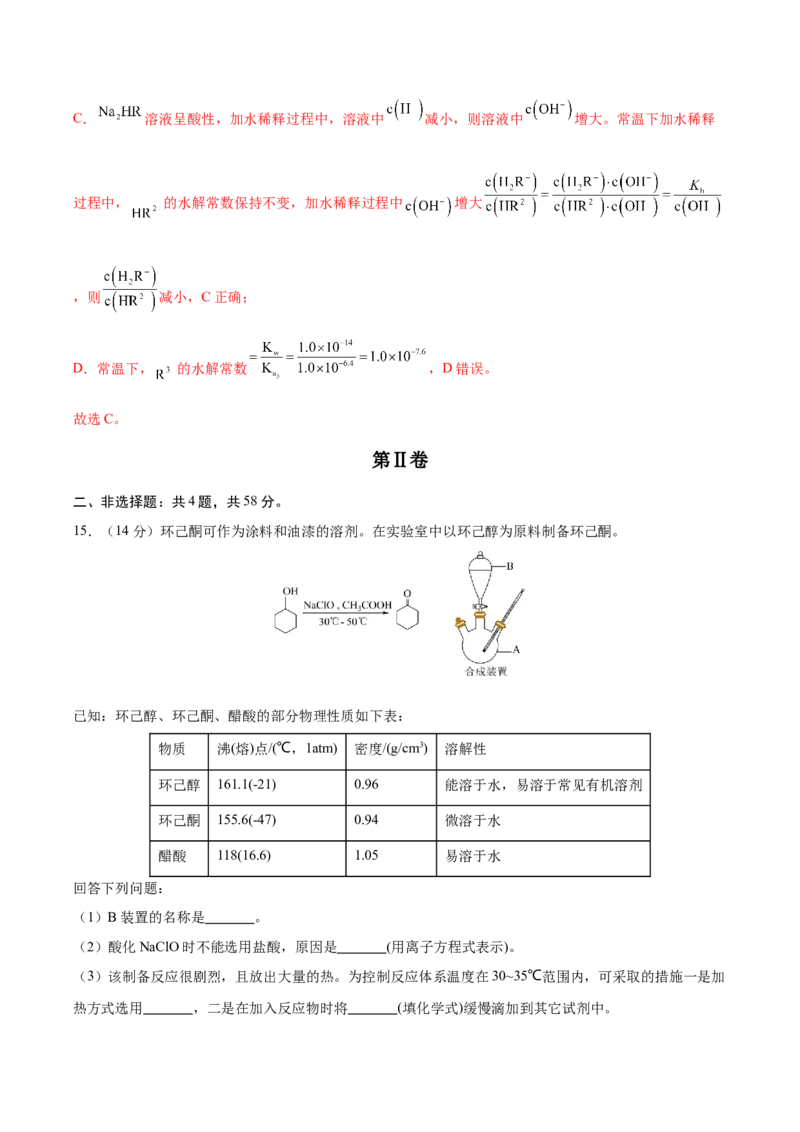
故选D。14.柠檬酸是番茄中最常见的天然酸性物质,其分子结构简式为 (用 表示)。常温
下,用 溶液滴定 溶液的滴定曲线如图所示。已知常温下柠
檬酸的电离常数为: 。下列叙述正确的是
A.a点溶液中,
B.b点溶液中,
C.常温下 溶液加水稀释过程中, 减小
D.常温下 的水解常数为
【答案】C
【解析】A.a点溶液为 溶液,溶液呈酸性,电荷守恒为
,A错误;
B.b点溶液为 溶液,溶液呈酸性, 的电离程度大于 的水解程度,故离子浓度大小为
,B错误;C. 溶液呈酸性,加水稀释过程中,溶液中 减小,则溶液中 增大。常温下加水稀释
过程中, 的水解常数保持不变,加水稀释过程中 增大
,则 减小,C正确;
D.常温下, 的水解常数 ,D错误。
故选C。
第Ⅱ卷
二、非选择题:共4题,共58分。
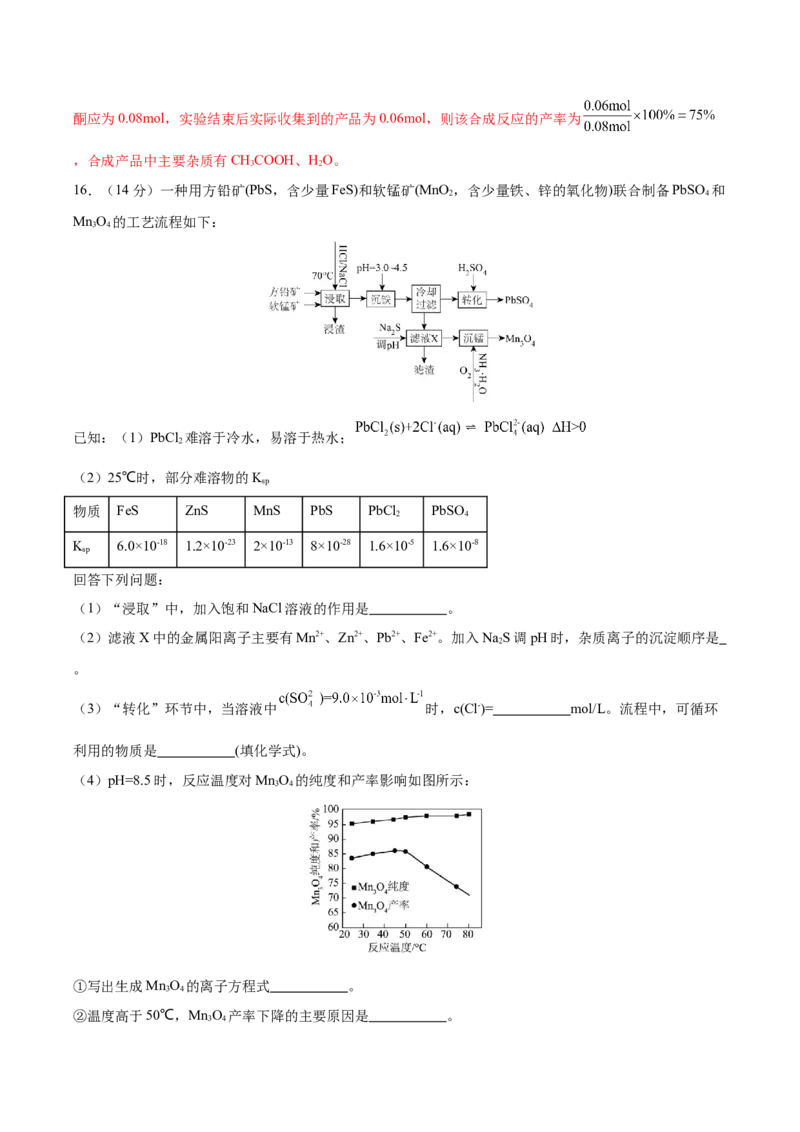
15.(14分)环己酮可作为涂料和油漆的溶剂。在实验室中以环己醇为原料制备环己酮。
已知:环己醇、环己酮、醋酸的部分物理性质如下表:
物质 沸(熔)点/(℃,1atm) 密度/(g/cm3) 溶解性
环己醇 161.1(-21) 0.96 能溶于水,易溶于常见有机溶剂
环己酮 155.6(-47) 0.94 微溶于水
醋酸 118(16.6) 1.05 易溶于水
回答下列问题:
(1)B装置的名称是 。
(2)酸化NaClO时不能选用盐酸,原因是 (用离子方程式表示)。
(3)该制备反应很剧烈,且放出大量的热。为控制反应体系温度在30~35℃范围内,可采取的措施一是加
热方式选用 ,二是在加入反应物时将 (填化学式)缓慢滴加到其它试剂中。(4)制备反应完成后,向混合物中加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮、水和
(填写化学式)的混合物。
(5)环己酮的提纯过程为:
①在馏分中加NaCl固体至饱和,静置,分液;加NaCl的目的是 。
②加入无水MgSO 块状固体;目的是 。
4
③ (填操作名称)后进行蒸馏,收集150~155℃的馏分。
(6)数据处理。反应开始时加入8.4mL(0.08mol)环己醇,20mL冰醋酸和过量的NaClO溶液。实验结束后
收集到产品0.06mol,则该合成反应的产率为 。合成产品中主要杂质有 。
【答案】(1)分液漏斗(1分)
(2) (2分)
(3) 水浴(加热)(1分) NaClO(1分)
(4)CHCOOH(1分)
3
(5) 增大水层的密度,便于分层(2分) 除去有机物中的少量水(或干燥)(1分) 过滤(1分)
(6)75%(2分) CHCOOH、HO(2分)
3 2
【分析】控制反应体系温度在30~35℃范围内,将溶液缓慢滴加到环己醇中反应制备环己酮,制备反应完
成后,向混合物中加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮和水、CHCOOH的混合
3
物,在馏分中加NaCl固体至饱和,静置,分液,在有机层中加入MgSO 块状固体,干燥,过滤后进行蒸
4
馏,收集150~155℃的馏分,得到环己酮。
【解析】(1)由装置图知,B装置的名称是分液漏斗;
(2)盐酸和NaClO能发生氧化还原反应,对应的离子方程式为 ,故酸化
NaClO时不能选用盐酸;
(3)为控制反应体系温度在30~35℃范围内,可采取水浴加热的加热方式,且在加入反应物时将NaClO
缓慢滴加到其它试剂中,避免反应太过剧烈,短时间内放出大量热;
(4)制备反应完成后,向混合物中加入适量水,蒸馏,收集95~100℃的馏分,参考表格中的沸点信息
知,得到主要含环己酮、水和CHCOOH的混合物;
3
(5)提纯环己酮过程中,①在馏分中加NaCl固体至饱和,可增大水层的密度,便于混合液分层而析出环
己酮;②无水MgSO 块状固体是一种干燥剂,加入无水MgSO 块状固体可除去有机物中的少量水;③过
4 4
滤后进行蒸馏,收集150~155℃的馏分,即可得到环己酮;
(6)反应开始时加入了8.4mL(0.08mol)环己醇,20mL冰醋酸和过量的NaClO溶液,则理论上得到的环己酮应为0.08mol,实验结束后实际收集到的产品为0.06mol,则该合成反应的产率为
,合成产品中主要杂质有CHCOOH、HO。
3 2
16.(14分)一种用方铅矿(PbS,含少量FeS)和软锰矿(MnO ,含少量铁、锌的氧化物)联合制备PbSO 和
2 4
MnO 的工艺流程如下:
3 4
已知:(1)PbCl 难溶于冷水,易溶于热水;
2
(2)25℃时,部分难溶物的K
sp
物质 FeS ZnS MnS PbS PbCl PbSO
2 4
K 6.0×10-18 1.2×10-23 2×10-13 8×10-28 1.6×10-5 1.6×10-8
sp
回答下列问题:
(1)“浸取”中,加入饱和NaCl溶液的作用是 。
(2)滤液X中的金属阳离子主要有Mn2+、Zn2+、Pb2+、Fe2+。加入NaS调pH时,杂质离子的沉淀顺序是
2
。
(3)“转化”环节中,当溶液中 时,c(Cl-)= mol/L。流程中,可循环
利用的物质是 (填化学式)。
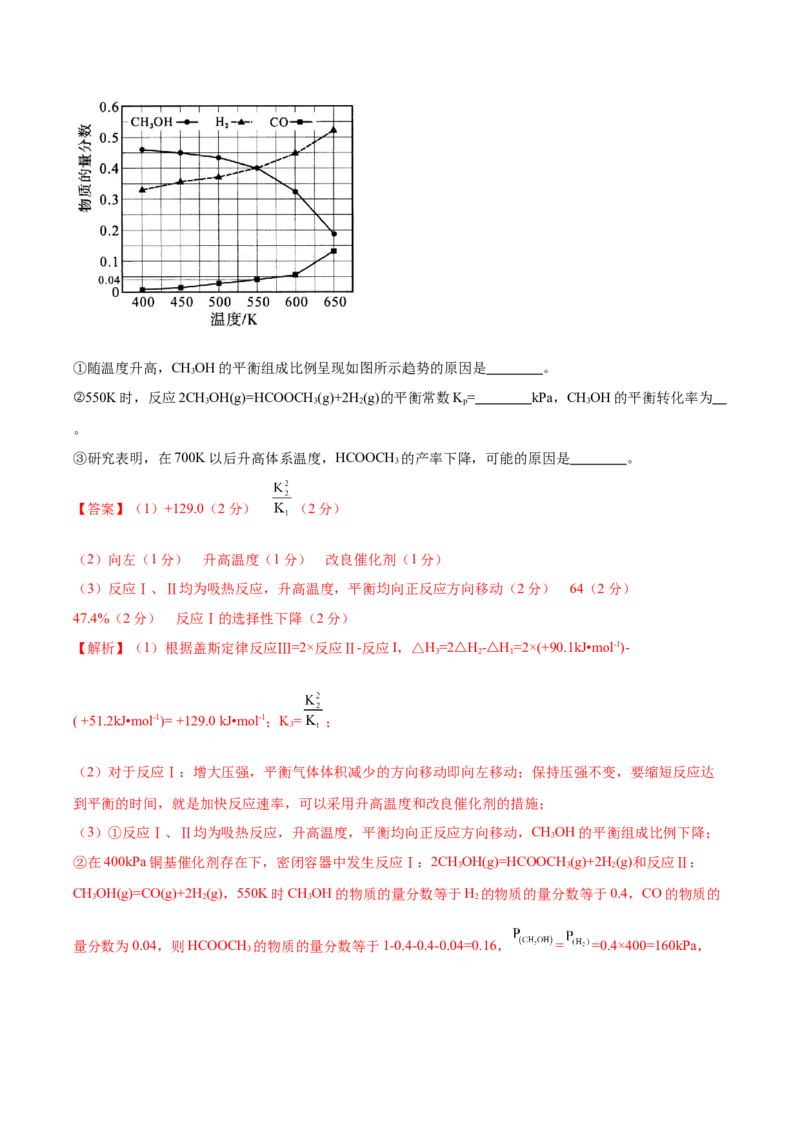
(4)pH=8.5时,反应温度对MnO 的纯度和产率影响如图所示:
3 4
①写出生成MnO 的离子方程式 。
3 4
②温度高于50℃,MnO 产率下降的主要原因是 。
3 4(5)已知中心离子或原子上含有未成对电子的物质均有顺磁性。研究表明,MnO 的结构可表示为如图所
3 4
示,则MnO 的简单氧化物形式可写作 ,MnO (填“有”或“无”)顺磁性。
3 4 3 4
【答案】(1)增大Cl-浓度,促进 正向移动,生成 PbCl ,减少矿物
表面PbCl 的堆积,提高浸出率(2分)
2
(2)Pb2+、Zn2+、Fe2+(3分)
(3)3(1分) HCl(1分)
(4) (2分) 升高温度,氨水挥发、分解,导致
Mn(OH) 的产量减少(2分)
2
(5)2MnO•MnO (2分) 有(1分)
2
【分析】方铅矿主要成分为PbS,含有杂质FeS,软锰矿主要成分为MnO ,还有少量含少量铁、锌的氧化
2
物等,加入盐酸、氯化钠溶液,盐酸、氯化钠、PbS、MnO 反应生成S和PbCl ,FeS被MnO 氧化为S
2 2
和Fe3+;铁、锌的氧化物和盐酸反应生成硫酸铁、硫酸亚铁和硫酸锌;过滤出沉淀S,调节溶液的 pH至
3.0-4.5,使酸浸液中 Fe3+完全生成氢氧化铁沉淀;冷却使PbCl 转化为PbC1 并沉淀,过滤出PbC1 固
2 2
体,PbC1 固体和硫酸溶液反应转化为PbSO 固体;滤液X中的金属阳离子主要有Mn2+、Zn2+、Pb2+、
2 4
Fe2+,加入硫化钠溶液调pH时,根据溶度积可得,Pb2+、Zn2+、Fe2+依次沉淀,过滤除去滤渣,滤液中有氯
化锰,加入氨水并通通入氧气,得到产品 MnO。
3 4
【解析】(1)根据分析及题目信息,PbCl 难溶于冷水,易溶于热水,且存在平衡
2
,则“浸取”中,加入饱和NaCl溶液的作用是:增大Cl-浓度,促
进 正向移动,生成 PbCl ,减少矿物表面PbCl 的堆积,提高浸出
2
率。
(2)根据分析及题目中25℃时,部分难溶物的K ,加入硫化钠溶液调pH时, Pb2+、Zn2+、Fe2+依次沉
sp
淀,生成对应硫化物。(3)“转化”环节中,发生反应PbC1 (s)+ (aq) PbSO (s)+2Cl-(aq),当溶液中
2 4
时, ,则c(Cl-)= =3 。“转化”环节
中,生成了HCl,根据流程及分析,HCl可循环利用。
(4)①氯化锰、氨水、氧气反应生成MnO、氯化铵、水,反应方程式为
3 4
,离子方程式为
。
②根据pH=8.5时,反应温度对MnO 的纯度和产率影响图像可得,温度高于50℃,MnO 产率下降,其
3 4 3 4
主要原因是升高温度,氨水挥发、分解,导致Mn(OH) 的产量减少。
2
(5)根据MnO 的结构图可得,MnO 的简单氧化物形式可写作2MnO•MnO ;中心离子或原子上含有未
3 4 3 4 2
成对电子的物质均有顺磁性,锰原子的价层电子排布为3d54s2,含有未成对电子,故MnO 有顺磁性。
3 4
17.(15分)甲酸甲酯(HCOOCH )是一种重要的有机合成中间体,可通过甲醇催化脱氢法制备,其工艺过
3
程包含以下反应:
反应Ⅰ:2CHOH(g)=HCOOCH (g)+2H(g) K, H=+51.2kJ•mol-1
3 3 2 1 1
反应Ⅱ:CHOH(g)=CO(g)+2H (g) K, H=+90.△1kJ•mol-1
3 2 2 2
回答下列问题: △
(1)反应HCOOCH (g)=2CO(g)+2H(g)的 H= kJ•mol-1,K= (用K、K 表示)。
3 2 3 3 1 2
(2)对于反应Ⅰ:增大压强,平衡 △ 移动(填“向左”“向右”或“不”)。保持压强不变,要缩短
反应达到平衡的时间,可采取的措施是 、 。
(3)在400kPa、铜基催化剂存在下,向密闭容器中通入CHOH进行Ⅰ、Ⅱ两个反应。体系中气体平衡组
3
成比例(物质的量分数)随温度变化的理论计算结果如图所示。①随温度升高,CHOH的平衡组成比例呈现如图所示趋势的原因是 。
3
②550K时,反应2CHOH(g)=HCOOCH (g)+2H(g)的平衡常数K= kPa,CHOH的平衡转化率为
3 3 2 p 3
。
③研究表明,在700K以后升高体系温度,HCOOCH 的产率下降,可能的原因是 。
3
【答案】(1)+129.0(2分) (2分)
(2)向左(1分) 升高温度(1分) 改良催化剂(1分)
(3)反应Ⅰ、Ⅱ均为吸热反应,升高温度,平衡均向正反应方向移动(2分) 64(2分)
47.4%(2分) 反应Ⅰ的选择性下降(2分)
【解析】(1)根据盖斯定律反应Ⅲ=2×反应Ⅱ-反应I,△H=2△H -△H=2×(+90.1kJ•mol-1)-
3 2 1
( +51.2kJ•mol-1)= +129.0 kJ•mol-1;K= ;
3
(2)对于反应Ⅰ:增大压强,平衡气体体积减少的方向移动即向左移动;保持压强不变,要缩短反应达
到平衡的时间,就是加快反应速率,可以采用升高温度和改良催化剂的措施;
(3)①反应Ⅰ、Ⅱ均为吸热反应,升高温度,平衡均向正反应方向移动,CHOH的平衡组成比例下降;
3
②在400kPa铜基催化剂存在下,密闭容器中发生反应Ⅰ:2CHOH(g)=HCOOCH (g)+2H(g)和反应Ⅱ:
3 3 2
CHOH(g)=CO(g)+2H (g),550K时CHOH的物质的量分数等于H 的物质的量分数等于0.4,CO的物质的
3 2 3 2
量分数为0.04,则HCOOCH 的物质的量分数等于1-0.4-0.4-0.04=0.16, = =0.4×400=160kPa,
3P =0.04×400=16 kPa, =0.16×400=64 kPa,K= = ;根据碳原子守
(CO) p
恒,CHOH的平衡转化率= ;在700K以后升高体系温度,HCOOCH 的
3 3
产率下降,可能的原因是反应Ⅰ的选择性下降。
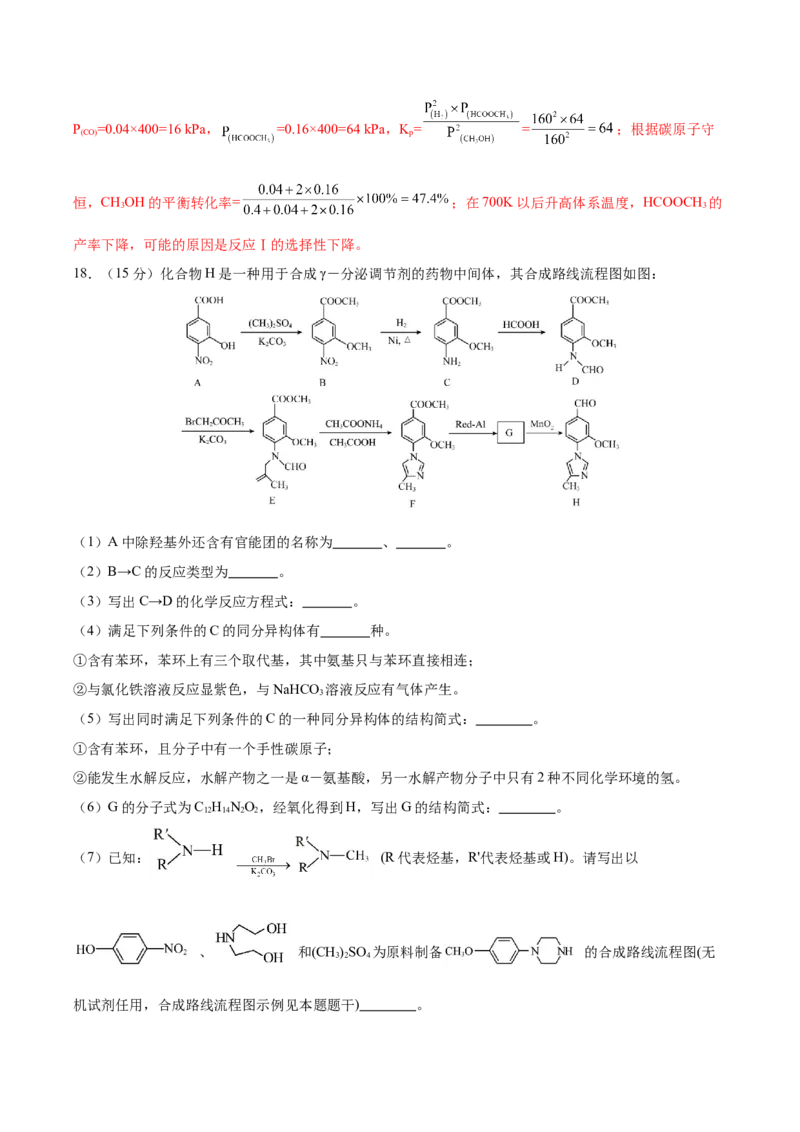
18.(15分)化合物H是一种用于合成γ-分泌调节剂的药物中间体,其合成路线流程图如图:
(1)A中除羟基外还含有官能团的名称为 、 。
(2)B→C的反应类型为 。
(3)写出C→D的化学反应方程式: 。
(4)满足下列条件的C的同分异构体有 种。
①含有苯环,苯环上有三个取代基,其中氨基只与苯环直接相连;
②与氯化铁溶液反应显紫色,与NaHCO 溶液反应有气体产生。
3
(5)写出同时满足下列条件的C的一种同分异构体的结构简式: 。
①含有苯环,且分子中有一个手性碳原子;
②能发生水解反应,水解产物之一是α-氨基酸,另一水解产物分子中只有2种不同化学环境的氢。
(6)G的分子式为C H NO,经氧化得到H,写出G的结构简式: 。
12 14 2 2
(7)已知: (R代表烃基,R'代表烃基或H)。请写出以
、 和(CH)SO 为原料制备 的合成路线流程图(无
3 2 4
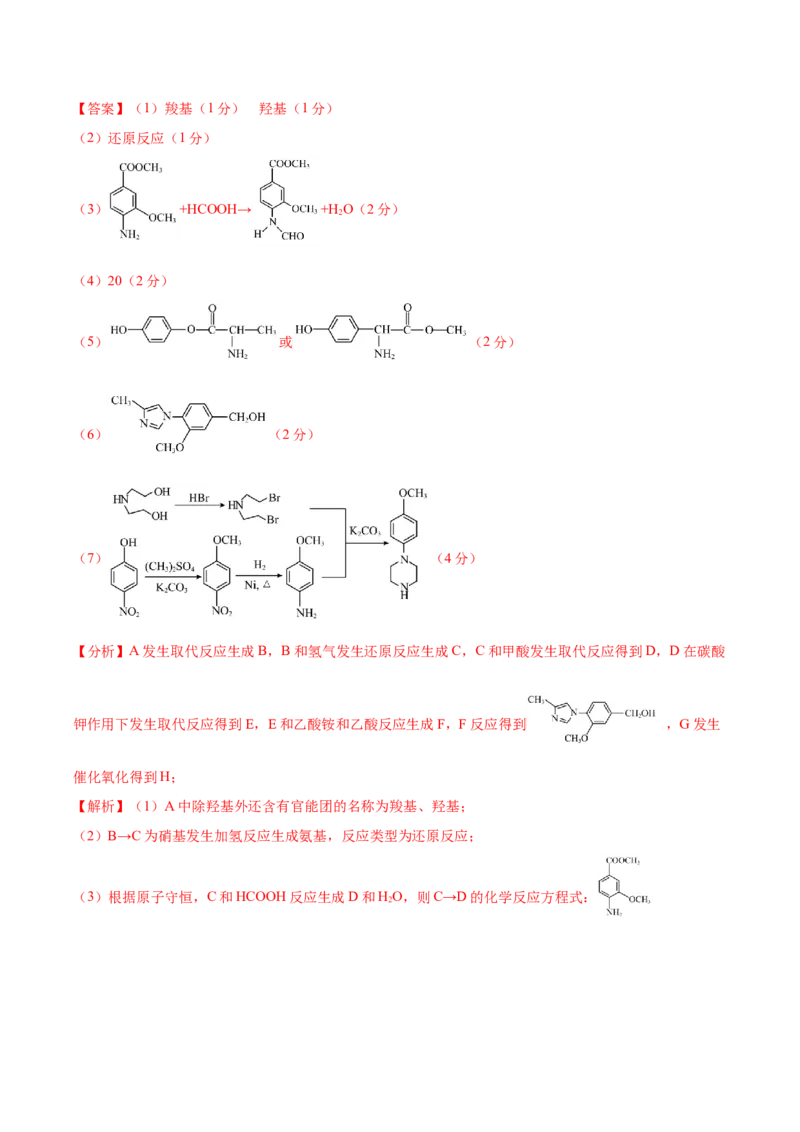
机试剂任用,合成路线流程图示例见本题题干) 。【答案】(1)羧基(1分) 羟基(1分)
(2)还原反应(1分)
(3) +HCOOH→ +H O(2分)
2
(4)20(2分)
(5) 或 (2分)
(6) (2分)
(7) (4分)
【分析】A发生取代反应生成B,B和氢气发生还原反应生成C,C和甲酸发生取代反应得到D,D在碳酸
钾作用下发生取代反应得到E,E和乙酸铵和乙酸反应生成F,F反应得到 ,G发生
催化氧化得到H;
【解析】(1)A中除羟基外还含有官能团的名称为羧基、羟基;
(2)B→C为硝基发生加氢反应生成氨基,反应类型为还原反应;
(3)根据原子守恒,C和HCOOH反应生成D和HO,则C→D的化学反应方程式:
2+HCOOH→ +H O;
2
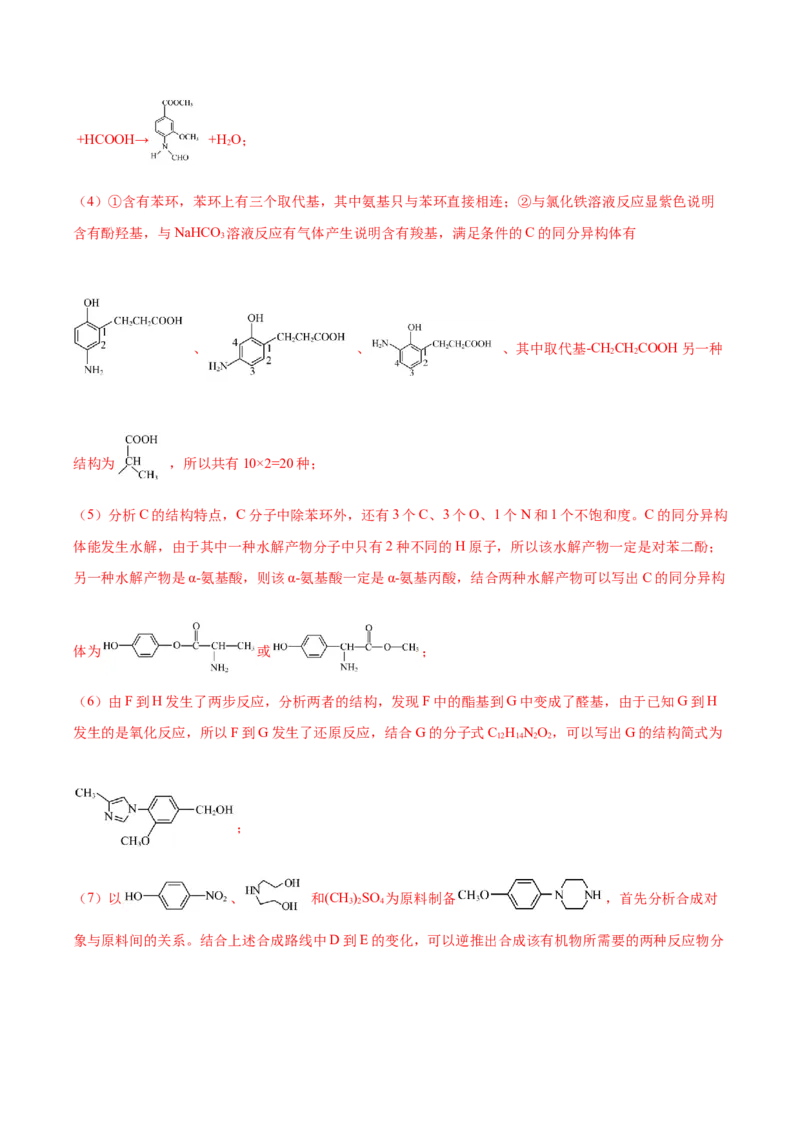
(4)①含有苯环,苯环上有三个取代基,其中氨基只与苯环直接相连;②与氯化铁溶液反应显紫色说明
含有酚羟基,与NaHCO 溶液反应有气体产生说明含有羧基,满足条件的C的同分异构体有
3
、 、 、其中取代基-CHCHCOOH另一种
2 2
结构为 ,所以共有10×2=20种;
(5)分析C的结构特点,C分子中除苯环外,还有3个C、3个O、1个N和1个不饱和度。C的同分异构
体能发生水解,由于其中一种水解产物分子中只有2种不同的H原子,所以该水解产物一定是对苯二酚;
另一种水解产物是α-氨基酸,则该α-氨基酸一定是α-氨基丙酸,结合两种水解产物可以写出C的同分异构
体为 或 ;
(6)由F到H发生了两步反应,分析两者的结构,发现F中的酯基到G中变成了醛基,由于已知G到H
发生的是氧化反应,所以F到G发生了还原反应,结合G的分子式C H NO,可以写出G的结构简式为
12 14 2 2
;
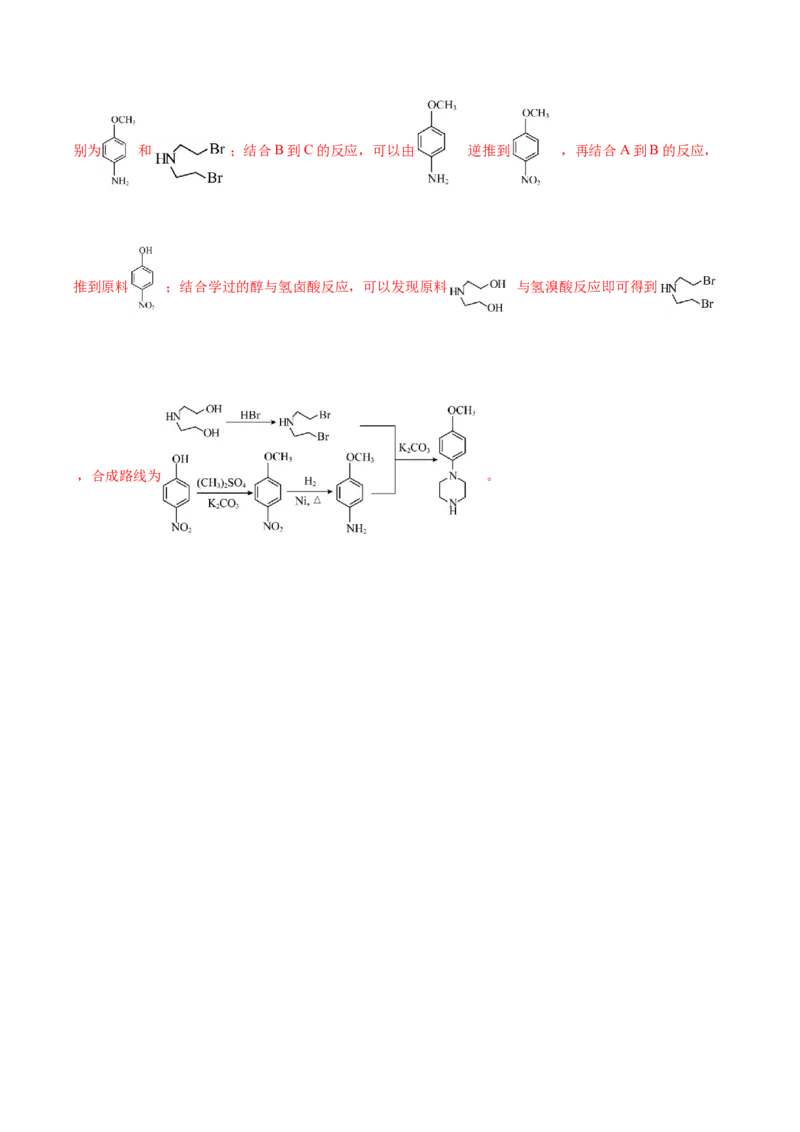
(7)以 、 和(CH)SO 为原料制备 ,首先分析合成对
3 2 4
象与原料间的关系。结合上述合成路线中D到E的变化,可以逆推出合成该有机物所需要的两种反应物分别为 和 ;结合B到C的反应,可以由 逆推到 ,再结合A到B的反应,
推到原料 ;结合学过的醇与氢卤酸反应,可以发现原料 与氢溴酸反应即可得到
,合成路线为 。