文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(湖南专用)
黄金卷07
(考试时间:75分钟;试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 O-16 Ni-59
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.化学与生产、生活和科技都密切相关。下列有关说法错误的是
A.“司南之勺,投之于地,其柢(勺柄)指南”中“司南之勺”的主要成分为
B.“用胶泥刻字 烧令坚”所描写的印刷术陶瓷活字属于传统无机非金属材料
C.活性炭具有除异味和杀菌作用
D.垃圾分类有多种方法,废纸、玻璃属于可回收垃圾,废电池、废药品属于有害垃圾
【答案】C
【详解】A.司南之勺具有磁性,主要成分为 ,A正确;
B.印刷术陶瓷属于硅酸盐材料,为传统无机非金属材料,B正确;
C.活性炭具有除异味作用,但不可杀菌,C错误;
D.活性炭具有除异味和杀菌作用,D正确。 故选C。
2.芹䒮中的活性物质—芩黄素具有抗肿瘤、抗病毒的功能,其分子的结构简式如图所示。下列有关芩黄
素的说法错误的是
A.能发生加聚反应,但不能与甲醛发生缩聚反应
B.含有四种官能团,与 溶液作用显紫色
C.分子中碳原子的杂化方式均相同
D.苯环上的一氯代物有四种
【答案】A
【详解】A.碳碳双键能发生加聚反应,苯环上与酚羟基相邻的位置上有氢原子(其中有1个酚羟基的对位
上也有氢原子),能与甲醛发生缩聚反应,A错误;B.该物质中含有羟基、醚键、酮羰基、碳碳双键四种官能团,其中的酚羟基能与 溶液作用显紫色,
B正确;
C.分子中碳原子的杂化方式均为 ,C正确;
D.苯环上的一氯代物 六个位置,3,5等效,4,6等效,所以共有四种,
D正确;故答案为:A。
3.下列实验操作规范且能达到相应实验目的的是
选项 实验目的 实验操作
A 测定饱和氯水的 用玻璃棒蘸取待测溶液点在 试纸上
B 制备 向 溶液中加入足量的浓氨水,过滤
C 配制 溶液 将 固体溶于蒸馏水,再滴加硫酸直至溶液澄清
除去乙酸乙酯中的乙
D 加入乙醇、浓硫酸,加热
酸
A.A B.B C.C D.D
【答案】B
【详解】A.氯水具有强氧化性,不能用 试纸测定其pH,A错误;
B.氨水不能溶解氢氧化铝,向 溶液中加入足量的浓氨水,过滤即可制备氢氧化铝,B正确;
C.为防止铁离子水解,配制 溶液时将 固体溶于盐酸中,然后再稀释,C错误;
D.除去乙酸乙酯中的乙酸,应该加入饱和碳酸钠溶液,然后分液,D错误;
答案选B。
4.下列化学用语表示正确的是
A.溴的简化电子排布式:B.1-丁醇的键线式:
C. 形成的 键模型:
D.水的VSEPR模型:
【答案】D
【详解】A.溴位于周期表中第4周期第ⅤⅡA族,核外电子数35,电子排布式为 ,选项
A错误;
B.1-丁醇的键线式为 ,而 为1-丙醇,选项B错误;
C. 形成的 键模型: ,选项C错误;
D.HO中价层电子对个数=2+ =4,且含有2个孤电子对,所以HO的VSEPR模型为四面体
2 2
,选项D正确;答案选D。
5.周期表中ⅤA族元素及其化合物作用广泛。氨是重要的化工原料;肼( )的燃烧热为 ,
是常用的火箭燃料;由磷酸钙、石英砂和碳粉在电弧炉中熔烧可生成白磷( )和CO;在一定条件下白磷可
转化为黑鳞;在700~900℃条件下, 与 可制得半导体材料砷化镓晶体;铋酸钠( )不
溶于冷水,在酸性条件下与 反应生成 、 ,在钢铁工业中可用于锰元素的分析测定。下
列化学反应表示正确的是
A.肼的燃烧热的热化学方程式: kJ⋅mol
B.制单质磷:C.制砷化镓晶体:
D.铋酸钠氧化 ;
【答案】D
【详解】A.燃烧热是指1mol纯物质在氧气中完全燃烧生成稳定的氧化物所放出的热量,肼的燃烧热的热
化学方程式应为 kJ⋅mol ,A错误;
B.由磷酸钙、石英砂和碳粉在电弧炉中熔烧可生成白磷( )和CO,则制单质磷的反应方程式应为
,B错误;
C.在700~900℃条件下, 与 可制得半导体材料砷化镓晶体,则制砷化镓晶体的方程式应
为 ,C错误;
D.铋酸钠( )不溶于冷水,在酸性条件下与 反应生成 、 ,则铋酸钠氧化 的
离子方程式为 ,D正确; 故选D。
6. (赤血盐)、 (黄血盐)是常用于 、 的实验室检验试剂。一定条件下,可发
生如下两个反应:
① ,固态混合,释放 ;
② ,溶液混合,消耗 。
下列有关说法错误的是
A. 检验: (蓝色)B. 含有离子键、极性键、配位键
C. 氧化性强于
D.两个反应方向不一致,原因可能是溶液中 与 的配位能力强于
【答案】C
【详解】A. 检验: (蓝色),故A正确;
B.配合物 含有离子键、极性键、配位键,故B正确;
C.根据反应 可知, 氧化性强于 ,故C错误;
D.两个反应方向不一致,原因可能是溶液中 与 的配位能力强于 ,故D正确;
答案选C。
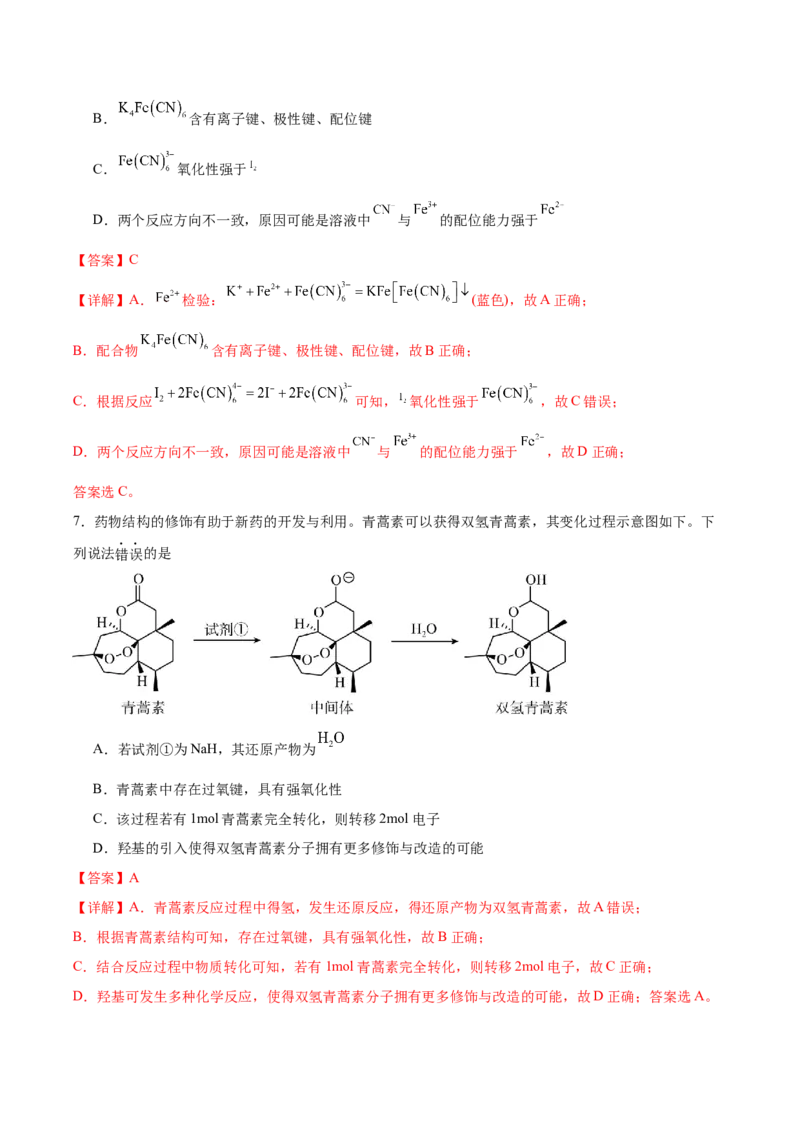
7.药物结构的修饰有助于新药的开发与利用。青蒿素可以获得双氢青蒿素,其变化过程示意图如下。下
列说法错误的是
A.若试剂①为NaH,其还原产物为
B.青蒿素中存在过氧键,具有强氧化性
C.该过程若有1mol青蒿素完全转化,则转移2mol电子
D.羟基的引入使得双氢青蒿素分子拥有更多修饰与改造的可能
【答案】A
【详解】A.青蒿素反应过程中得氢,发生还原反应,得还原产物为双氢青蒿素,故A错误;
B.根据青蒿素结构可知,存在过氧键,具有强氧化性,故B正确;
C.结合反应过程中物质转化可知,若有1mol青蒿素完全转化,则转移2mol电子,故C正确;
D.羟基可发生多种化学反应,使得双氢青蒿素分子拥有更多修饰与改造的可能,故D正确;答案选A。8.在硫酸铜溶液中加入过量浓氨水,可形成[Cu(NH ) (H O) ]2+。下列有关说法错误的是
3 4 2 2
A.配离子中两种配体的中心原子杂化方式和VSEPR模型均相同
B.基态原子第一电离能:N>O>S
C.键角:BF>H O>NH
3 2 3
D.配离子[Cu(NH ) (H O) ]2+的空间结构是八面体形
3 4 2 2
【答案】C
【详解】A.两种配体即分别为HO和NH 中,中心原子的价层电子对数分别为:2+ =4,3+
2 3
=4,杂化方式均为sp3杂化,VSEPR模型均为四面体形,A正确;
B.同主族元素,从上到下,第一电离能减小,故第一电离能O>S;同周期元素,从左到右,第一电离能
呈增大趋势,但N原子2p轨道处于半满状态,更稳定,故第一电离能N>O,所以基态原子第一电离能:
N>O>S,B正确;
C.BF、HO、NH 中心原子的价层电子对数分别为:3+ =3,2+ =4,3+ =4,它们分别
3 2 3
是sp2杂化、sp3杂化、sp3杂化,所以BF 键角最大,为120°; HO中O原子有两对孤电子对,NH 只有1
3 2 3
对孤电子对,根据孤电子对-孤电子对排斥力>孤电子对-成键电子对排斥力>成键电子对-成键电子对排斥力,
所以键角NH > H O;故键角:BF> NH > H O,C错误;
3 2 3 3 2
D.配离子[Cu(NH ) (H O) ]2+的配位数为4+2=6,空间结构是八面体形,D正确;故答案为:C。
3 4 2 2
9.工业上可用克劳斯工艺处理含HS的尾气获得硫黄,工艺流程如下.
2
已知反应炉中部分 发生反应: 。下列说法错误的是
A.可用品红溶液检验排放的气体中是否含有二氧化硫
B.每回收 单质硫,理论上消耗氧气的体积为 (标准状况)
C.催化转化器中发生的反应为
D.为提高 转化为S的比例,理论上应控制反应炉中 的转化率约为
【答案】B【分析】由题干已知信息可知,反应炉中部分HS发生反应: ,催化转化器中发
2
生反应为: ,生成的硫蒸气经硫冷凝器可将硫冷凝下来,变为固体和气体分离,据
此分析解题。
【详解】A.利用SO 可使品红溶液褪色的特性,故可用品红溶液检验排放的气体中是否含有二氧化硫,A
2
正确;
B.每回收 单质硫的物质的量为: =1mol,根据分析可知,生成1molS需SO 的物质的量为
2
mol,生成 molSO 需要O 的物质的量为:0.5mol,故理论上消耗氧气的体积为0.5mol×22.4L/
2 2
mol=11.2L,B错误;
C.由分析可知,催化转化器中发生的反应为 ,C正确;
D.根据反应方程式 、 可知,为提高 转化为S的比例,
理论上应控制反应炉中 的转化率约为 ,D正确;故答案为:B。
10.研究微生物燃料电池不仅可以获得高效能源,还能对工业污水等进行处理。利用微生物燃料电池处理
含硫废水并电解制备KIO 的原理如图所示,下列说法正确的是
3
A.光照强度大小不影响KIO 的制备速率
3
B.右侧电池中K+通过阳离子交换膜从P极移向Q极C.电极N处发生电极反应:S-6e-+4H O= +8H+
2
D.不考虑损耗,电路中每消耗1 molO,理论上Q极可制得342.4 g KIO
2 3
【答案】C
【分析】石墨电极M处,CO 在光合菌、光照条件下转化为O,O 在M极放电生成HO,发生还原反应,
2 2 2 2
M为正极,正极电极反应式为O+4e-+4H+=2H O,N极为负极,硫氧化菌将FeS 氧化为S,硫再放电生成
2 2 x
,负极电极反应式为S-6e-+4H O= +8H+,H+通过质子交换膜由右室移向左室;铂电极P为阴极,
2
铂电极Q为阳极,阴极反应式为2HO+2e-=H ↑+2OH-,阳极反应式为I+12OH--10e-=2IO +6H O,阴极生
2 2 2 2
成氢氧根离子,而阳极生成的IO 比消耗的OH-少,溶液中K+通过阳离子交换膜从Q极移向P极。
【详解】A.光照强度大小影响单位时间内生成氧气的量,即影响电流强度,会影响KIO 的制备速率,故
3
A错误;
B.铂电极P为阴极,铂电极Q为阳极,阴极生成氢氧根离子,而阳极生成的IO 比消耗的OH-少,溶液中
K+通过阳离子交换膜从Q极移向P极,故B错误;
C.N极为负极,硫氧化菌将FeS 氧化为S,硫再放电生成 ,负极电极反应式为S-6e-+4H O=
x 2
+8H+,故C正确;
D.不考虑损耗,电路中每消耗1molO ,转移电子为4mol,阳极反应式为I+12OH--10e-=2IO +6H O,可
2 2 2
知生成KIO 为4mol× =0.8mol,理论上Q极可制得KIO 的质量为0.8mol×214g/mol=171.2g,故D错误;
3 3
故选:C。
11.一种分解氯化铵实现产物分离的物质转化关系如下,其中 代表 或 中的一种。下
列说法正确的是A.a、c分别是
B. 既可以是 ,也可以是
C.已知 为副产物,则通入水蒸气可减少 的产生
D.等压条件下,反应①、②的反应热之和,小于氯化铵直接分解的反应热
【答案】C
【分析】 分解的产物是 和 ,分解得到的 与 反应生成 , 又可
以分解得到 和 ,则a为 ,b为 ,c为 ,d为 。
【详解】A.由分析可知,a为 ,c为 ,A项错误;
B.d为 ,B错误;
C.可以水解生成 ,通入水蒸气可以减少 的生成,C正确;
D.反应①和反应②相加即为氯化铵直接分解的反应,由盖斯定律可知,等压条件下,反应①、反应②的反应热之和等于氯化铵直接分解的反应热,D错误;故选C。
12.一定条件下,丙烯与HCl反应生成 和 的反应历程如图所示。下列说法正
确的是
A.丙烯与HCl的反应是吸热反应
B.合成 的反应中,第Ⅱ步为反应的决速步
C.其他条件不变,适当升高温度可以提高加成产物中 的比例
D. 的焓变等于第一步与第二步正反应活化能的差
值
【答案】C
【详解】A.由图可知,无论是生成 氯丙烷还是生成 氯丙烷,反应物的总能量总是高于生成物的总
能量,则丙烯与HCl的反应是放热反应,A错误;
B.在合成 氯丙烷的反应中,第Ⅰ步反应的活化能更大,即第Ⅰ步的反应速率慢,故第Ⅰ步为反应的决
速步,B错误;
C.由图可知: ,升高温度,平衡正向移动,故其他条件不变,
适当升高温度可以提高加成产物中 的比例,C正确;
D.由图像可知,第一步与第二步正反应活化能的差值不是反应物和生成物的能量差,即该差值不是反应
的焓变,D错误;故选C。
13.25℃时,某小组做如下两组实验:实验Ⅰ:分别往浓度均为 、 溶液中通入 至 ;
实验Ⅱ:在1.0L、 溶液中加入 固体,充分反应。
[已知:25℃, 的电离常数 、 ; 、
。混合后溶液体积变化忽略不计]。下列说法不正确的是
A. 、 溶液中水的电离程度:
B.实验Ⅰ结束后, 、 溶液中均有
C.实验Ⅱ的转化存在平衡常数:
D.实验Ⅱ中,改用饱和 溶液, 的平衡转化率减小
【答案】D
【详解】A.碳酸根的第一步水解程度远远大于第二步水解程度,所以 、 溶液中
水解程度 ,水的电离程度 ,A正确;
B.单一的NaHCO 溶液呈弱碱性,需要通入少量的二氧化碳才能呈中性,此时溶液中以 离子为主,
3
还有少量的碳酸根离子和碳酸分子,B正确;
C.实验Ⅱ发生反应: ,平衡常数K= =
= ,C正确;
D.该反应: 可看作气体平衡反应中的等体积类型,增大 溶液浓度,等同于等体积气体反应中的增大压强,平衡不移动, 转化率不变,D错
误;
故选D。
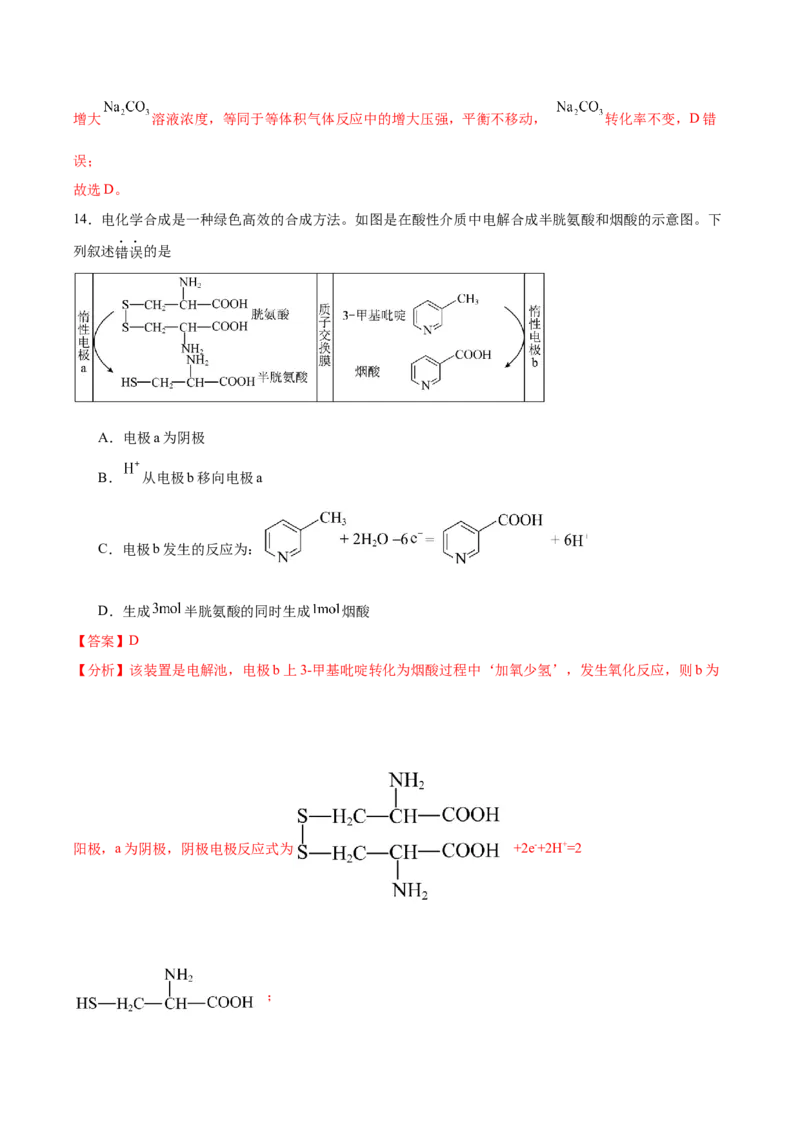
14.电化学合成是一种绿色高效的合成方法。如图是在酸性介质中电解合成半胱氨酸和烟酸的示意图。下
列叙述错误的是
A.电极a为阴极
B. 从电极b移向电极a
C.电极b发生的反应为:
D.生成 半胱氨酸的同时生成 烟酸
【答案】D
【分析】该装置是电解池,电极b上3-甲基吡啶转化为烟酸过程中‘加氧少氢’,发生氧化反应,则b为
阳极,a为阴极,阴极电极反应式为 +2e-+2H+=2
;【详解】A.a极上硫元素化合价升高,a为阴极,A正确;
B.电解池中阳离子移向阴极,则H+移向a电极,B正确;
C.电极b上3-甲基吡啶转化为烟酸过程中发生氧化反应,在酸性介质中电极反应式为:
,C正确;
D.根据电子守恒可得关系式: ~6e-~6 ,
因此生成6mol半胱氨酸的同时生成 烟酸,D错误;
故选:D。
二、非选择题:本题共4小题,共58分。
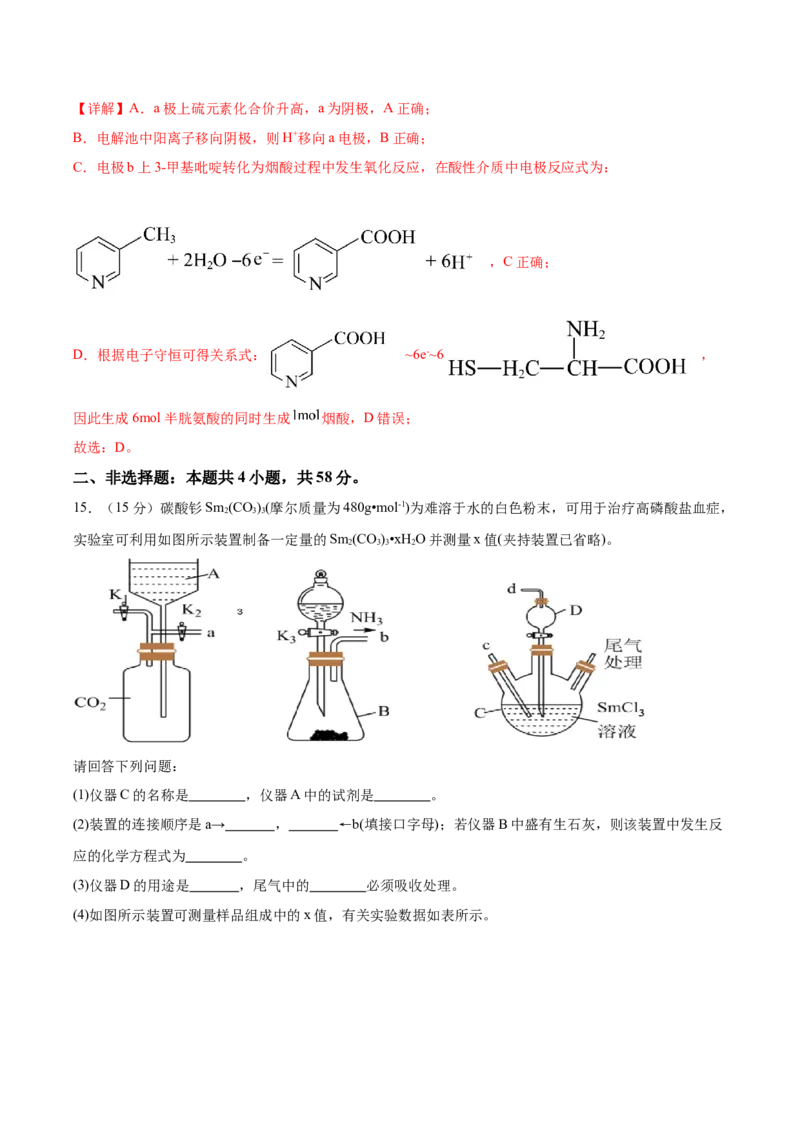
15.(15分)碳酸钐Sm (CO)(摩尔质量为480g•mol-1)为难溶于水的白色粉末,可用于治疗高磷酸盐血症,
2 3 3
实验室可利用如图所示装置制备一定量的Sm (CO)•xH O并测量x值(夹持装置已省略)。
2 3 3 2
请回答下列问题:
(1)仪器C的名称是 ,仪器A中的试剂是 。
(2)装置的连接顺序是a→ , ←b(填接口字母);若仪器B中盛有生石灰,则该装置中发生反
应的化学方程式为 。
(3)仪器D的用途是 ,尾气中的 必须吸收处理。
(4)如图所示装置可测量样品组成中的x值,有关实验数据如表所示。装置 E G
实验前仪器与试剂总质量\g m m
1 3
实验后仪器与试剂总质量\g m m
2 4
①加热前后均要通入一段时间的N。加热前通入N 的操作是 ,装置H的作用是 。
2 2
②x= (用含m、m、m、m 的代数式表示)。
1 2 3 4
【答案】(1) 三颈烧瓶 (1分) 饱和碳酸氢钠溶液(1分)
(2) c (1分) d (1分) (2分)
(3)防止NH 溶解产生倒吸现象 (2分) NH (1分)
3 3
(4)打开K、K 和K,缓缓通入一段时间的N (2分) 防止空气中CO、HO进入装置G中干扰实验
4 5 6 2 2 2
(2分) (2分)
【分析】装置A中产生 和装置B中产生的 ,通入装置C中,与 溶液反应生成
晶体;
【详解】(1)仪器C的名称是三颈烧瓶,将仪器A中溶液滴入集气瓶中将 出,因此 不能溶解在
相应的溶液中,也不能与相应溶液反应,故仪器A中的试剂应是饱和 溶液;
(2)由于氨气极易溶于水,需要设置防倒吸装置,故氨气从d口进入,故装置的连接顺序是 ,
;在题给制气装置中,制备 的试剂是CaO、浓氨水,反应的化学方程式为;
(3) 极易溶于水,仪器D的用途是防止倒吸,尾气中 有毒,因此 必须用相应的试剂吸收处
理;
(4)①加热时 分解为水、 、 ,水用浓硫酸吸收, 用碱石灰吸收。加热
前通入 的操作是打开 和 ,再缓缓通入 ,H装置的作用是防止空气中二氧化碳、水干扰实
验;
②由表中数据知, ,E中固体质量减少了 ,此值与生成的 、 质
量和相等,故 , 分解的化学方程
式为 ,故有 ,解得
。
16.(14分)研究含氮元素物质的反应对生产、生活、科研等方面具有重要的意义。
(1)NO 的排放主要来自于汽车尾气,包含NO 和NO,有人提出用活性炭对NO 进行吸收,发生如下反应:
x 2 x
C(s)+2NO(g) N(g)+CO (g) △H=﹣34.0kJ/mol。对于反应T℃时,借助传感器测得反应在不同时间点上
2 2 1
各物质的浓度如下:
0 10 20 30 40 50
NO 1.00 0.58 0.40 0.40 0.48 0.48
N 0 0.21 0.30 0.30 0.36 0.36
2
①0~10min内,NO的平均反应速率v(NO)= ,当升高反应温度,该反应的平衡常数K
(选填“增大”、“减小“或“不变”)。
②30min后。只改变某一条件,反应重新达到平衡;根据上表中的数据判断改变的条件可能是(填字母)。
a.加入一定量的活性炭 b.通入一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂。
(2)科研人员发现碘蒸气存在能大幅度提高NO的分解速率,反应历程为
2
第一步:I(g)→2I(g)(快反应)
2
第二步:I(g)+NO(g)→N (g)+IO(g)(慢反应)
2 2
第三步:2IO(g)+2N O(g)→2N (g)+2O(g)+I (g)(快反应)
2 2 2 2
实验表明,含碘时NO分解速率方程v=k•c(NO)•[(I )]0.5(k为速率常数),下列表述正确的是 (填
2 2 2
字母)。
A.I(g)是反应的催化剂,I(g)浓度增大,NO分解反应速率增大
2 2 2
B.第二步是整个反应的决速步骤
C.I(g)能降低反应的焓变,从而化学反应速率增大
2
(3)工业生产硝酸的核心反应之一是在恒压装置中将NO转化为NO :
2
反应Ⅰ.NO(g)+ O(g) NO (g) △H
2 2
目前认为反应Ⅰ分两步进行:
反应Ⅱ.2NO(g) NO(g) △H<0(快速平衡)
2 2
反应Ⅲ.NO(g)+O(g) 2NO (g)
2 2 2 2
反应Ⅲ的速率方程为v=k•p(N O)•p(O )
2 2 2
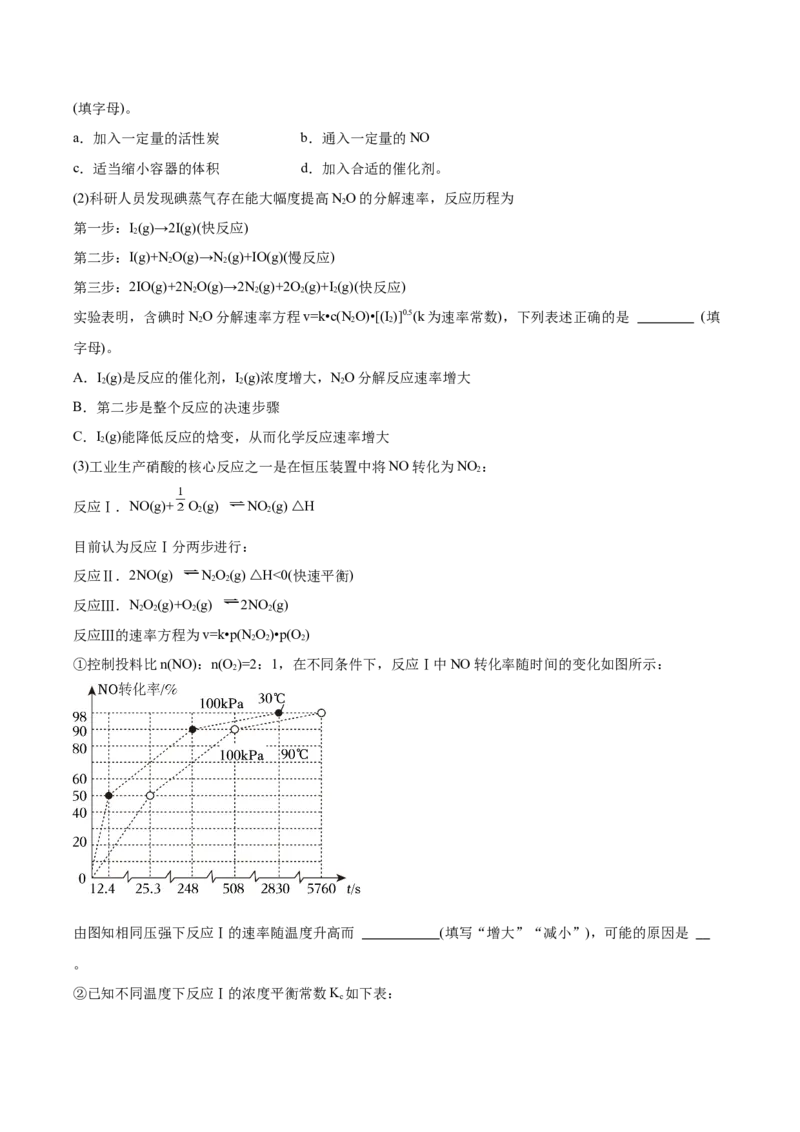
①控制投料比n(NO):n(O )=2:1,在不同条件下,反应Ⅰ中NO转化率随时间的变化如图所示:
2
由图知相同压强下反应Ⅰ的速率随温度升高而 (填写“增大”“减小”),可能的原因是
。
②已知不同温度下反应Ⅰ的浓度平衡常数K 如下表:
c温度/℃ 27 77 127 177 227 500
平衡常数K 1.1×106 1.3×104 3.7×103 5.61×102 1.2×102 1.0
c
NO由NH 催化氧化得到,而催化后的产物气体往往高于800°C,为使反应I顺利进行,再进行反应。“急
3
刷冷却”的原因有:低温下有利于反应速率增大; 。
(4)为避免汽车尾气中的氮氧化合物对大气的污染。需给汽车安装尾气净化装置。在净化装置中CO和NO
发生反应2NO(g)+2CO(g)=N (g)+2CO (g) △H=﹣746.8kJ•mol﹣1,实验测得:v =k •p(NO)•p(CO),v =k
2 2 正 正 2 逆
•p(N )•p((CO ),其中k 、k 分别为正、逆反应速率常数,只与温度有关;p为气体分压(分压=物质的量
逆 2 2 正 逆
分数×总压)。一定温度下在刚性密闲容器中充入CO、NO和N 物质的量之比为2 : 2 : 1,压强为pkPa.达
2 0
平衡时压强为0.9pkPa,则 = 。
0
【答案】(1) 0.042mol•(L•min)﹣1 (2分) 减小 (1分) bc(2分)
(2)AB(2分)
(3) 减小(1分) 反应Ⅱ放热,且快速平衡,升温使反应Ⅱ逆向移动,体系中NO 的浓度减小,进而
2 2
使反应Ⅲ速率减小,反应Ⅲ是决速步(2分) 有利于平衡正向移动,提高反应物的转化率,除去气体
中的水蒸气(2分)
(4) (2分)
【详解】(1)①0~10min内,NO的平均反应速率 ,
该反应是放热反应,温度升高平衡逆向移动,故答案为:0.042mol•(L•min)﹣1;减小;
②30min后,CO的浓度增大,N 的浓度增大,以此解题;
2
a.加入一定量的活性炭,平衡不移动,CO和N 的浓度不变,a错误;
2
b.通入一定量的NO,平衡正向移动,CO和N 的浓度增大,b正确;
2
c.该反应前后气体计量系数不变,适当缩小容器的体积,相当于加压,平衡不移动,CO和N 的浓度增大,
2
且增大的倍数相同,c正确;
d.加入合适的催化剂,不影响化学平衡,CO和N 的浓度不变,d错误;
2
故答案为:bc;(2)由速率公式,即速率方程v=k•c(NO)•[(I )]0.2(k为速率常数),可知碘蒸气的浓度增大,NO分解反应
2 2 2
速率增大,
A.I(g)是反应的催化剂,I(g)浓度增大,NO分解反应速率增大,故A正确;
2 7 2
B.慢反应步骤是整个反应的决速步骤,第二步是整个反应的决速步骤,故B正确;
C.催化剂不改变反应的焓变,故C错误;
故选AB;
(3)(①由不同温度下的NO的转化率随着温度的变化示意图,相同压强条件下,低温条件下,在相同的
时间转化率最大,则反应速率大,温度低反应速率大,可能的原因是反应Ⅱ是放热反应,且快速平衡,升
温使反应Ⅱ逆向移动,体系中NO 的浓度减小,进而导致反应Ⅲ速率下降或者使反应Ⅲ的速率常数k的升
2 2
高不如NO 的浓度减小对其速率影响显著,故答案为:减小;反应Ⅱ放热,且快速平衡,升温使反应Ⅱ逆
2 2
向移动,体系中NO 的浓度减小,进而使反应Ⅲ速率减小,反应Ⅲ是决速步;
2 2
②由数据信息分析,反应放热,低温下有利于反应速率增大,冷凝水蒸气,同时有利于平衡向正向移动,
提高反应物的转化率,故答案为:有利于平衡正向移动,提高反应物的转化率,除去气体中的水蒸气;
(4)依据在净化装置中CO和NO发生反应,列出三段式:
,解得a = 0.1P,则该反应的压强平衡常数
0
。
17.(14分)某废镍催化剂的主要成分是 合金,还含有少量Cr、Fe及不溶于酸碱的有机物。采用
如下工艺流程回收其中的镍,制备镍的氧化物( )。
回答下列问题:(1)“碱浸”时发生的主要反应离子方程式为 。
(2)“溶解”后的溶液中,所含金属离子有 、 、 、 、 。
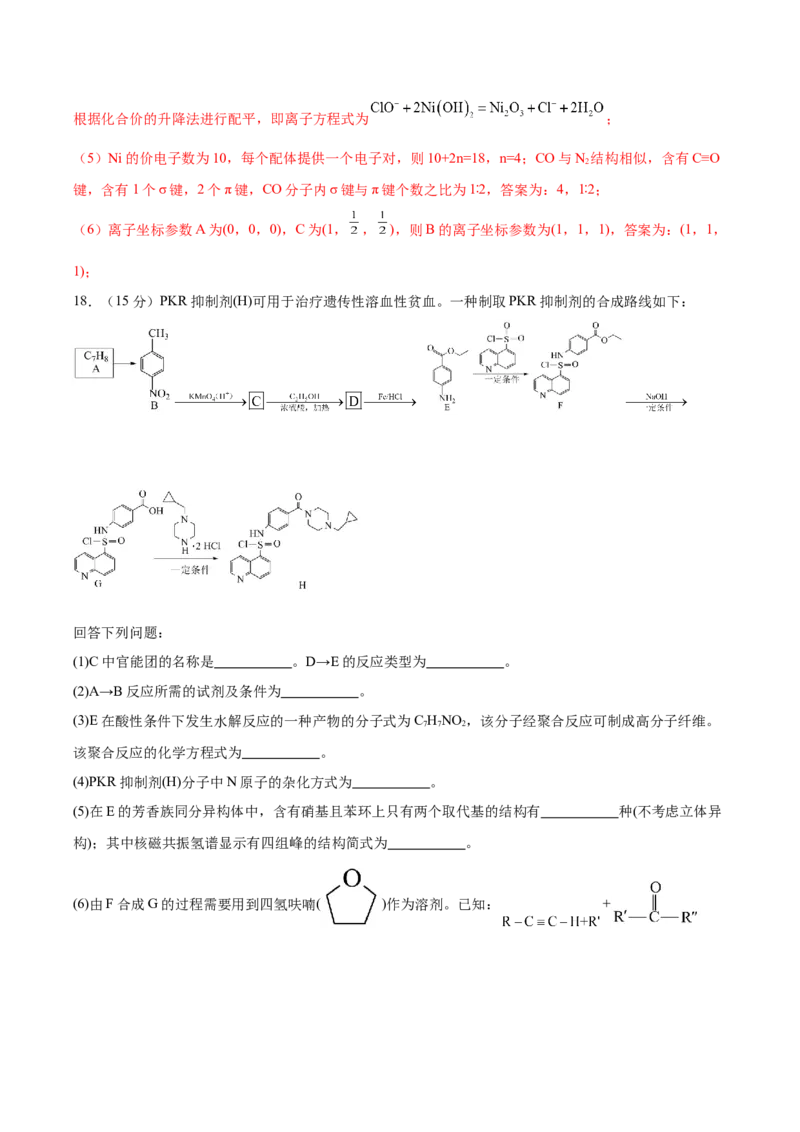
(3)在空气中煅烧 ,其热重曲线如图1所示,300~400 ℃时 转化为 ,反应的化学方程式
为 ;400~450℃生成的固体产物的化学式为 。
(4) 工业上可用电解法制取 。用NaOH溶液调节 溶液pH至7.5,加入适量硫酸钠后采用惰性电
极进行电解。电解过程中产生的 有80%在弱碱性条件下生成 ,再把二价镍氧化为三价镍。写出
氧化 生成 的离子方程式 。
(5)金属镍的配合物 的中心原子的价电子数与配体提供的成键电子总数之和为18,则n=
;CO与 结构相似,CO分子内 键与 键个数之比为 。
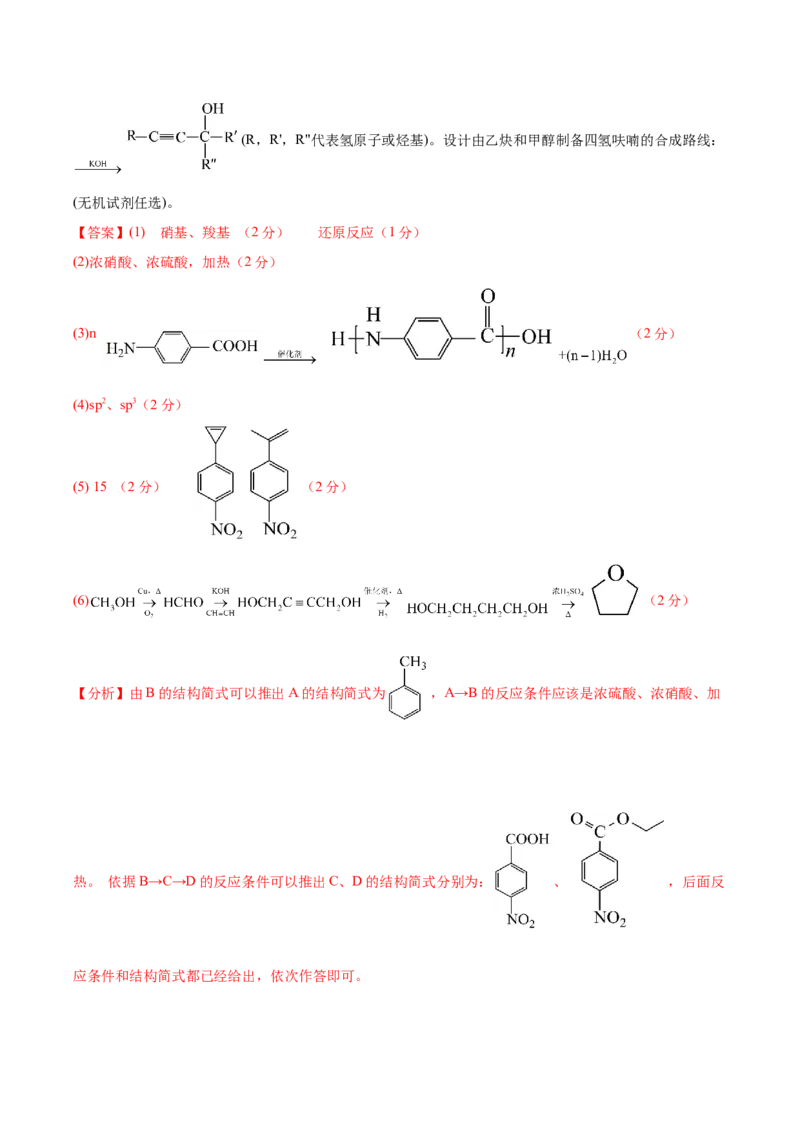
(6)NiO的晶胞结构如图2所示,其中离子坐标参数A为(0,0,0),C为(1, , ),则B的离子坐标参数
为 。
【答案】(1) (2分)(2) (1分)
(3) (2分) (2分)
(4) (2分)
(5) 4 (2分) 1∶2(1分)
(6)(1,1,1)(2分)
【分析】将废镍催化剂碱浸,Al和NaOH反应生成偏铝酸钠,Ni、Cr、Fe、有机物不与碱反应,则“滤液
1”的主要溶质为 、NaAlO ;通过灼烧,除去有机物;加入硫酸、硝酸,使Ni、Cr、Fe溶解生成
2
Ni2+、Cr3+、Fe2+、Fe3+;加入NaClO,使Fe2+完全转化为Fe3+,调节溶液pH,使Cr3+、Fe3+转化为
Cr(OH) 、Fe(OH) 沉淀;加入碳酸钠,使Ni2+转化为NiCO 沉淀,滤液2中含有硫酸钠、硝酸钠、碳酸钠
3 3 3
和次氯酸钠;过滤后得到的NiCO 中含有杂质,应洗涤、干燥后,再煅烧,最终得到镍的氧化物。
3
【详解】(1)“碱浸”时发生的主要反应是铝和氢氧化钠反应,离子方程式为:
;
(2)由分析可知,“溶解”后的溶液中,所含金属离子有 ,Ni2+、Fe3+,答案为: ;
(3) 转化为 ,反应的化学方程式为 ;设
1mol 在 下分解为 ,1mol 的质量为 ,由图可知,
在 下分解固体残留率为67.5%,则分解后 的质量为 ,根据Ni
原子守恒可知,生成 的物质的量为 , =80.3g,得到 ,故
生成产物的化学式为 ,答案为: , ;
(4)ClO-把Ni(OH) 氧化成Ni O,本身被还原成Cl-,因此离子方程式为ClO-+Ni(OH) →Ni O+Cl-,
2 2 3 2 2 3根据化合价的升降法进行配平,即离子方程式为 ;
(5)Ni的价电子数为10,每个配体提供一个电子对,则10+2n=18,n=4;CO与N 结构相似,含有C≡O
2
键,含有1个σ键,2个π键,CO分子内σ键与π键个数之比为1∶2,答案为:4,1∶2;
(6)离子坐标参数A为(0,0,0),C为(1, , ),则B的离子坐标参数为(1,1,1),答案为:(1,1,
1);
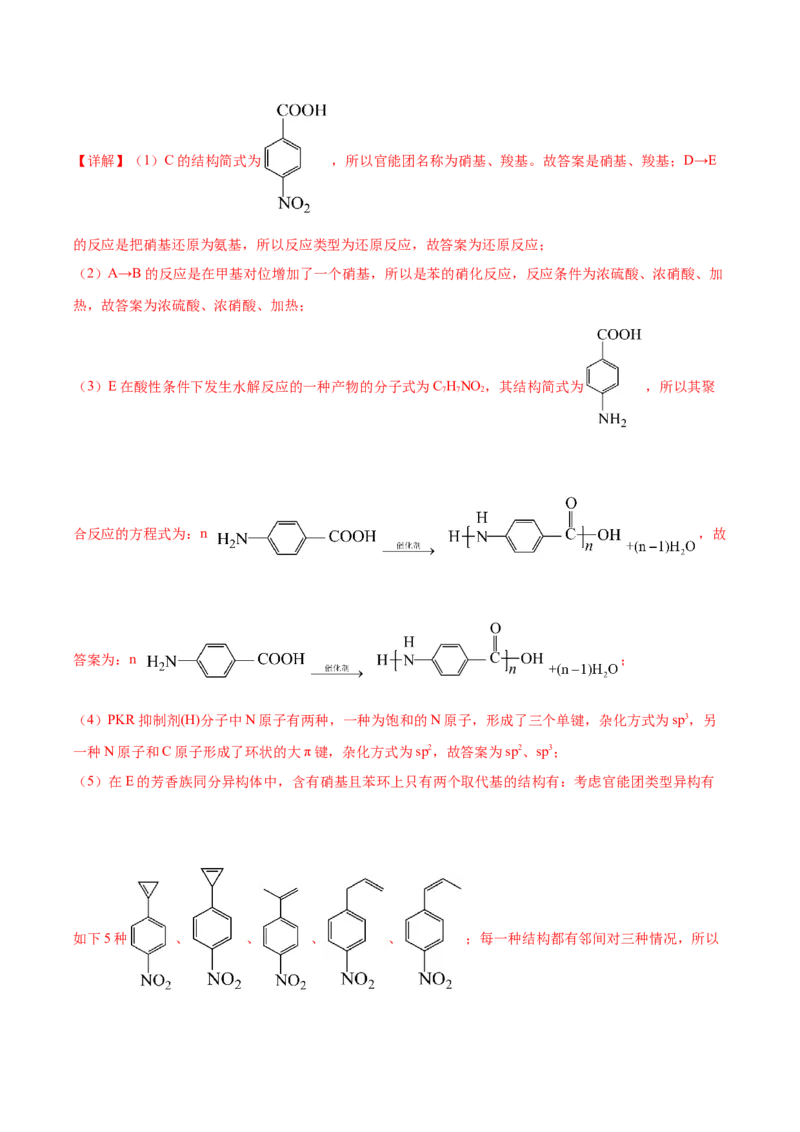
18.(15分)PKR抑制剂(H)可用于治疗遗传性溶血性贫血。一种制取PKR抑制剂的合成路线如下:
回答下列问题:
(1)C中官能团的名称是 。D→E的反应类型为 。
(2)A→B反应所需的试剂及条件为 。
(3)E在酸性条件下发生水解反应的一种产物的分子式为C HNO ,该分子经聚合反应可制成高分子纤维。
7 7 2
该聚合反应的化学方程式为 。
(4)PKR抑制剂(H)分子中N原子的杂化方式为 。
(5)在E的芳香族同分异构体中,含有硝基且苯环上只有两个取代基的结构有 种(不考虑立体异
构);其中核磁共振氢谱显示有四组峰的结构简式为 。
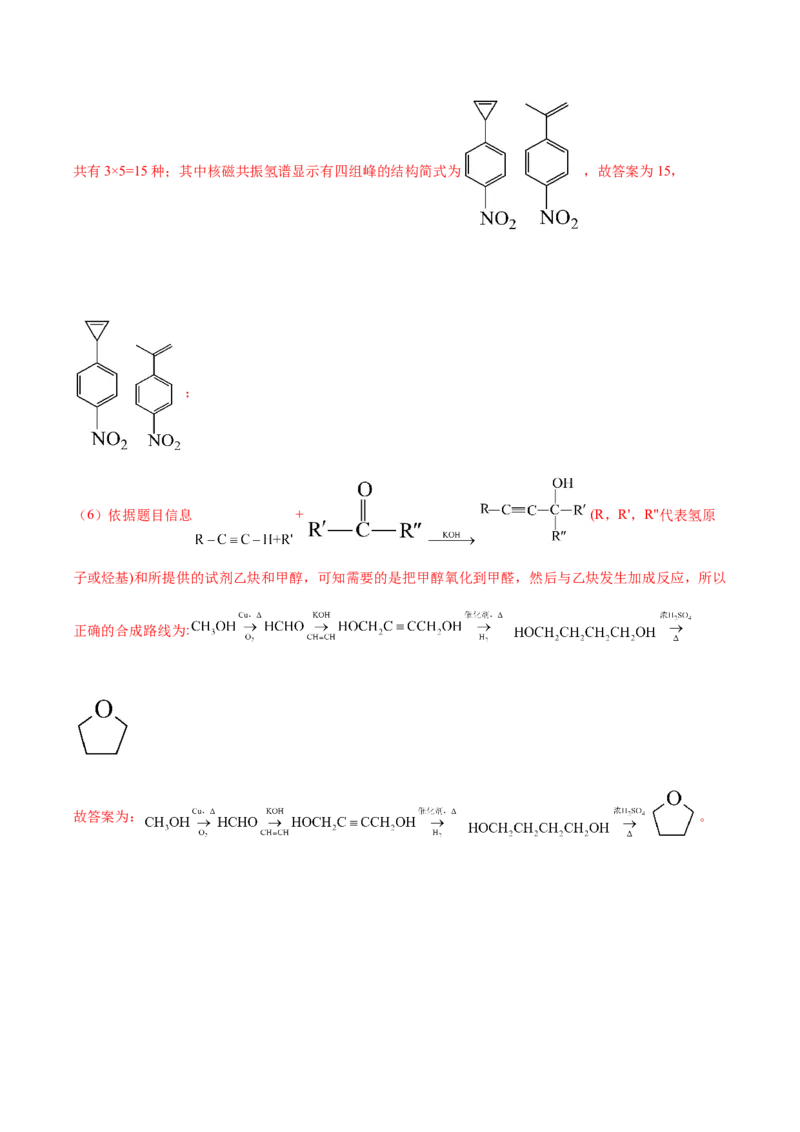
(6)由F合成G的过程需要用到四氢呋喃( )作为溶剂。已知: +(R,R',R"代表氢原子或烃基)。设计由乙炔和甲醇制备四氢呋喃的合成路线:
(无机试剂任选)。
【答案】(1) 硝基、羧基 (2分) 还原反应(1分)
(2)浓硝酸、浓硫酸,加热(2分)
(3)n (2分)
(4)sp2、sp3(2分)
(5) 15 (2分) (2分)
(6) (2分)
【分析】由B的结构简式可以推出A的结构简式为 ,A→B的反应条件应该是浓硫酸、浓硝酸、加
热。 依据B→C→D的反应条件可以推出C、D的结构简式分别为: 、 ,后面反
应条件和结构简式都已经给出,依次作答即可。【详解】(1)C的结构简式为 ,所以官能团名称为硝基、羧基。故答案是硝基、羧基;D→E
的反应是把硝基还原为氨基,所以反应类型为还原反应,故答案为还原反应;
(2)A→B的反应是在甲基对位增加了一个硝基,所以是苯的硝化反应,反应条件为浓硫酸、浓硝酸、加
热,故答案为浓硫酸、浓硝酸、加热;
(3)E在酸性条件下发生水解反应的一种产物的分子式为C HNO ,其结构简式为 ,所以其聚
7 7 2
合反应的方程式为:n ,故
答案为:n ;
(4)PKR抑制剂(H)分子中N原子有两种,一种为饱和的N原子,形成了三个单键,杂化方式为sp3,另
一种N原子和C原子形成了环状的大π键,杂化方式为sp2,故答案为sp2、sp3;
(5)在E的芳香族同分异构体中,含有硝基且苯环上只有两个取代基的结构有:考虑官能团类型异构有
如下5种 、 、 、 、 ;每一种结构都有邻间对三种情况,所以共有3×5=15种;其中核磁共振氢谱显示有四组峰的结构简式为 ,故答案为15,
;
(6)依据题目信息 + (R,R',R"代表氢原
子或烃基)和所提供的试剂乙炔和甲醇,可知需要的是把甲醇氧化到甲醛,然后与乙炔发生加成反应,所以
正确的合成路线为:
故答案为: 。