文档内容
主观题突破四
1.(13分)氮及其化合物在工农业生产中有着重要应用,减少氮的氧化物在大气中的排放是环境保护的
重要内容之一。
Ⅰ.一定条件下,用CH 催化还原可消除NO污染。
4
已知:
①CH(g)+2NO (g) N(g)+CO (g)+2HO(g) ΔH=-865.0 kJ·mol-1
4 2 2 2 2
②2NO(g)+O (g) 2NO (g) ΔH=-112.5 kJ·mol-1
2 2
(1)N 和O 完全反应,每生成2.24 L(标准状况)NO时,吸收8.9 kJ的热量,则CH(g)+4NO(g) 2N(g)
2 2 4 2
+CO (g)+2HO(g) ΔH= kJ·mol-1;一定温度下,往一容积不变的密闭容器中加入适量的CH
2 2 4
和NO,下列条件能判断该反应到达平衡状态的有 (填字母)。
A.混合气体的平均相对分子质量不变
B.v (NO)=4v (CO)
消耗 消耗 2
C.单位时间里有4n mol C—H断开同时有4n mol O—H断开
D.混合气体的压强不变
混合气体的密度不变
(2)将2 mol NO(g)、1 mol O (g)和2 mol He(g)通入反应器,在温度T、压强p条件下进行反应②和
2
2NO (g) NO(g)。平衡时,若O、NO 与NO 三者的物质的量相等,则NO转化率为
2 2 4 2 2 2 4
,反应②平衡常数K = (用含p的代数式表示)。
p
Ⅱ.利用如图所示原理去除NO:
(3)基态N原子中,电子占据的最高能级为 能级,该能级轨道的形状为 ;电解池中阴极
反应式为 。
(4)A口每产生224 mL O (体积已换算成标准状况,不考虑O 的溶解),可处理NO的物质的量为
2 2
mol。
2.(13分)(2024·皖豫名校联盟一模)甲醇是重要的化工原料之一,也可用作燃料,利用合成气(主要成分
为CO、CO 和H)可以合成甲醇,涉及的反应如下:
2 2
反应ⅰ:CO(g)+2H (g) CHOH(g) ΔH
2 3 1
反应ⅱ:CO (g)+3H(g) CHOH(g)+H O(g) ΔH=-49.9 kJ·mol-1
2 2 3 2 2
反应ⅲ:CO (g)+H(g) CO(g)+HO(g) ΔH=+41.6 kJ·mol-1
2 2 2 3请回答下列问题:
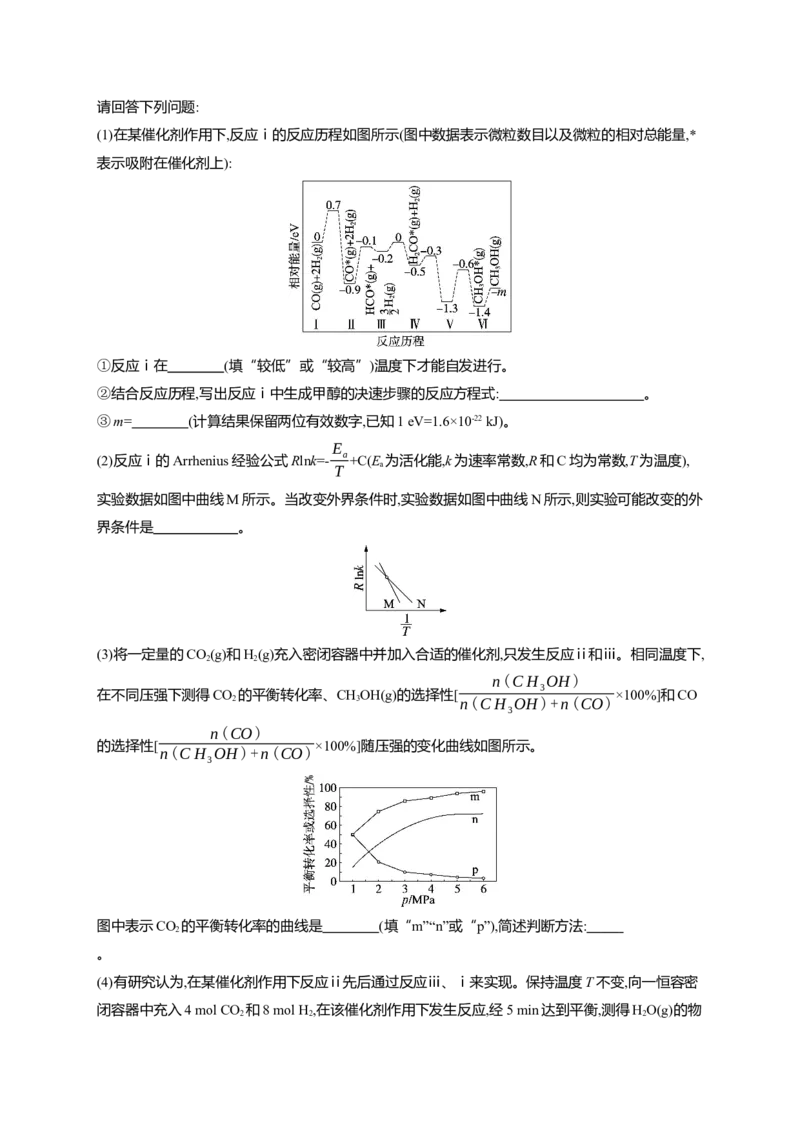
(1)在某催化剂作用下,反应ⅰ的反应历程如图所示(图中数据表示微粒数目以及微粒的相对总能量,*
表示吸附在催化剂上):
①反应ⅰ在 (填“较低”或“较高”)温度下才能自发进行。
②结合反应历程,写出反应ⅰ中生成甲醇的决速步骤的反应方程式: 。
③m= (计算结果保留两位有效数字,已知1 eV=1.6×10-22 kJ)。
E
a
(2)反应ⅰ的Arrhenius经验公式Rlnk=- +C(E 为活化能,k为速率常数,R和C均为常数,T为温度),
T a
实验数据如图中曲线M所示。当改变外界条件时,实验数据如图中曲线N所示,则实验可能改变的外
界条件是 。
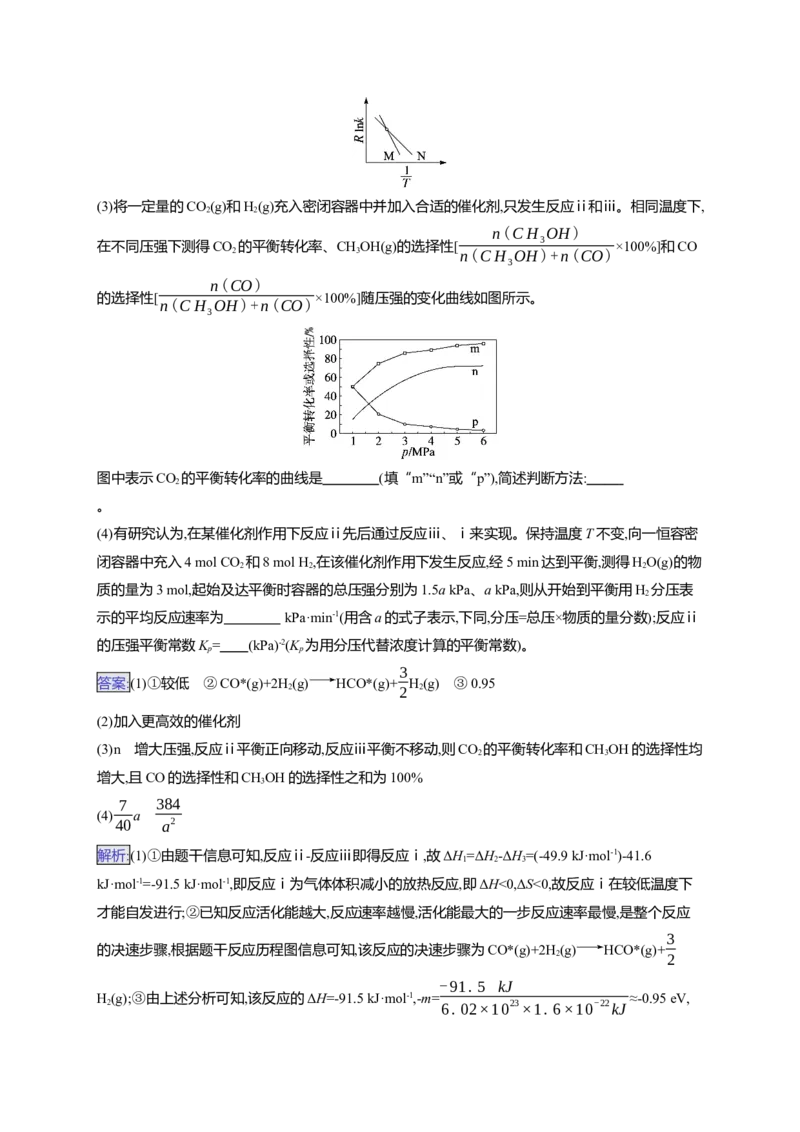
(3)将一定量的CO(g)和H(g)充入密闭容器中并加入合适的催化剂,只发生反应ⅱ和ⅲ。相同温度下,
2 2
n(CH OH)
3
在不同压强下测得CO 的平衡转化率、CHOH(g)的选择性[ ×100%]和CO
2 3 n(CH OH)+n(CO)
3
n(CO)
的选择性[ ×100%]随压强的变化曲线如图所示。
n(CH OH)+n(CO)
3
图中表示CO 的平衡转化率的曲线是 (填“m”“n”或“p”),简述判断方法:
2
。
(4)有研究认为,在某催化剂作用下反应ⅱ先后通过反应ⅲ、ⅰ来实现。保持温度T不变,向一恒容密
闭容器中充入4 mol CO 和8 mol H ,在该催化剂作用下发生反应,经5 min达到平衡,测得HO(g)的物
2 2 2质的量为3 mol,起始及达平衡时容器的总压强分别为1.5a kPa、a kPa,则从开始到平衡用H 分压表
2
示的平均反应速率为 kPa·min-1(用含a的式子表示,下同,分压=总压×物质的量分数);反应ⅱ
的压强平衡常数K = (kPa)-2(K 为用分压代替浓度计算的平衡常数)。
p p
3.(15分)(2024·湖南卷)丙烯腈(CH CHCN)是一种重要的化工原料。工业上以N 为载气,用TiO 作
2 2 2
催化剂生产CH CHCN的流程如下。
2
已知:①进料混合气进入两釜的流量恒定,两釜中反应温度恒定;
②反应釜Ⅰ中发生的反应为
ⅰ:HOCH CHCOOC H(g) CH CHCOOC H(g)+HO(g) ΔH
2 2 2 5 2 2 5 2 1
③反应釜Ⅱ中发生的反应为
ⅱ:CH CHCOOC H(g)+NH (g) CH CHCONH (g)+C HOH(g) ΔH
2 2 5 3 2 2 2 5 2
ⅲ:CH CHCONH (g) CH CHCN(g)+H O(g) ΔH
2 2 2 2 3
④在此生产条件下,酯类物质可能发生水解。
回答下列问题。
(1)总反应HOCH CHCOOC H(g)+NH (g) CH CHCN(g)+C HOH(g)+2H O(g) ΔH=
2 2 2 5 3 2 2 5 2
(用含ΔH、ΔH 和ΔH 的代数式表示)。
1 2 3
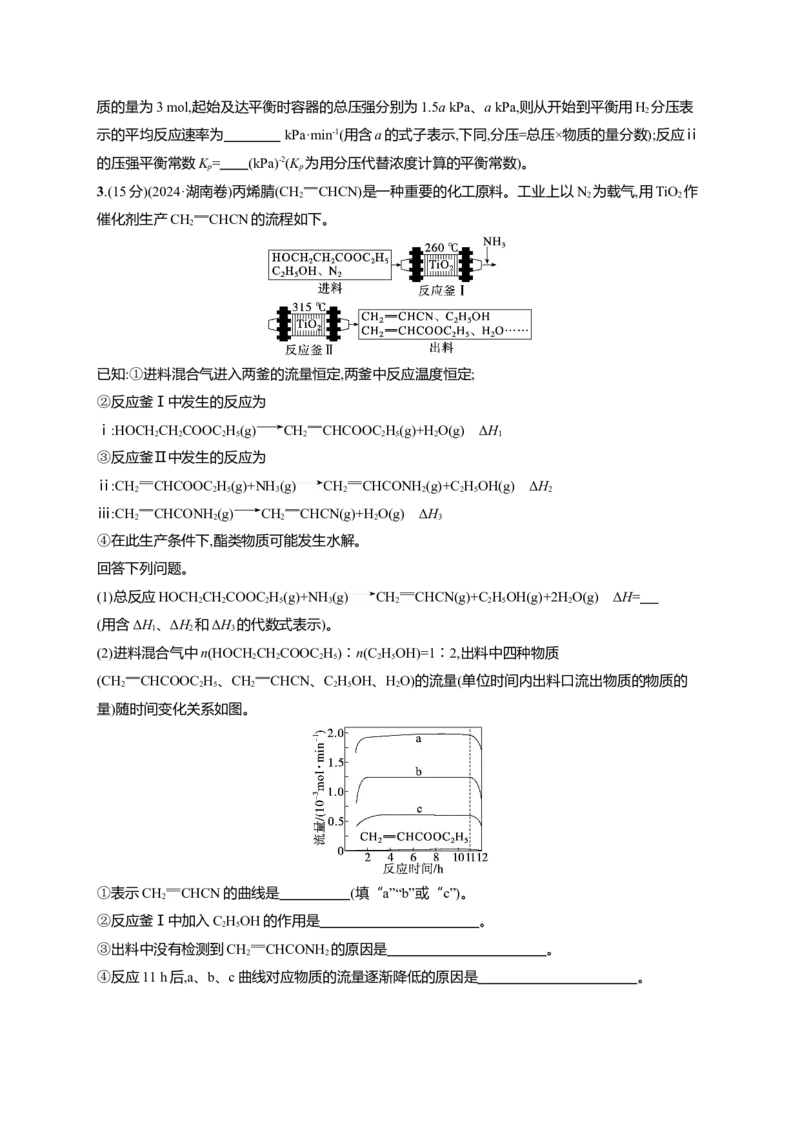
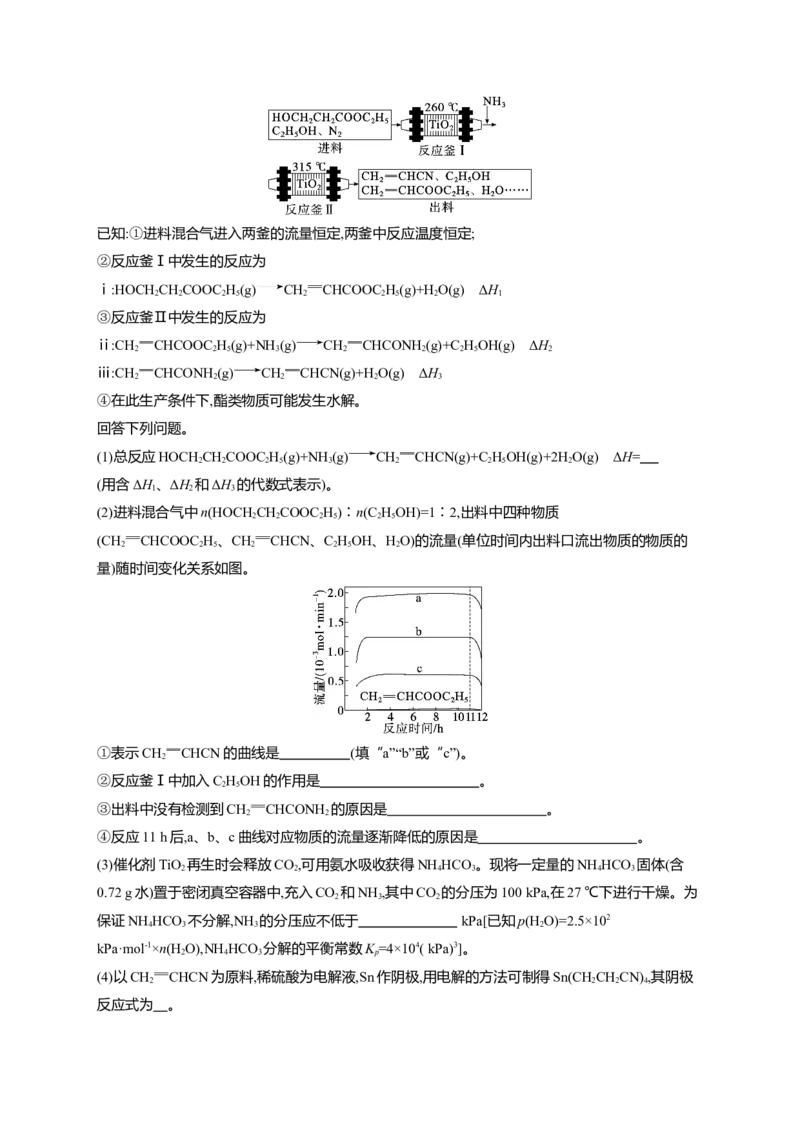
(2)进料混合气中n(HOCHCHCOOC H)∶n(C HOH)=1∶2,出料中四种物质
2 2 2 5 2 5
(CH CHCOOC H、CH CHCN、C HOH、HO)的流量(单位时间内出料口流出物质的物质的
2 2 5 2 2 5 2
量)随时间变化关系如图。
①表示CH CHCN的曲线是 (填“a”“b”或“c”)。
2
②反应釜Ⅰ中加入C HOH的作用是 。
2 5
③出料中没有检测到CH CHCONH 的原因是 。
2 2
④反应11 h后,a、b、c曲线对应物质的流量逐渐降低的原因是 。(3)催化剂TiO 再生时会释放CO,可用氨水吸收获得NH HCO 。现将一定量的NH HCO 固体(含
2 2 4 3 4 3
0.72 g水)置于密闭真空容器中,充入CO 和NH ,其中CO 的分压为100 kPa,在27 ℃下进行干燥。为
2 3 2
保证NH HCO 不分解,NH 的分压应不低于 kPa[已知p(H O)=2.5×102
4 3 3 2
kPa·mol-1×n(H O),NH HCO 分解的平衡常数K =4×104( kPa)3]。
2 4 3 p
(4)以CH CHCN为原料,稀硫酸为电解液,Sn作阴极,用电解的方法可制得Sn(CH CHCN) ,其阴极
2 2 2 4
反应式为 。
4.(15分)(2024·江苏南京一模)“碳中和”目标如期实现的关键技术之一是CO 的资源化再利用。
2
(1)氨的饱和食盐水捕获CO 是其利用的方法之一,反应原理为:NaCl(aq)+NH (g)+CO (g)+HO(l)
2 3 2 2
NaHCO (s)+NH Cl(aq)。该反应常温下能自发进行的原因是
3 4
。
(2)XO基掺杂NaCO 形成XO-Na CO(X=Mg、Ca、Cd等),能用于捕获CO,原理如图所示。已知阳
2 3 2 3 2
离子电荷数越高、半径越小,阴离子越易受其影响而分解。
①X=Ca时,再生的化学方程式为 。
②X=Mg相比X=Ca,其优点有 。
(3)催化电解吸收CO 的KOH溶液可将CO 转化为有机物。
2 2
①HCO-
在阴极放电生成CHCOO-的电极反应式为 。
3 3
②碱性溶液有利于抑制阴极上副产物的产生,该副产物的化学式为 。
(4)在催化剂作用下,以CO 和H 为原料合成CHOH,主要反应为:
2 2 3
反应Ⅰ:CO (g)+3H(g) CHOH(g)+H O(g) ΔH=-49 kJ·mol-1
2 2 3 2 1
反应Ⅱ:CO (g)+H(g) CO(g)+HO(g) ΔH=+41 kJ·mol-1
2 2 2 2
保持压强3 MPa,将起始n(CO)∶n(H )=1∶3的混合气体匀速通过装有催化剂的反应管,测得出口处
2 2
n (CH OH)
生成 3
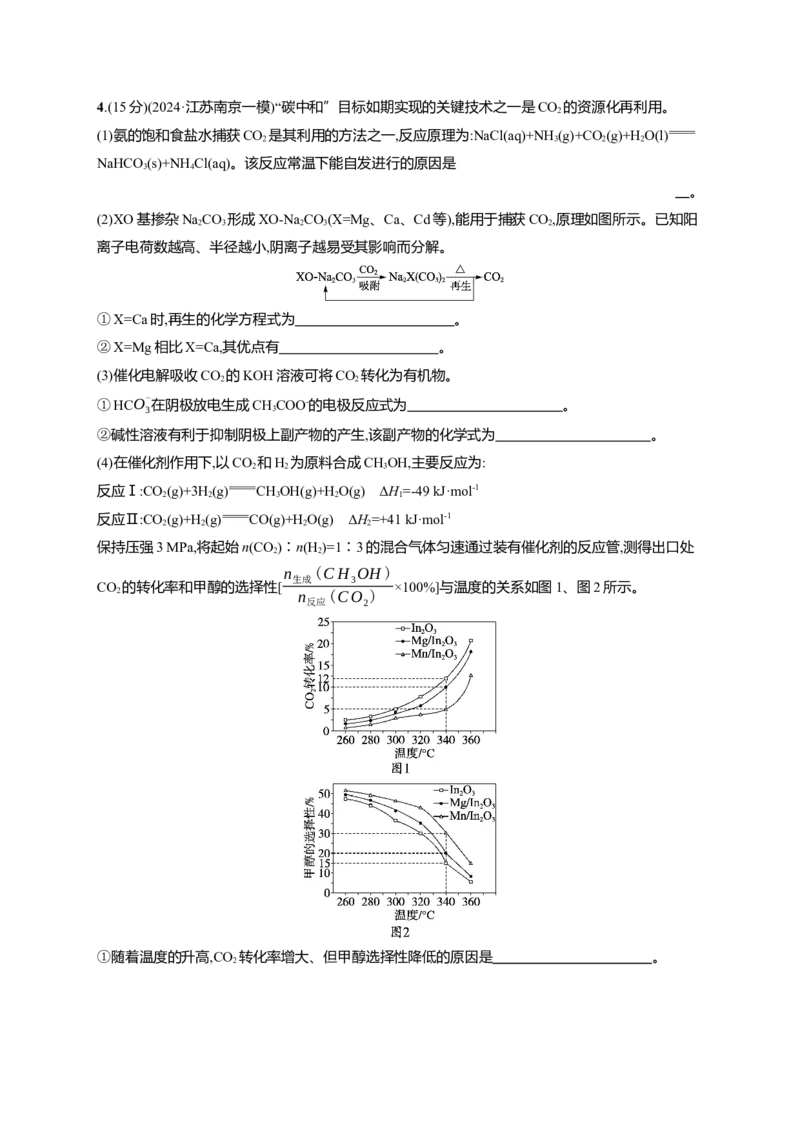
CO 的转化率和甲醇的选择性[ ×100%]与温度的关系如图1、图2所示。
2 n (CO )
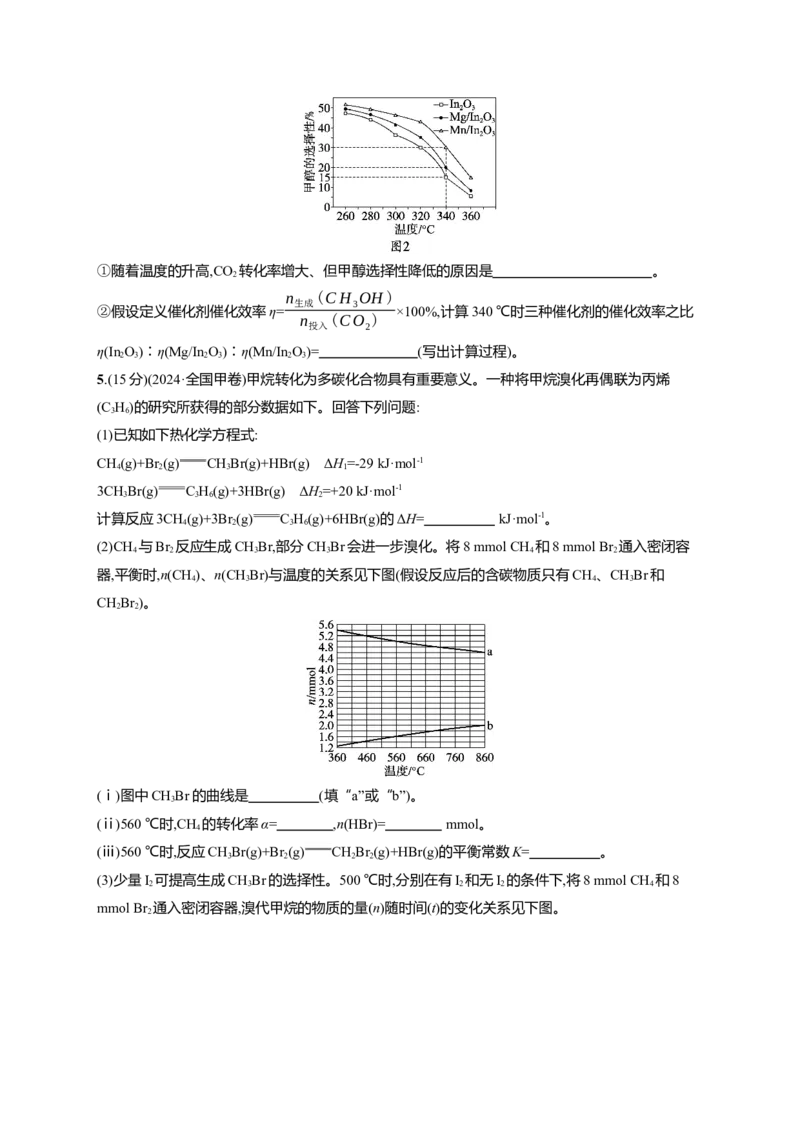
反应 2①随着温度的升高,CO 转化率增大、但甲醇选择性降低的原因是 。
2
n (CH OH)
生成 3
②假设定义催化剂催化效率η= ×100%,计算340 ℃时三种催化剂的催化效率之比
n (CO )
投入 2
η(InO)∶η(Mg/In O)∶η(Mn/In O)= (写出计算过程)。
2 3 2 3 2 3
5.(15分)(2024·全国甲卷)甲烷转化为多碳化合物具有重要意义。一种将甲烷溴化再偶联为丙烯
(C H)的研究所获得的部分数据如下。回答下列问题:
3 6
(1)已知如下热化学方程式:
CH(g)+Br (g) CHBr(g)+HBr(g) ΔH=-29 kJ·mol-1
4 2 3 1
3CHBr(g) C H(g)+3HBr(g) ΔH=+20 kJ·mol-1
3 3 6 2
计算反应3CH(g)+3Br (g) C H(g)+6HBr(g)的ΔH= kJ·mol-1。
4 2 3 6
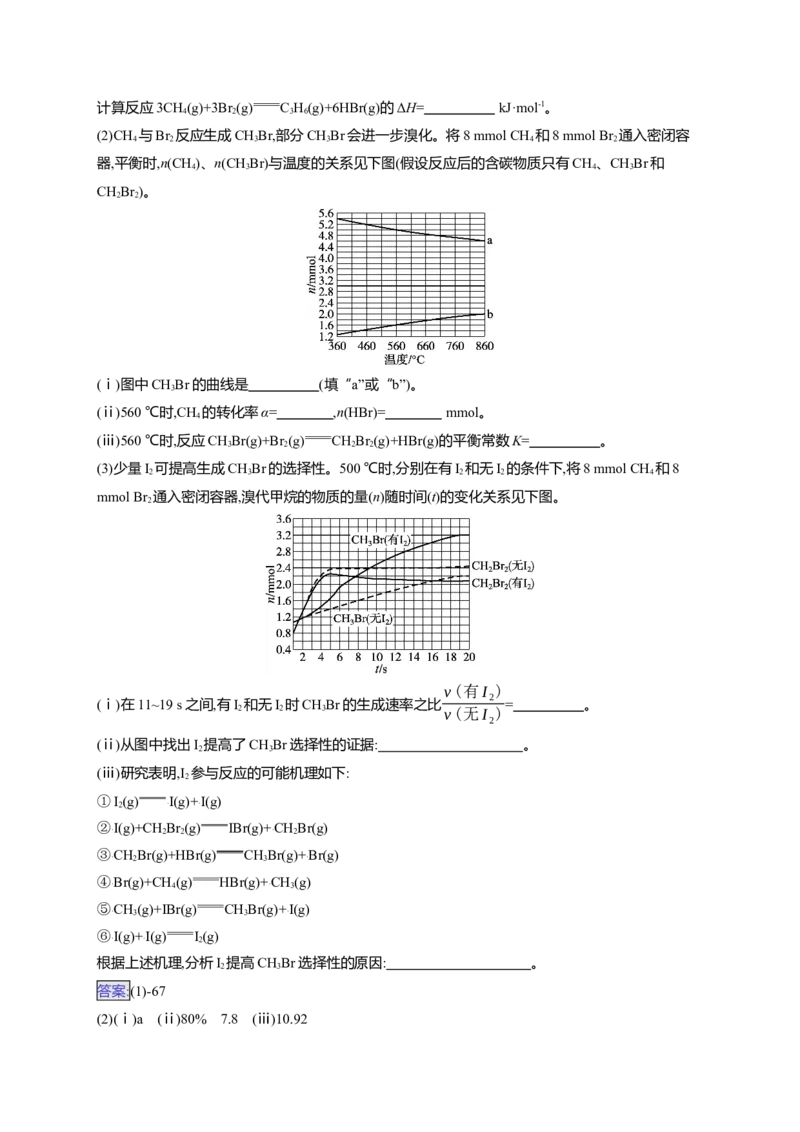
(2)CH 与Br 反应生成CHBr,部分CHBr会进一步溴化。将8 mmol CH 和8 mmol Br 通入密闭容
4 2 3 3 4 2
器,平衡时,n(CH)、n(CHBr)与温度的关系见下图(假设反应后的含碳物质只有CH、CHBr和
4 3 4 3
CHBr )。
2 2
(ⅰ)图中CHBr的曲线是 (填“a”或“b”)。
3
(ⅱ)560 ℃时,CH 的转化率α= ,n(HBr)= mmol。
4
(ⅲ)560 ℃时,反应CHBr(g)+Br (g) CHBr (g)+HBr(g)的平衡常数K= 。
3 2 2 2
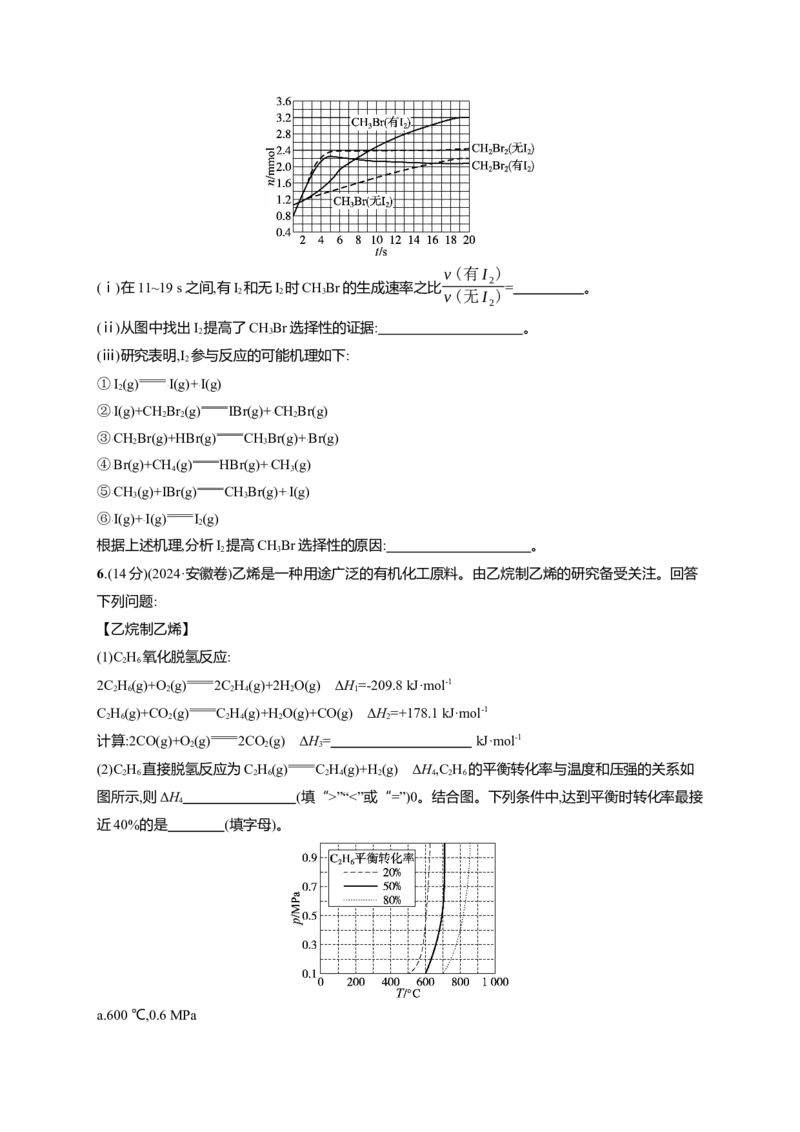
(3)少量I 可提高生成CHBr的选择性。500 ℃时,分别在有I 和无I 的条件下,将8 mmol CH 和8
2 3 2 2 4
mmol Br 通入密闭容器,溴代甲烷的物质的量(n)随时间(t)的变化关系见下图。
2v(有I )
2
(ⅰ)在11~19 s之间,有I 和无I 时CHBr的生成速率之比 = 。
2 2 3 v(无I )
2
(ⅱ)从图中找出I 提高了CHBr选择性的证据: 。
2 3
(ⅲ)研究表明,I 参与反应的可能机理如下:
2
①I(g) I(g)+I(g)
2 · ·
②I(g)+CHBr (g) IBr(g)+CHBr(g)
· 2 2 · 2
③CHBr(g)+HBr(g) CHBr(g)+Br(g)
· 2 3 ·
④Br(g)+CH (g) HBr(g)+CH(g)
· 4 · 3
⑤CH(g)+IBr(g) CHBr(g)+I(g)
· 3 3 ·
⑥I(g)+I(g) I(g)
· · 2
根据上述机理,分析I 提高CHBr选择性的原因: 。
2 3
6.(14分)(2024·安徽卷)乙烯是一种用途广泛的有机化工原料。由乙烷制乙烯的研究备受关注。回答
下列问题:
【乙烷制乙烯】
(1)C H 氧化脱氢反应:
2 6
2C H(g)+O(g) 2C H(g)+2HO(g) ΔH=-209.8 kJ·mol-1
2 6 2 2 4 2 1
C H(g)+CO (g) C H(g)+HO(g)+CO(g) ΔH=+178.1 kJ·mol-1
2 6 2 2 4 2 2
计算:2CO(g)+O (g) 2CO(g) ΔH= kJ·mol-1
2 2 3
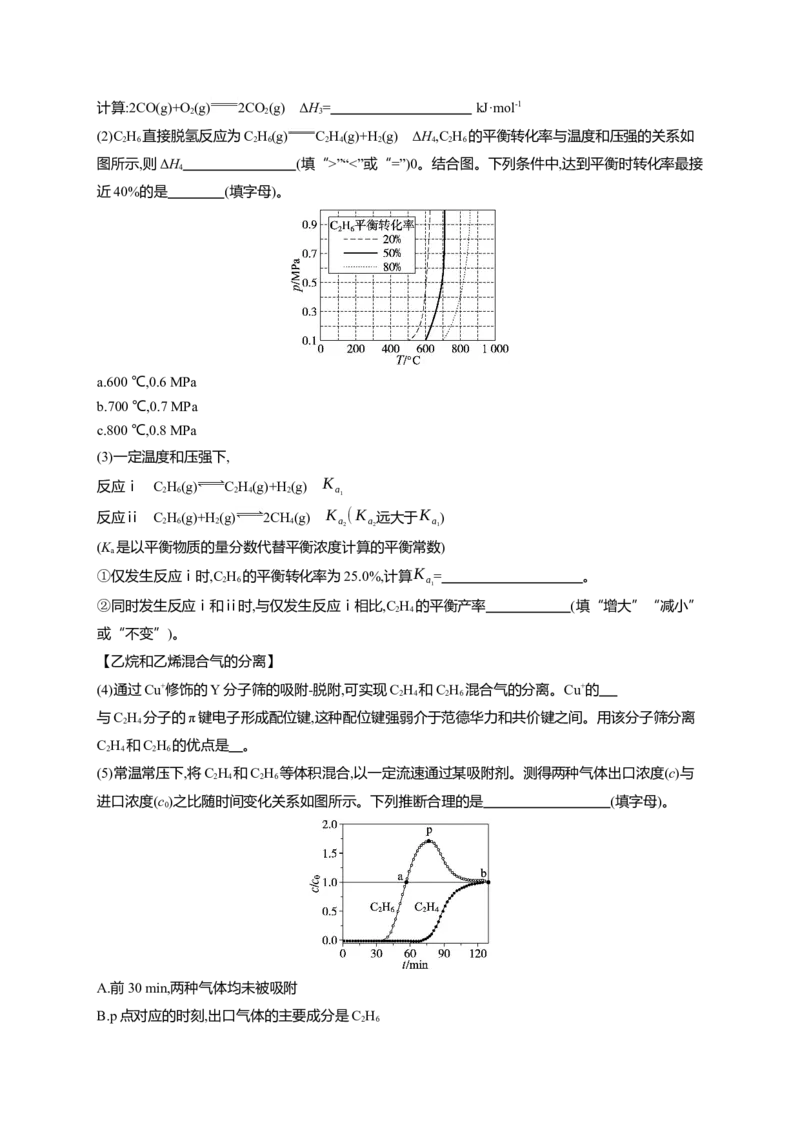
(2)C H 直接脱氢反应为C H(g) C H(g)+H(g) ΔH,C H 的平衡转化率与温度和压强的关系如
2 6 2 6 2 4 2 4 2 6
图所示,则ΔH (填“>”“<”或“=”)0。结合图。下列条件中,达到平衡时转化率最接
4
近40%的是 (填字母)。
a.600 ℃,0.6 MPab.700 ℃,0.7 MPa
c.800 ℃,0.8 MPa
(3)一定温度和压强下,
反应ⅰ C H(g) C H(g)+H(g) K
2 6 2 4 2 a
1
反应ⅱ C H(g)+H(g) 2CH(g) K (K 远大于 K )
2 6 2 4 a a a
2 2 1
(K 是以平衡物质的量分数代替平衡浓度计算的平衡常数)
a
①仅发生反应ⅰ时,C H 的平衡转化率为25.0%,计算 K = 。
2 6 a
1
②同时发生反应ⅰ和ⅱ时,与仅发生反应ⅰ相比,C H 的平衡产率 (填“增大”“减小”
2 4
或“不变”)。
【乙烷和乙烯混合气的分离】
(4)通过Cu+修饰的Y分子筛的吸附-脱附,可实现C H 和C H 混合气的分离。Cu+的
2 4 2 6
与C H 分子的π键电子形成配位键,这种配位键强弱介于范德华力和共价键之间。用该分子筛分离
2 4
C H 和C H 的优点是 。
2 4 2 6
(5)常温常压下,将C H 和C H 等体积混合,以一定流速通过某吸附剂。测得两种气体出口浓度(c)与
2 4 2 6
进口浓度(c)之比随时间变化关系如图所示。下列推断合理的是 (填字母)。
0
A.前30 min,两种气体均未被吸附
B.p点对应的时刻,出口气体的主要成分是C H
2 6
C.a~b对应的时间段内,吸附的C H 逐渐被C H 替代
2 6 2 4
主观题突破四
1.(13分)氮及其化合物在工农业生产中有着重要应用,减少氮的氧化物在大气中的排放是环境保护的
重要内容之一。
Ⅰ.一定条件下,用CH 催化还原可消除NO污染。
4
已知:
①CH(g)+2NO (g) N(g)+CO (g)+2HO(g) ΔH=-865.0 kJ·mol-1
4 2 2 2 2
②2NO(g)+O (g) 2NO (g) ΔH=-112.5 kJ·mol-1
2 2(1)N 和O 完全反应,每生成2.24 L(标准状况)NO时,吸收8.9 kJ的热量,则CH(g)+4NO(g) 2N(g)
2 2 4 2
+CO (g)+2HO(g) ΔH= kJ·mol-1;一定温度下,往一容积不变的密闭容器中加入适量的CH
2 2 4
和NO,下列条件能判断该反应到达平衡状态的有 (填字母)。
A.混合气体的平均相对分子质量不变
B.v (NO)=4v (CO)
消耗 消耗 2
C.单位时间里有4n mol C—H断开同时有4n mol O—H断开
D.混合气体的压强不变
混合气体的密度不变
(2)将2 mol NO(g)、1 mol O (g)和2 mol He(g)通入反应器,在温度T、压强p条件下进行反应②和
2
2NO (g) NO(g)。平衡时,若O、NO 与NO 三者的物质的量相等,则NO转化率为
2 2 4 2 2 2 4
,反应②平衡常数K = (用含p的代数式表示)。
p
Ⅱ.利用如图所示原理去除NO:
(3)基态N原子中,电子占据的最高能级为 能级,该能级轨道的形状为 ;电解池中阴极
反应式为 。
(4)A口每产生224 mL O (体积已换算成标准状况,不考虑O 的溶解),可处理NO的物质的量为
2 2
mol。
5
答案:(1)-1 155.5 BC (2)60%
2p
(3)2p 哑铃形
2HSO-
+2e-+2H+
SO2-
+2H O
3 2 4 2
(4)0.02
2.24 L
解析:(1)N 和O 完全反应,每生成2.24 L(标准状况)NO时n(NO)= =0.1 mol,吸收
2 2 22.4 L·mol-1
8.9 kJ的热量,则生成2 mol NO吸收热量Q=8.9 kJ×20=178 kJ,即热化学方程式为③N(g)+O(g)
2 2
2NO(g) ΔH=+178 kJ·mol-1,根据盖斯定律,反应①+②-③整理可得CH(g)+4NO(g) 2N(g)+CO (g)
4 2 2
+2H O(g) ΔH=-1 155.5 kJ·mol-1;
2
反应前后气体质量守恒,物质的量不变,故而平均相对分子质量一直不变,不能作为平衡的标志,A错误。
达到平衡时不同物质按计量数成比例,B正确。同理,C正确。整个反应过程气体压强不变,不能作为
平衡的标志,D错误。反应前后气体质量守恒,体积不变,故而密度不变,不能作为平衡的标志,E错误。(2)由题目信息可知,设平衡时n(NO)=x mol,n(NO )=n(O )=n(N O)=y mol,根据N守恒可得x+3y=2,根
2 2 2 4
据O守恒可得x+8y=4;解得n(NO)=x mol=0.8 mol,n(NO )=n(O )=n(N O)=y mol=0.4 mol。NO转化率
2 2 2 4
2-0.8
为 ×100%=60%;平衡时混合气体总物质的量为0.8 mol+0.4 mol×3+2 mol=4 mol,反应②平衡
2
0.4
( p)2
4 5
常数K = = 。
p 0.8 0.4 2p
( p)2× p
4 4
(3)基态N原子核外电子排布为1s22s22p3,基态N原子中,电子占据的最高能级为2p能级,该能级轨道
的形状为哑铃形。由图可知,电解池中阴极的亚硫酸氢根离子得到电子发生还原反应生成SO2-
,反
2 4
应式为2HSO-
+2e-+2H+
SO2-
+2H O。
3 2 4 2
(4)A口每产生224 mL O (体积已换算成标准状况,不考虑O 的溶解)为0.01 mol,NO得到电子生成0
2 2
价的氮气,根据电子守恒可知,2NO~4e-~O ,则可处理NO的物质的量为0.02 mol。
2
2.(13分)(2024·皖豫名校联盟一模)甲醇是重要的化工原料之一,也可用作燃料,利用合成气(主要成分
为CO、CO 和H)可以合成甲醇,涉及的反应如下:
2 2
反应ⅰ:CO(g)+2H (g) CHOH(g) ΔH
2 3 1
反应ⅱ:CO (g)+3H(g) CHOH(g)+H O(g) ΔH=-49.9 kJ·mol-1
2 2 3 2 2
反应ⅲ:CO (g)+H(g) CO(g)+HO(g) ΔH=+41.6 kJ·mol-1
2 2 2 3
请回答下列问题:
(1)在某催化剂作用下,反应ⅰ的反应历程如图所示(图中数据表示微粒数目以及微粒的相对总能量,*
表示吸附在催化剂上):
①反应ⅰ在 (填“较低”或“较高”)温度下才能自发进行。
②结合反应历程,写出反应ⅰ中生成甲醇的决速步骤的反应方程式: 。
③m= (计算结果保留两位有效数字,已知1 eV=1.6×10-22 kJ)。
E
a
(2)反应ⅰ的Arrhenius经验公式Rlnk=- +C(E 为活化能,k为速率常数,R和C均为常数,T为温度),
T a
实验数据如图中曲线M所示。当改变外界条件时,实验数据如图中曲线N所示,则实验可能改变的外
界条件是 。(3)将一定量的CO(g)和H(g)充入密闭容器中并加入合适的催化剂,只发生反应ⅱ和ⅲ。相同温度下,
2 2
n(CH OH)
3
在不同压强下测得CO 的平衡转化率、CHOH(g)的选择性[ ×100%]和CO
2 3 n(CH OH)+n(CO)
3
n(CO)
的选择性[ ×100%]随压强的变化曲线如图所示。
n(CH OH)+n(CO)
3
图中表示CO 的平衡转化率的曲线是 (填“m”“n”或“p”),简述判断方法:
2
。
(4)有研究认为,在某催化剂作用下反应ⅱ先后通过反应ⅲ、ⅰ来实现。保持温度T不变,向一恒容密
闭容器中充入4 mol CO 和8 mol H ,在该催化剂作用下发生反应,经5 min达到平衡,测得HO(g)的物
2 2 2
质的量为3 mol,起始及达平衡时容器的总压强分别为1.5a kPa、a kPa,则从开始到平衡用H 分压表
2
示的平均反应速率为 kPa·min-1(用含a的式子表示,下同,分压=总压×物质的量分数);反应ⅱ
的压强平衡常数K = (kPa)-2(K 为用分压代替浓度计算的平衡常数)。
p p
3
答案:(1)①较低 ②CO*(g)+2H(g) HCO*(g)+ H(g) ③0.95
2 2 2
(2)加入更高效的催化剂
(3)n 增大压强,反应ⅱ平衡正向移动,反应ⅲ平衡不移动,则CO 的平衡转化率和CHOH的选择性均
2 3
增大,且CO的选择性和CHOH的选择性之和为100%
3
7 384
(4) a
40 a2
解析:(1)①由题干信息可知,反应ⅱ-反应ⅲ即得反应ⅰ,故ΔH=ΔH-ΔH=(-49.9 kJ·mol-1)-41.6
1 2 3
kJ·mol-1=-91.5 kJ·mol-1,即反应ⅰ为气体体积减小的放热反应,即ΔH<0,ΔS<0,故反应ⅰ在较低温度下
才能自发进行;②已知反应活化能越大,反应速率越慢,活化能最大的一步反应速率最慢,是整个反应
3
的决速步骤,根据题干反应历程图信息可知,该反应的决速步骤为CO*(g)+2H(g) HCO*(g)+
2 2
-91.5 kJ
H(g);③由上述分析可知,该反应的ΔH=-91.5 kJ·mol-1,-m= ≈-0.95 eV,
2 6.02×1023×1.6×10-22kJE
a
则m=0.95;(2)由题干信息可知,反应ⅰ的Arrhenius经验公式Rlnk=- +C(E 为活化能,k为速率常数,
T a
R和C均为常数,T为温度),与M相比,N曲线的活化能降低,则实验改变外界条件为加入更高效催化
剂;
(3)已知反应ⅱ:CO (g)+3H(g) CHOH(g)+H O(g),反应ⅲ:CO (g)+H(g) CO(g)+HO(g)可知,增
2 2 3 2 2 2 2
大压强,反应ⅱ平衡正向移动,反应ⅲ平衡不移动,则CO 的平衡转化率和CHOH的选择性均增大,且
2 3
CO的选择性和CHOH的选择性之和为100%,结合题干图像可知,m为CHOH的选择性,p为CO的
3 3
选择性,n为CO 的平衡转化率曲线;
2
(4)有研究认为,在某催化剂作用下反应ⅱ先后通过反应ⅲ、ⅰ来实现,保持温度T不变,向一恒容密闭
容器中充入4 mol CO 和8 mol H ,在该催化剂作用下发生反应,经5 min达到平衡,测得HO(g)的物质
2 2 2
的量为3 mol,则进行三段式分析为:
CO(g) + H (g) CO(g) + H O(g)
2 2 2
起始量/mol 4 8 0 0
转化量/mol 3 3 3 3
平衡量/mol 1 5 3 3
CO(g) + 2H (g) CHOH(g)
2 3
起始量/mol 3 5 0
转化量/mol x 2x x
平衡量/mol 3-x 5-2x x
4+8 1.5akPa
起始及达平衡时容器的总压强分别为1.5a kPa、a kPa,则有: = ,解
1+3-x+5-2x+x+3 akPa
5-2x 5-2×2 a
得x=2 mol,则H 的平衡分压为 ×a kPa= ×a kPa= kPa,则从开始到平衡用H 分压表
2 12-2x 12-2×2 8 2
8 a
×1.5akPa- kPa
示的平均反应速率为12 8 7 a kPa·min-1,平衡时CO、H、CHOH、HO的
= 2 2 3 2
5min 40
1 1 a a a 3a
平衡分压分别为 ×a kPa= ×a kPa= kPa, kPa、 kPa、 kPa;反应ⅱ的压强平
12-2x 12-2×2 8 8 4 8
a 3a
kPa× kPa
p(CH OH)p(H O) 4 8 384
衡常数K = 3 2 = = (kPa)-2。
p p(CO
2
)p3(H
2
) a
kPa×(
a
kPa)3
a2
8 8
3.(15分)(2024·湖南卷)丙烯腈(CH CHCN)是一种重要的化工原料。工业上以N 为载气,用TiO 作
2 2 2
催化剂生产CH CHCN的流程如下。
2已知:①进料混合气进入两釜的流量恒定,两釜中反应温度恒定;
②反应釜Ⅰ中发生的反应为
ⅰ:HOCH CHCOOC H(g) CH CHCOOC H(g)+HO(g) ΔH
2 2 2 5 2 2 5 2 1
③反应釜Ⅱ中发生的反应为
ⅱ:CH CHCOOC H(g)+NH (g) CH CHCONH (g)+C HOH(g) ΔH
2 2 5 3 2 2 2 5 2
ⅲ:CH CHCONH (g) CH CHCN(g)+H O(g) ΔH
2 2 2 2 3
④在此生产条件下,酯类物质可能发生水解。
回答下列问题。
(1)总反应HOCH CHCOOC H(g)+NH (g) CH CHCN(g)+C HOH(g)+2H O(g) ΔH=
2 2 2 5 3 2 2 5 2
(用含ΔH、ΔH 和ΔH 的代数式表示)。
1 2 3
(2)进料混合气中n(HOCHCHCOOC H)∶n(C HOH)=1∶2,出料中四种物质
2 2 2 5 2 5
(CH CHCOOC H、CH CHCN、C HOH、HO)的流量(单位时间内出料口流出物质的物质的
2 2 5 2 2 5 2
量)随时间变化关系如图。
①表示CH CHCN的曲线是 (填“a”“b”或“c”)。
2
②反应釜Ⅰ中加入C HOH的作用是 。
2 5
③出料中没有检测到CH CHCONH 的原因是 。
2 2
④反应11 h后,a、b、c曲线对应物质的流量逐渐降低的原因是 。
(3)催化剂TiO 再生时会释放CO,可用氨水吸收获得NH HCO 。现将一定量的NH HCO 固体(含
2 2 4 3 4 3
0.72 g水)置于密闭真空容器中,充入CO 和NH ,其中CO 的分压为100 kPa,在27 ℃下进行干燥。为
2 3 2
保证NH HCO 不分解,NH 的分压应不低于 kPa[已知p(H O)=2.5×102
4 3 3 2
kPa·mol-1×n(H O),NH HCO 分解的平衡常数K =4×104( kPa)3]。
2 4 3 p
(4)以CH CHCN为原料,稀硫酸为电解液,Sn作阴极,用电解的方法可制得Sn(CH CHCN) ,其阴极
2 2 2 4
反应式为 。答案:(1)ΔH+ΔH+ΔH
1 2 3
(2)①c ②降低HOCH CHCOOC H 的分压,有利于反应ⅰ正向移动,同时增大乙醇的浓度可以使酯
2 2 2 5
的水解程度降低,从而提高
CH CHCOOC H 的产率 ③CH CHCONH 在反应釜Ⅱ的温度下可彻底分解 ④反应时间过长,
2 2 5 2 2
催化剂中毒活性降低,反应速率减小,故产物减少
(3)40
(4)Sn+4CH CHCN+4e-+4H+ Sn(CH CHCN)
2 2 2 4
解析:工业上以N 为载气,用TiO 作催化剂,由HOCH CHCOOC H 和C HOH为进料气体生产
2 2 2 2 2 5 2 5
CH CHCN,在反应釜Ⅰ中发生反应ⅰ:HOCH CHCOOC H(g) CH CHCOOC H(g)+HO(g),
2 2 2 2 5 2 2 5 2
加入NH 后,在反应釜Ⅱ中发生反应ⅱ:CH CHCOOC H(g)+NH (g) CH CHCONH (g)
3 2 2 5 3 2 2
+C HOH(g),反应ⅲ:CH CHCONH (g) CH CHCN(g)+H O(g),故产物的混合气体中有CH
2 5 2 2 2 2 2
CHCN、C HOH、未反应完的CH CHCOOC H 和水。
2 5 2 2 5
(1)根据盖斯定律,总反应HOCH CHCOOC H(g)+NH (g) CH CHCN(g)+C HOH(g)+2H O(g)可
2 2 2 5 3 2 2 5 2
以由反应ⅰ+反应ⅱ+反应ⅲ得到,故ΔH=ΔH+ΔH+ΔH。
1 2 3
(2)①根据总反应HOCH CHCOOC H(g)+NH (g) CH CHCN(g)+C HOH(g)+2H O(g),设进料混
2 2 2 5 3 2 2 5 2
合气中n(HOCHCHCOOC H)=1 mol,n(C HOH)=2 mol,出料气中CH CHCOOC H 含量很少,则生
2 2 2 5 2 5 2 2 5
成CH CHCN(g)、C HOH(g)的物质的量约为1 mol,生成HO(g)的物质的量约为2 mol,故出料气
2 2 5 2
中C HOH(g)的物质的量共约3 mol,出料气中
2 5
CH CHCN、C HOH、HO的物质的量之比约为1∶3∶2,因此曲线c表示CH CHCN的曲线。
2 2 5 2 2
②已知进料混合气进入两釜的流量恒定,反应釜Ⅰ中发生反应ⅰ是气体体积增大的反应,故加入
C HOH降低HOCH CHCOOC H 的分压有利于反应ⅰ正向移动,同时增大乙醇的浓度可以使酯的
2 5 2 2 2 5
水解程度降低从而提高CH CHCOOC H 的产率。
2 2 5
③丙烯酰胺(CH CHCONH )的分解温度为160~170 ℃,出料中没有检测到CH CHCONH 的原因
2 2 2 2
是CH CHCONH 在反应釜Ⅱ的温度下可彻底分解。
2 2
④反应11 h后,a、b、c曲线对应物质的流量逐渐降低的原因是反应时间过长,催化剂中毒活性降低,
反应速率减小,故产物减少。
(3)0.72 g水的物质的量为0.04 mol,故p(H O)=2.5×102 kPa·mol-1×n(H O)=10 kPa,NH HCO 分解的化
2 2 4 3
学方程式为NH HCO (s) NH (g)+CO (g)+HO(g),故NH HCO 分解的平衡常数
4 3 3 2 2 4 3
K =p(NH )·p(CO)·p(H O)=4×104(kPa)3,解得p(NH )=40 kPa,故为保证NH HCO 不分解,NH 的分压应
p 3 2 2 3 4 3 3
不低于40 kPa。
(4)Sn(CH CHCN) 是有机化合物,在水中不电离,以CH CHCN为原料,稀硫酸为电解液,Sn作阴极,
2 2 4 2
用电解的方法可制得Sn(CH CHCN) ,故阴极的电极反应式为Sn+4CH CHCN+4e-+4H+
2 2 4 2
Sn(CH CHCN) 。
2 2 44.(15分)(2024·江苏南京一模)“碳中和”目标如期实现的关键技术之一是CO 的资源化再利用。
2
(1)氨的饱和食盐水捕获CO 是其利用的方法之一,反应原理为:NaCl(aq)+NH (g)+CO (g)+HO(l)
2 3 2 2
NaHCO (s)+NH Cl(aq)。该反应常温下能自发进行的原因是
3 4
。
(2)XO基掺杂NaCO 形成XO-Na CO(X=Mg、Ca、Cd等),能用于捕获CO,原理如图所示。已知阳
2 3 2 3 2
离子电荷数越高、半径越小,阴离子越易受其影响而分解。
①X=Ca时,再生的化学方程式为 。
②X=Mg相比X=Ca,其优点有 。
(3)催化电解吸收CO 的KOH溶液可将CO 转化为有机物。
2 2
①HCO-
在阴极放电生成CHCOO-的电极反应式为 。
3 3
②碱性溶液有利于抑制阴极上副产物的产生,该副产物的化学式为 。
(4)在催化剂作用下,以CO 和H 为原料合成CHOH,主要反应为:
2 2 3
反应Ⅰ:CO (g)+3H(g) CHOH(g)+H O(g) ΔH=-49 kJ·mol-1
2 2 3 2 1
反应Ⅱ:CO (g)+H(g) CO(g)+HO(g) ΔH=+41 kJ·mol-1
2 2 2 2
保持压强3 MPa,将起始n(CO)∶n(H )=1∶3的混合气体匀速通过装有催化剂的反应管,测得出口处
2 2
n (CH OH)
生成 3
CO 的转化率和甲醇的选择性[ ×100%]与温度的关系如图1、图2所示。
2 n (CO )
反应 2
①随着温度的升高,CO 转化率增大、但甲醇选择性降低的原因是 。
2n (CH OH)
生成 3
②假设定义催化剂催化效率η= ×100%,计算340 ℃时三种催化剂的催化效率之比
n (CO )
投入 2
η(InO)∶η(Mg/In O)∶η(Mn/In O)= (写出计算过程)。
2 3 2 3 2 3
答案:(1)反应ΔH<0
(2)①NaCa(CO) CaO-Na CO+CO ↑(或NaCa(CO) CaO+Na CO+CO ↑) ②等质量的
2 3 2 2 3 2 2 3 2 2 3 2
MgO和CaO相比,MgO吸收的CO 的量多;Ca2+和Mg2+电荷数相等、Mg2+半径小,再生时MgCO 分解
2 3
温度低,更节能
(3)①11HCO-
+8e-
CHCOO-+9CO2-
+4H O ②H
3 3 3 2 2
(4)①随着温度升高,反应Ⅰ和反应Ⅱ速率加快,消耗的CO 增多。反应Ⅰ的ΔH<0,反应Ⅱ的ΔH>0,随
2
着温度升高,反应Ⅰ正向进行程度小,反应Ⅱ正向进行程度大,CO 转化率升高、但CHOH选择性降
2 3
低 ②18∶20∶15
解析:(1)该反应为熵减的反应,该反应常温下能自发进行,反应ΔH<0。
(2)①X=Ca时,Na Ca(CO) 加热生成CaO-Na CO 和CO,再生的化学方程式为NaCa(CO) CaO-
2 3 2 2 3 2 2 3 2
NaCO+CO ↑或
2 3 2
NaCa(CO) CaO+Na CO+CO ↑;
2 3 2 2 3 2
②已知阳离子电荷数越高、半径越小,阴离子越易受其影响而分解,所以X=Mg相比X=Ca,其优点有
等质量的MgO和CaO相比,MgO吸收的CO 的量多;Ca2+和Mg2+电荷数相等、Mg2+半径小,再生时
2
MgCO 分解温度低,更节能。
3
(3)①催化电解吸收CO 的KOH溶液可将CO
转化为有机物,HCO-
在阴极放电生成CHCOO-,电极
2 2 3 3
反应式为11HCO-
+8e-
CHCOO-+9CO2-
+4H O;
3 3 3 2
②电解时,H+可在阴极得到电子生成H,碱性溶液有利于抑制H 的产生。
2 2
(4)①随着温度升高,反应Ⅰ和反应Ⅱ速率加快,消耗的CO 增多。反应Ⅰ的ΔH<0,反应Ⅱ的ΔH>0,随
2
着温度升高,反应Ⅰ正向进行程度小,反应Ⅱ正向进行程度大,CO 转化率升高、但CHOH选择性降
2 3
低;
②由图可知,340 ℃时InO、Mg/In O、Mn/In O 的CO 的转化率分别为12%、10%和5%,In O、
2 3 2 3 2 3 2 2 3
Mg/In O、Mn/In O 甲醇的选择性分别为15%、20%和30%,所以η(InO)∶η(Mg/In O)∶η(Mn/
2 3 2 3 2 3 2 3
InO)=(12%×15%)∶(10%×20%)∶(5%×30%)=18∶20∶15。
2 3
5.(15分)(2024·全国甲卷)甲烷转化为多碳化合物具有重要意义。一种将甲烷溴化再偶联为丙烯
(C H)的研究所获得的部分数据如下。回答下列问题:
3 6
(1)已知如下热化学方程式:
CH(g)+Br (g) CHBr(g)+HBr(g) ΔH=-29 kJ·mol-1
4 2 3 1
3CHBr(g) C H(g)+3HBr(g) ΔH=+20 kJ·mol-1
3 3 6 2计算反应3CH(g)+3Br (g) C H(g)+6HBr(g)的ΔH= kJ·mol-1。
4 2 3 6
(2)CH 与Br 反应生成CHBr,部分CHBr会进一步溴化。将8 mmol CH 和8 mmol Br 通入密闭容
4 2 3 3 4 2
器,平衡时,n(CH)、n(CHBr)与温度的关系见下图(假设反应后的含碳物质只有CH、CHBr和
4 3 4 3
CHBr )。
2 2
(ⅰ)图中CHBr的曲线是 (填“a”或“b”)。
3
(ⅱ)560 ℃时,CH 的转化率α= ,n(HBr)= mmol。
4
(ⅲ)560 ℃时,反应CHBr(g)+Br (g) CHBr (g)+HBr(g)的平衡常数K= 。
3 2 2 2
(3)少量I 可提高生成CHBr的选择性。500 ℃时,分别在有I 和无I 的条件下,将8 mmol CH 和8
2 3 2 2 4
mmol Br 通入密闭容器,溴代甲烷的物质的量(n)随时间(t)的变化关系见下图。
2
v(有I )
2
(ⅰ)在11~19 s之间,有I 和无I 时CHBr的生成速率之比 = 。
2 2 3 v(无I )
2
(ⅱ)从图中找出I 提高了CHBr选择性的证据: 。
2 3
(ⅲ)研究表明,I 参与反应的可能机理如下:
2
①I(g) I(g)+I(g)
2 · ·
②I(g)+CHBr (g) IBr(g)+CHBr(g)
· 2 2 · 2
③CHBr(g)+HBr(g) CHBr(g)+Br(g)
· 2 3 ·
④Br(g)+CH (g) HBr(g)+CH(g)
· 4 · 3
⑤CH(g)+IBr(g) CHBr(g)+I(g)
· 3 3 ·
⑥I(g)+I(g) I(g)
· · 2
根据上述机理,分析I 提高CHBr选择性的原因: 。
2 3
答案:(1)-67
(2)(ⅰ)a (ⅱ)80% 7.8 (ⅲ)10.923
(3)(ⅰ) (或3∶2) (ⅱ)5 s以后有I 催化的CHBr 的含量逐渐降低,有I 催化的CHBr的含量陡然上
2 2 2 2 2 3
升 (ⅲ)I 的投入消耗了部分CHBr ,使得消耗的CHBr 发生反应生成了CHBr
2 2 2 2 2 3
解析:(1)将第一个热化学方程式命名为①,将第二个热化学方程式命名为②。根据盖斯定律,将方程
式①乘以3再加上方程式②,即①×3+②,得热化学方程式3CH(g)+3Br (g) C H(g)+6HBr(g)的
4 2 3 6
ΔH=-29 kJ·mol-1×3+20 kJ·mol-1=-67 kJ·mol-1。
(2)(ⅰ)根据CH(g)+Br (g) CHBr(g)+HBr(g)为放热反应知,升高温度,平衡逆向移动,CH (g)的含量
4 2 3 4
增多,CH Br(g)的含量减少,故CHBr的曲线为a。
3 3
8 mmol-1.6 mmol
(ⅱ)560 ℃时反应达平衡,剩余的CH(g)的物质的量为1.6 mmol,其转化率α=
4 8 mmol
×100%=80%;若只发生一步反应,则生成6.4 mmol CH Br,但此时剩余CHBr的物质的量为5.0 mmol,
3 3
说明还有1.4 mmol CH Br发生反应生成CHBr ,则此时生成的HBr的物质的量n=6.4 mmol+1.4
3 2 2
mmol=7.8 mmol。
(ⅲ)由(ⅱ)分析知,平衡时,反应中各组分的物质的量分别为n(CHBr)=5.0 mmol,n(Br)=0.2
3 2
mmol,n(CHBr )=1.4 mmol,n(HBr)=7.8 mmol,故该反应的平衡常数K=
2 2
1.4 7.8
×
c(CH Br )·c(HBr) V V
2 2 = =10.92。
c(CH Br)·c(Br ) 5.0 0.2
3 2 ×
V V
3.2 2.6
- 0.075
(3)(ⅰ)11~19 s时,有I 的生成速率v= V V mol·L-1·s-1= mmol·L-1·s-1,无I 的生成速率
2 V 2
8
0.075
2.2 1.8
- 0.05 v(有I ) V 3
v= V V mol·L-1·s-1= mmol·L-1·s-1。生成速率之比 2 = = 。
V v(无I ) 0.05 2
8 2
V
(ⅱ)从图中可以看出,大约5 s以后有I 催化的CHBr 的含量逐渐降低,有I 催化的CHBr的含量陡然
2 2 2 2 3
上升,因此,可以利用此变化判断I 提高了CHBr的选择性。
2 3
(ⅲ)根据反应机理可知,I 的投入消耗了部分CHBr ,同时也消耗了部分HBr,使得消耗的CHBr 发生
2 2 2 2 2
反应生成了CHBr,提高了CHBr的选择性。
3 3
6.(14分)(2024·安徽卷)乙烯是一种用途广泛的有机化工原料。由乙烷制乙烯的研究备受关注。回答
下列问题:
【乙烷制乙烯】
(1)C H 氧化脱氢反应:
2 6
2C H(g)+O(g) 2C H(g)+2HO(g) ΔH=-209.8 kJ·mol-1
2 6 2 2 4 2 1
C H(g)+CO (g) C H(g)+HO(g)+CO(g) ΔH=+178.1 kJ·mol-1
2 6 2 2 4 2 2计算:2CO(g)+O (g) 2CO(g) ΔH= kJ·mol-1
2 2 3
(2)C H 直接脱氢反应为C H(g) C H(g)+H(g) ΔH,C H 的平衡转化率与温度和压强的关系如
2 6 2 6 2 4 2 4 2 6
图所示,则ΔH (填“>”“<”或“=”)0。结合图。下列条件中,达到平衡时转化率最接
4
近40%的是 (填字母)。
a.600 ℃,0.6 MPa
b.700 ℃,0.7 MPa
c.800 ℃,0.8 MPa
(3)一定温度和压强下,
反应ⅰ C H(g) C H(g)+H(g) K
2 6 2 4 2 a
1
反应ⅱ C H(g)+H(g) 2CH(g) K (K 远大于 K )
2 6 2 4 a a a
2 2 1
(K 是以平衡物质的量分数代替平衡浓度计算的平衡常数)
a
①仅发生反应ⅰ时,C H 的平衡转化率为25.0%,计算 K = 。
2 6 a
1
②同时发生反应ⅰ和ⅱ时,与仅发生反应ⅰ相比,C H 的平衡产率 (填“增大”“减小”
2 4
或“不变”)。
【乙烷和乙烯混合气的分离】
(4)通过Cu+修饰的Y分子筛的吸附-脱附,可实现C H 和C H 混合气的分离。Cu+的
2 4 2 6
与C H 分子的π键电子形成配位键,这种配位键强弱介于范德华力和共价键之间。用该分子筛分离
2 4
C H 和C H 的优点是 。
2 4 2 6
(5)常温常压下,将C H 和C H 等体积混合,以一定流速通过某吸附剂。测得两种气体出口浓度(c)与
2 4 2 6
进口浓度(c)之比随时间变化关系如图所示。下列推断合理的是 (填字母)。
0
A.前30 min,两种气体均未被吸附
B.p点对应的时刻,出口气体的主要成分是C H
2 6C.a~b对应的时间段内,吸附的C H 逐渐被C H 替代
2 6 2 4
1
答案:(1)-566 (2)> b (3)① ②增大 (4)4s空轨道 分离彻底,操作简单,能耗低 (5)BC
15
解析:(1)2CO(g)+O (g) 2CO(g)的焓变为ΔH-2ΔH=-566 kJ·mol-1。
2 2 1 2
(2)从图中可知,压强相同的情况下,随着温度升高,C H 的平衡转化率增大,因此该反应为吸热反
2 6
应,ΔH>0。600 ℃,0.6 MPa时,C H 的平衡转化率约为20%,a错误;700 ℃,0.7 MPa时,C H 的平衡转化
4 2 6 2 6
率约为50%,最接近40%,b正确;700 ℃,0.8 MPa时,C H 的平衡转化率接近50%,升高温度,该反应的化
2 6
学平衡正向移动,C H 转化率增大,因此800 ℃,0.8 MPa时,C H 的平衡转化率大于50%,c错误。故选
2 6 2 6
b。
(3)①设C H 的初始物质的量为1 mol,列三段式,代入数据计算,过程如下:
2 6
C H(g) C H(g) + H (g)
2 6 2 4 2
起始/mol 1 0 0
变化/mol 0.25 0.25 0.25
平衡/mol 0.75 0.25 0.25
0.25 0.25
×
1.25 1.25 1
K = =
a 1 0.75 15
1.25
②由题干信息“在一定温度和条件下”,只发生反应ⅰ时,随着反应进行,气体总物质的量增大,压强
增大促使化学平衡逆向移动;同时发生反应ⅰ和反应ⅱ,因 K 远大于 K ,C H 以反应ⅱ为主,反应ⅱ
a a 2 6
2 1
为等体积反应,但对反应ⅰ来说,反应ⅱ的发生相当于在单独发生反应ⅰ的基础上减小了压强,则反应
ⅰ化学平衡正向移动,C H 平衡产率增大。
2 4
(4)Cu+的4s空轨道与C H 分子的π键电子形成配位键。Cu+修饰的Y分子筛只吸附C H,使C H 与
2 4 2 4 2 4
C H 气体分离较彻底,且气体只要通过分子筛即可分离,所以操作简单。由于C H 与分子筛之间的作
2 6 2 4
用力较弱,所以C H 从分子筛上脱附时消耗的能量低。
2 4
c c
(5)前30 min, =0,出口浓度c为0,说明两种气体均被吸附,A错误;p点时,C H 对应的 ≈1.75,出口
c 2 6 c
0 0
c
处C H 浓度较大,而C H 对应的 较小,出口处C H 浓度较小,说明此时出口处气体的主要成分为
2 6 2 4 c 2 4
0
c c
C H,B正确;a点处C H 的 =1,说明此时C H 不再吸附在吸附剂上,而a点后C H 的 >1,说明原来
2 6 2 6 c 2 6 2 6 c
0 0
c
吸附的吸附剂上的C H 也开始脱落,同时从图中可知,a点后一段时间,C H 的 仍为0,说明是吸附的
2 6 2 4 c
0
C H 逐渐被C H 替代,p—b点之间,吸附的C H 仍在被C H 替代,但是速率相对之前有所减小,同时
2 6 2 4 2 6 2 4c
吸附剂可能因吸附量有限等原因无法一直吸附C H,因此p点后C H 的 也逐步增大,直至等于1,此
2 4 2 4 c
0
时吸附剂不能再吸附两种物质,C正确。