文档内容
主观题突破五
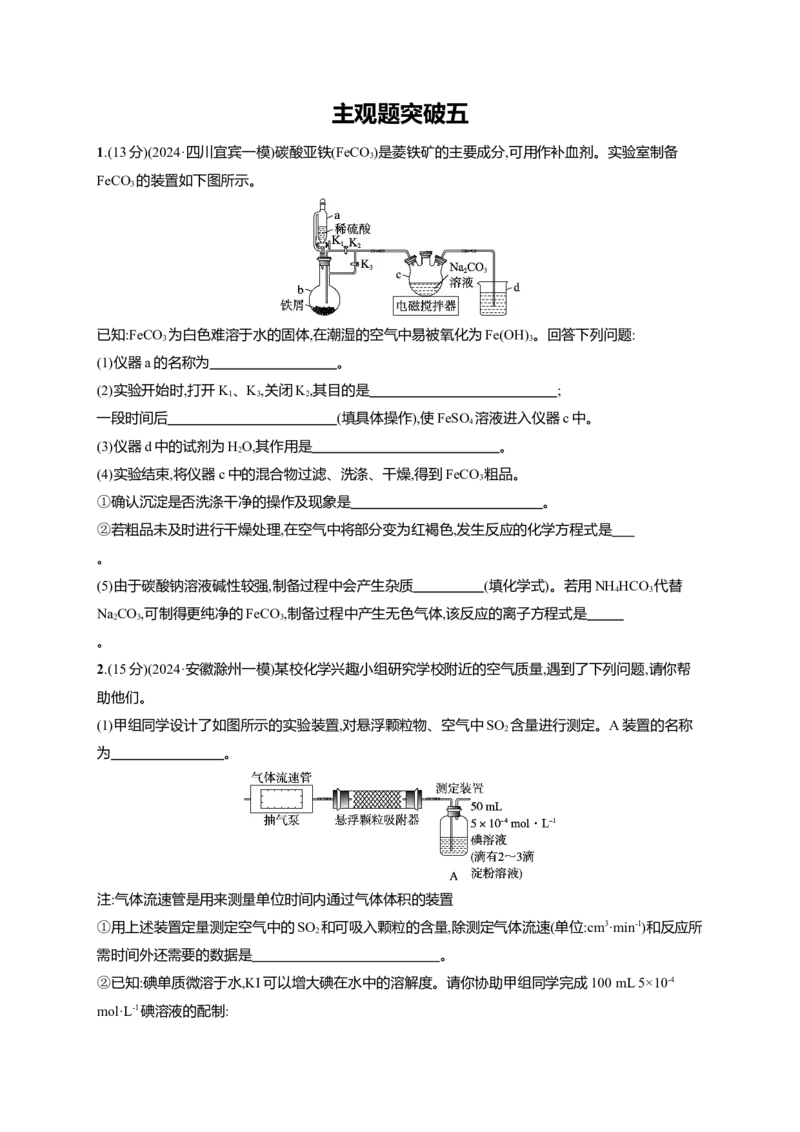
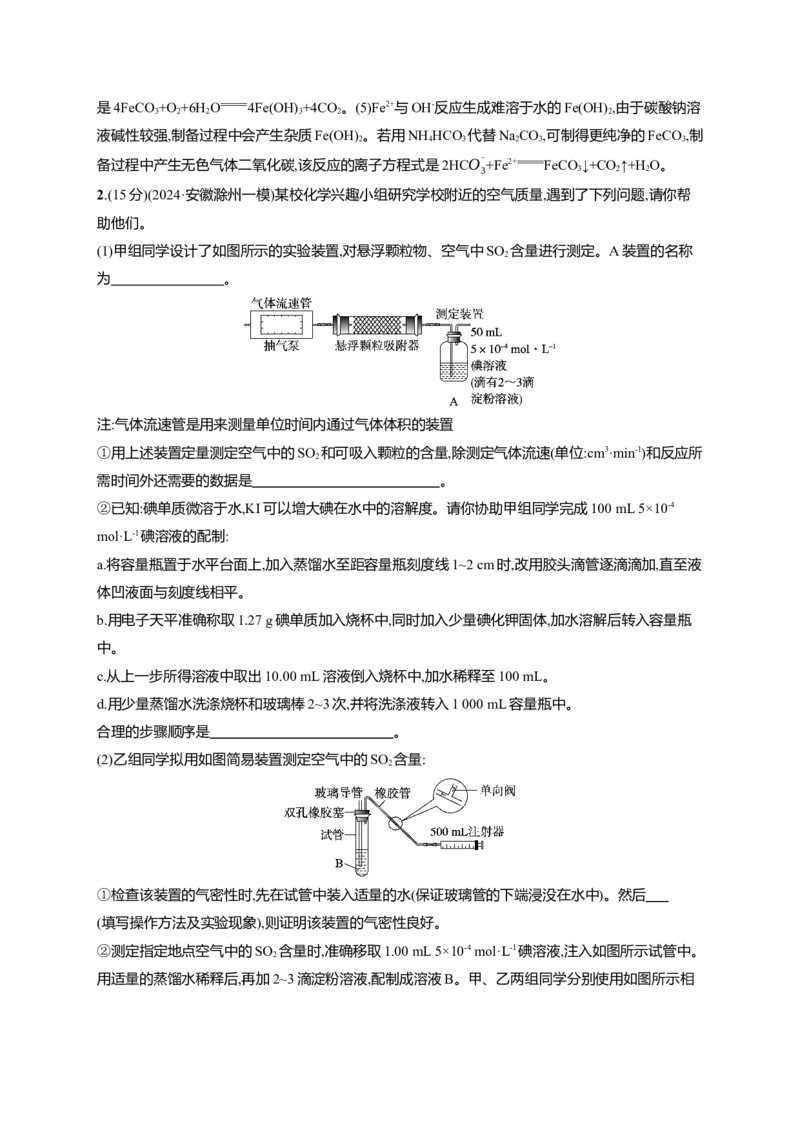
1.(13分)(2024·四川宜宾一模)碳酸亚铁(FeCO)是菱铁矿的主要成分,可用作补血剂。实验室制备
3
FeCO 的装置如下图所示。
3
已知:FeCO 为白色难溶于水的固体,在潮湿的空气中易被氧化为Fe(OH) 。回答下列问题:
3 3
(1)仪器a的名称为 。
(2)实验开始时,打开K、K,关闭K,其目的是 ;
1 3 2
一段时间后 (填具体操作),使FeSO 溶液进入仪器c中。
4
(3)仪器d中的试剂为HO,其作用是 。
2
(4)实验结束,将仪器c中的混合物过滤、洗涤、干燥,得到FeCO 粗品。
3
①确认沉淀是否洗涤干净的操作及现象是 。
②若粗品未及时进行干燥处理,在空气中将部分变为红褐色,发生反应的化学方程式是
。
(5)由于碳酸钠溶液碱性较强,制备过程中会产生杂质 (填化学式)。若用NH HCO 代替
4 3
NaCO,可制得更纯净的FeCO,制备过程中产生无色气体,该反应的离子方程式是
2 3 3
。
2.(15分)(2024·安徽滁州一模)某校化学兴趣小组研究学校附近的空气质量,遇到了下列问题,请你帮
助他们。
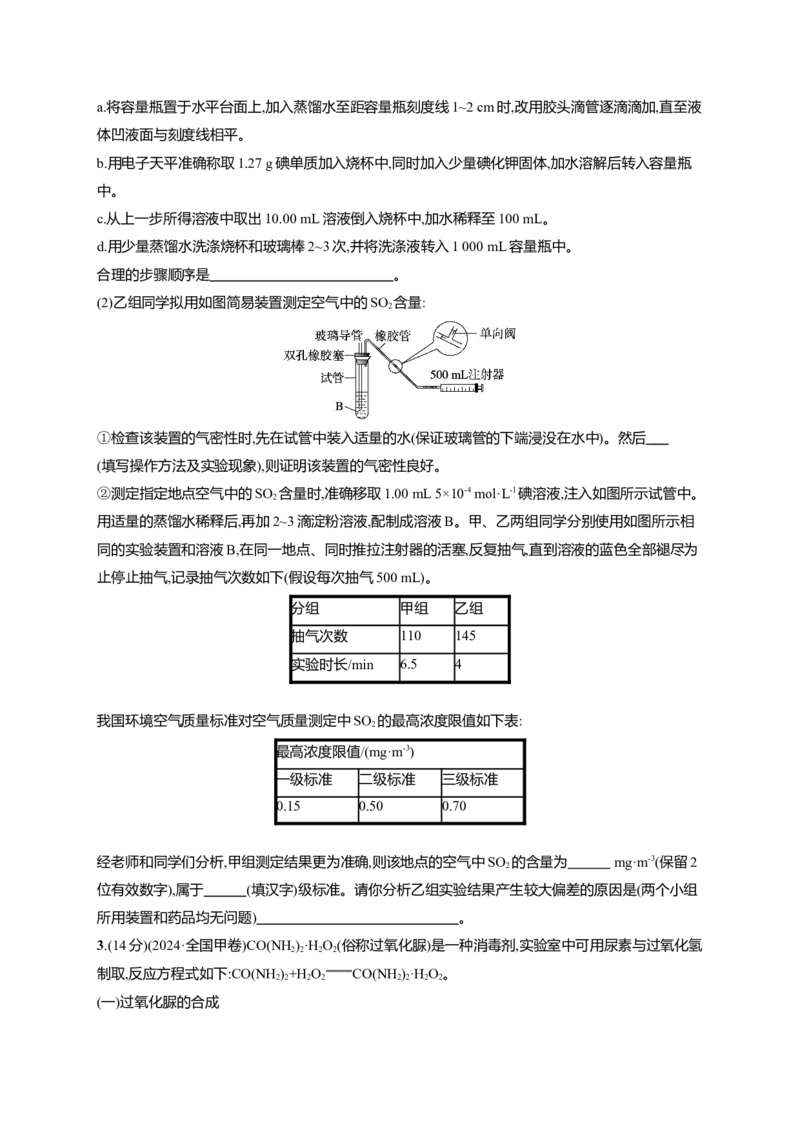
(1)甲组同学设计了如图所示的实验装置,对悬浮颗粒物、空气中SO 含量进行测定。A装置的名称
2
为 。
注:气体流速管是用来测量单位时间内通过气体体积的装置
①用上述装置定量测定空气中的SO 和可吸入颗粒的含量,除测定气体流速(单位:cm3·min-1)和反应所
2
需时间外还需要的数据是 。
②已知:碘单质微溶于水,KI可以增大碘在水中的溶解度。请你协助甲组同学完成100 mL 5×10-4
mol·L-1碘溶液的配制:a.将容量瓶置于水平台面上,加入蒸馏水至距容量瓶刻度线1~2 cm时,改用胶头滴管逐滴滴加,直至液
体凹液面与刻度线相平。
b.用电子天平准确称取1.27 g碘单质加入烧杯中,同时加入少量碘化钾固体,加水溶解后转入容量瓶
中。
c.从上一步所得溶液中取出10.00 mL溶液倒入烧杯中,加水稀释至100 mL。
d.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液转入1 000 mL容量瓶中。
合理的步骤顺序是 。
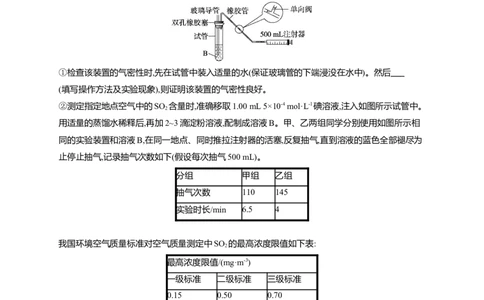
(2)乙组同学拟用如图简易装置测定空气中的SO 含量:
2
①检查该装置的气密性时,先在试管中装入适量的水(保证玻璃管的下端浸没在水中)。然后
(填写操作方法及实验现象),则证明该装置的气密性良好。
②测定指定地点空气中的SO 含量时,准确移取1.00 mL 5×10-4 mol·L-1碘溶液,注入如图所示试管中。
2
用适量的蒸馏水稀释后,再加2~3滴淀粉溶液,配制成溶液B。甲、乙两组同学分别使用如图所示相
同的实验装置和溶液B,在同一地点、同时推拉注射器的活塞,反复抽气,直到溶液的蓝色全部褪尽为
止停止抽气,记录抽气次数如下(假设每次抽气500 mL)。
分组 甲组 乙组
抽气次数 110 145
实验时长/min 6.5 4
我国环境空气质量标准对空气质量测定中SO 的最高浓度限值如下表:
2
最高浓度限值/(mg·m-3)
一级标准 二级标准 三级标准
0.15 0.50 0.70
经老师和同学们分析,甲组测定结果更为准确,则该地点的空气中SO 的含量为 mg·m-3(保留2
2
位有效数字),属于 (填汉字)级标准。请你分析乙组实验结果产生较大偏差的原因是(两个小组
所用装置和药品均无问题) 。
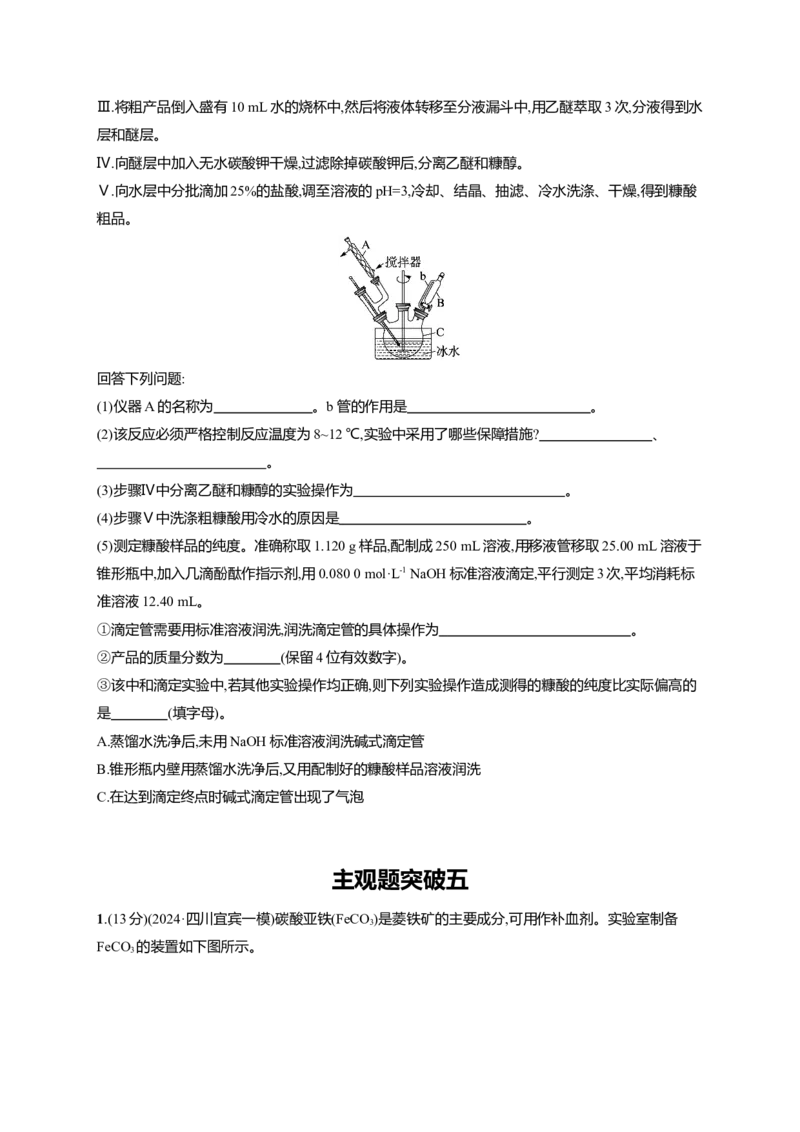
3.(14分)(2024·全国甲卷)CO(NH)·H O(俗称过氧化脲)是一种消毒剂,实验室中可用尿素与过氧化氢
2 2 2 2
制取,反应方程式如下:CO(NH )+H O CO(NH)·H O。
2 2 2 2 2 2 2 2
(一)过氧化脲的合成烧杯中分别加入25 mL 30% HO(ρ=1.11 g·cm-3)、40 mL蒸馏水和12.0 g尿素,搅拌溶解。30 ℃下反
2 2
应40 min,冷却结晶、过滤、干燥,得白色针状晶体9.4 g。
(二)过氧化脲性质检测
Ⅰ.过氧化脲溶液用稀硫酸酸化后,滴加KMnO 溶液,紫红色消失。
4
Ⅱ.过氧化脲溶液用稀硫酸酸化后,加入KI溶液和四氯化碳,振荡,静置。
(三)产品纯度测定
溶液配制:称取一定量产品,用蒸馏水溶解后配制成100 mL溶液。
滴定分析:量取25.00 mL过氧化脲溶液至锥形瓶中,加入一定量稀硫酸,用准确浓度的KMnO 溶液滴
4
定至微红色,记录滴定体积,计算纯度。
回答下列问题:
(1)过滤中使用到的玻璃仪器有 (写出两种即可)。
(2)过氧化脲的产率为 。
(3)性质检测Ⅱ中的现象为 。性质检测Ⅰ和Ⅱ分别说明过氧化
脲具有的性质是 。
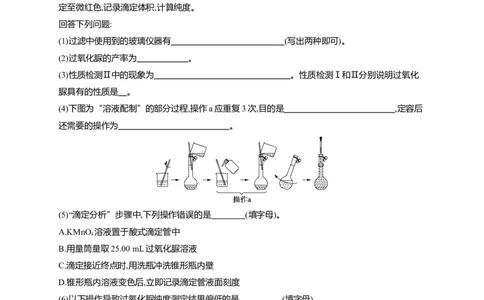
(4)下图为“溶液配制”的部分过程,操作a应重复3次,目的是 ,定容后
还需要的操作为 。
(5)“滴定分析”步骤中,下列操作错误的是 (填字母)。
A.KMnO 溶液置于酸式滴定管中
4
B.用量筒量取25.00 mL过氧化脲溶液
C.滴定接近终点时,用洗瓶冲洗锥形瓶内壁
D.锥形瓶内溶液变色后,立即记录滴定管液面刻度
(6)以下操作导致过氧化脲纯度测定结果偏低的是 (填字母)。
A.容量瓶中液面超过刻度线
B.滴定管水洗后未用KMnO 溶液润洗
4
C.摇动锥形瓶时KMnO 溶液滴到锥形瓶外
4
D.滴定前滴定管尖嘴处有气泡,滴定后气泡消失
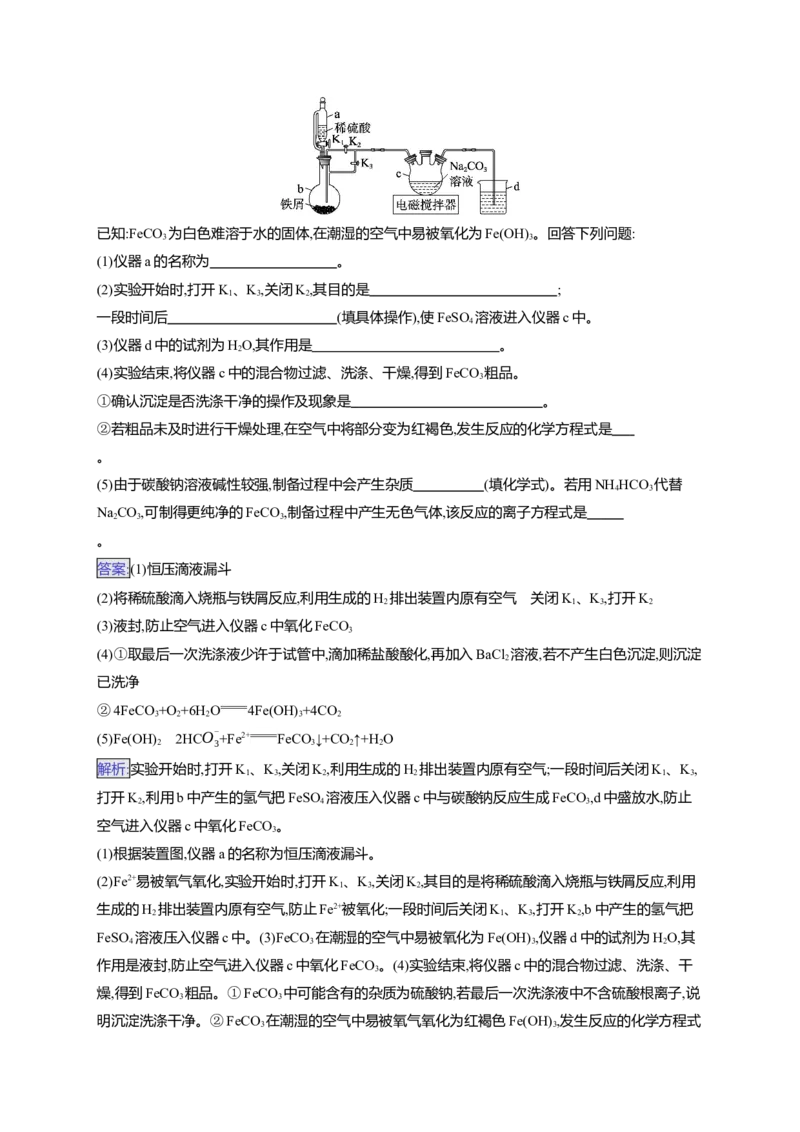
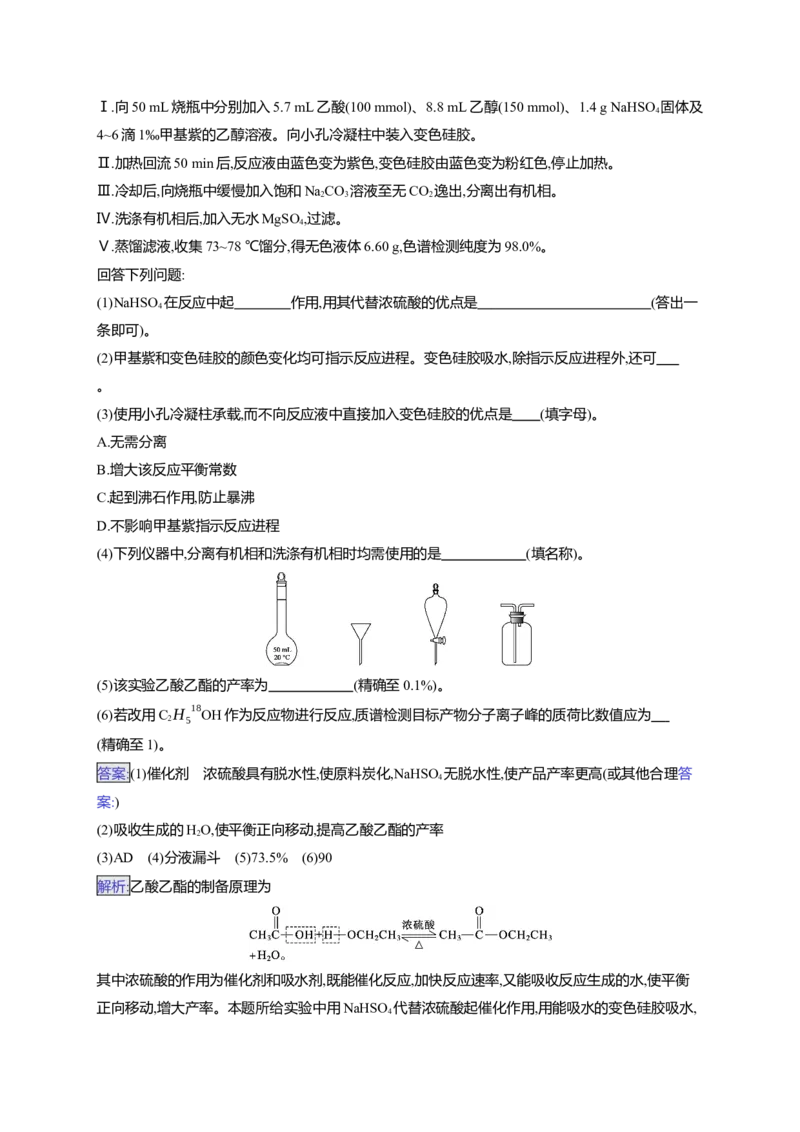
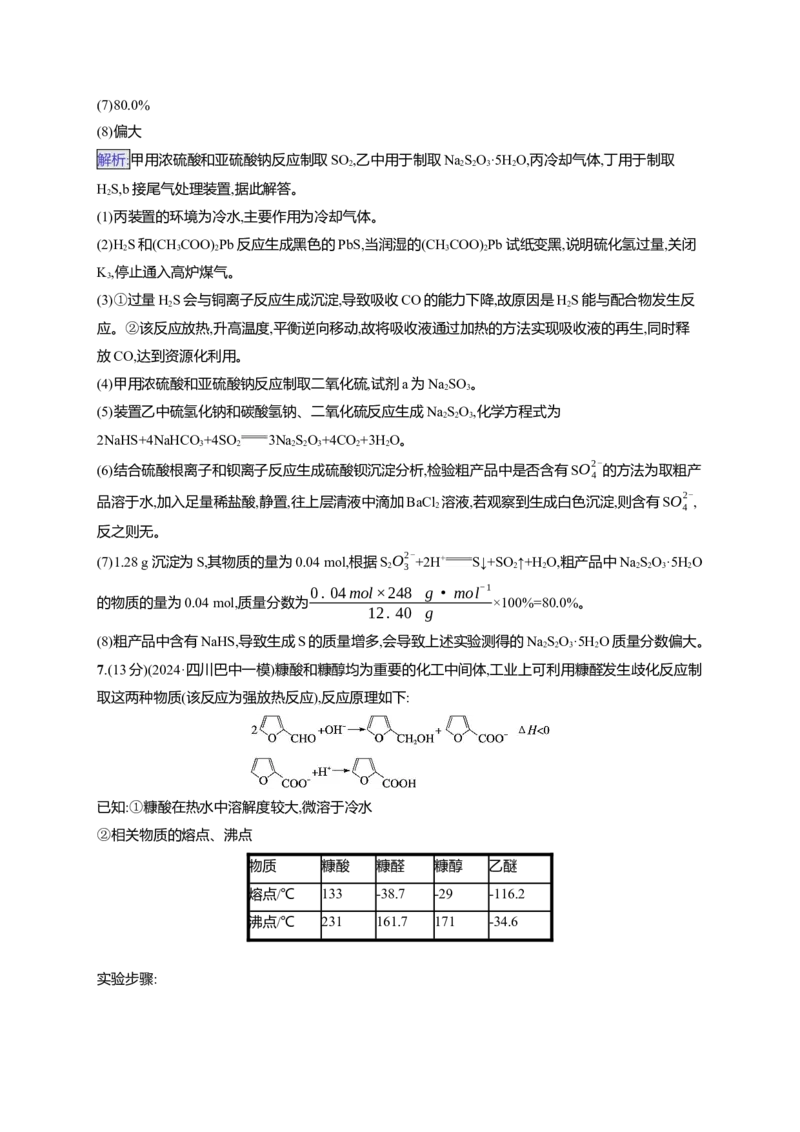
4.(14分)(2024·黑吉辽卷)某实验小组为实现乙酸乙酯的绿色制备及反应过程可视化,设计实验方案如
下:Ⅰ.向50 mL烧瓶中分别加入5.7 mL乙酸(100 mmol)、8.8 mL乙醇(150 mmol)、1.4 g NaHSO 固体及
4
4~6滴1‰甲基紫的乙醇溶液。向小孔冷凝柱中装入变色硅胶。
Ⅱ.加热回流50 min后,反应液由蓝色变为紫色,变色硅胶由蓝色变为粉红色,停止加热。
Ⅲ.冷却后,向烧瓶中缓慢加入饱和NaCO 溶液至无CO 逸出,分离出有机相。
2 3 2
Ⅳ.洗涤有机相后,加入无水MgSO ,过滤。
4
Ⅴ.蒸馏滤液,收集73~78 ℃馏分,得无色液体6.60 g,色谱检测纯度为98.0%。
回答下列问题:
(1)NaHSO 在反应中起 作用,用其代替浓硫酸的优点是 (答出一
4
条即可)。
(2)甲基紫和变色硅胶的颜色变化均可指示反应进程。变色硅胶吸水,除指示反应进程外,还可
。
(3)使用小孔冷凝柱承载,而不向反应液中直接加入变色硅胶的优点是 (填字母)。
A.无需分离
B.增大该反应平衡常数
C.起到沸石作用,防止暴沸
D.不影响甲基紫指示反应进程
(4)下列仪器中,分离有机相和洗涤有机相时均需使用的是 (填名称)。
(5)该实验乙酸乙酯的产率为 (精确至0.1%)。
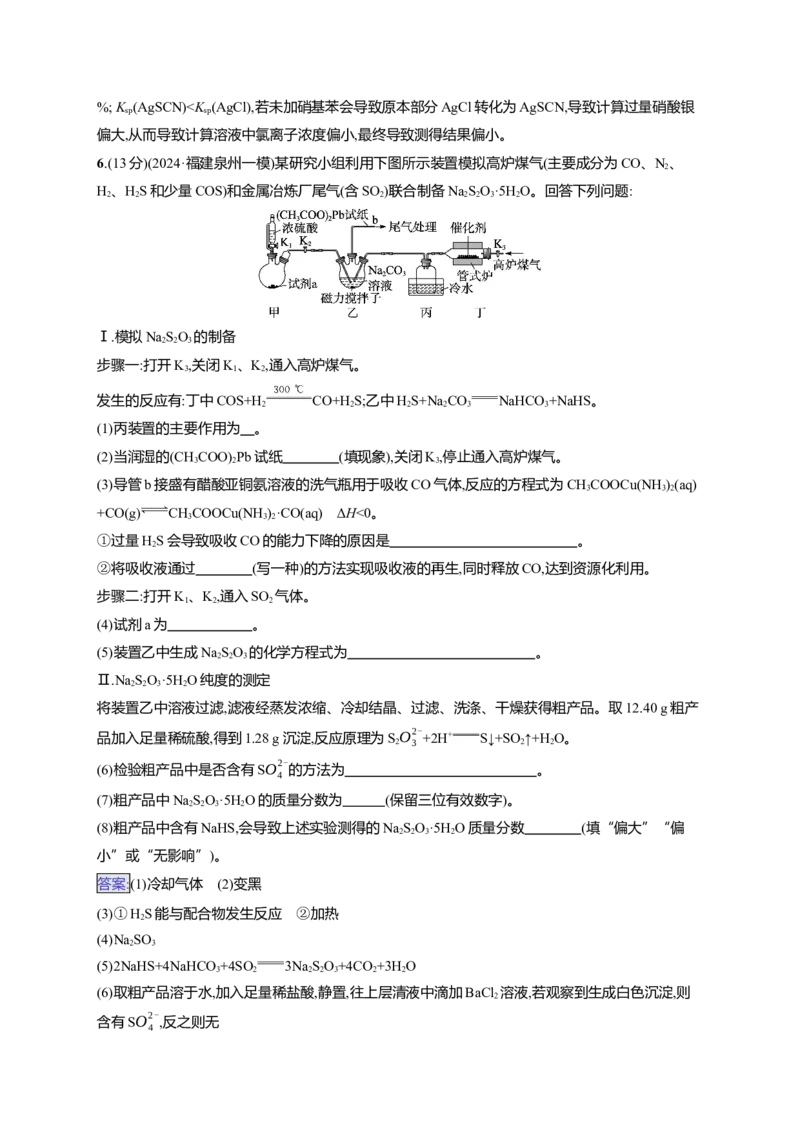
(6)若改用C H 18 OH作为反应物进行反应,质谱检测目标产物分子离子峰的质荷比数值应为
2 5
(精确至1)。
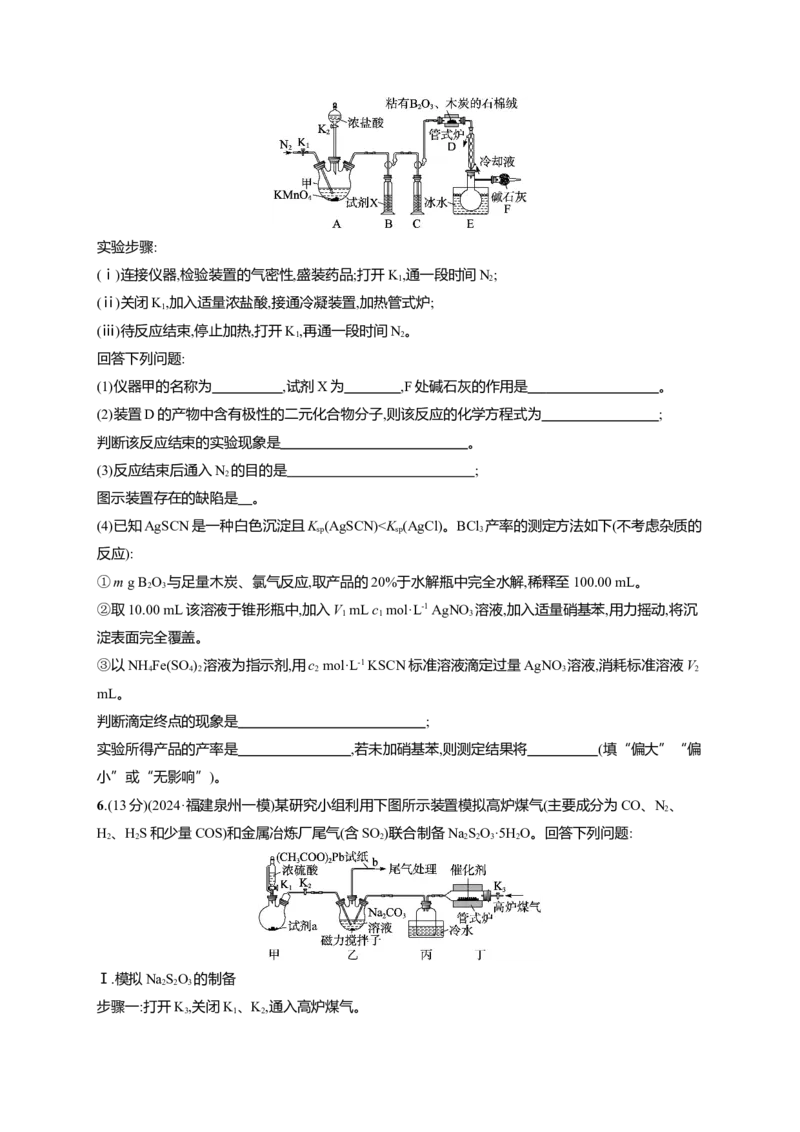
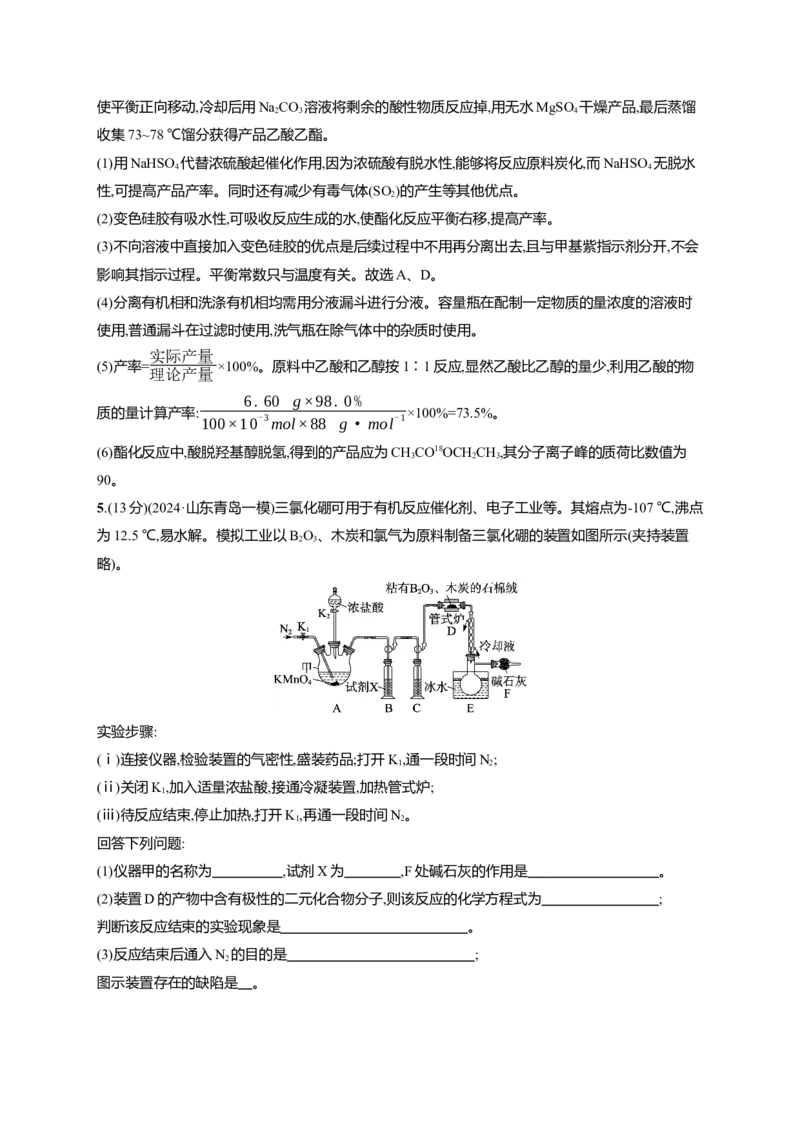
5.(13分)(2024·山东青岛一模)三氯化硼可用于有机反应催化剂、电子工业等。其熔点为-107 ℃,沸点
为12.5 ℃,易水解。模拟工业以B O、木炭和氯气为原料制备三氯化硼的装置如图所示(夹持装置
2 3
略)。实验步骤:
(ⅰ)连接仪器,检验装置的气密性,盛装药品;打开K,通一段时间N;
1 2
(ⅱ)关闭K,加入适量浓盐酸,接通冷凝装置,加热管式炉;
1
(ⅲ)待反应结束,停止加热,打开K,再通一段时间N。
1 2
回答下列问题:
(1)仪器甲的名称为 ,试剂X为 ,F处碱石灰的作用是 。
(2)装置D的产物中含有极性的二元化合物分子,则该反应的化学方程式为 ;
判断该反应结束的实验现象是 。
(3)反应结束后通入N 的目的是 ;
2
图示装置存在的缺陷是 。
(4)已知AgSCN是一种白色沉淀且K (AgSCN)