文档内容
大题突破练(一) 化学工艺流程题
1.(2024·河北卷)V O 是制造钒铁合金、金属钒的原料,也是重要的催化剂。以苛化泥为焙烧添加剂
2 5
从石煤中提取VO 的工艺,具有钒回收率高、副产物可回收和不产生气体污染物等优点。工艺流程
2 5
如下。
已知:ⅰ.石煤是一种含VO 的矿物,杂质为大量Al O 和少量CaO等;苛化泥的主要成分为CaCO 、
2 3 2 3 3
NaOH、NaCO 等。
2 3
ⅱ.高温下,苛化泥的主要成分可与Al O 反应生成偏铝酸盐;室温下,偏钒酸钙[Ca(VO )]和偏铝酸钙
2 3 3 2
均难溶于水。
回答下列问题:
(1)钒原子的价层电子排布式为 ;焙烧生成的偏钒酸盐中钒的化合价为 ,产生
的气体①为 (填化学式)。
(2)水浸工序得到滤渣①和滤液,滤渣①中含钒成分为偏钒酸钙,滤液中杂质的主要成分为
(填化学式)。
(3)在弱碱性环境下,偏钒酸钙经盐浸生成碳酸钙,发生反应的离子方程式为
;CO 加压导入盐浸工序可提高浸出率的原因为 ;浸取后
2
低浓度的滤液①进入 (填工序名称),可实现钒元素的充分利用。
(4)洗脱工序中洗脱液的主要成分为 (填化学式)。
(5)下列不利于沉钒过程的两种操作为 (填字母)。
a.延长沉钒时间
b.将溶液调至碱性
c.搅拌
d.降低NH Cl溶液的浓度
4
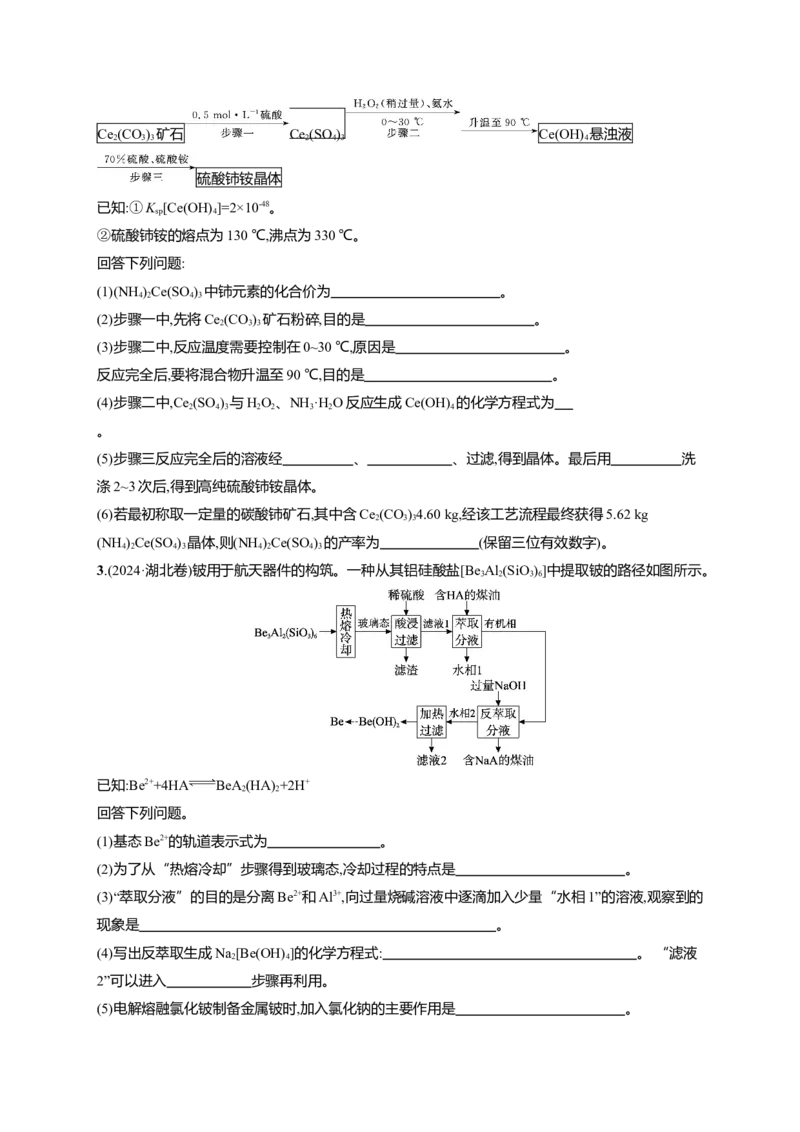
2.(2024·广西北海一模)硫酸铈铵[(NH )Ce(SO)]微溶于水,不溶于乙醇,溶于无机酸,可用作分析试剂、
4 2 4 3
氧化剂。某工厂用碳酸铈[Ce (CO)]矿石制备硫酸铈铵的工艺流程如图:
2 3 3Ce (CO) 矿石 Ce (SO ) Ce(OH) 悬浊液
2 3 3 2 4 3 4
硫酸铈铵晶体
已知:①K [Ce(OH) ]=2×10-48。
sp 4
②硫酸铈铵的熔点为130 ℃,沸点为330 ℃。
回答下列问题:
(1)(NH )Ce(SO) 中铈元素的化合价为 。
4 2 4 3
(2)步骤一中,先将Ce (CO) 矿石粉碎,目的是 。
2 3 3
(3)步骤二中,反应温度需要控制在0~30 ℃,原因是 。
反应完全后,要将混合物升温至90 ℃,目的是 。
(4)步骤二中,Ce (SO ) 与HO、NH ·H O反应生成Ce(OH) 的化学方程式为
2 4 3 2 2 3 2 4
。
(5)步骤三反应完全后的溶液经 、 、过滤,得到晶体。最后用 洗
涤2~3次后,得到高纯硫酸铈铵晶体。
(6)若最初称取一定量的碳酸铈矿石,其中含Ce (CO)4.60 kg,经该工艺流程最终获得5.62 kg
2 3 3
(NH )Ce(SO) 晶体,则(NH )Ce(SO) 的产率为 (保留三位有效数字)。
4 2 4 3 4 2 4 3
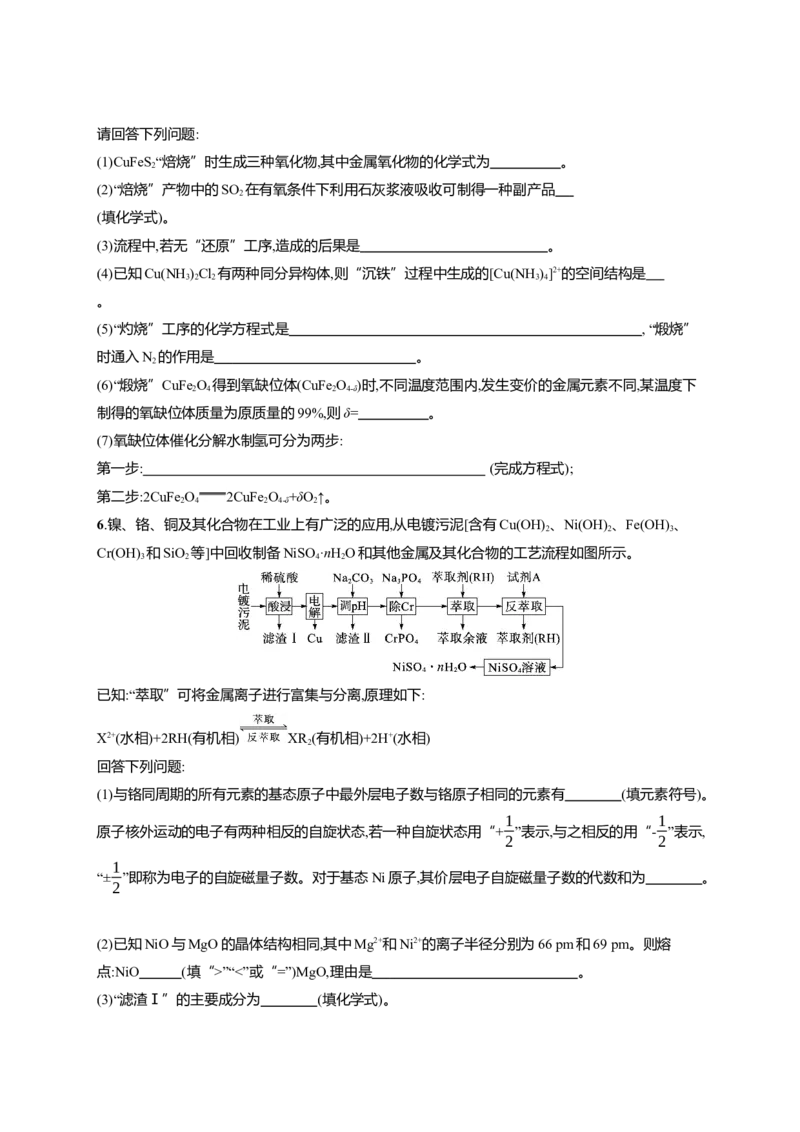
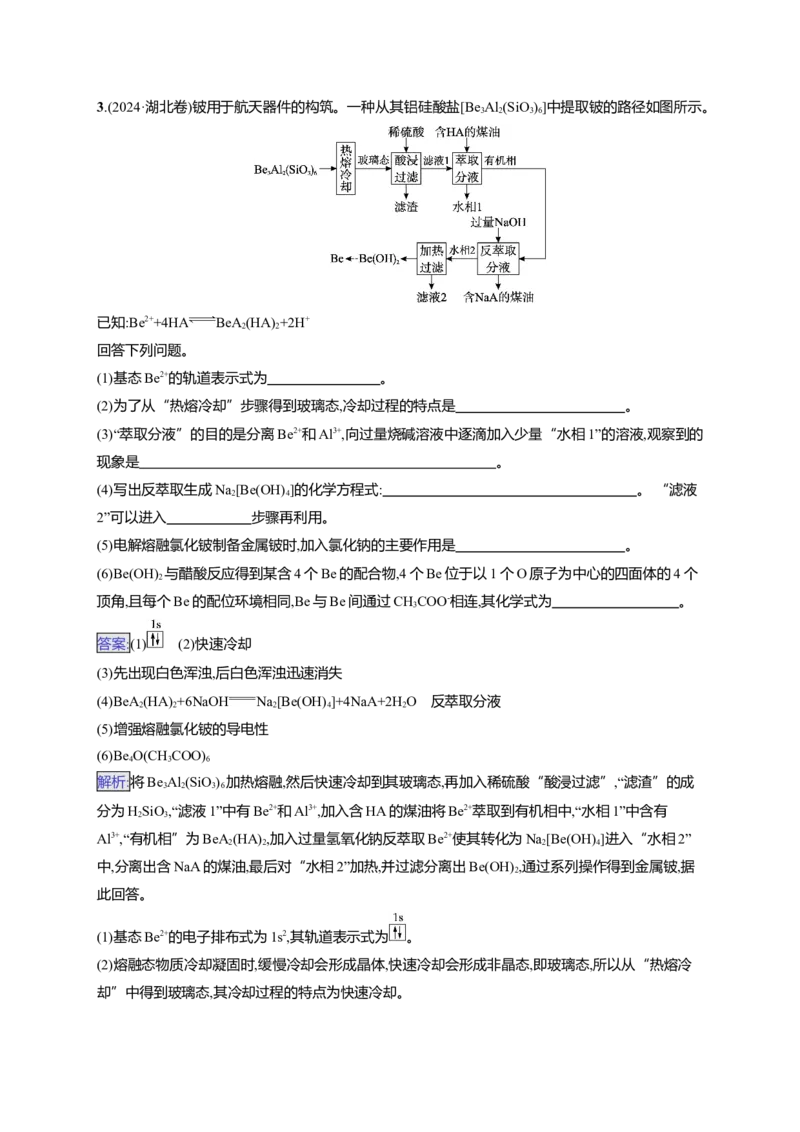
3.(2024·湖北卷)铍用于航天器件的构筑。一种从其铝硅酸盐[Be Al (SiO)]中提取铍的路径如图所示。
3 2 3 6
已知:Be2++4HA BeA(HA) +2H+
2 2
回答下列问题。
(1)基态Be2+的轨道表示式为 。
(2)为了从“热熔冷却”步骤得到玻璃态,冷却过程的特点是 。
(3)“萃取分液”的目的是分离Be2+和Al3+,向过量烧碱溶液中逐滴加入少量“水相1”的溶液,观察到的
现象是 。
(4)写出反萃取生成Na[Be(OH) ]的化学方程式: 。 “滤液
2 4
2”可以进入 步骤再利用。
(5)电解熔融氯化铍制备金属铍时,加入氯化钠的主要作用是 。(6)Be(OH) 与醋酸反应得到某含4个Be的配合物,4个Be位于以1个O原子为中心的四面体的4个
2
顶角,且每个Be的配位环境相同,Be与Be间通过CHCOO-相连,其化学式为 。
3
4.(2024·吉林白山二模)钪(Sc)及其化合物在电子、超导合金和催化剂等领域有重要应用。一种利用
钛白废酸液(含Sc3+、TiO2+、Fe3+的硫酸废液)和赤泥(含有Sc O、Al O、Fe O、SiO)联合制备
2 3 2 3 2 3 2
Sc O 的工艺流程如图所示。回答下列问题:
2 3
已知:25 ℃时,K [Sc(OH) ]=1×10-30。
sp 3
(1)基态Fe3+的简化电子排布式为 。
(2)为提高“浸取”速率,可采取的措施有 (写出一条即可),“浸
渣”的主要成分是 (写化学式);水相中含有的金属离子主要是 (写离
子符号)。
(3)“除钛”时,加入HO 的作用是 。
2 2
(4)25 ℃时,若使“反萃取”后水溶液中的Sc3+沉淀完全(离子浓度≤10-5 mol·L-1),应控制溶液的pH不
低于 (保留两位有效数字)。
(5)写出草酸钪晶体[Sc (C O)·6H O]“灼烧”时发生反应的化学方程式:
2 2 4 3 2
。
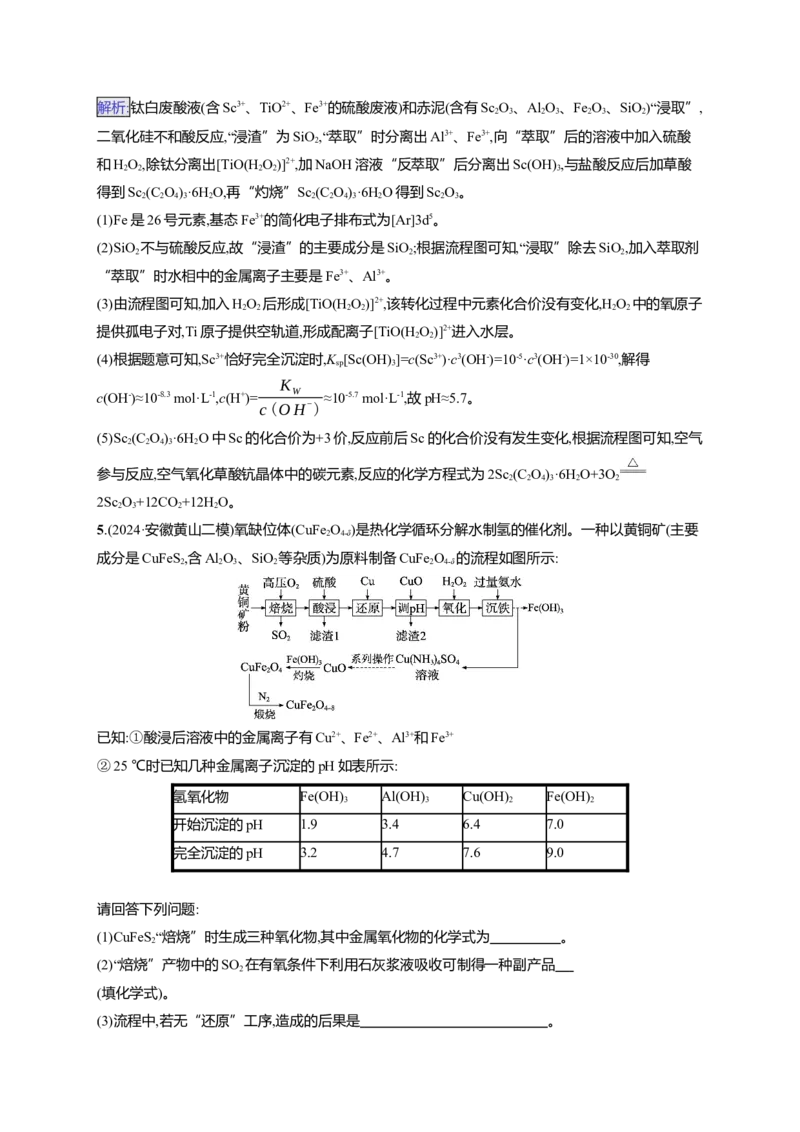
5.(2024·安徽黄山二模)氧缺位体(CuFe O )是热化学循环分解水制氢的催化剂。一种以黄铜矿(主要
2 4-δ
成分是CuFeS,含Al O、SiO 等杂质)为原料制备CuFe O 的流程如图所示:
2 2 3 2 2 4-δ
已知:①酸浸后溶液中的金属离子有Cu2+、Fe2+、Al3+和Fe3+
②25 ℃时已知几种金属离子沉淀的pH如表所示:
氢氧化物 Fe(OH) Al(OH) Cu(OH) Fe(OH)
3 3 2 2
开始沉淀的pH 1.9 3.4 6.4 7.0
完全沉淀的pH 3.2 4.7 7.6 9.0请回答下列问题:
(1)CuFeS “焙烧”时生成三种氧化物,其中金属氧化物的化学式为 。
2
(2)“焙烧”产物中的SO 在有氧条件下利用石灰浆液吸收可制得一种副产品
2
(填化学式)。
(3)流程中,若无“还原”工序,造成的后果是 。
(4)已知Cu(NH )Cl 有两种同分异构体,则“沉铁”过程中生成的[Cu(NH )]2+的空间结构是
3 2 2 3 4
。
(5)“灼烧”工序的化学方程式是 , “煅烧”
时通入N 的作用是 。
2
(6)“煅烧”CuFe O 得到氧缺位体(CuFe O )时,不同温度范围内,发生变价的金属元素不同,某温度下
2 4 2 4-δ
制得的氧缺位体质量为原质量的99%,则δ= 。
(7)氧缺位体催化分解水制氢可分为两步:
第一步: (完成方程式);
第二步:2CuFe O 2CuFe O +δO↑。
2 4 2 4-δ 2
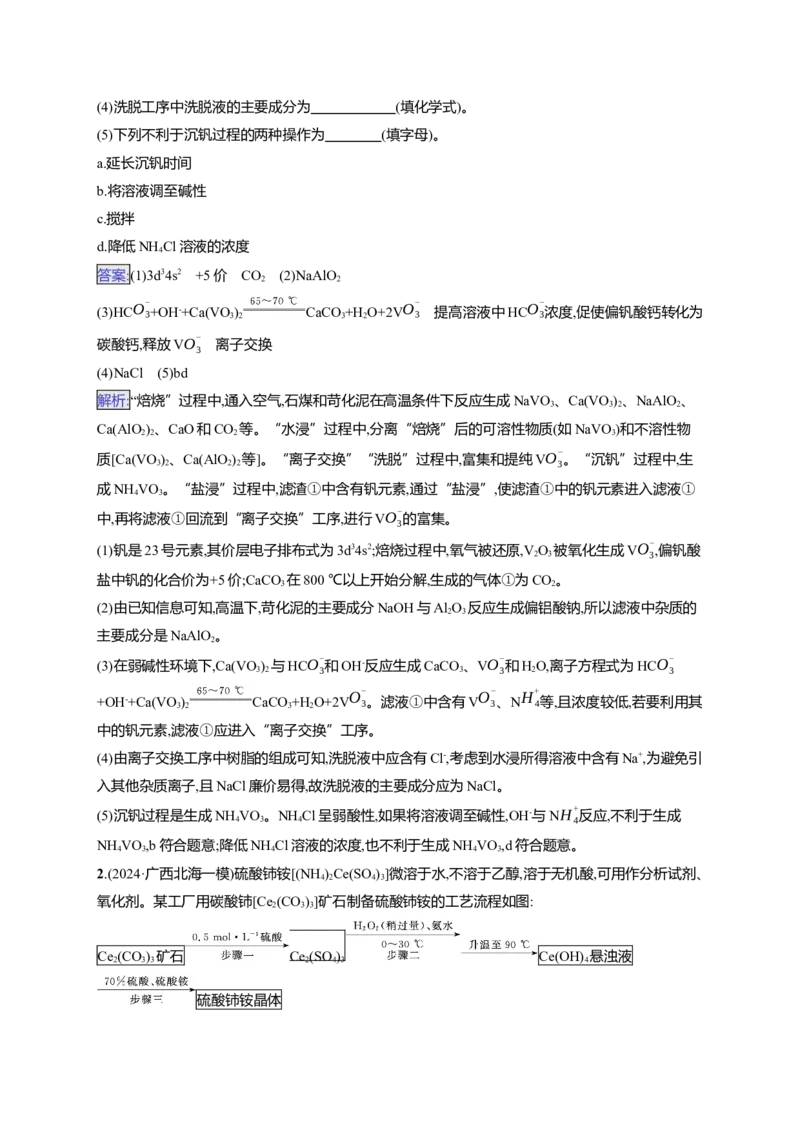
6.镍、铬、铜及其化合物在工业上有广泛的应用,从电镀污泥[含有Cu(OH) 、Ni(OH) 、Fe(OH) 、
2 2 3
Cr(OH) 和SiO 等]中回收制备NiSO ·nHO和其他金属及其化合物的工艺流程如图所示。
3 2 4 2
已知:“萃取”可将金属离子进行富集与分离,原理如下:
X2+(水相)+2RH(有机相) XR (有机相)+2H+(水相)
2
回答下列问题:
(1)与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有 (填元素符号)。
1 1
原子核外运动的电子有两种相反的自旋状态,若一种自旋状态用“+ ”表示,与之相反的用“- ”表示,
2 2
1
“± ”即称为电子的自旋磁量子数。对于基态Ni原子,其价层电子自旋磁量子数的代数和为 。
2
(2)已知NiO与MgO的晶体结构相同,其中Mg2+和Ni2+的离子半径分别为66 pm和69 pm。则熔
点:NiO (填“>”“<”或“=”)MgO,理由是 。
(3)“滤渣Ⅰ”的主要成分为 (填化学式)。(4)电解之后加入碳酸钠调节pH的目的是 。
(5)“反萃取”时加入的试剂A为 。
(6)“反萃取”得到的NiSO 溶液,在碱性条件下可被NaClO氧化生成NiOOH沉淀,该反应的离子方程
4
式为 。
(7)资料显示,硫酸镍结晶水合物的形态与温度有如表关系:
温度 低于30.8 ℃ 30.8~53.8 ℃ 53.8~280 ℃ 高于280 ℃
晶体形态 NiSO ·7H O NiSO ·6H O 多种结晶水合物 NiSO
4 2 4 2 4
由NiSO 溶液获得NiSO ·7H O晶体的操作依次是蒸发浓缩、 、 过滤、洗涤、干燥。
4 4 2
大题突破练(一) 化学工艺流程题
1.(2024·河北卷)V O 是制造钒铁合金、金属钒的原料,也是重要的催化剂。以苛化泥为焙烧添加剂
2 5
从石煤中提取VO 的工艺,具有钒回收率高、副产物可回收和不产生气体污染物等优点。工艺流程
2 5
如下。
已知:ⅰ.石煤是一种含VO 的矿物,杂质为大量Al O 和少量CaO等;苛化泥的主要成分为CaCO 、
2 3 2 3 3
NaOH、NaCO 等。
2 3
ⅱ.高温下,苛化泥的主要成分可与Al O 反应生成偏铝酸盐;室温下,偏钒酸钙[Ca(VO )]和偏铝酸钙
2 3 3 2
均难溶于水。
回答下列问题:
(1)钒原子的价层电子排布式为 ;焙烧生成的偏钒酸盐中钒的化合价为 ,产生
的气体①为 (填化学式)。
(2)水浸工序得到滤渣①和滤液,滤渣①中含钒成分为偏钒酸钙,滤液中杂质的主要成分为
(填化学式)。
(3)在弱碱性环境下,偏钒酸钙经盐浸生成碳酸钙,发生反应的离子方程式为
;CO 加压导入盐浸工序可提高浸出率的原因为 ;浸取后
2
低浓度的滤液①进入 (填工序名称),可实现钒元素的充分利用。(4)洗脱工序中洗脱液的主要成分为 (填化学式)。
(5)下列不利于沉钒过程的两种操作为 (填字母)。
a.延长沉钒时间
b.将溶液调至碱性
c.搅拌
d.降低NH Cl溶液的浓度
4
答案:(1)3d34s2 +5价 CO (2)NaAlO
2 2
(3)HC O
3
- +OH-+Ca(VO
3
)
2
CaCO
3
+H
2
O+2V O
3
- 提高溶液中HC O
3
- 浓度,促使偏钒酸钙转化为
碳酸钙,释放VO-
离子交换
3
(4)NaCl (5)bd
解析:“焙烧”过程中,通入空气,石煤和苛化泥在高温条件下反应生成NaVO 、Ca(VO )、NaAlO 、
3 3 2 2
Ca(AlO)、CaO和CO 等。“水浸”过程中,分离“焙烧”后的可溶性物质(如NaVO )和不溶性物
2 2 2 3
质[Ca(VO )、Ca(AlO)
等]。“离子交换”“洗脱”过程中,富集和提纯VO-
。“沉钒”过程中,生
3 2 2 2 3
成NH VO 。“盐浸”过程中,滤渣①中含有钒元素,通过“盐浸”,使滤渣①中的钒元素进入滤液①
4 3
中,再将滤液①回流到“离子交换”工序,进行VO-
的富集。
3
(1)钒是23号元素,其价层电子排布式为3d34s2;焙烧过程中,氧气被还原,V O
被氧化生成VO-
,偏钒酸
2 3 3
盐中钒的化合价为+5价;CaCO 在800 ℃以上开始分解,生成的气体①为CO。
3 2
(2)由已知信息可知,高温下,苛化泥的主要成分NaOH与Al O 反应生成偏铝酸钠,所以滤液中杂质的
2 3
主要成分是NaAlO 。
2
(3)在弱碱性环境下,Ca(VO )
与HCO-
和OH-反应生成CaCO
、VO- 和HO,离子方程式为HCO-
3 2 3 3 3 2 3
O- O- H+
+OH-+Ca(VO
3
)
2
CaCO
3
+H
2
O+2V 3。滤液①中含有V 3、N 4等,且浓度较低,若要利用其
中的钒元素,滤液①应进入“离子交换”工序。
(4)由离子交换工序中树脂的组成可知,洗脱液中应含有Cl-,考虑到水浸所得溶液中含有Na+,为避免引
入其他杂质离子,且NaCl廉价易得,故洗脱液的主要成分应为NaCl。
(5)沉钒过程是生成NH VO 。NH
Cl呈弱酸性,如果将溶液调至碱性,OH-与NH+
反应,不利于生成
4 3 4 4
NH VO ,b符合题意;降低NH Cl溶液的浓度,也不利于生成NH VO ,d符合题意。
4 3 4 4 3
2.(2024·广西北海一模)硫酸铈铵[(NH )Ce(SO)]微溶于水,不溶于乙醇,溶于无机酸,可用作分析试剂、
4 2 4 3
氧化剂。某工厂用碳酸铈[Ce (CO)]矿石制备硫酸铈铵的工艺流程如图:
2 3 3
Ce (CO) 矿石 Ce (SO ) Ce(OH) 悬浊液
2 3 3 2 4 3 4
硫酸铈铵晶体已知:①K [Ce(OH) ]=2×10-48。
sp 4
②硫酸铈铵的熔点为130 ℃,沸点为330 ℃。
回答下列问题:
(1)(NH )Ce(SO) 中铈元素的化合价为 。
4 2 4 3
(2)步骤一中,先将Ce (CO) 矿石粉碎,目的是 。
2 3 3
(3)步骤二中,反应温度需要控制在0~30 ℃,原因是 。
反应完全后,要将混合物升温至90 ℃,目的是 。
(4)步骤二中,Ce (SO ) 与HO、NH ·H O反应生成Ce(OH) 的化学方程式为
2 4 3 2 2 3 2 4
。
(5)步骤三反应完全后的溶液经 、 、过滤,得到晶体。最后用 洗
涤2~3次后,得到高纯硫酸铈铵晶体。
(6)若最初称取一定量的碳酸铈矿石,其中含Ce (CO)4.60 kg,经该工艺流程最终获得5.62 kg
2 3 3
(NH )Ce(SO) 晶体,则(NH )Ce(SO) 的产率为 (保留三位有效数字)。
4 2 4 3 4 2 4 3
答案:(1)+4价
(2)增大溶解过程中固体与稀硫酸的接触面积,加快溶解速率
(3)温度过高会导致过氧化氢分解、氨水挥发 除去过量的过氧化氢
(4)Ce (SO )+H O+6NH·H O 2Ce(OH) ↓+3(NH)SO
2 4 3 2 2 3 2 4 4 2 4
(5)蒸发浓缩 冷却结晶 乙醇
(6)60.6%
解析:碳酸铈[Ce (CO)]矿石用硫酸浸取,Ce3+进入溶液,加入过氧化氢将+3价Ce氧化为+4价Ce,加入
2 3 3
氨水升温至90 ℃得到Ce(OH) 悬浊液,加入硫酸、硫酸铵得到硫酸铈铵晶体。
4
(1)(NH )Ce(SO) 中铵根、硫酸根化合价分别为+1、-2价,根据化合价代数和为零,可知铈元素的化
4 2 4 3
合价为+4价。
(3)过氧化氢不稳定、氨水易挥发,所以反应温度需要控制在0~30 ℃。反应完全后,要将混合物升温
至90 ℃,目的是除去过量的过氧化氢。
(4)Ce (SO ) 与HO、NH ·H O反应生成Ce(OH) ,反应中Ce化合价由+3价变为+4价、过氧化氢中
2 4 3 2 2 3 2 4
氧化合价由-1价变为-2价,结合电子守恒、质量守恒可知,化学方程式为Ce (SO )+H O+6NH·H O
2 4 3 2 2 3 2
2Ce(OH) ↓+3(NH)SO 。
4 4 2 4
(5)硫酸铈铵微溶于水,不溶于乙醇,故最后用乙醇洗涤2~3次后,得到高纯硫酸铈铵晶体。
(6)由Ce守恒可知,Ce (CO)~2(NH)Ce(SO),则(NH )Ce(SO) 的产率为
2 3 3 4 2 4 3 4 2 4 3
5.62×103g
4.60×103g ×100%≈60.6%。
×2×464 g·mol-1
460 g·mol-13.(2024·湖北卷)铍用于航天器件的构筑。一种从其铝硅酸盐[Be Al (SiO)]中提取铍的路径如图所示。
3 2 3 6
已知:Be2++4HA BeA(HA) +2H+
2 2
回答下列问题。
(1)基态Be2+的轨道表示式为 。
(2)为了从“热熔冷却”步骤得到玻璃态,冷却过程的特点是 。
(3)“萃取分液”的目的是分离Be2+和Al3+,向过量烧碱溶液中逐滴加入少量“水相1”的溶液,观察到的
现象是 。
(4)写出反萃取生成Na[Be(OH) ]的化学方程式: 。 “滤液
2 4
2”可以进入 步骤再利用。
(5)电解熔融氯化铍制备金属铍时,加入氯化钠的主要作用是 。
(6)Be(OH) 与醋酸反应得到某含4个Be的配合物,4个Be位于以1个O原子为中心的四面体的4个
2
顶角,且每个Be的配位环境相同,Be与Be间通过CHCOO-相连,其化学式为 。
3
答案:(1) (2)快速冷却
(3)先出现白色浑浊,后白色浑浊迅速消失
(4)BeA(HA) +6NaOH Na[Be(OH) ]+4NaA+2HO 反萃取分液
2 2 2 4 2
(5)增强熔融氯化铍的导电性
(6)Be O(CH COO)
4 3 6
解析:将Be Al (SiO) 加热熔融,然后快速冷却到其玻璃态,再加入稀硫酸“酸浸过滤”,“滤渣”的成
3 2 3 6
分为HSiO,“滤液1”中有Be2+和Al3+,加入含HA的煤油将Be2+萃取到有机相中,“水相1”中含有
2 3
Al3+,“有机相”为BeA(HA) ,加入过量氢氧化钠反萃取Be2+使其转化为Na[Be(OH) ]进入“水相2”
2 2 2 4
中,分离出含NaA的煤油,最后对“水相2”加热,并过滤分离出Be(OH) ,通过系列操作得到金属铍,据
2
此回答。
(1)基态Be2+的电子排布式为1s2,其轨道表示式为 。
(2)熔融态物质冷却凝固时,缓慢冷却会形成晶体,快速冷却会形成非晶态,即玻璃态,所以从“热熔冷
却”中得到玻璃态,其冷却过程的特点为快速冷却。(3)“滤液1”中有Be2+和Al3+,加入含HA的煤油将Be2+萃取到有机相中,则“水相1”中含有Al3+,向过量
烧碱溶液中逐滴加入少量“水相1”的溶液,发生反应:Al3++3OH- Al(OH) ↓、Al(OH) +OH-
3 3
[Al(OH) ]-,可观察到的现象为先出现白色浑浊,后白色浑浊迅速消失。
4
(4)反萃取生成Na[Be(OH) ]的化学方程式为BeA(HA) +6NaOH Na[Be(OH) ]+4NaA+2HO;“滤
2 4 2 2 2 4 2
液2”的主要成分为NaOH,可进入“反萃取分液”步骤再利用。
(5)氯化铍熔融态导电性弱,电解熔融氯化铍制备金属铍时,加入氯化钠的主要作用为增强熔融氯化铍
的导电性。
(6)由题意可知,该配合物中有4个Be位于四面体的4个顶角,四面体中心只有1个O,Be与Be之间总
共有6个CHCOO-,则该配合物的化学式为Be O(CH COO) 。
3 4 3 6
4.(2024·吉林白山二模)钪(Sc)及其化合物在电子、超导合金和催化剂等领域有重要应用。一种利用
钛白废酸液(含Sc3+、TiO2+、Fe3+的硫酸废液)和赤泥(含有Sc O、Al O、Fe O、SiO)联合制备
2 3 2 3 2 3 2
Sc O 的工艺流程如图所示。回答下列问题:
2 3
已知:25 ℃时,K [Sc(OH) ]=1×10-30。
sp 3
(1)基态Fe3+的简化电子排布式为 。
(2)为提高“浸取”速率,可采取的措施有 (写出一条即可),“浸
渣”的主要成分是 (写化学式);水相中含有的金属离子主要是 (写离
子符号)。
(3)“除钛”时,加入HO 的作用是 。
2 2
(4)25 ℃时,若使“反萃取”后水溶液中的Sc3+沉淀完全(离子浓度≤10-5 mol·L-1),应控制溶液的pH不
低于 (保留两位有效数字)。
(5)写出草酸钪晶体[Sc (C O)·6H O]“灼烧”时发生反应的化学方程式:
2 2 4 3 2
。
答案:(1)[Ar]3d5
(2)将赤泥碾碎(或适当升高温度、搅拌等) SiO Fe3+、Al3+
2
(3)提供配体,生成配离子[TiO(HO)]2+进入水层
2 2
(4)5.7
(5)2Sc (C O)·6H O+3O 2Sc O+12CO +12H O
2 2 4 3 2 2 2 3 2 2解析:钛白废酸液(含Sc3+、TiO2+、Fe3+的硫酸废液)和赤泥(含有Sc O、Al O、Fe O、SiO)“浸取”,
2 3 2 3 2 3 2
二氧化硅不和酸反应,“浸渣”为SiO,“萃取”时分离出Al3+、Fe3+,向“萃取”后的溶液中加入硫酸
2
和HO,除钛分离出[TiO(HO)]2+,加NaOH溶液“反萃取”后分离出Sc(OH) ,与盐酸反应后加草酸
2 2 2 2 3
得到Sc (C O)·6H O,再“灼烧”Sc (C O)·6H O得到Sc O。
2 2 4 3 2 2 2 4 3 2 2 3
(1)Fe是26号元素,基态Fe3+的简化电子排布式为[Ar]3d5。
(2)SiO 不与硫酸反应,故“浸渣”的主要成分是SiO;根据流程图可知,“浸取”除去SiO,加入萃取剂
2 2 2
“萃取”时水相中的金属离子主要是Fe3+、Al3+。
(3)由流程图可知,加入HO 后形成[TiO(HO)]2+,该转化过程中元素化合价没有变化,H O 中的氧原子
2 2 2 2 2 2
提供孤电子对,Ti原子提供空轨道,形成配离子[TiO(HO)]2+进入水层。
2 2
(4)根据题意可知,Sc3+恰好完全沉淀时,K [Sc(OH) ]=c(Sc3+)·c3(OH-)=10-5·c3(OH-)=1×10-30,解得
sp 3
K
c(OH-)≈10-8.3 mol·L-1,c(H+)= W ≈10-5.7 mol·L-1,故pH≈5.7。
c(OH-)
(5)Sc (C O)·6H O中Sc的化合价为+3价,反应前后Sc的化合价没有发生变化,根据流程图可知,空气
2 2 4 3 2
参与反应,空气氧化草酸钪晶体中的碳元素,反应的化学方程式为2Sc (C O)·6H O+3O
2 2 4 3 2 2
2Sc O+12CO +12H O。
2 3 2 2
5.(2024·安徽黄山二模)氧缺位体(CuFe O )是热化学循环分解水制氢的催化剂。一种以黄铜矿(主要
2 4-δ
成分是CuFeS,含Al O、SiO 等杂质)为原料制备CuFe O 的流程如图所示:
2 2 3 2 2 4-δ
已知:①酸浸后溶液中的金属离子有Cu2+、Fe2+、Al3+和Fe3+
②25 ℃时已知几种金属离子沉淀的pH如表所示:
氢氧化物 Fe(OH) Al(OH) Cu(OH) Fe(OH)
3 3 2 2
开始沉淀的pH 1.9 3.4 6.4 7.0
完全沉淀的pH 3.2 4.7 7.6 9.0
请回答下列问题:
(1)CuFeS “焙烧”时生成三种氧化物,其中金属氧化物的化学式为 。
2
(2)“焙烧”产物中的SO 在有氧条件下利用石灰浆液吸收可制得一种副产品
2
(填化学式)。
(3)流程中,若无“还原”工序,造成的后果是 。(4)已知Cu(NH )Cl 有两种同分异构体,则“沉铁”过程中生成的[Cu(NH )]2+的空间结构是
3 2 2 3 4
。
(5)“灼烧”工序的化学方程式是 , “煅烧”
时通入N 的作用是 。
2
(6)“煅烧”CuFe O 得到氧缺位体(CuFe O )时,不同温度范围内,发生变价的金属元素不同,某温度下
2 4 2 4-δ
制得的氧缺位体质量为原质量的99%,则δ= 。
(7)氧缺位体催化分解水制氢可分为两步:
第一步: (完成方程式);
第二步:2CuFe O 2CuFe O +δO↑。
2 4 2 4-δ 2
答案:(1)CuO、Fe O (2)CaSO
3 4 4
(3)还原工序是将Fe3+还原为Fe2+,若没有还原工序,Fe3+会形成Fe(OH) 进入滤渣2中
3
(4)平面正方形
(5)CuO+2Fe(OH) CuFe O+3H O 作保护气
3 2 4 2
(6)0.15
(7)CuFe O +δHO CuFe O+δH↑
2 4-δ 2 2 4 2
解析:氧气具有氧化性,已知酸浸后溶液中的金属离子有Cu2+、Fe2+、Al3+和Fe3+,CuFeS “焙烧”生成
2
三种氧化物,可知三种氧化物为SO 、CuO、Fe O;加入硫酸,金属氧化物转化为相应的硫酸盐,“滤渣
2 3 4
1”为SiO,加入Cu还原Fe3+为Fe2+,加入CuO调节pH使Al3+沉淀,而Cu2+和Fe2+不沉淀,“滤渣2”中有
2
Al(OH) 、CuO、Cu,加HO 将Fe2+氧化为Fe3+,加入过量的氨水反应生成Cu(NH )SO ,Fe3+生成
3 2 2 3 4 4
Fe(OH) 沉淀,Cu(NH)SO 经过系列操作生成CuO,灼烧CuO和Fe(OH) 生成CuFe O,在N 作保护气
3 3 4 4 3 2 4 2
下“煅烧”生成CuFe O 。
2 4-δ
(1)由分析知金属氧化物的化学式为CuO、Fe O。
3 4
(2)“焙烧”产物中的SO 在有氧条件下利用石灰浆液Ca(OH) 吸收可制得的一种副产品是CaSO。
2 2 4
(4)已知Cu(NH )Cl 有两种同分异构体,可知其结构不是四面体结构,而是平面四边形结构,故
3 2 2
[Cu(NH )]2+的空间结构为平面正方形。
3 4
(5)灼烧CuO和Fe(OH) 生成CuFe O,N 作保护气,防止生成物被氧化。
3 2 4 2
16δ
(6)“煅烧”CuFe O 得到氧缺位体(CuFe O ),质量减少的是氧气质量, ×100%=1-
2 4 2 4-δ 64+2×56+4×16
99%,δ=0.15。
(7)制取氢气的总反应为2HO 2H↑+O ↑,结合第二步反应2CuFe O 2CuFe O +δO↑,可知第
2 2 2 2 4 2 4-δ 2
一步反应为CuFe O +δHO CuFe O+δH↑。
2 4-δ 2 2 4 2
6.镍、铬、铜及其化合物在工业上有广泛的应用,从电镀污泥[含有Cu(OH) 、Ni(OH) 、Fe(OH) 、
2 2 3
Cr(OH) 和SiO 等]中回收制备NiSO ·nHO和其他金属及其化合物的工艺流程如图所示。
3 2 4 2已知:“萃取”可将金属离子进行富集与分离,原理如下:
X2+(水相)+2RH(有机相) XR (有机相)+2H+(水相)
2
回答下列问题:
(1)与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有 (填元素符号)。
1 1
原子核外运动的电子有两种相反的自旋状态,若一种自旋状态用“+ ”表示,与之相反的用“- ”表示,
2 2
1
“± ”即称为电子的自旋磁量子数。对于基态Ni原子,其价层电子自旋磁量子数的代数和为 。
2
(2)已知NiO与MgO的晶体结构相同,其中Mg2+和Ni2+的离子半径分别为66 pm和69 pm。则熔
点:NiO (填“>”“<”或“=”)MgO,理由是 。
(3)“滤渣Ⅰ”的主要成分为 (填化学式)。
(4)电解之后加入碳酸钠调节pH的目的是 。
(5)“反萃取”时加入的试剂A为 。
(6)“反萃取”得到的NiSO 溶液,在碱性条件下可被NaClO氧化生成NiOOH沉淀,该反应的离子方程
4
式为 。
(7)资料显示,硫酸镍结晶水合物的形态与温度有如表关系:
温度 低于30.8 ℃ 30.8~53.8 ℃ 53.8~280 ℃ 高于280 ℃
晶体形态 NiSO ·7H O NiSO ·6H O 多种结晶水合物 NiSO
4 2 4 2 4
由NiSO 溶液获得NiSO ·7H O晶体的操作依次是蒸发浓缩、 、 过滤、洗涤、干燥。
4 4 2
答案:(1)K、Cu -1(或+1)
(2)< Mg2+的半径比Ni2+的小,MgO的离子键比NiO的强
(3)SiO
2
(4)使铁离子形成Fe(OH) 沉淀,除去铁元素
3
(5)H SO (或硫酸)
2 4
(6)2Ni2++ClO-+4OH- 2NiOOH↓+Cl-+H O
2
(7)冷却至30.8 ℃以下结晶解析:(1)铬元素的基态原子中最外层电子排布为4s1,与铬同周期最外层电子排布为4s1的元素还有
K、Cu。基态Ni原子的价层电子轨道表示式为 ,则其价层电子自旋磁量子数的
代数和为-1(或+1)。
(2)NiO与MgO都是离子晶体,Mg2+的半径比Ni2+的小,MgO的离子键比NiO的强,则熔
点:NiO