文档内容
第五章 化工生产中的重要非金
属元素
第一节 硫及其化合物
第 1 课时 硫和二氧化硫
学业要求 核心素养对接
1.能列举、描述、辨识硫、二氧化硫、三
氧化硫的重要物理性质、化学性质及实
1.让学生仔细探讨二氧化硫转化为三氧
验现象。 化硫可逆反应,以培养学生变化观念与
平衡思想。2.通过二氧化硫性质的实验,
2.能说明二氧化硫转化为三氧化硫的可
培养学生科学研究与创新意识。
逆反应。
[知 识 梳 理]
知识点一 自然界中的硫
行走在生命边缘的采硫人
自然界的硫单质存在于火山口附近,人们可以直接开采,硫元素在自然界除了以
游离态的形式存在,还以哪些化合态的形式存在?单质硫有什么样的性质?带着这些问题完成下列知识点:
1.硫的常见化合价及代表物
化合价 代表物
-2价 H S 、S2-
2
0价 S
+4价 SO 、H SO 、Na SO
2 2 3 2 3
+6价 SO 、H SO 、Na SO
3 2 4 2 4
2.硫的性质
硫(俗称硫黄)是一种黄色晶体,质脆,易研成粉末。硫难溶于水,微溶于酒精,易溶
于二硫化碳。CS 可用于洗涤内壁附着硫的试管
2
硫的化学性质比较活泼,能与许多金属单质及非金属单质发生化学反应。
S+Fe=====FeS硫化亚铁 S+2Cu=====Cu S硫化亚铜
2
S+H =====H S硫化氢 S+O =====SO
2 2 2 2
硫的氧化性弱与变价金属反应金属生成低价
知识点二 二氧化硫和三氧化硫
不法商贩进行中药材加工,为什么要熏硫?熏硫的实质是什么?为什么要禁止?
完成下列知识点,你就会明白:
1.二氧化硫(SO )
2
(1)物理性质
颜色 气味 状态 密度 毒性 水溶性
无色 刺激性 气态 比空气大 有毒 易溶于水,1∶40
(2)化学性质
①酸性氧化物的通性:
a.与水反应:课本实验[实验5-1,pH试纸变红色]
二氧化硫与水反应的化学方程式为H O + SO H SO 。
2 2 2 3
不能漂白酸碱指示剂,但氯水、Na O 不但会使酸碱指示剂变色,还会漂白它们
2 2b.与碱反应:二氧化硫与 NaOH 溶液反应的化学方程式为 2NaOH +
SO == =Na SO + H O(碱过量)或 NaOH + SO == =NaHSO (SO 过量)。
2 2 3 2 2 3 2
c.与碱性氧化物反应:二氧化硫与氧化钙反应的化学方程式为 CaO +
SO ===== CaSO 。
2 3
②漂白性:
a.[实验5-2],振荡后溶液褪色,再加热后,溶液颜色恢复红色。
b.SO 与某些有色物质生成不稳定的无色物质,这种无色物质易分解而使有色物
2
质恢复到原来的颜色。
③还原性:
二氧化硫与氧气反应的化学方程式为2SO + O 2SO 。
2 2 3
SO 还可以与溴水、KMnO (H+)、Fe3+等反应,并且出现颜色变化,但不是SO 的
2 4 2
漂白性而是还原性
④氧化性:
二氧化硫与硫化氢反应的化学方程式为SO + 2H S == =3S ↓ + 2H O
2 2 2
(3)SO 的用途
2
①漂白纸浆、毛、丝、草帽辫等;
②用于杀菌消毒。
2.三氧化硫
三氧化硫具有酸性氧化物的通性,主要反应如下:
SO
3
3.可逆反应
化学上通常把向生成物方向进行的反应叫做正反应,向反应物方向进行的反应叫
做逆反应。像这种在同一条件下,既能向正反应方向进行,同时又能向逆反应方
向进行的反应,叫做可逆反应。
微判断
(1)自然界中不存在游离态的硫单质( )
(2)S能氧化Fe,使Fe生成+3价铁的化合物( )
(3)S在空气中燃烧生成SO ,在过量的纯O 中燃烧生成SO ( )
2 2 3
(4)SO 和CO 可用澄清石灰水鉴别( )
2 2
(5)SO 使品红溶液褪色是因为SO 具有强氧化性( )
2 2(6)SO 的水溶液存在SO 、H SO 的原因是SO 与H O反应为可逆反应( )
2 2 2 3 2 2
答案 (1)× (2)× (3)× (4)× (5)× (6)√
微训练
1.下列说法不正确的是( )
A.硫是一种淡黄色的不溶于水的晶体
B.硫的化合物常存在于火山喷出的气体中和矿泉水里
C.硫易燃烧,其燃烧产物是大气污染物之一
D.硫在空气中的燃烧产物是二氧化硫,在纯氧中的燃烧产物是三氧化硫
解析 硫在空气和纯氧中燃烧都生成SO ,SO 在催化剂存在且加热条件下与O
2 2 2
反应生成SO ,D项错误。
3
答案 D
2.下列关于硫的说法不正确的是( )
A.试管内壁附着的硫可用二硫化碳溶解除去
B.游离态的硫存在于火山喷口附近或地壳的岩层里
C.单质硫既有氧化性,又有还原性
D.硫在过量纯氧中的燃烧产物是三氧化硫
解析 硫单质或含硫物质在空气中燃烧时应生成SO ,而不能直接生成SO 。
2 3
答案 D
3.下列化合物能由两种单质直接化合生成的是( )
A.Fe S B.CuS
2 3
C.SO D.SO
3 2
解析 硫的氧化性较弱,与变价金属铁、铜化合时,只能生成低价态的金属硫化
物FeS和Cu S。
2
答案 D
4.写出下列反应的离子方程式
(1)NaOH溶液中通入过量SO :______________________________________
2
______________________________________________________________。
(2)Ca(OH) 溶液中通入少量SO :______________________________________
2 2
_____________________________________________________________。
(3)SO 通 入 氯 水 中 :
2_____________________________________________________
_________________________________________________________________。
答案 (1)OH-+SO ===HSO
2
(2)Ca2++2OH-+SO ===CaSO ↓+H O
2 3 2
(3)SO +Cl +2H O===4H++SO+2Cl-
2 2 2
微思考
1.常见的漂白剂有哪些,它们的漂白原理是什么?
提示
漂白剂 原理
氧化有色物质
SO 与有色物质化合
2
活性炭 吸附有色物质
2.如何证明混合气体中同时存在CO 、SO 气体?
2 2
提示 当CO 、SO 同时存在时,要先用品红溶液验证SO 的存在,再通入足量酸
2 2 2
性KMnO 溶液除去SO ,再将剩余气体通入澄清石灰水,澄清石灰水变浑浊,证
4 2
明CO 的存在。
2
学习任务1 二氧化硫、次氯酸的漂白原理
[文献摘抄]
漂白剂一般是氧化剂,通过获得被漂白物中发色基团的共轭电子对中的电子来去
除发色基团的负面影响;二氧化硫氧化性没那么强(+4价),因此只能算是勉强与
发色基团中的电子对发生作用,不能稳定持久的发挥作用。参照上图可以看出。
请结合上述文献材料,回答下列问题:1.分别将SO 和Cl 通入品红溶液中并加热,现象有何不同?若分别通入紫色石
2 2
蕊溶液中呢?
提示
(1)
(2)
2.把SO 和Cl 同时通入溶液中,溶液的漂白性是“强强联合”吗?
2 2
提示 若将等物质的量的Cl 和SO 气体混合后,在溶液中发生反应:SO +Cl +
2 2 2 2
2H O===H SO +2HCl,从而失去漂白能力。
2 2 4
SO 的漂白性
2
(1)SO 的漂白具有选择性,可以漂白品红溶液,以及棉、麻等物品,但不能漂白酸
2
碱指示剂,如石蕊、酚酞等。
(2)SO 能使溴水、酸性KMnO 溶液褪色。是因为SO 的还原性而非漂白性
2 4 2
(3)利用氯水、SO 的漂白性,可以鉴别Cl 和SO ,方法是将气体分别通入品红溶
2 2 2
液,品红溶液均褪色,然后再加热褪色后的溶液,恢复红色的通入的是SO ,不恢
2
复原来红色的通入的为Cl 。
2
【例题1】 下列说法正确的是( )
A.因为SO 具有漂白性,所以它能使品红溶液、溴水、酸性KMnO 溶液、石蕊试
2 4
液褪色
B.能使品红溶液褪色的不一定是SO
2
C.SO 、漂白粉、活性炭、Na O 都能使红墨水褪色,其原理相同
2 2 2
D.盐酸能使滴有酚酞的NaOH溶液褪色,所以盐酸也有漂白性
解析 A选项中SO 使溴水、酸性KMnO 溶液褪色是因为SO 具有还原性,能使
2 4 2
品红褪色是漂白性,SO 不能使指示剂褪色,所以A选项错误;B选项正确,因为
2
能使品红褪色的物质很多,不仅仅是SO ;C选项错误,因为这些漂白剂的漂白原
2理不相同;D选项错误,溶液褪色的原理是盐酸中和NaOH溶液使碱性变弱,并
不是盐酸具有漂白性。
答案 B
变式训练1 氯水和SO 都具有漂白作用,能使品红溶液褪色。若将等物质的量
2
的Cl 、SO 混合后再通入品红与BaCl 的混合溶液,能观察到的现象是( )
2 2 2
①溶液很快褪色 ②溶液不褪色 ③出现沉淀 ④不出现沉淀
A.①② B.①③
C.②③ D.②④
解析 Cl 和SO 等物质的量混合通入品红与BaCl 的混合溶液,涉及的化学反应
2 2 2
为Cl +SO +2H O===H SO +2HCl、BaCl +H SO ===BaSO ↓+2HCl,相应的
2 2 2 2 4 2 2 4 4
现象是溶液不会褪色,出现白色沉淀BaSO 。
4
答案 C
学习任务2 二氧化硫与二氧化碳的鉴别及净化
情景:
资料一:SO 是唯一在葡萄酒生产中普遍应用的添加剂。它在葡萄酒工艺中的作
2
用一般总结为以下几条:①选择性杀菌。作为一种杀菌剂,不同微生物对SO 的
2
耐受力是有不同的,其中细菌最为敏感,加入SO 后最先被杀死;其次是柠檬型
2
酵母;酿酒酵母对SO 耐受力则比较强。所以可以通过SO 来选择发酵微生物。②
2 2
澄清作用。③抗氧化作用。④增酸,调节发酵基质达到合适的酸度。SO 在葡萄酒
2
生产中发挥着巨大的作用,但是过量和不当使用也会带来一些问题,尤其是二氧
化硫对人体的健康影响日益受人重视,因此葡萄酒科研和生产实践中也在不断研
究尝试减少二氧化硫的使用。
资料二:SO 的排放造成了大气污染,酸雨的形成,工业上常用CaO除去SO 气体。
2 2
结合上述资料请回答:
1.资料中提到SO 有抗氧化作用,可以增酸,为什么?
2
提示 SO 具有还原性,SO 溶于水显酸性。
2 2
2.资料二中,SO 可用CaO除去,为什么?体现了SO 的什么性质?
2 2
提示 SO +CaO=====CaSO ,体现了SO 作为酸性氧化物的性质。
2 3 2
3.我们还学过CO 也是酸性氧化物。
2CO 和SO 均为酸性氧化物,在性质上具有一定的相似性,结合已有的知识探究
2 2
能否用澄清石灰水鉴别CO 和SO ,为什么?
2 2
提示 不能用澄清石灰水鉴别SO 和CO ,因为二者通入澄清石灰水时,现象相
2 2
同,即开始产生白色沉淀,后来沉淀溶解消失。
4.已知:酸性H SO >H CO ,除去CO 中的SO 可用哪些方法?
2 3 2 3 2 2
提示 (1)将混合气体通入足量的饱和NaHCO 溶液中;(2)将混合气体通入足量
3
的酸性KMnO 溶液。
4
1.SO 和CO 的性质比较
2 2
SO CO
2 2
无色、有刺激性气味、易液化、易溶于 无色、无味、能溶于水
物理性质
水(1∶40) (1∶1)
与水反应 SO +H OH SO (中强酸) CO +H OH CO (弱酸)
2 2 2 3 2 2 2 3
Ca(OH) ――→CaCO ――
与碱反应 Ca(OH) ――→CaSO ――→Ca(HSO ) 2 3
2 3 3 2 →Ca(HCO )
3 2
能使品红溶液褪色,又能使澄清石灰水 不能使品红溶液褪色,但能
鉴定存在
变浑浊 使澄清石灰水变浑浊
2.SO 鉴别的一般方法
2
(1)利用物理性质鉴别
气味:用标准的闻气体气味法,SO 有刺激性气味。
2
(2)利用化学性质鉴别
①氧化性:与硫化氢气体混合,有淡黄色固体生成。
②还原性:将气体通入稀氯水(或稀溴水、或酸性高锰酸钾溶液)中,溶液褪色;将
气体通入氯化铁溶液中,氯化铁溶液由黄色变成浅绿色。
(3)漂白性:将气体通入品红溶液中,能使品红溶液褪色;加热颜色又恢复。
【例题2】 某化学兴趣小组为了探究常温下某非金属氧化物形成的未知气体的
成分。该小组成员将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发
现浑浊又变澄清,由此该小组成员对气体的成分提出猜想。
[提出猜想]
猜想1:该气体为CO
2
猜想2:该气体为SO
2
猜想3.________________为了验证猜想,该小组设计实验加以探究:
[实验探究]
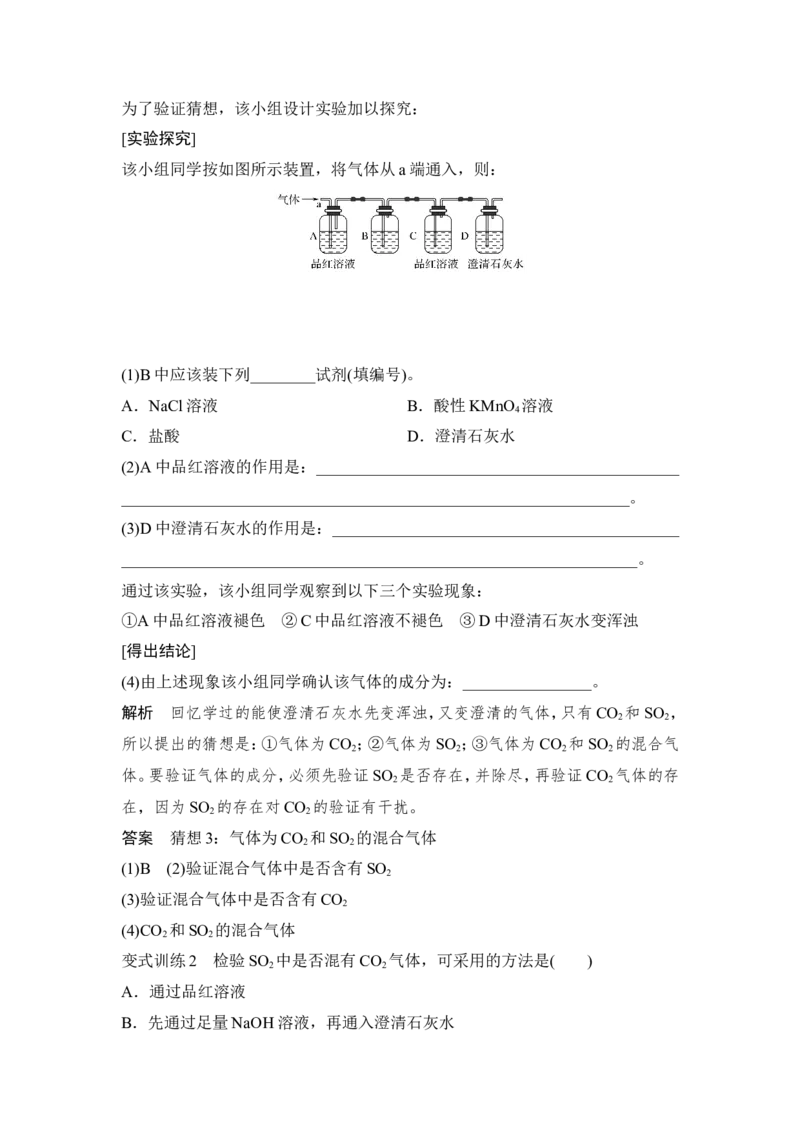
该小组同学按如图所示装置,将气体从a端通入,则:
(1)B中应该装下列________试剂(填编号)。
A.NaCl溶液 B.酸性KMnO 溶液
4
C.盐酸 D.澄清石灰水
(2)A中品红溶液的作用是:_____________________________________________
_______________________________________________________________。
(3)D中澄清石灰水的作用是:___________________________________________
________________________________________________________________。
通过该实验,该小组同学观察到以下三个实验现象:
①A中品红溶液褪色 ②C中品红溶液不褪色 ③D中澄清石灰水变浑浊
[得出结论]
(4)由上述现象该小组同学确认该气体的成分为:________________。
解析 回忆学过的能使澄清石灰水先变浑浊,又变澄清的气体,只有CO 和SO ,
2 2
所以提出的猜想是:①气体为CO ;②气体为SO ;③气体为CO 和SO 的混合气
2 2 2 2
体。要验证气体的成分,必须先验证SO 是否存在,并除尽,再验证CO 气体的存
2 2
在,因为SO 的存在对CO 的验证有干扰。
2 2
答案 猜想3:气体为CO 和SO 的混合气体
2 2
(1)B (2)验证混合气体中是否含有SO
2
(3)验证混合气体中是否含有CO
2
(4)CO 和SO 的混合气体
2 2
变式训练2 检验SO 中是否混有CO 气体,可采用的方法是( )
2 2
A.通过品红溶液
B.先通过足量NaOH溶液,再通入澄清石灰水C.通过澄清石灰水
D.先通过足量酸性KMnO 溶液,再通过澄清石灰水
4
解析 A选项检验的是SO ;B选项不管是否混有CO 都不会产生白色沉淀;C选
2 2
项不管有没有CO 都会产生白色沉淀,不能验证有无CO ;只有D选项,足量酸
2 2
性KMnO 溶液将SO 完全吸收,通过澄清石灰水,若有白色沉淀生成则一定有
4 2
CO ,若无沉淀则无CO 。
2 2
答案 D
学习任务3 (核心素养)SO 性质的综合应用
2
一、知识要点
1.酸性氧化物通性。
2.还原性
3.氧化性
4.漂白性
二、核心素养
实验现象⇒培养学生的证据推理意识
实验设计⇒提升学生的实验探究素养
【素养解题】
[典例示范] 某化学实验兴趣小组的同学用如图装置通入SO 气体进行实验。
2
(1)请填写表中空格:
管中棉花的位置 ① ② ③ ④
淀粉和碘
棉花浸取试剂 石蕊试液 品红溶液 氢硫酸
水混合液
现象 褪色 浅黄色
体现SO 的性质 酸性氧化物 漂白性 氧化性
2
(2) 写 出 ③ 中 发 生 反 应 的 化 学 方 程 式
_______________________________________
_____________________________________________________________。
[性质验证解题思维模型]
明晰性质 ①酸性氧化物⇒变红与现象 ②漂白性⇒褪色
分析现象 淀粉和碘水混合液褪色⇒I 被还原⇒SO +I +
2 2 2
与原理 2H 2 O===H 2 SO 4 +2HI
涉及SO 的几种常见变色反应
2
(1)SO 通入石蕊试液中变红⇒酸性氧化物
2
智能储备 (2)SO 通入(酸性)KMnO 溶液中褪色⇒还原性
2 4
(3)SO 通入品红溶液中褪色⇒漂白性
2
(4)SO 通入滴有酚酞的NaOH溶液中褪色⇒酸性氧化物
2
答案 (1)①变红色 ②褪色 ③还原性
(2)I +SO +2H O===H SO +2HI
2 2 2 2 4
三、对点训练
1.下列说法正确的是( )
A.硫单质常存在于火山喷口附近
B.进行SO 性质探究实验时,多余的SO 应排到实验室外
2 2
C.SO 气体通入BaCl 溶液中会产生白色沉淀
2 2
D.硫在空气中的燃烧产物是SO ,在纯氧中的燃烧产物是SO
2 3
解析 SO 不与BaCl 溶液反应,C错误;硫不论在空气中燃烧,还是在纯氧中的
2 2
燃烧其产物均是SO 。
2
答案 A
2.下列化学实验中,能证明某种中学常见气体为SO 的是(双选)( )
2
①能使澄清的石灰水变浑浊 ②能使湿润的蓝色石蕊试纸变红 ③既能使品红
溶液褪色又能使澄清的石灰水变浑浊 ④将其通入足量的NaOH溶液中,再滴加
BaCl 溶液,有白色沉淀生成,该沉淀溶于稀盐酸 ⑤通入溴水,能使溴水褪色,
2
再滴加Ba(NO ) 溶液,有白色沉淀产生。
3 2
A.都能证明 B.都不能证明
C.③能证明 D.⑤能证明
解析 ①能使澄清的石灰水变浑浊的,还可能是CO ;②酸性气体不仅SO 一种;
2 2
④CO 也可以存在此现象。
2
答案 CD
3.下列溶液中,不能鉴别CO 、SO 气体的是( )
2 2①石灰水 ②H S水溶液 ③酸性KMnO 溶液 ④溴水 ⑤氯水 ⑥品红溶液
2 4
A.①⑤ B.②③④⑤⑥
C.只有① D.③④
解析 SO 和CO 都是酸性氧化物,都能使澄清的石灰水变浑浊,但SO 气体具
2 2 2
有漂白性、还原性和氧化性,所以只有①不能鉴别二者。
答案 C
4.关于SO 的叙述中,不正确的是( )
2
A.SO 在有的反应中显示氧化性,有的反应中显示还原性
2
B.SO 是酸性氧化物,溶于水生成亚硫酸
2
C.SO 能使酸性KMnO 溶液褪色,说明SO 具有漂白性
2 4 2
D.SO 气体通入品红溶液中,溶液褪色
2
解析 A项,SO 中硫元素化合价为+4价,处于硫元素的中间价态,因此既有氧
2
化性,又有还原性;B项,SO +H OH SO ;C项,体现了SO 的还原性;D项,
2 2 2 3 2
SO 具有漂白性,能使品红溶液褪色。
2
答案 C[学 考 练]
1.下列说法中错误的是( )
A.二氧化硫能漂白某些物质,说明它具有氧化性
B.二氧化硫的水溶液能使紫色石蕊溶液变红,但不能使之褪色
C.将足量二氧化硫通入酸性高锰酸钾溶液中,溶液褪色,说明二氧化硫具有还原
性
D.二氧化硫漂白过的草帽过一段时间后又会恢复到原来的颜色
解析 SO 的漂白作用不同于HClO,不是利用其强氧化性而是与有色物质化合
2
生成无色不稳定物质,A错,D正确。二氧化硫水溶液显酸性但不具有漂白石蕊溶
液的能力,B正确。SO 具有还原性能被酸性KMnO 溶液氧化,C正确。
2 4
答案 A
2.下列五种有色溶液与SO 作用,均能褪色,其实质相同的是( )
2
①品红溶液 ②KMnO 酸性溶液 ③滴有酚酞的NaOH溶液 ④溴水 ⑤淀粉
4
碘溶液
A.①④ B.①②④
C.②③⑤ D.②④⑤
解析 ①中SO 与品红化合生成不稳定的无色物质;②④⑤中KMnO 、Br 、I 和
2 4 2 2
SO 之间发生氧化还原反应导致褪色;③是SO 作为酸性氧化物和碱反应导致
2 2
OH-浓度减小溶液褪色。
答案 D
3.下列物质能使品红溶液褪色,其中是利用强氧化性漂白的是( )
①活性炭 ②过氧化钠 ③氯水 ④二氧化硫 ⑤臭氧
A.①③④ B.②③⑤
C.①②③④ D.②③④⑤
解析 ①活性炭是吸附性(物理性质)漂白;④SO 是化合性漂白;其他三种均是
2
利用强氧化性来漂白的。
答案 B
4.下列物质能与SO 气体反应,但无沉淀产生的是( )
2
①溴水 ②Ba(OH) 溶液 ③石灰水 ④Na CO 溶液
2 2 3⑤稀硫酸 ⑥Na SO 溶液 ⑦Na SO 溶液
2 4 2 3
A.只有① B.①④⑤
C.④⑥⑦ D.①④⑦
解析 ①溴水与SO 的反应为Br +SO +2H O===H SO +2HBr;②Ba(OH) 溶
2 2 2 2 2 4 2
液与SO 的反应为Ba(OH) +SO ===BaSO ↓+H O,生成沉淀;③石灰水与SO
2 2 2 3 2 2
的反应为Ca(OH) +SO ===CaSO ↓+H O,生成沉淀;④Na CO 溶液与SO 的
2 2 3 2 2 3 2
反应为 Na CO +SO ===Na SO +CO ;稀硫酸、Na SO 溶液与 SO 不反应;
2 3 2 2 3 2 2 4 2
⑦Na SO 与SO 的反应为Na SO +SO +H O===2NaHSO ,所以符合要求的是
2 3 2 2 3 2 2 3
①④⑦。
答案 D
5.如图是研究二氧化硫性质的微型实验装置。现用 60%硫酸溶液和亚硫酸钠晶
体反应制取SO 气体,实验现象很明显,且不易污染空气。下列说法中错误的是
2
(双选)( )
A.紫色石蕊溶液变蓝色
B.品红溶液褪色,因SO 具有漂白性
2
C.溴水橙色褪去,是因为SO 具有漂白性
2
D.含酚酞的NaOH溶液红色变浅
解析 SO 的水溶液显酸性,能使紫色石蕊溶液变红,故A错误;SO 有漂白性,
2 2
能使品红溶液褪色,B正确;SO 有强还原性,与溴水发生反应:Br +SO +
2 2 2
2H O===H SO +2HBr,使溴水褪色,C 错误;SO 能与 NaOH 溶液反应生成
2 2 4 2
Na SO ,使红色变浅或褪色,D正确。
2 3
答案 AC
6.下列离子方程式正确的是(双选)( )
A.向NaOH溶液中通入少量SO :SO +OH-===HSO
2 2
B.向氯水中通入少量SO :Cl +SO +2H O===4H++2Cl-+SO
2 2 2 2
C.将SO 通入到饱和NaHCO 溶液中:SO + HCO=== HSO+CO ↑
2 3 2 2D.将SO 通入到BaCl 溶液中:SO +H O+Ba2+===BaSO ↓+2H+
2 2 2 2 3
解析 SO 与过量NaOH溶液反应生成Na SO 和水,反应离子方程式为 SO +
2 2 3 2
2OH-===SO+H O,A项错误;B项正确;H SO 的酸性比H CO 强,SO 通入饱
2 2 3 2 3 2
和NaHCO 溶液中,反应的离子方程式为:SO +HCO===HSO+CO ,C项正确;
3 2 2
H SO 酸性比盐酸弱,故SO 通入到BaCl (或CaCl )溶液中不反应,D项错误,答
2 3 2 2 2
案为B项。
答案 BC
7.为了除去混入二氧化碳中的二氧化硫和氧气,下列试剂的使用顺序正确的是(
)
①饱和Na CO 溶液;②饱和NaHCO 溶液;③浓硫酸;④灼热的铜网;⑤碱石灰
2 3 3
A.①③④ B.②③④
C.②①③ D.③④⑤
解析 因为亚硫酸酸性较碳酸强,故饱和碳酸氢钠溶液可以除去SO ,加热时Cu
2
与O 生成CuO,故灼热铜网用于除O ,浓硫酸与CO 不反应,可除水蒸气。
2 2 2
答案 B
8.如图所示是一套检验气体性质的实验装置。向装置中缓慢通入气体X,若关闭
活塞,则品红溶液无变化而澄清的石灰水变浑浊;若打开活塞,则品红溶液褪色。
据此判断气体X和洗气瓶内溶液Y分别可能为( )
① ② ③ ④
X SO H S CO Cl
2 2 2 2
饱和的NaHCO 溶
Y 3 浓硫酸 Na SO 溶液 Na CO 溶液
液 2 3 2 3
A.①④ B.①②
C.②③ D.③④
解析 SO 、氯水均具有漂白性,且均与 NaHCO 溶液、Na CO 溶液反应生成
2 3 2 3
CO ,A项正确。
2答案 A
9.某同学用如下图所示装置探究SO 的性质及其有关实验。
2
(1)实验室用亚硫酸钠固体和一定浓度的硫酸反应制备SO 气体,写出该反应的
2
化学方程式:______________________________________________________
___________________________________________________________________。
(2)分别将SO 气体通入下列C溶液中,请回答下列问题:
2
①将少量SO 气体通入紫色石蕊溶液中,现象是__________________________,
2
继续通入过量SO 气体,现象是___________________________________
2
_______________________________________________________。
②将SO 气体通入酸性KMnO 溶液中,现象是_____________________________
2 4
___________________________________________________________,
其反应的离子方程式为:________________________________________________
③将SO 气体慢慢通入澄清石灰水中,现象是______________________________
2
____________________________________________________________。
④若C中为双氧水,则通入SO 气体后,请大胆判断所得溶液是________(填溶质
2
的化学式)。若该同学制备的SO 气体中混有CO 气体,产生杂质的原因可能是亚
2 2
硫酸钠固体中混有________,要证明气体中既有SO 又有CO ,应该选用的试剂
2 2
依次为________________________________________________
______________________________________________________________。
解析 ①SO 通入水中生成H SO ,H SO H++HSO,HSOH++SO,溶液
2 2 3 2 3
呈酸性,遇到石蕊溶液显红色。②SO 通入酸性KMnO 溶液中,MnO氧化SO ,
2 4 2
自身被还原为Mn2+,所以溶液颜色逐渐变浅或紫红色消失。③SO 通入澄清石灰
2
水 中 : SO + Ca(OH) ===CaSO ↓ + H O , 过 量 时 SO + CaSO +
2 2 3 2 2 3
H O===Ca(HSO ) 。④证明气体中既有SO 又有CO ,首先证明有SO ,再除去
2 3 2 2 2 2
SO ,防止干扰CO 的检验。
2 2
答案 (1)Na SO +H SO ===Na SO +SO ↑+H O
2 3 2 4 2 4 2 2(2)①溶液变红 不褪色 ②溶液颜色逐渐变浅或紫红色消失 5SO +2MnO+
2
2H O===5SO+2Mn2++4H+ ③溶液变浑浊,后又变澄清 ④H SO 碳酸盐或
2 2 4
碳酸氢盐 品红溶液、酸性KMnO 溶液、品红溶液、澄清石灰水
4
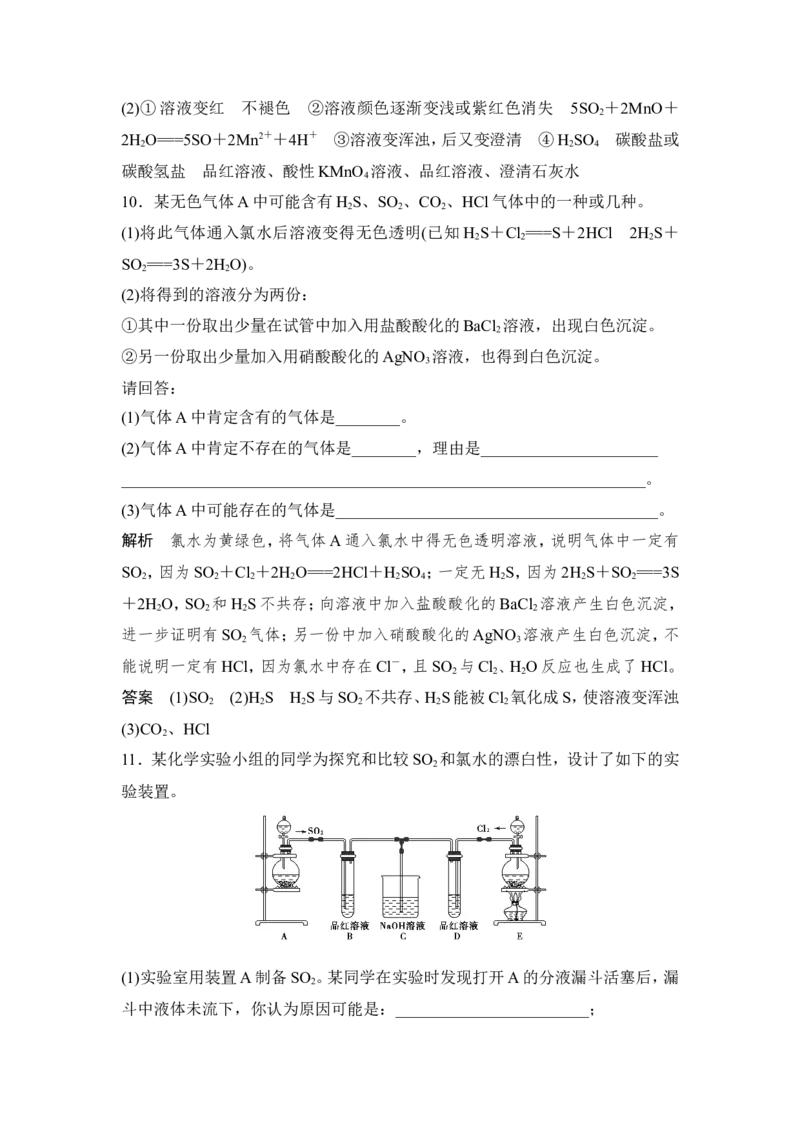
10.某无色气体A中可能含有H S、SO 、CO 、HCl气体中的一种或几种。
2 2 2
(1)将此气体通入氯水后溶液变得无色透明(已知H S+Cl ===S+2HCl 2H S+
2 2 2
SO ===3S+2H O)。
2 2
(2)将得到的溶液分为两份:
①其中一份取出少量在试管中加入用盐酸酸化的BaCl 溶液,出现白色沉淀。
2
②另一份取出少量加入用硝酸酸化的AgNO 溶液,也得到白色沉淀。
3
请回答:
(1)气体A中肯定含有的气体是________。
(2)气体A中肯定不存在的气体是________,理由是______________________
_________________________________________________________________。
(3)气体A中可能存在的气体是________________________________________。
解析 氯水为黄绿色,将气体A通入氯水中得无色透明溶液,说明气体中一定有
SO ,因为SO +Cl +2H O===2HCl+H SO ;一定无H S,因为2H S+SO ===3S
2 2 2 2 2 4 2 2 2
+2H O,SO 和H S不共存;向溶液中加入盐酸酸化的BaCl 溶液产生白色沉淀,
2 2 2 2
进一步证明有SO 气体;另一份中加入硝酸酸化的AgNO 溶液产生白色沉淀,不
2 3
能说明一定有HCl,因为氯水中存在Cl-,且SO 与Cl 、H O反应也生成了HCl。
2 2 2
答案 (1)SO (2)H S H S与SO 不共存、H S能被Cl 氧化成S,使溶液变浑浊
2 2 2 2 2 2
(3)CO 、HCl
2
11.某化学实验小组的同学为探究和比较SO 和氯水的漂白性,设计了如下的实
2
验装置。
(1)实验室用装置A制备SO 。某同学在实验时发现打开A的分液漏斗活塞后,漏
2
斗中液体未流下,你认为原因可能是:________________________;(2) 实 验 室 用 装 置 E 制 备 Cl , 其 反 应 的 化 学 方 程 式 为 MnO +
2 2
4HCl(浓)=====MnCl +Cl ↑+2H O。若有6 mol的HCl参加反应,则转移的电
2 2 2
子总数为________;
(3)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是
B:________,D:________;
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为
B:____________________________________________________________。
D:_____________________________________________________________。
解析 (1)A中分液漏斗的玻璃塞没有取下,漏斗内气体与空气不连通,故打开活
塞后液体不能流下。(2)根据制取Cl 的反应原理可知,每生成1 mol Cl ,消耗4
2 2
mol HCl,转移2 mol电子,故有6 mol HCl参加反应,则转移3 mol电子。(3)SO
2
具有漂白性,可使品红溶液褪色,但其漂白性是可逆的。加热后会恢复原来的颜
色;Cl 通入品红溶液时与H O反应生成HCl和HClO,HClO具有强氧化性,会把
2 2
品红氧化而褪色,且该过程不可逆,故加热不会恢复原来的颜色。
答案 (1)分液漏斗的玻璃塞没有取下来
(2)3N (3)①品红褪色 品红褪色 ②褪色的品红溶液又恢复成红色 无明显
A
现象
[能 力 练]
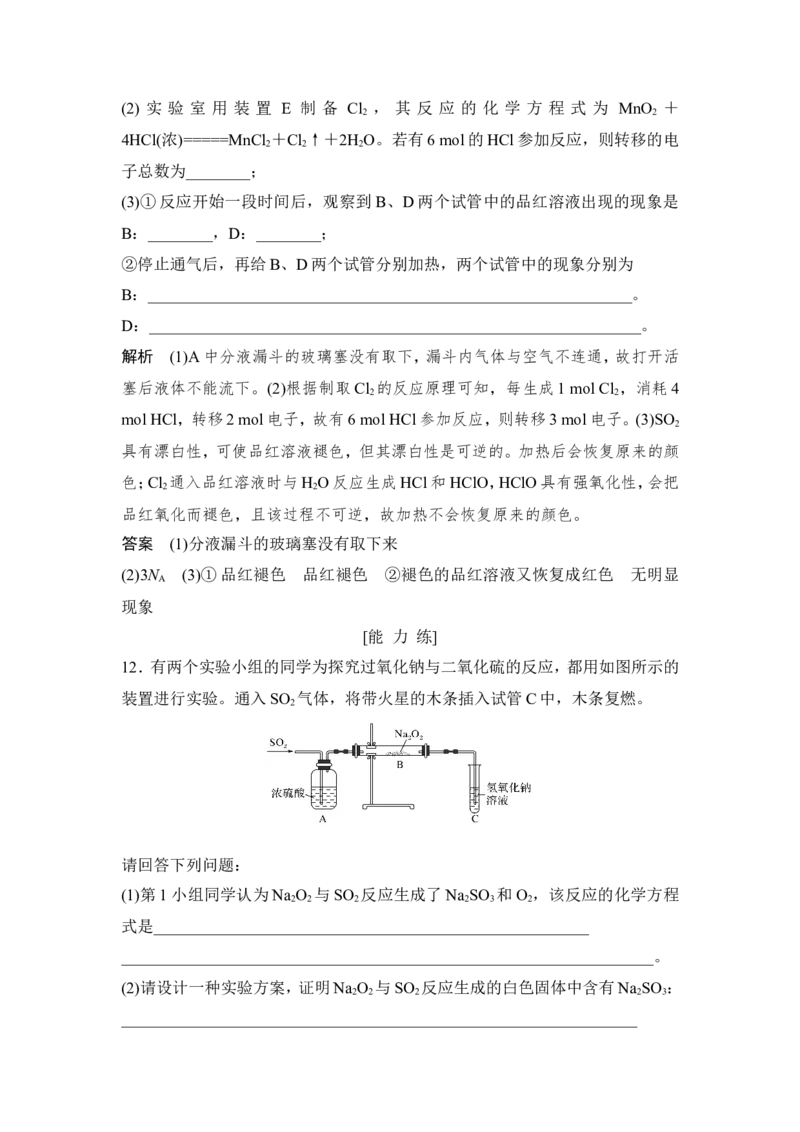
12.有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如图所示的
装置进行实验。通入SO 气体,将带火星的木条插入试管C中,木条复燃。
2
请回答下列问题:
(1)第1小组同学认为Na O 与SO 反应生成了Na SO 和O ,该反应的化学方程
2 2 2 2 3 2
式是______________________________________________________
__________________________________________________________________。
(2)请设计一种实验方案,证明Na O 与SO 反应生成的白色固体中含有Na SO :
2 2 2 2 3
______________________________________________________________________________________________________________________________。
(3)第2小组同学认为Na O 与SO 反应除了能生成Na SO 与O 外,还有Na SO
2 2 2 2 3 2 2 4
生成。为检验是否有Na SO 生成,他们设计了如下方案:
2 4
――→――→
上述方案是否合理?____________。请简要说明两点理由:
①______________________________________________________________;
②________________________________________________________________。
解析 (1)已知“Na O 与SO 反应生成了Na SO 和O ”,再联想Na O 与CO 反
2 2 2 2 3 2 2 2 2
应生成了Na CO 和O ,即得答案。
2 3 2
(2)证明含Na SO 即证明含SO。SO的特征反应是与H+反应生成能使品红溶液、
2 3
酸性高锰酸钾溶液、溴水等有色液体褪色的有刺激性气味的无色气体SO 。
2
(3)该项实验目的是检验是否有Na SO 生成,即检验是否存在SO。但是,“第2
2 4
小组同学认为Na O 与SO 反应除了生成Na SO 和O 外,还有Na SO 生成”,即
2 2 2 2 3 2 2 4
被检样品中混有Na SO ,Na SO 易被Na O 、HNO 氧化为Na SO ,所以该实验方
2 3 2 3 2 2 3 2 4
案不合理。
答案 (1)2Na O +2SO ===2Na SO +O
2 2 2 2 3 2
(2)取少量试样于试管中,加入足量稀硫酸(或稀盐酸),将产生的气体导入品红溶
液。若品红溶液褪色,说明白色固体中含有Na SO
2 3
(3)不合理
①稀硝酸能将BaSO 氧化为BaSO
3 4
②如果反应后的固体中还残留Na O ,它溶于水后能将BaSO 氧化成BaSO
2 2 3 4
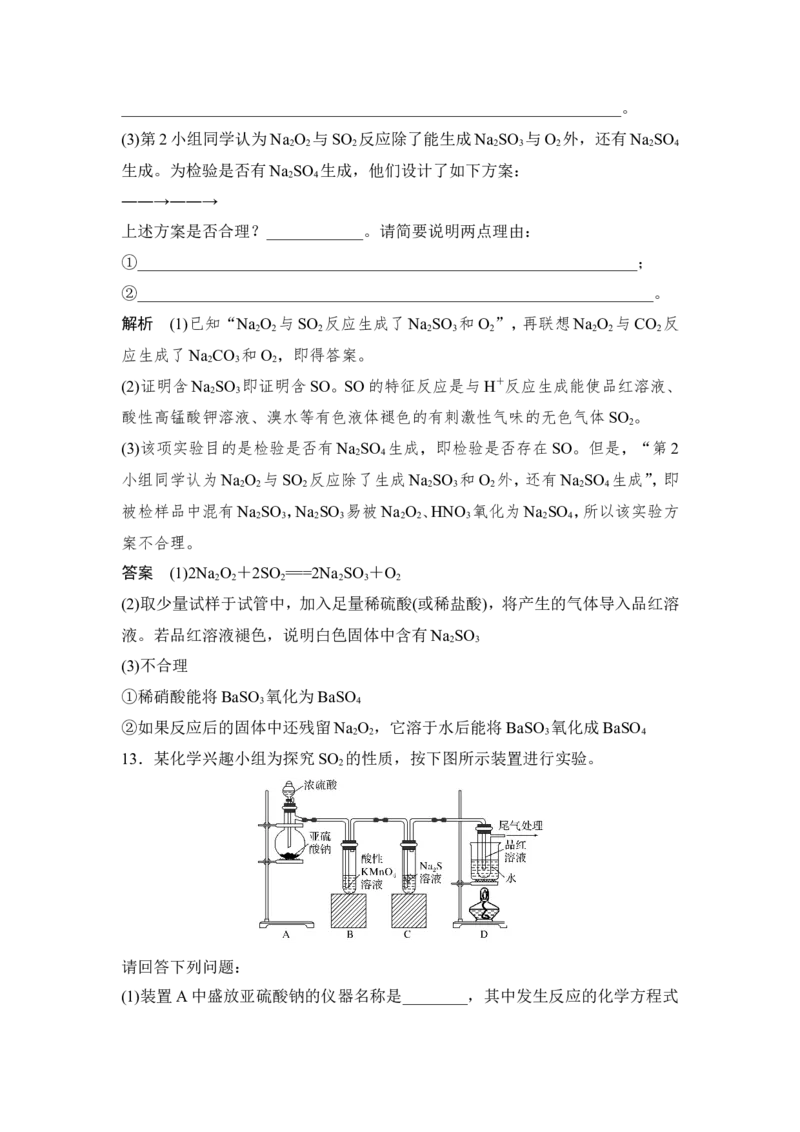
13.某化学兴趣小组为探究SO 的性质,按下图所示装置进行实验。
2
请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是________,其中发生反应的化学方程式为_______________________________________________________________;
(2)实验过程中,装置 B、C中发生的现象分别是________________________、
________________________,这些现象分别说明 SO 具有的性质是________和
2
________ ; 装 置 B 中 发 生 反 应 的 离 子 方 程 式 为
______________________________。
(3)装置D的目的是探究SO 与品红溶液作用的可逆性,请写出实验操作及现象
2
_____________________________________________________________________
___________________________________________________________________;
(4)尾气可采用________溶液吸收。
解析 (1)常见烧瓶有:圆底烧瓶、平底烧瓶和蒸馏烧瓶,图示中带支管的为蒸馏
烧瓶。(2)SO 因有还原性,能使酸性高锰酸钾溶液褪色,离子反应为:5SO +
2 2
2MnO+2H O===5SO+2Mn2++4H+;SO 能与-2价的S反应生成硫沉淀,体现
2 2
氧化性:SO +4H++2S2-===3S↓+2H O。(3)SO 与品红溶液作用的可逆性指:
2 2 2
SO 使品红溶液褪色,加热后又恢复红色,注意实验操作中品红溶液褪色后要关
2
闭分液漏斗的旋塞。(4)SO 为酸性氧化物,一般用碱性溶液吸收,也可用酸性高锰
2
酸钾等强氧化性溶液吸收。
答案 (1)蒸馏烧瓶 Na SO +H SO (浓)===Na SO +SO ↑+H O (2)溶液由紫
2 3 2 4 2 4 2 2
红色变为无色 无色溶液中出现黄色浑浊 还原性 氧化性 5SO +2MnO+
2
2H O===2Mn2++5SO+4H+
2
(3)品红溶液褪色后,关闭分液漏斗的旋塞,点燃酒精灯加热,溶液恢复为红色
(4)NaOH