文档内容
2012~2013 学年度河源中学实验学校九年级
化学第二次段考试卷
说 明:本试卷共6页,25题.满分100分。考试用时80分钟。
注意事项:
1、答题前,考生务必在答题卡上用黑色字迹的钢笔或签字笔填写准考证号、姓名、试
室号、座位号。
2、选择题每小题选出答案后,写在相应的位置。
3、非选择题必须用黑色字迹钢笔或签字笔作答,答案必须写在答题卡各题目指定区
域内相应位置上;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅
笔和涂改液。不按以上要求作答的答案无效。
4、考生必须保持答题卡的整洁。考试结束后,将答题卡交回。
5、不准使用计算器。
可能用到的相对原子质量:H—1、C—12、N—14、O—16、Cl—35.5、K—39、S—32
第Ⅰ卷 选择题(共30分)
一、单项选择题(本大题包括15小题,每小题2分,共30分。每小题有四个选项,其
中只有一个选项符合题意)
1.日常生活中发生的下列变化都属于化学变化的一组是…………………【 】
A、玻璃杯被摔碎、米饭变馊 B、酒精挥发、湿衣服晾干
C、蜡烛燃烧、乒乓球变瘪 D、菜刀生锈、牛奶变酸
2.前年4月19日,温家宝总理批示:严查安徽“杀人奶粉”。经检测“杀人奶粉”中
的蛋白质、钙、磷、锌、铁等成份含量严重不足,营养价值比米汤还差。这里所说的
钙、磷、锌、铁是指…………………………………………….……【 】
A.元素 B.分子 C.原子 D.单质
3.某种电池的正极材料由锂(Li)、钴(Co)和氧元素组成,三种元素的化合价分别是
+1、+3、-2,则该物质的化学式为……………………………………【 】
A.LiCoO B. LiCoO C. LiCoO D. LiCoO
4 3 2
4.过氧化氢(HO)的水溶液俗称双氧水,在医疗上可作为消毒杀菌剂。下列关于
2 2
1HO 的一些说法正确的是…………………………………………………【 】
2 2
A. 双氧水由两个氢原子和两个氧原子构成
B. H O 分子由一个氢分子和一个氧分子构成
2 2
C. HO 由氢元素和氧元素组成
2 2
D. HO 中氢元素和氧元素的质量之比为1:1
2 2
5. 下列物质的命名,错误的是…………………………………………………【 】
A、CaCl 氯化钙 B、FeSO 硫酸铁 C、Zn(NO ) 硝酸锌 D、Na SO 硫酸钠
2 4 3 2 2 4
6.黑火药是我国古代四大发明之一。把木炭粉、硫黄粉和硝酸钾按一定比例混合,可
以制得黑火药。点燃时发生如下反应: 2KNO + S + 3C === K S + 3CO + X其中X
3 2 2
的化学式为……………………………………………………………………【 】
A、N B、NO C、SO D、NO
2 2 2 2 5
7. 用“分子的观点”解释下列现象,不正确的是………………………………【 】
A、轮胎充气—分子间有间隔 B、湿衣晾干—分子不停地运动
C、气体受热膨胀—分子间间隔变大 D、水结成冰—分子本身发生变化
8. 下列化学方程式书写正确的是……………………………………………【 】
A.氧化汞加热分解: HgO △ H g+O ↑
2
B.铁在氧气中燃烧: 3Fe+2O 点燃 FeO
2 3 4
C.铝片投入稀硫酸中: Al+H SO =AlSO +H ↑
2 4 4 2
D.碳在氧气中燃烧: C+O = CO
2 2
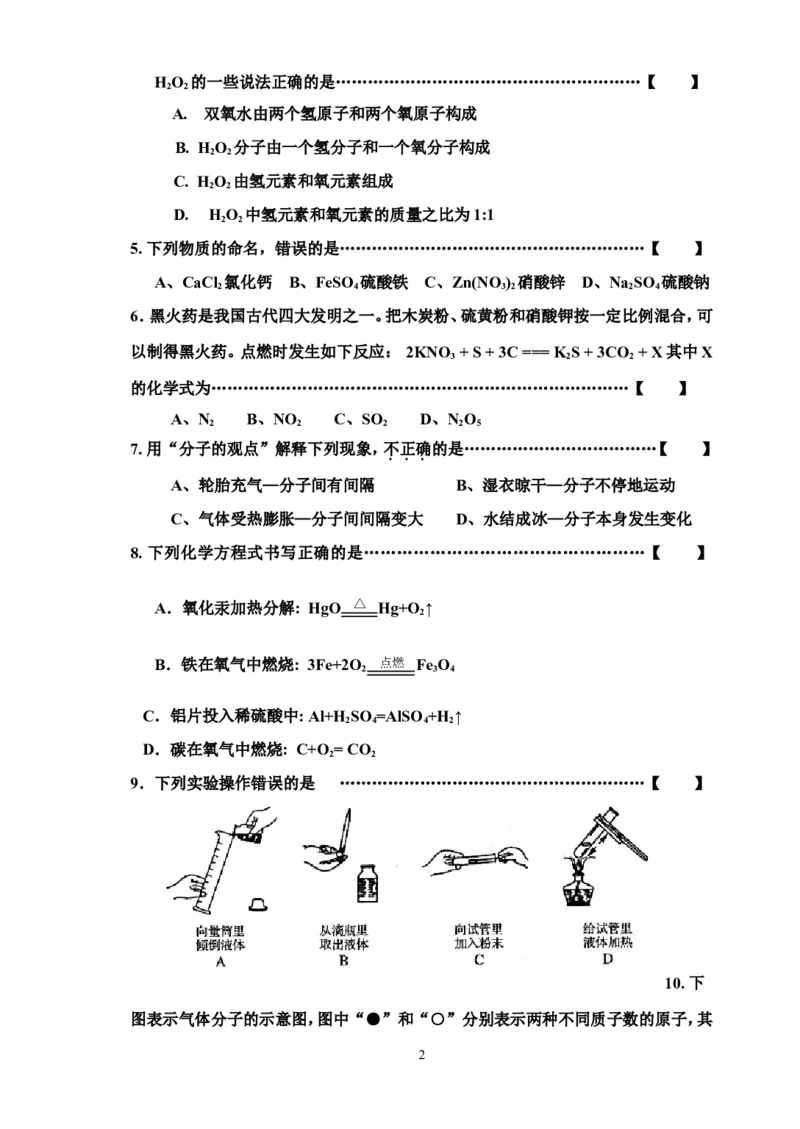
9.下列实验操作错误的是 …………………………………………………【 】
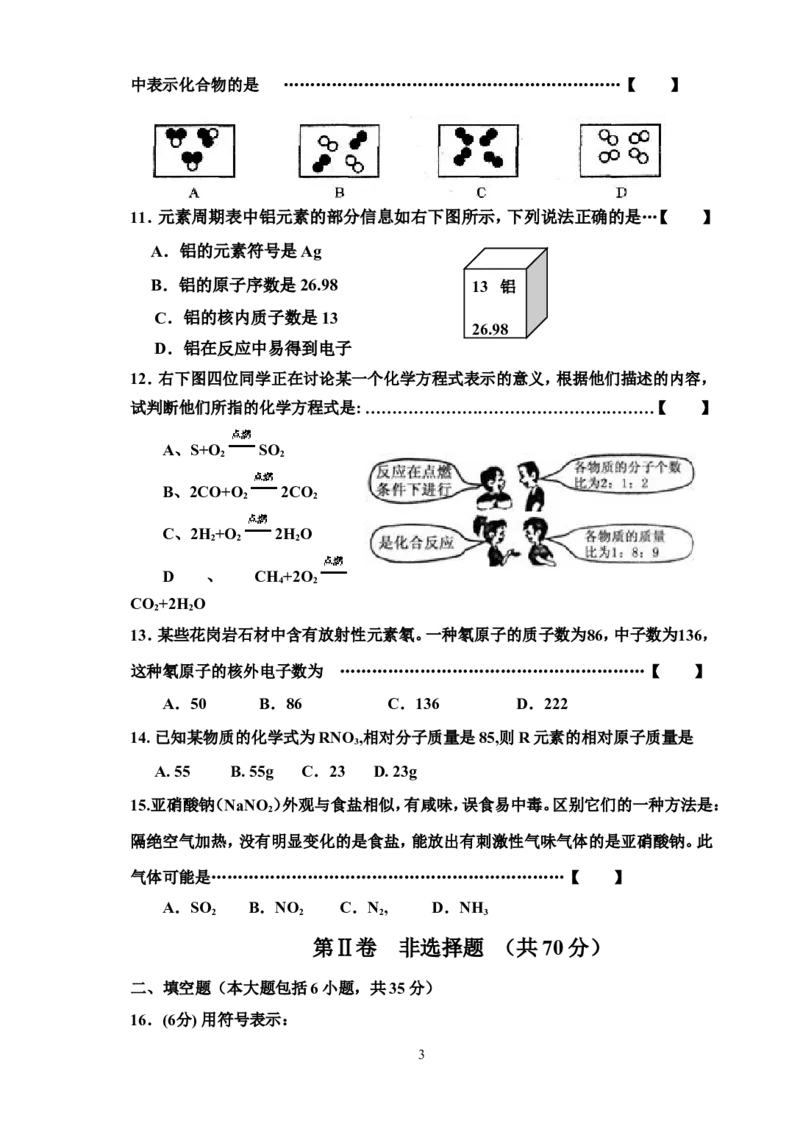
10. 下
图表示气体分子的示意图,图中“●”和“○”分别表示两种不同质子数的原子,其
2中表示化合物的是 ………………………………………………………【 】
11.元素周期表中铝元素的部分信息如右下图所示,下列说法正确的是…【 】
A.铝的元素符号是Ag
B.铝的原子序数是26.98 13 铝
C.铝的核内质子数是13
26.98
D.铝在反应中易得到电子
12.右下图四位同学正在讨论某一个化学方程式表示的意义,根据他们描述的内容,
试判断他们所指的化学方程式是: ………………………………………………【 】
A、S+O SO
2 2
B、2CO+O 2CO
2 2
C、2H+O 2HO
2 2 2
D 、 CH +2O
4 2
CO +2H O
2 2
13.某些花岗岩石材中含有放射性元素氡。一种氡原子的质子数为86,中子数为136,
这种氡原子的核外电子数为 …………………………………………………【 】
A.50 B.86 C.136 D.222
14. 已知某物质的化学式为RNO ,相对分子质量是85,则R元素的相对原子质量是
3
A. 55 B. 55g C.23 D. 23g
15.亚硝酸钠(NaNO )外观与食盐相似,有咸味,误食易中毒。区别它们的一种方法是:
2
隔绝空气加热,没有明显变化的是食盐,能放出有刺激性气味气体的是亚硝酸钠。此
气体可能是…………………………………………………………【 】
A.SO B.NO C.N, D.NH
2 2 2 3
第Ⅱ卷 非选择题 (共70分)
二、填空题(本大题包括6小题,共35分)
16.(6分) 用符号表示:
3(1)氧元素________;(2)2个氮分子 ;(3)3个氢原子__________;
(4)2个镁离子 ;(5)4个硫离子_______;(6)氢氧根离子_______。
17.(5分) 某元素在人体内能调节体液平衡等,缺乏该元素会造成心率不齐,过量时会
x
使人恶心腹泻。该元素的原子结构示意图为 ,则 =______,该原子有
______个电子层,该原子易_____(填“失”或“得”)电子,形成______(填离子符
号),碳酸钾的化学式为 。
18.(4分)(1)学校、家庭、办公室常用的净水器的基本原理可用
右图所示的简易净水装置表示。其中所用的小卵石、石英沙
等的作用是 ,起吸附作用的是 ;
(2)长期饮用硬水对人体健康不利。要检验日常使用的自来
水是不是硬水,可用 检验,倘若检验得出是硬水,生
活中可采用降低水的硬度的方法是 。
19.(6分)为了节省石油资源和有效地减少汽车尾气对环境的污染,我国正在逐步推
广使用在汽油中加入适量乙醇作为汽车燃料(车用乙醇汽油)。乙醇的化学式是
CHO,在物质分类中属于 (填“单质”或“化合物”),乙醇中碳元素和氢
2 6
元素的质量比是 ,乙醇在空气中燃烧时生成二氧化碳和水,写出该反应
的化学方程式 。
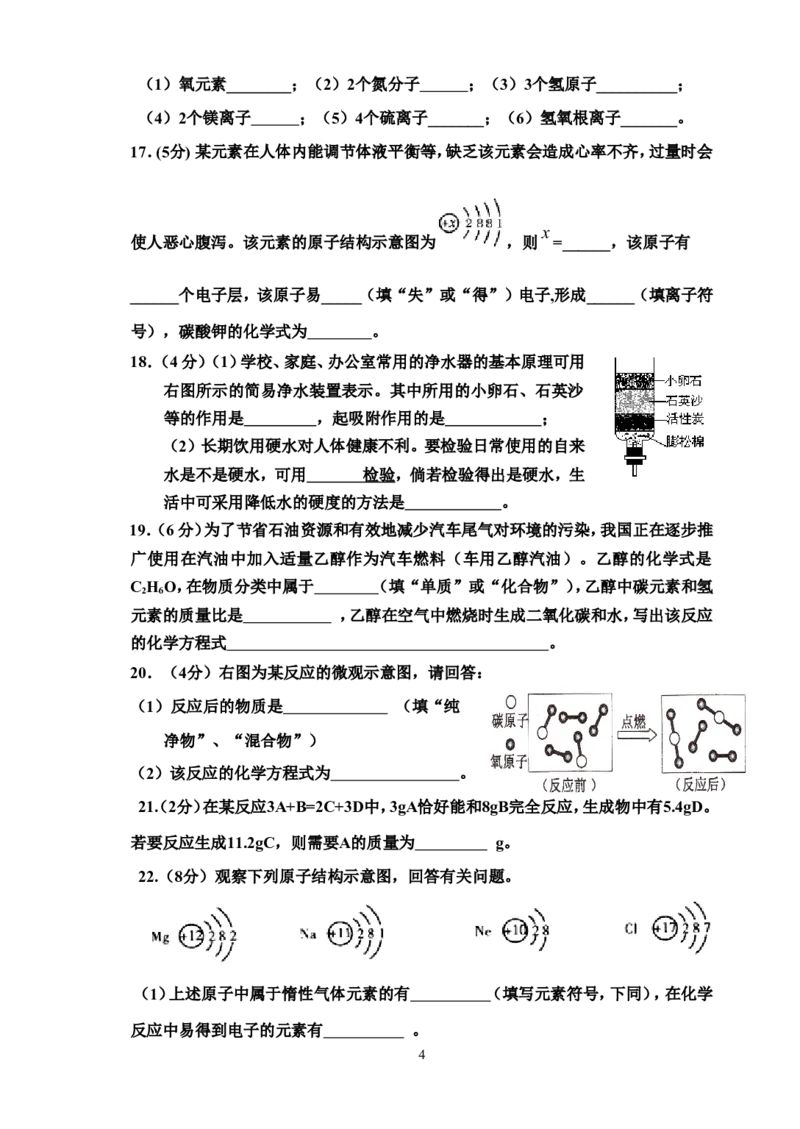
20.(4分)右图为某反应的微观示意图,请回答:
(1)反应后的物质是 (填“纯
净物”、“混合物”)
(2)该反应的化学方程式为 。
21(. 2分)在某反应3A+B=2C+3D中,3gA恰好能和8gB完全反应,生成物中有5.4gD。
若要反应生成11.2gC,则需要A的质量为 g。
22.(8分)观察下列原子结构示意图,回答有关问题。
(1)上述原子中属于惰性气体元素的有 (填写元素符号,下同),在化学
反应中易得到电子的元素有 。
4(2)氯化钠是由 和 构成(用符号表示),镁元素与氯元素所
形成化合物的化学式为 。
(3)硫酸镁的化学式为 ;已知氮化钠的化学式为Na N,则氮元素的化合价
3
为 ;已知硫元素呈现负价时与水中氧元素相同,则硫化钠的化学式为
。
三、实验探究题(本题包括2小题,共19分)
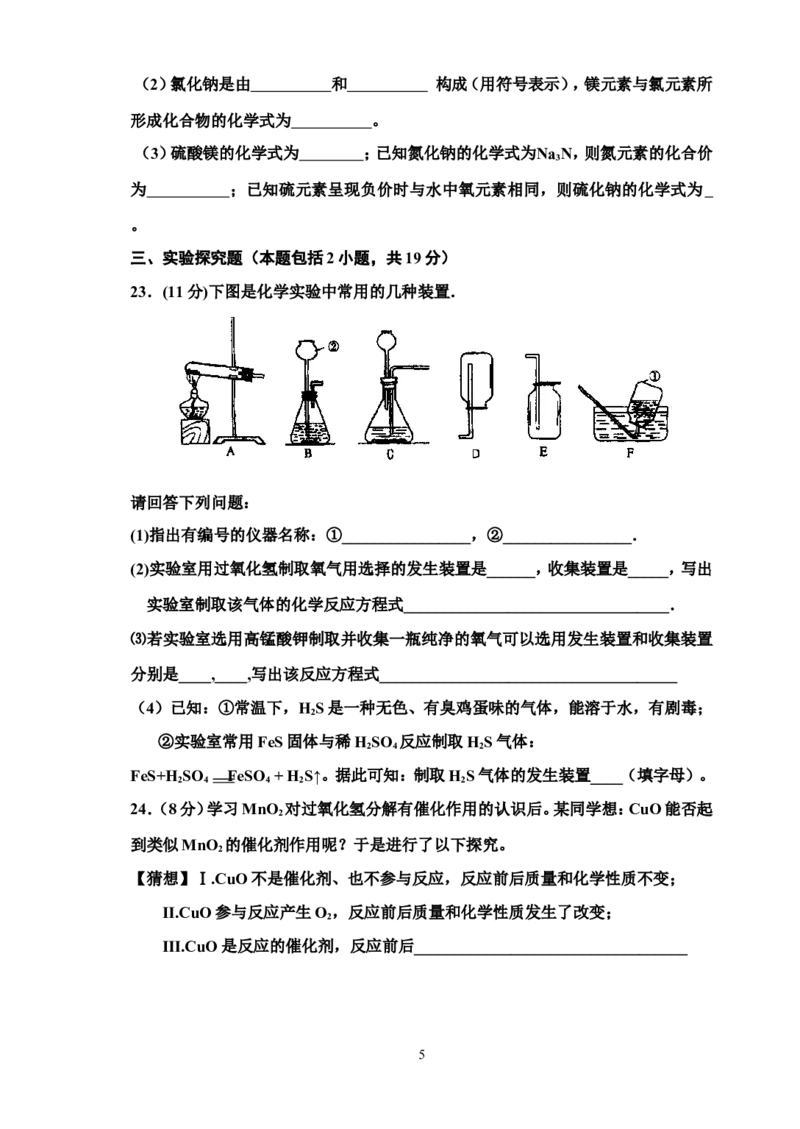
23.(11分)下图是化学实验中常用的几种装置.
请回答下列问题:
(1)指出有编号的仪器名称:①________________,②________________.
(2)实验室用过氧化氢制取氧气用选择的发生装置是______,收集装置是_____,写出
实验室制取该气体的化学反应方程式_________________________________.
⑶若实验室选用高锰酸钾制取并收集一瓶纯净的氧气可以选用发生装置和收集装置
分别是____,____,写出该反应方程式_____________________________________
(4)已知:①常温下,HS是一种无色、有臭鸡蛋味的气体,能溶于水,有剧毒;
2
②实验室常用FeS固体与稀HSO 反应制取HS气体:
2 4 2
FeS+HSO FeSO + HS↑。据此可知:制取HS气体的发生装置____(填字母)。
2 4 4 2 2
24.(8分)学习MnO 对过氧化氢分解有催化作用的认识后。某同学想:CuO能否起
2
到类似MnO 的催化剂作用呢?于是进行了以下探究。
2
【猜想】Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O,反应前后质量和化学性质发生了改变;
2
Ⅲ.CuO是反应的催化剂,反应前后__________________________________
5【实验】用天平称量0.2gCuO,取5ml 5%的过氧化氢溶液于试管中,进行如下实验:
(
1
)
填写下表:
步骤③现象 步骤⑥结果 步骤⑦现象 结 论
溶液中有气泡放出 猜想Ⅰ、Ⅱ不成
带火星的木条复燃 立;猜想Ⅲ成立。
(2) 步骤①的目的是___________________________________
(3) 步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、__________
(4) 过 氧 化 氢 能 被 CuO 催 化 分 解 放 出 O 的 化 学 方 程 式 为
2
____________________
四、计算题(本大题包括2小题,共16分)
25(. 8分)蛋白质在人体胃肠内与水反应,最终生成氨基酸被人体吸收。丙氨酸(化学
式为CHON)就是其中的一种。请回答下列问题:
3 7 2
(1)丙氨酸分子中C、H、O、N各原子个数比为 。
(2)丙氨酸的相对分子质量是 。
(3) 氮元素的质量分数为 (计算结果精确到0.1%)。
(4).欲从丙氨酸中获取28g的氮元素需要丙氨酸的质量为 g
26.(8分)把氯酸钾和二氧化锰的混合物共7g放在试管中加热,完全反应后,冷却。
称得剩余固体5.08g。
求:⑴根据质量守恒定律计算可制得氧气多少克?
⑵剩余固体中含有什么物质?各多少克?
62012~2013 学年度河中实验学校九年级
化学第二次段考参考答案
一、 选择题(每题2分,共30分)
题
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
号
答
D A D C B A D B B A C C B C B
案
二、 填空题(6题,共35分)
16.(1)、O ; (2)、 2N ;(3)、 3H ;
2
(4)、2Mg2+ ;(5)、4S2- ;(6)、OH- ;
17、 19 ;4 ;失 ;K+; KCO
2 3
18.(1)、过滤 ;活性炭 ; (2)、肥皂水 ;煮沸 ;
点燃
19 、 化 合 物 ; 4:1 ;
C HO+3O===== =2CO +3H O
2 6 2 点燃 2 2
20、混合物 ;2CO+ O====2CO ;
2 2
21、6
22、(1)Ne Cl (2) Na+ 、Cl- MgCl (3)MgSO 、-3 、NaS
2 4 2
三、实验题探究题(2题共19分)
23、(1)、①集气瓶;②长颈漏斗;
(2)、B ;E或F;2HO MnO 2HO+O↑
2 2 2 2 2
(3)、 A ; F ;2KMnO KMnO +MnO+O ↑
4 2 4 2 2
(4)、、B
24、【猜想】Ⅲ、质量和化学性质不变
【实验】(1)有气泡放出 CuO质量仍为0.2g 带火星的木条复燃
(2)与步骤③对比,检验加入CuO前后双氧水分解速度有无变化
7(3)玻璃棒(答滤纸不给分)
四、计算题(本大题包括2小题,共16分)
25. (1)、 3 : 7:2 : 1
(2)、 89
(3)、15.7%
(4)、178g
26.⑴、根据质量守恒定律氧气的质量为:7g-5.08g=1.92g
(2)、设完全氯酸钾反应后生成氯化钾的质量为x
149 96
X 1.92g
列出比例是求解得x=2.98g。
反应后的混合物中有氯化钾和二氧化锰质量分别为:2.98g;2.1g
答:。。。。。。
8