文档内容
2015-2016学年山西省太原市九年级(上)培优化学试卷(一)
一、选择题:(每小题有一个正确答案,每小题2分,共20分)
1.由石灰石、水、纯碱为原料制烧碱,所发生的化学反应类型中不包括( )
A.分解反应B.置换反应 C.化合反应 D.复分解反应
2.现有烧杯、试管、量筒、铁架台、铁夹、酒精灯、集气瓶、玻璃片、水槽、玻璃导管、胶皮导管、单孔橡
皮管、药匙十三种实验仪器,用这些仪器不能进行下列实验的是( )
A.配制100克20%的氢氧化钠溶液
B.氢气还原氧化铜
C.制取氧气
D.粗盐的提纯
3.如果一个碳12原子的相对原子质量为24,则不会改变的是( )
A.氧原子的相对质量
B.一个碳12原子的质量
C.硫酸的相对分子质量
D.10g二氧化碳所含的分子个数
4.具有相同质子数的粒子,一定是( )
[来源:Zxxk.Com]
A.同一种元素的粒子B.同一种原子
C.同一种分子 D.无法确定
5.20世纪初,一些化学家提出了酸碱质子理论.这种理论认为,凡能放出质子(H+)的分子或离子都
是酸;凡能结合质子的分子或离子都是碱.根据这一理论,下列物质中既属于酸又属于碱的是( )
A.HNO B.HCO ﹣ C.NH + D.SO 2﹣
3 3 4 4
6.在托盘天平的两边各放一只烧杯,调节天平至平衡,向两烧杯中分别注入等质量、等质量分数稀盐
酸,然后向右盘的烧杯中放入一定质量的铁,同时向左盘的烧杯中放入与铁等质量的铝,待充分反应
后,不可能出现的现象是( )
A.天平仍然平衡B.天平指针偏向铁一方
C.天平指针偏向铝一方 D.铁和铝均有剩余
7.鉴别①MgSO 4②NaOH ③CuCl 2④KNO
3
四种溶液,不用其他任何试剂,可用先被辨认出来的物质鉴
别剩余物质,则被鉴别出物质顺序正确的是( )
A.①②③④B.③①②④ C.④③②① D.③②①④
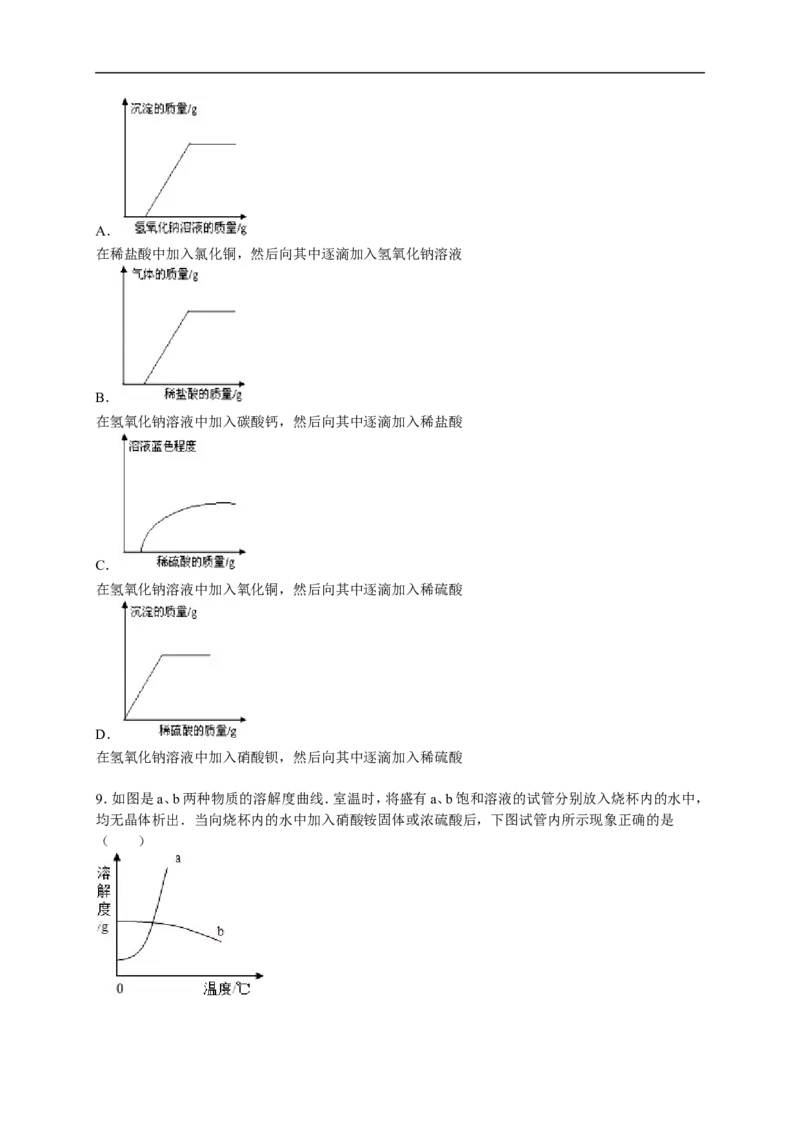
8.探究中和反应是否发生的方法有多种.小华同学进行了以下四个实验,并用图象分别描述了实验
过程中的现象.其中,依据图示现象不能判断中和反应一定发生的是( )A.
在稀盐酸中加入氯化铜,然后向其中逐滴加入氢氧化钠溶液
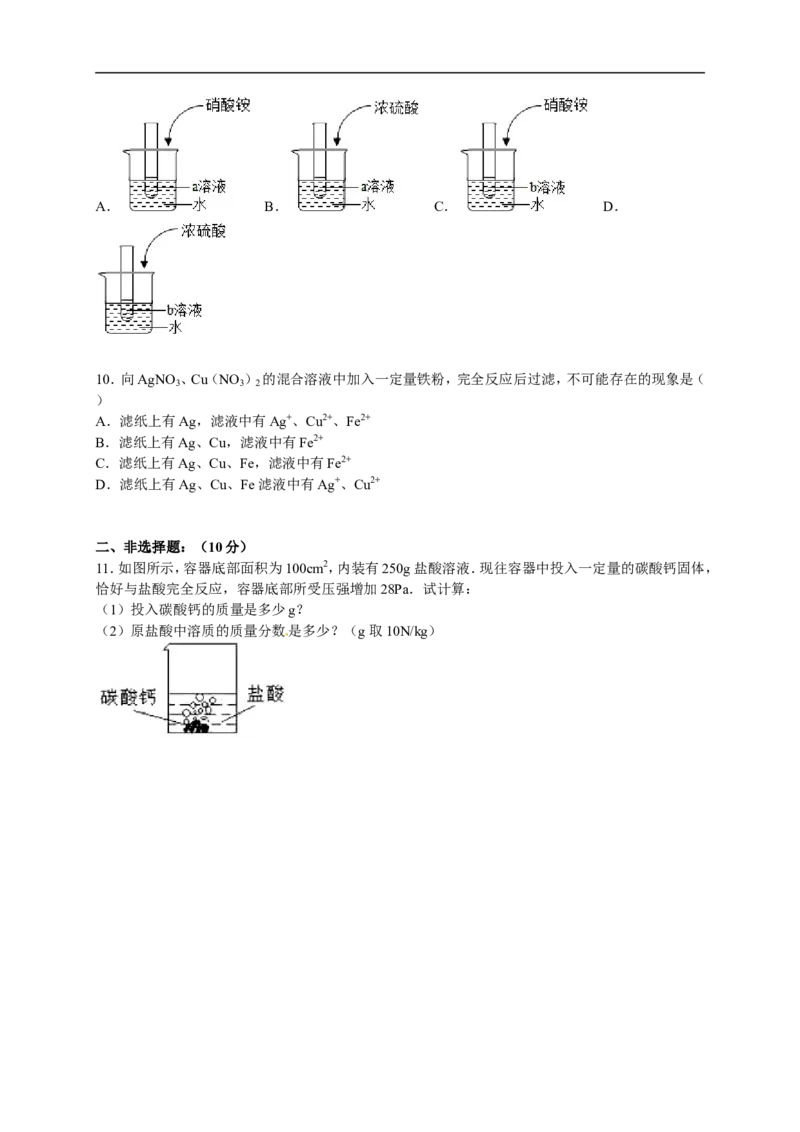
B.
在氢氧化钠溶液中加入碳酸钙,然后向其中逐滴加入稀盐酸
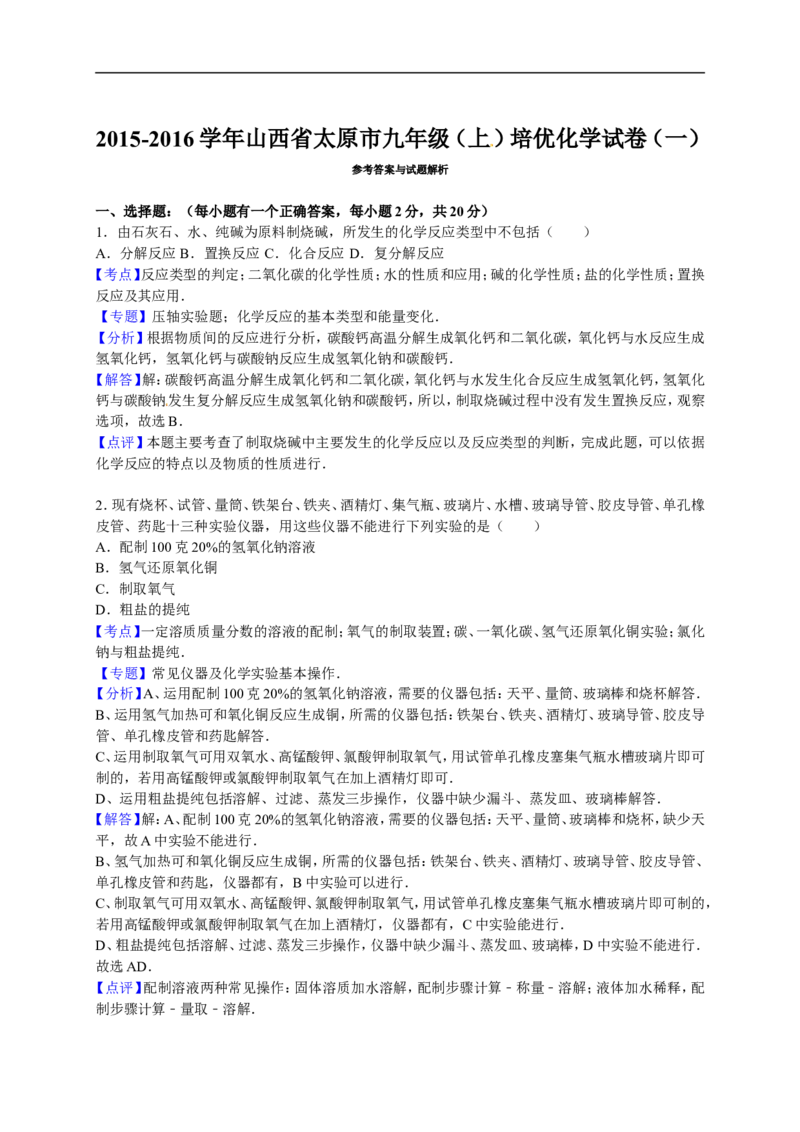
C.
在氢氧化钠溶液中加入氧化铜,然后向其中逐滴加入稀硫酸
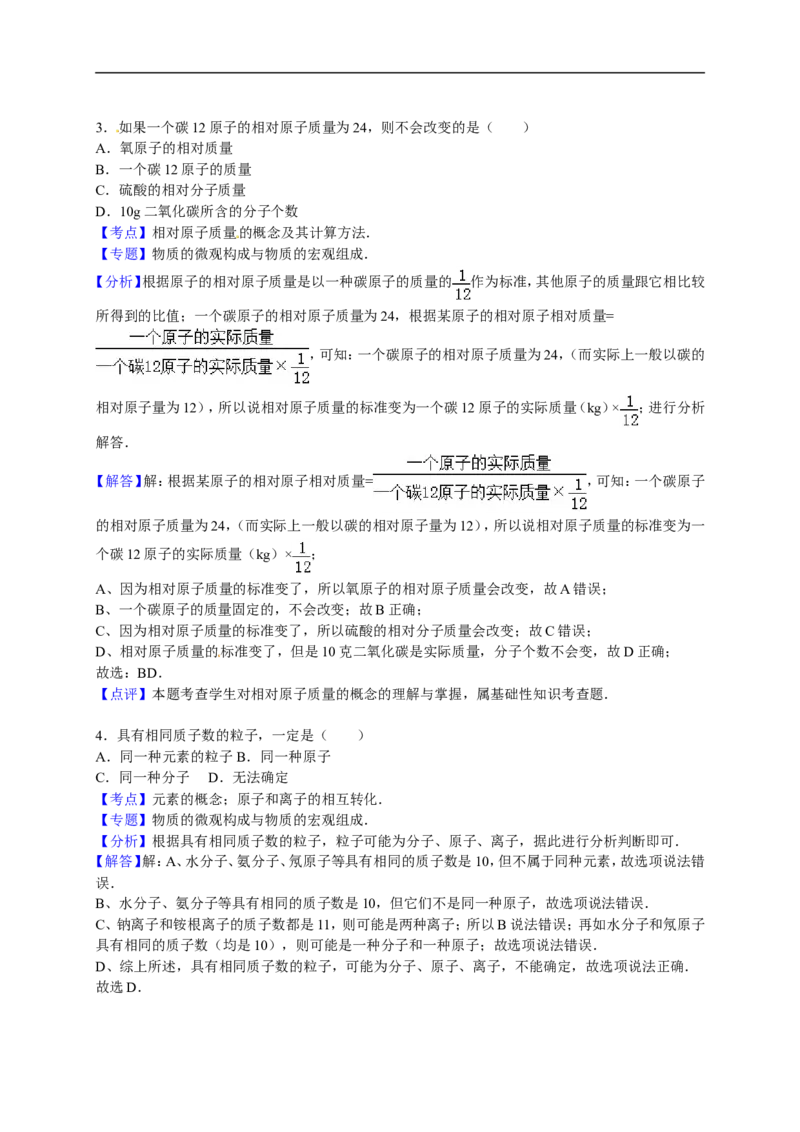
D.
在氢氧化钠溶液中加入硝酸钡,然后向其中逐滴加入稀硫酸
9.如图是a、b两种物质的溶解度曲线.室温时,将盛有a、b饱和溶液的试管分别放入烧杯内的水中,
均无晶体析出.当向烧杯内的水中加入硝酸铵固体或浓硫酸后,下图试管内所示现象正确的是
( )A. B. C. D.
10.向AgNO 、Cu(NO )的混合溶液中加入一定量铁粉,完全反应后过滤,不可能存在的现象是(
3 3 2
)
A.滤纸上有Ag,滤液中有Ag+、Cu2+、Fe2+
B.滤纸上有Ag、Cu,滤液中有Fe2+
C.滤纸上有Ag、Cu、Fe,滤液中有Fe2+
[来源:学&科&网Z&X&X&K]
D.滤纸上有Ag、Cu、Fe 滤液中有Ag+、Cu2+
二、非选择题:(10分)
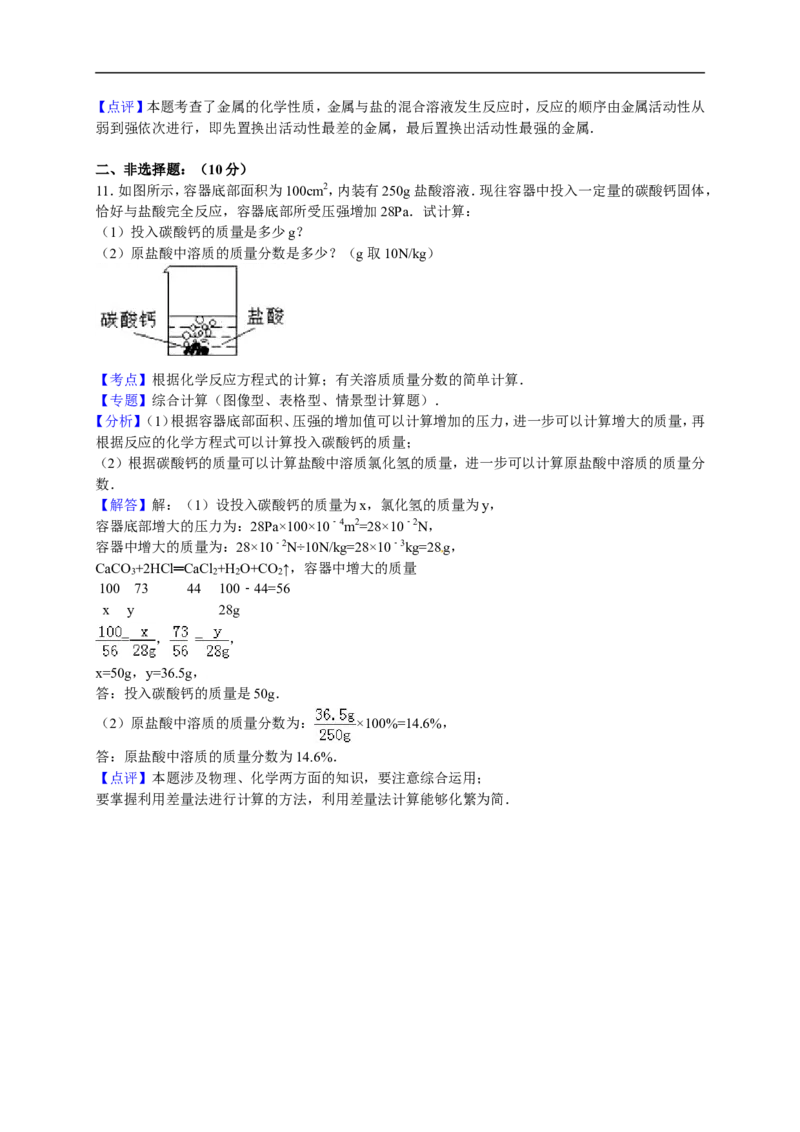
11.如图所示,容器底部面积为100cm2,内装有250g 盐酸溶液.现往容器中投入一定量的碳酸钙固体,
恰好与盐酸完全反应,容器底部所受压强增加28Pa.试计算:
(1)投入碳酸钙的质量是多少g?
(2)原盐酸中溶质的质量分数是多少?(g 取10N/kg)2015-2016 学年山西省太原市九年级(上)培优化学试卷(一)
参考答案与试题解析
一、选择题:(每小题有一个正确答案,每小题2分,共20分)
1.由石灰石、水、纯碱为原料制烧碱,所发生的化学反应类型中不包括( )
A.分解反应B.置换反应 C.化合反应 D.复分解反应
【考点】反应类型的判定;二氧化碳的化学性质;水的性质和应用;碱的化学性质;盐的化学性质;置换
反应及其应用.
【专题】压轴实验题;化学反应的基本类型和能量变化.
【分析】根据物质间的反应进行分析,碳酸钙高温分解生成氧化钙和二氧化碳,氧化钙与水反应生成
氢氧化钙,氢氧化钙与碳酸钠反应生成氢氧化钠和碳酸钙.
【解答】解:碳酸钙高温分解生成氧化钙和二氧化碳,氧化钙与水发生化合反应生成氢氧化钙,氢氧化
钙与碳酸钠发生复分解反应生成氢氧化钠和碳酸钙,所以,制取烧碱过程中没有发生置换反应,观察
选项,故选B.
【点评】本题主要考查了制取烧碱中主要发生的化学反应以及反应类型的判断,完成此题,可以依据
化学反应的特点以及物质的性质进行.
2.现有烧杯、试管、量筒、铁架台、铁夹、酒精灯、集气瓶、玻璃片、水槽、玻璃导管、胶皮导管、单孔橡
皮管、药匙十三种实验仪器,用这些仪器不能进行下列实验的是( )
A.配制100克20%的氢氧化钠溶液
[来源:学科网]
B.氢气还原氧化铜
C.制取氧气
D.粗盐的提纯
【考点】一定溶质质量分数的溶液的配制;氧气的制取装置;碳、一氧化碳、氢气还原氧化铜实验;氯化
钠与粗盐提纯.
【专题】常见仪器及化学实验基本操作.
【分析】A、运用配制100克20%的氢氧化钠溶液,需要的仪器包括:天平、量筒、玻璃棒和烧杯解答.
B、运用氢气加热可和氧化铜反应生成铜,所需的仪器包括:铁架台、铁夹、酒精灯、玻璃导管、胶皮导
管、单孔橡皮管和药匙解答.
C、运用制取氧气可用双氧水、高锰酸钾、氯酸钾制取氧气,用试管单孔橡皮塞集气瓶水槽玻璃片即可
制的,若用高锰酸钾或氯酸钾制取氧气在加上酒精灯即可.
D、运用粗盐提纯包括溶解、过滤、蒸发三步操作,仪器中缺少漏斗、蒸发皿、玻璃棒解答.
【解答】解:A、配制100克20%的氢氧化钠溶液,需要的仪器包括:天平、量筒、玻璃棒和烧杯,缺少天
平,故A中实验不能进行.
B、氢气加热可和氧化铜反应生成铜,所需的仪器包括:铁架台、铁夹、酒精灯、玻璃导管、胶皮导管、
单孔橡皮管和药匙,仪器都有,B中实验可以进行.
C、制取氧气可用双氧水、高锰酸钾、氯酸钾制取氧气,用试管单孔橡皮塞集气瓶水槽玻璃片即可制的,
若用高锰酸钾或氯酸钾制取氧气在加上酒精灯,仪器都有,C中实验能进行.
D、粗盐提纯包括溶解、过滤、蒸发三步操作,仪器中缺少漏斗、蒸发皿、玻璃棒,D中实验不能进行.
故选AD.
【点评】配制溶液两种常见操作:固体溶质加水溶解,配制步骤计算﹣称量﹣溶解;液体加水稀释,配
制步骤计算﹣量取﹣溶解.3.如果一个碳12原子的相对原子质量为24,则不会改变的是( )
A.氧原子的相对质量
B.一个碳12原子的质量
C.硫酸的相对分子质量
D.10g二氧化碳所含的分子个数
【考点】相对原子质量的概念及其计算方法.
【专题】物质的微观构成与物质的宏观组成.
【分析】根据原子的相对原子质量是以一种碳原子的质量的 作为标准,其他原子的质量跟它相比较
所得到的比值;一个碳原子的相对原子质量为24,根据某原子的相对原子相对质量=
,可知:一个碳原子的相对原子质量为24,(而实际上一般以碳的
相对原子量为12),所以说相对原子质量的标准变为一个碳12原子的实际质量(kg)× ;进行分析
解答.
【解答】解:根据某原子的相对原子相对质量= ,可知:一个碳原子
的相对原子质量为24,(而实际上一般以碳的相对原子量为12),所以说相对原子质量的标准变为一
个碳12原子的实际质量(kg)× ;
A、因为相对原子质量的标准变了,所以氧原子的相对原子质量会改变,故A错误;
B、一个碳原子的质量固定的,不会改变;故B正确;
C、因为相对原子质量的标准变了,所以硫酸的相对分子质量会改变;故C错误;
D、相对原子质量的标准变了,但是10克二氧化碳是实际质量,分子个数不会变,故D正确;
故选:BD.
【点评】本题考查学生对相对原子质量的概念的理解与掌握,属基础性知识考查题.
4.具有相同质子数的粒子,一定是( )
A.同一种元素的粒子B.同一种原子
C.同一种分子 D.无法确定
【考点】元素的概念;原子和离子的相互转化.
【专题】物质的微观构成与物质的宏观组成.
【分析】根据具有相同质子数的粒子,粒子可能为分子、原子、离子,据此进行分析判断即可.
【解答】解:A、水分子、氨分子、氖原子等具有相同的质子数是10,但不属于同种元素,故选项说法错
误.
B、水分子、氨分子等具有相同的质子数是10,但它们不是同一种原子,故选项说法错误.
C、钠离子和铵根离子的质子数都是11,则可能是两种离子;所以B说法错误;再如水分子和氖原子
具有相同的质子数(均是10),则可能是一种分子和一种原子;故选项说法错误.
D、综上所述,具有相同质子数的粒子,可能为分子、原子、离子,不能确定,故选项说法正确.
故选D.【点评】本题考查具有相同质子数的微粒,学生应明确常见的粒子有分子、原子、离子,利用举例的方
法来判断说法的正误是正确解答本题的捷径.
5.20世纪初,一些化学家提出了酸碱质子理论.这种理论认为,凡能放出质子(H+)的分子或离子都
是酸;凡能结合质子的分子或离子都是碱.根据这一理论,下列物质中既属于酸又属于碱的是( )
A.HNO B.HCO ﹣ C.NH + D.SO 2﹣
3 3 4 4
【考点】常见的氧化物、酸、碱和盐的判别.
【专题】化学物质的分类思想;物质的分类.
【分析】根据题意,凡能放出质子(H+)的分子或离子都是酸;凡能结合质子的分子或离子都是碱;据此
进行分析判断.
【解答】解:A、硝酸能放出质子(H+),但不能结合质子,属于酸,不属于碱,故选项错误.
B、HCO ﹣能结合质子(H+)生成水和二氧化碳,能放出质子(H+),生成碳酸根离子,既属于酸又属于
3
碱,故选项正确.
C、NH +能放出质子(H+),但不能结合质子,属于酸,不属于碱,故选项错误.
4
D、硫酸根离子能结合质子(H+)生成硫酸,但不能放出质子(H+),属于碱,不属于酸,故选项错误.
故选:B.
【点评】本题难度不大,理解凡能放出质子(H+)的分子或离子都是酸、凡能结合质子的分子或离子都
是碱是正确金属本题的关键.
[来源:Z_xx_k.Com]
6.在托盘天平的两边各放一只烧杯,调节天平至平衡,向两烧杯中分别注入等质量、等质量分数稀盐
酸,然后向右盘的烧杯中放入一定质量的铁,同时向左盘的烧杯中放入与铁等质量的铝,待充分反应
后,不可能出现的现象是( )
A.天平仍然平衡B.天平指针偏向铁一方
C.天平指针偏向铝一方 D.铁和铝均有剩余
【考点】金属活动性顺序及其应用;根据化学反应方程式的计算.
【专题】压轴实验题;有关化学方程式的计算;金属与金属材料.
【分析】根据物质之间的反应以及反应的化学方程式进行分析,从酸过量和金属过量两个方面分析.
【解答】解:若酸过量,则金属全部参加反应,设金属的质量为54,由铁生成的氢气的质量为x,
2Al+6HCl═2AlCl +3H ↑
3 2
54 6
Fe+2HCl═FeCl2+H ↑
2
56 2
54 x
=
x=1.9
可以看出相同质量的铝和铁与足量的盐酸反应,铝生成的氢气质量比铁多,故天平会指向加铁的一
方,
若酸量不足,则酸全部参加反应,相同的酸生成氢气的质量相等,故天平会仍然平衡,金属铝和铁有
可能全部剩余,
观察选项,故选C.
【点评】本题考查了金属与酸反应与物理知识的结合,完成此题,可以依据物质间反应的化学方程式
以及酸过量或金属过量的角度进行.7.鉴别①MgSO 4②NaOH ③CuCl 2④KNO
3
四种溶液,不用其他任何试剂,可用先被辨认出来的物质鉴
别剩余物质,则被鉴别出物质顺序正确的是( )
A.①②③④B.③①②④ C.④③②① D.③②①④
【考点】酸、碱、盐的鉴别.
【专题】物质的鉴别题.
【分析】四种物质中,只有氯化铜溶液呈蓝色,所以根据溶液颜色可以首先鉴别出氯化铜;然后把蓝色
氯化铜溶液分别滴入另三种溶液,出现蓝色沉淀的为氢氧化钠;再把氢氧化钠溶液分别滴入所余两种
溶液,出现白色沉淀为硫酸镁,无明显现象为硝酸钾.
【解答】解:氯化铜溶液为蓝色溶液,可以首先鉴别出来;然后利用氢氧化钠与氯化铜生成蓝色氢氧化
铜沉淀,鉴别出氢氧化钠;再使用氢氧化钠能与硫酸镁生成氢氧化镁沉淀而鉴别出硫酸镁,最后所余
物质则为硝酸钾;被鉴别出物质顺序③②①④.
故选D
【点评】不用任何其它试剂鉴别物质类问题,通常使用溶液的颜色或特殊物质的反应现象首先把该物
质鉴别出来.
8.探究中和反应是否发生的方法有多种.小华同学进行了以下四个实验,并用图象分别描述了实验
过程中的现象.其中,依据图示现象不能判断中和反应一定发生的是( )
A.
在稀盐酸中加入氯化铜,然后向其中逐滴加入氢氧化钠溶液
B.
在氢氧化钠溶液中加入碳酸钙,然后向其中逐滴加入稀盐酸
C.
在氢氧化钠溶液中加入氧化铜,然后向其中逐滴加入稀硫酸D.
在氢氧化钠溶液中加入硝酸钡,然后向其中逐滴加入稀硫酸
【考点】中和反应及其应用;酸的化学性质;碱的化学性质.
【专题】常见的酸 酸的通性.
【分析】向含有碱的混合溶液中加入酸或含有碱的溶液中加入酸,酸要和碱反应,即先要发生中和反
应,再进行其它反应同时出现现象,其判断依据就是观察图象一开始是否有一段体现了中和反应的发
生过程,即没有现象发生的一段图象其纵坐标为零,而后对选项反应的具体分析找到解决此问题的突
破口.
【解答】解:A、在稀盐酸中加入氯化铜,然后向其中逐滴加入NaOH溶液,在酸性的环境下氢氧化铜
难以沉淀,所以必须先把盐酸消耗掉才能生成沉淀,根据图象可以判断出酸碱的中和反应的发生,故
A能判断中和反应一定发生;
B、在NaOH溶液中加入CaCO ,然后向其中逐滴加入稀盐酸,在酸性环境中碳酸钠不能存在,所以稀
3
盐酸要先和氢氧化钠反应,然后才会和碳酸钙反应生成气体和碳酸钠,故B能判断中和反应一定发
生;
C、在NaOH溶液中加入CuO,然后向其中逐滴加入稀硫酸,溶液颜色体现主要来自于硫酸铜的浓度,
而氢氧化钠可以和硫酸铜反应生成氢氧化铜沉淀,所以必须将氢氧化钠完全消耗之后才能够形成硫
酸铜溶液,即硫酸要和氢氧化钠反应然后才能观察到蓝色溶液,故C能判断中和反应一定发生.
D、硫酸和硝酸钡反应生成难溶的硫酸钡沉淀,而体现不出中和反应的发生,故D不能判断中和反应
一定发生.
故选D.
【点评】此题是对化学反应及图象的考查,解题的重点是能正确的分析变化的过程,读懂图象并与反
应相结合是解题的关键所在,是一道训练学生分析问题能力的习题.
9.如图是a、b两种物质的溶解度曲线.室温时,将盛有a、b饱和溶液的试管分别放入烧杯内的水中,
均无晶体析出.当向烧杯内的水中加入硝酸铵固体或浓硫酸后,下图试管内所示现象正确的是
( )A. B. C. D.
【考点】溶解时的吸热或放热现象;结晶的原理、方法及其应用;固体溶解度曲线及其作用.
【专题】结合课本知识的信息;压轴实验题.
【分析】根据硝酸铵溶于水使溶液的温度降低,浓硫酸溶于水使溶液的温度升高.a物质的溶解度随温
度升高而增大,b物质的溶解度随温度升高而减小来考虑本题.
【解答】解:A、硝酸铵溶于水使溶液的温度降低,a物质的溶解度减小所以会有晶体析出,故A正确;
B、浓硫酸溶于水使溶液的温度升高.a物质的溶解度增大,不会有晶体析出,故B错误;
C、硝酸铵溶于水使溶液的温度降低,b物质的溶解度增大不会有晶体析出,故C错误;
D、浓硫酸溶于水使溶液的温度升高,b物质的溶解度减小,会有晶体析出,故D错误.
故选A.
【点评】通过回答本题知道了硝酸铵溶于水使溶液的温度降低,浓硫酸溶于水使溶液的温度升高,溶
解度增大不会有晶体析出,溶解度减小会有晶体析出.
10.向AgNO 、Cu(NO )的混合溶液中加入一定量铁粉,完全反应后过滤,不可能存在的现象是(
3 3 2
)
A.滤纸上有Ag,滤液中有Ag+、Cu2+、Fe2+
B.滤纸上有Ag、Cu,滤液中有Fe2+
C.滤纸上有Ag、Cu、Fe,滤液中有Fe2+
D.滤纸上有Ag、Cu、Fe 滤液中有Ag+、Cu2+
【考点】金属的化学性质.
【专题】金属与金属材料.
【分析】在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金
属从其盐溶液中置换出来,金属铁加入硝酸铜和硝酸银的混合溶液中铁会把银和铜置换出来;由于反
应情况与所加入铁粉的量密切相关,可从铁由不足量到过量分别进行分析.
【解答】解:根据金属活动性,铁能把银和铜从溶液中置换出来,首先置换活动性最弱的银,然后置换
铜;根据加入的铁的多少,
A、当铁的量很少时,只能置换出少量的银,此时滤渣中只有银;滤液中有Ag+、Cu2+、Fe2+,故A可能;
B、当铁置换出银后还有剩余,就能置换出铜,此时滤渣中含有银和铜;铜完全被置换后,滤液中有
Fe2+,故B可能;
C、当铁过量,完全置换出铜和银后还有剩余,此时滤出固体中组成最复杂,含有铜、铁、银三种金属,
滤液中只有Fe2+,故C可能;
D、滤纸上有Ag、Cu、Fe 滤液中有Ag+、Cu2+不可能,因为铁会继续置换Ag+、Cu2+,故D符合题意;
故选项为:D.【点评】本题考查了金属的化学性质,金属与盐的混合溶液发生反应时,反应的顺序由金属活动性从
弱到强依次进行,即先置换出活动性最差的金属,最后置换出活动性最强的金属.
二、非选择题:(10分)
11.如图所示,容器底部面积为100cm2,内装有250g 盐酸溶液.现往容器中投入一定量的碳酸钙固体,
恰好与盐酸完全反应,容器底部所受压强增加28Pa.试计算:
(1)投入碳酸钙的质量是多少g?
(2)原盐酸中溶质的质量分数是多少?(g 取10N/kg)
【考点】根据化学反应方程式的计算;有关溶质质量分数的简单计算.
【专题】综合计算(图像型、表格型、情景型计算题).
【分析】(1)根据容器底部面积、压强的增加值可以计算增加的压力,进一步可以计算增大的质量,再
根据反应的化学方程式可以计算投入碳酸钙的质量;
(2)根据碳酸钙的质量可以计算盐酸中溶质氯化氢的质量,进一步可以计算原盐酸中溶质的质量分
数.
【解答】解:(1)设投入碳酸钙的质量为x,氯化氢的质量为y,
容器底部增大的压力为:28Pa×100×10﹣4m2=28×10﹣2N,
容器中增大的质量为:28×10﹣2N÷10N/kg=28×10﹣3kg=28g,
CaCO +2HCl═CaCl +H O+CO ↑,容器中增大的质量
3 2 2 2
100 73 44 100﹣44=56
x y 28g
= , = ,
x=50g,y=36.5g,
[来源:学_科_网]
答:投入碳酸钙的质量是50g.
(2)原盐酸中溶质的质量分数为: ×100%=14.6%,
答:原盐酸中溶质的质量分数为14.6%.
【点评】本题涉及物理、化学两方面的知识,要注意综合运用;
要掌握利用差量法进行计算的方法,利用差量法计算能够化繁为简.