文档内容
《铁 金属材料》单元测试(基础巩固)
学校:___________姓名:___________班级:___________考号:___________
一、单选题(共54分)
1.(本题3分)铁的下列性质中不属于纯铁的物理性质是
A.质软 B.银白色 C.能导电 D.易生锈
【答案】D
【详解】
物理性质通常包括:颜色、状态、气味、密度、硬度、熔沸点、导电性、导热性、溶解性等,所以铁质软、
银白色、能导电,均为物理性质,而易生锈是指易被氧化,为化学性质;
综上所述答案为D。
2.(本题3分)下列有关铁及其化合物的说法错误的是
A.陨铁中存在游离态的铁
B.铁能与水蒸气反应,生成氧化铁和氢气
C.铁的氧化物都不溶于水,也不与水反应
D.氢氧化亚铁在空气中易被氧化成氢氧化铁
【答案】B
【详解】
A.游离态的铁主要存在陨铁中,A项正确;
B.铁能与水蒸气反应,生成四氧化三铁和氢气,B项错误;
C.铁的氧化物性质稳定,不溶于水,也不与水反应,C项正确;
D.氢氧化亚铁在空气中与氧气和水反应,被氧化成氢氧化铁,D项正确;
答案选B。
3.(本题3分)一些高档茶叶、点心等食品的包装盒中有一个小袋,将小袋打开,可以看到黑色粉末,部分
已变成棕褐色。将上述粉末溶于稀盐酸,取上层清液,滴入几滴氯水,再滴加KSCN溶液,溶液立即变为
红色。下列说法不正确的是
A.小袋中原来装有氧化铁 B.小袋中原来装有铁粉
C.该黑色粉末不可食用 D.该黑色粉末做抗氧化剂
【答案】A
【详解】
从题中信息“滴入几滴氰水,再滴加KSCN溶液,溶液立即变为红色”判断,该黑色粉末中含有铁元素。但由于先加入了氯水,故不能确定其一定含Fe3+,A项错误;该黑色粉末为还原铁粉,做抗氧化剂,防止高
档茶叶、点心等食品变质,B、C、D项正确;
故答案选A。
4.(本题3分)下列溶液能溶解铁且无新的固体和气体产生的是
A.CuSO 溶液 B.稀硫酸 C.FeCl 溶液 D.AgNO 溶液
4 3 3
【答案】C
【详解】
A.CuSO 溶液和铁反应生成铜单质和硫酸亚铁,生成了新的固体,故A不符合题意;
4
B.稀硫酸与铁反应生成硫酸亚铁和氢气,有气体产生,故B不符合题意;
C.FeCl 溶液与铁反应生成氯化亚铁,无新固体和气体生成,故C符合题意;
3
D.AgNO 溶液和铁反应生成银单质和硝酸亚铁,生成了新的固体,故D不符合题意。
3
综上所述,答案为C。
5.(本题3分)某学习小组进行了如图所示的实验,实验后组员之间的交流不合理的是
A.甲同学认为试管b中收集到的气体可点燃,且产生淡蓝色火焰
B.乙同学认为试管a中生成的黑色固体可能为四氧化三铁
C.丙同学认为将少量还原性铁粉放入试管中,加适量的水,加热也可实现该反应
D.丁同学认为用盐酸溶解生成固体所得溶液有颜色
【答案】C
【详解】
A.粉与水蒸气在高温条件下反应生成四氧化三铁和氢气,氢气燃烧产生蓝色火焰,故A正确;
B.因为铁与水蒸气在高温时发生反应生成四氧化三铁和氢气,故B正确;
C.铁粉在高温下才能与水蒸气反应,与水加热不反应,故C错误;
D.用盐酸溶解固体生成物得到氯化亚铁和氯化铁的混合溶液,溶液带有颜色,故D正确;
故选:C。
6.(本题3分)将1.12 g铁粉加入25mL2molL-1氯化铁溶液中充分反应(忽略溶液体积变化),下列分析正确
⋅的是
A.铁粉有剩余
B.Cl-浓度减小
C.向溶液中滴入无色KSCN溶液,溶液不变红
D.反应液质量增加1.12 g
【答案】D
【详解】
A.铁和氯化铁的物质的量分别是0.02 mol、0.05 mol,根据化学方程式Fe+2Fe3+=3Fe2+可知铁离子是过量
的,剩余0.01 mol铁离子,A错误;
B.氯离子不参加反应,浓度不变,B错误;
C.铁离子是过量的,滴入无色KSCN溶液,溶液变红,C错误;
D.根据A选项分析可知反应液增加的质量即为0.02 mol铁粉的质量,为0.02mol×56g/mol=1.12g,D正确;
综上所述答案为D。
7.(本题3分)下列有关铁、铁矿石与铁的氧化物的说法正确的是
A.赤铁矿的主要成分是Fe O,磁铁矿的主要成分是Fe O,Fe O 俗称铁红
2 3 3 4 2 3
B.在自然界中,不可能有游离态的铁存在
C.能通过化合反应制得Fe(OH) ,但不能通过化合反应制得FeCl
3 2
D.铁的氧化物能与酸反应生成盐和水,因此Fe O、Fe O、FeO都是碱性氧化物
3 4 2 3
【答案】A
【详解】
A.赤铁矿的主要成分是Fe O 俗称铁红,磁铁矿的主要成分是Fe O,故A正确;
2 3 3 4
B.在自然界中,铁陨石有游离态的铁存在,故B错误;
C.能通过 制得Fe(OH) ,也能通过 得FeCl ,故C错误;
3 2
D.分析铁的化合价可知Fe O 不是碱性氧化物,Fe O、FeO是碱性氧化物,故D错误;
3 4 2 3
故答案为:A
8.(本题3分)下列反应的离子方程式正确的是
A.铁钉放入硫酸铜溶液中:
B.硫酸铜溶液与Ca(OH) 溶液混合:
2
C.钠与水反应:D.氧化铁与稀盐酸混合:
【答案】D
【详解】
A.铁钉放入硫酸铜溶液中,发生金属之间的置换反应产生Cu单质,离子方程式为:Fe+Cu2+=Fe2++Cu,A
错误;
B.二者反应产生Cu(OH) 沉淀,离子方程式应该为:Cu2++2OH-=Cu(OH) ↓,B错误;
2 2
C.原子不守恒,电子不守恒,离子方程式应该是:2Na+2HO=2Na++2OH-+H ↑,C错误;
2 2
D.反应符合事实,遵循物质的拆分原则,D正确;
故合理选项是D。
9.(本题3分)要除去FeCl 溶液中少量的FeCl ,可行的方法是
2 3
A.滴入KSCN溶液
B.通入氯气
C.加入适量铜粉并过滤
D.加入适量铁粉并过滤
【答案】D
【详解】
A.硫氰化钾溶液是用于检验Fe3+,FeCl +3KSCN Fe(SCN) +3KCl,引入了新杂质,故A错误;
3 3
B.氯气与氯化亚铁溶液发生氧化还原反应,故B错误;
C.铜与氯化铁反应生成氯化铜和氯化亚铁,引入了新杂质,故C错误;
D.铁与氯化铁生成氯化亚铁,过量的铁粉过滤除去,故D正确;
故答案:D。
10.(本题3分)已知2Fe3++Fe=3Fe2+,将适量铁粉放入FeCl 溶液中,完全反应后,溶液中的Fe2+和Fe3+个数
3
相等,则已反应的Fe3+和未反应的Fe3+的个数之比是
A.2:3 B.3:2 C.1:2 D.1:1
【答案】A
【详解】
将适量铁粉放入FeCl 溶液中,发生2Fe3++Fe=3Fe2+,设参加反应的Fe3+为x个,则 反
3
应生成Fe2+为1.5x个,已知溶液中的Fe2+和Fe3+个数相等,则溶液中的Fe3+个数为1.5x, 则已反应的Fe3+和未反应的Fe3+的个数之比是 ,则A满足;
答案选A。
11.(本题3分)我国铝材工业水平处于世界领先行列。下列说法不正确的是
A.铝制餐具不宜长时间盛放酸性、碱性或咸的食物
B.常温下,铝制品耐腐蚀是因为铝不活泼
C.铝合金密度小、强度高,广泛应用于航空领域
D.工业上常用NaOH溶液去除铝表面的氧化膜
【答案】B
【详解】
A.酸、碱、盐等可直接侵蚀铝的氧化物且铝与酸、碱都能发生反应,所以铝制餐具不宜长时间盛放酸性、
碱性或咸的食物,故A正确;
B.常温下,铝制品耐腐蚀是因为铝表面被氧化后形成一层致密的氧化物薄膜,阻止金属继续被腐蚀,而
不是因为铝不活泼,故B错误;
C.合金的硬度大于其成分金属,铝合金密度小、强度高,广泛应用于航空领域,故C正确;
D.氧化铝为两性氧化物,能够与NaOH反应生成偏铝酸钠和水,工业上常用NaOH溶液去除铝表面的氧
化膜,故D正确;
答案选B。
12.(本题3分)下列物质中,不是既能跟盐酸反应,又能跟NaOH反应的是
A.NaHCO B.Al C.Al O D.Fe O
3 2 3 2 3
【答案】D
【详解】
A.NaHCO 能与盐酸反应生成CO,也能跟NaOH反应生成 ,A不符合题意;
3 2
B.Al能跟盐酸反应生成Al3+,也能跟NaOH反应生成 ,B不符合题意;
C.Al O 能跟盐酸反应生成Al3+,也能跟NaOH反应生成 ,C不符合题意;
2 3
D.Fe O 能跟盐酸反应生成Fe3+,不能跟NaOH反应,D符合题意;
2 3
故选D。
13.(本题3分)下列对金属和金属材料的认识中,不正确的是( )
A.生铁和钢的性能完全相同
B.铁在潮湿的空气中容易生锈C.赤铁矿的主要成分是氧化铁
D.回收废旧金属有利于节约金属资源
【答案】A
【详解】
A、生铁与钢含碳量不同,性能不同,生铁硬而脆,钢韧性强,故A说法错误;
B、铁在潮湿的空气中容易发生吸氧腐蚀或析氢腐蚀,加速铁的腐蚀,故B说法正确;
C、氧化铁为红棕色,Fe O 为黑色晶体,FeO为黑色固体,赤铁矿的主要成分是氧化铁,故C说法正确;
3 4
D、回收废旧金属有利于节约金属资源,故D说法正确;
答案为A。
14.(本题3分)一定质量的铝片分别和足量的氢氧化钠溶液和盐酸反应,相同情况下放出氢气的质量
A.一样多 B.与酸更多 C.与碱更多 D.无法确定
【答案】A
【详解】
根据2Al+2NaOH+2HO=2NaAlO +3H↑和2Al+6HCl=2AlCl +3H↑可知,两个方程式都是2Al~3H ,因
2 2 2 3 2 2
此Al相同且酸和碱都过量的情况下,生成的H 量相等,故选A。
2
15.(本题3分)区别镁铝,最好采用的方法是
A.投入沸水中 B.投入冷水中
C.投入盐酸中 D.投入烧碱溶液中
【答案】D
【详解】
A.Mg与沸水反应比较剧烈,可以生成H,由于沸水本身就有气泡产生,因此将Mg和Al投入沸水中现
2
象没有明显区别,A不符合题意;
B.Mg和Al投入冷水中均没有明显现象,B不符合题意;,
C.Mg和Al投入盐酸中反应均比较剧烈,有H 生成,C不符合题意;
2
D.Mg不与NaOH反应,Al可以反应生成H,2Al+2NaOH+2HO=2NaAlO +3H↑,现象有明显区别,
2 2 2 2
D符合题意;
故选D。
16.(本题3分)下列关于铁铝的性质叙述错误的是
A.补血剂中含有铁元素,人体缺铁,会引起贫血
B.铝是人体中一种微量元素,如果摄入过多,会患老年痴呆
C.铝的导热性比铁强,因而用铝锅煮食物比铁锅好D.硬铝是一种合金,硬度比纯铝大
【答案】C
【详解】
A.人体缺铁,会引起贫血,所以常用的补血剂中含有铁元素,故A正确;
B.人体内铝元素摄入量过多易患老年痴呆症,故B正确;
C.长期使用铝制品作炊具可使铝摄入过量,对健康不利,还可导致老年性痴呆的发生率增加,所以,炒
菜还是用铁锅好,而使用铁锅一定程度上能防止缺铁性贫血,故C错误.
D.硬铝硬铝,是指铝合金中以Cu为主要合金元素的一类铝合金,硬度比纯铝大,故D正确;
故选C。
17.(本题3分)下列说法正确的是( )
A.Al O 难溶于水,不跟水反应,所以它不是Al(OH) 对应的氧化物
2 3 3
B.因为Al O 是金属氧化物,所以它是碱性氧化物
2 3
C.Al O 能跟所有的酸碱溶液反应
2 3
D.Al O 能跟强的酸碱溶液反应是两性氧化物
2 3
【答案】D
【详解】
A.Al O 难溶于水,不跟水反应,但它是Al(OH) 对应的氧化物,A错误;
2 3 3
B.Al O 是两性氧化物,B错误;
2 3
C.Al O 是两性氧化物,能跟强酸强碱反应,不能与所有的酸碱溶液反应,C错误;
2 3
D.Al O 是两性氧化物,能跟强的酸碱溶液反应,D正确。
2 3
答案选D。
18.(本题3分)下列离子方程式中正确的是
A.向氯化亚铁溶液中通入氯气:2Fe2++Cl=2Fe3++2Cl-
2
B.Na与水反应:2Na+HO=2Na++OH-+H ↑
2 2
C.氧化亚铁与稀盐酸:FeO+2H+=Fe3++H O
2
D.氧化铝与氢氧化钠:Al O+6OH-=2Al(OH) +3H O
2 3 3 2
【答案】A
【详解】
A.Fe2+与Cl 反应生成Fe3+和Cl-,离子方程式为2Fe2++Cl=2Fe3++2Cl-,A正确;
2 2
B.Na与HO反应生成NaOH和H,离子方程式为2Na+2HO=2Na++2OH-+H ↑,B错误;
2 2 2 2C.FeO与HCl反应生成Fe2+和HO,离子方程式为FeO+2H+=Fe2++H O,C错误;
2 2
D.Al O 与NaOH反应生成NaAlO 和HO,离子方程式为Al O+2OH-=2 +HO,D错误;
2 3 2 2 2 3 2
故选A。
二、填空题(共6分)
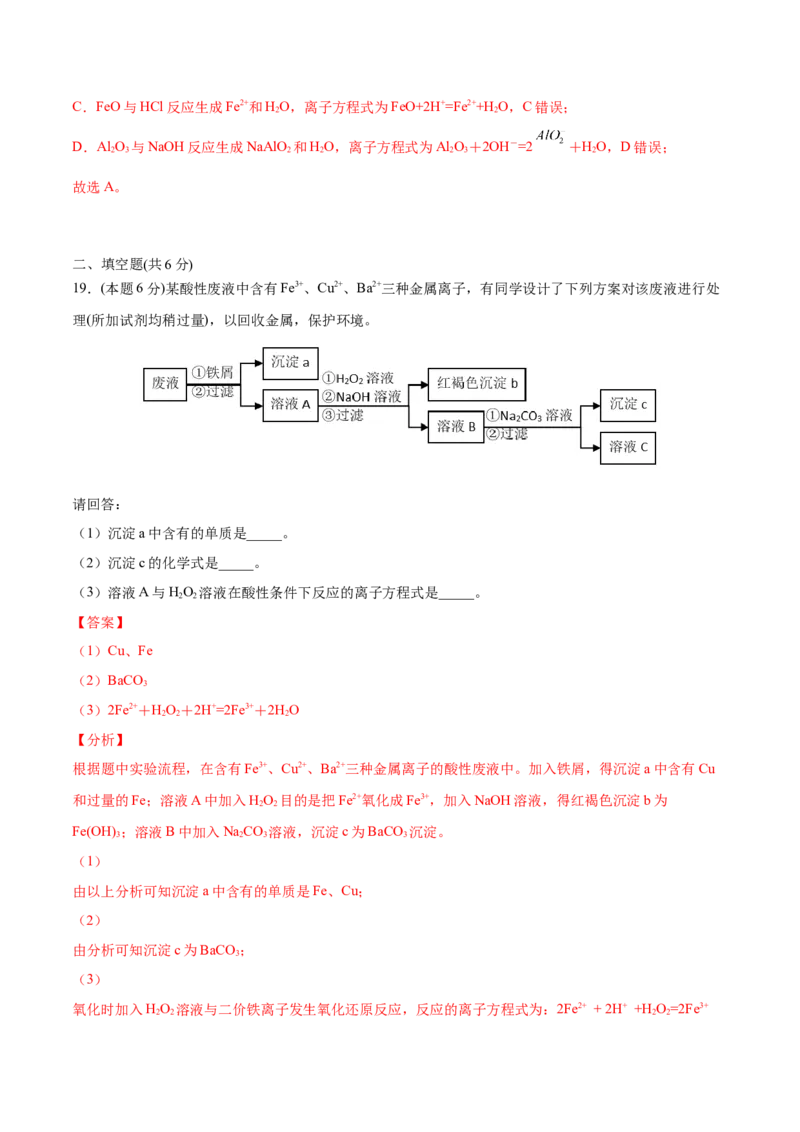
19.(本题6分)某酸性废液中含有Fe3+、Cu2+、Ba2+三种金属离子,有同学设计了下列方案对该废液进行处
理(所加试剂均稍过量),以回收金属,保护环境。
请回答:
(1)沉淀a中含有的单质是_____。
(2)沉淀c的化学式是_____。
(3)溶液A与HO 溶液在酸性条件下反应的离子方程式是_____。
2 2
【答案】
(1)Cu、Fe
(2)BaCO
3
(3)2Fe2++HO+2H+=2Fe3++2HO
2 2 2
【分析】
根据题中实验流程,在含有Fe3+、Cu2+、Ba2+三种金属离子的酸性废液中。加入铁屑,得沉淀a中含有Cu
和过量的Fe;溶液A中加入HO 目的是把Fe2+氧化成Fe3+,加入NaOH溶液,得红褐色沉淀b为
2 2
Fe(OH) ;溶液B中加入NaCO 溶液,沉淀c为BaCO 沉淀。
3 2 3 3
(1)
由以上分析可知沉淀a中含有的单质是Fe、Cu;
(2)
由分析可知沉淀c为BaCO ;
3
(3)
氧化时加入HO 溶液与二价铁离子发生氧化还原反应,反应的离子方程式为:2Fe2+ + 2H+ +H O=2Fe3+
2 2 2 2+2H O。
2
三、元素或物质推断题(共14分)
20.(本题14分)现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转
化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
请根据以上信息完成下列各题:
(1)写出下列物质的化学式:B_______,丙_______。
(2)写出实验室制备黄绿色气体乙的化学方程式:_______,反应过程⑦可能观察到的实验现象是:_______,
产生红褐色沉淀的化学方程式是 _______
(3)反应③中的离子方程式是_______
(4)反应⑤的离子方程式是_______
(5)反应⑦中如果可以长时间看到白色沉淀,应如何进行实验操作:_______。
【答案】Al HCl 4HCl(浓)+MnO Cl↑+MnCl +2H O 白色沉淀迅速变为灰绿色,最终变为红褐
2 2 2 2
色 4Fe(OH) +O +2H O=4Fe(OH) 2Al+2OH-+2H O= +3H ↑ 2Fe2++Cl=2Fe3++2Cl- 配制溶
2 2 2 3 2 2 2
液的蒸馏水煮沸,去除水中溶解的氧气(或胶头滴管末端进入氯化亚铁液面下滴加氢氧化钠溶液或氯化亚铁
液面上加入一层煤油隔绝空气)
【分析】
金属单质A焰色反应呈黄色,则A是Na,Na与HO反应产生气体甲是H,D溶液为NaOH,金属B和氢
2 2
氧化钠溶液反应,说明B为Al,黄绿色气体乙为Cl,气体甲和氯气反应生成丙为HCl,物质E为盐酸溶
2
液,物质D是氢氧化钠,D和物质G反应生成红褐色沉淀H为Fe(OH) ,盐酸与金属C反应产生金属氯化
3
物,该氯化物与NaOH溶液反应产生Fe(OH) ,则C是Fe,F为FeCl 、G为FeCl ,以此解答该题。
3 2 3
【详解】(1)根据分析可知,B为Al,丙为HCl;
(2)气体乙为氯气,实验室利用二氧化锰和浓盐酸共热制取氯气,化学方程式为4HCl(浓)+MnO
2
Cl↑+MnCl +2H O;反应⑦为FeCl 溶液与NaOH溶液反应生成Fe(OH) ,Fe(OH) 再被空气中的氧气氧化成
2 2 2 2 2 2
红褐色沉淀Fe(OH) 的过程,现象为:白色沉淀迅速变为灰绿色,最终变为红褐色,产生红褐色沉淀的化
3
学方程式为4Fe(OH) +O +2H O=4Fe(OH) ;
2 2 2 3
(3)反应③为铝和NaOH溶液的反应,生成偏铝酸钠、氢气,离子方程式为2Al+2OH-+2H O= +3H ↑;
2 2
(4)结合分析可知,反应⑤为FeCl 与Cl 反应生成FeCl ,其离子方程式是2Fe2++Cl=2Fe3++2Cl-;
2 2 3 2
(5)反应⑦中如果可以长时间看到白色沉淀,则需要隔绝氧气防止氢氧化亚铁被氧化,所以可以:配制溶液
的蒸馏水煮沸、胶头滴管末端进入氯化亚铁液面下滴加氢氧化钠溶液、氯化亚铁液面上加入一层煤油隔绝
空气。
四、实验题(共26分)
21.(本题12分)某实验小组对中学课本中可生成氢气的反应进行了研究,总结出三个可以生成H 的反应:
2
①Zn+盐酸;②Na+水;③Al+NaOH溶液。为点燃上述三个反应生成的H,他们设计了如右图所示的装置图:
2
请回答下列问题:
(1)写出Al和NaOH溶液反应的离子方程式_______________________________。
(2)在点燃H 之前必须先进行____________________________________________。
2
(3)实验小组在点燃用上述装置制得的H 时,①③实验获得成功,②却失败了。他们分析认为失败的原因是
2
Na与HO的反应速率太快,Na的用量又太少。于是他们准备增加钠的用量,可教师说太危险,你认为产生危
2
险的原因是___________________________。
(4)实验小组查阅钠、苯(一种不溶于水的液态有机物)、水的密度分别为0.97 g·mL-1、0.88 g·mL-1、1.00
g·mL-1,并据此对实验进行了改进。在改进后的实验中H 的生成速率____________。(填“减慢”或“加快”)
2
(5)将4.6gNa和8.1gAl投入到足量的水中,所得溶液的体积为200mL,则生成标准状况下的H 的体积是
2___________?该溶液中溶质的物质的量浓度是__________________?
【答案】.2Al+2H O+2OH—====2AlO —+3H ↑ 验纯 较多的钠与水反应放出大量的热,使试管内H 与
2 2 2 2
O 的混合气点燃而爆炸 减慢 8.96 L 1 mol·L-1
2
【详解】
(1)Al和NaOH溶液反应生成偏铝酸钠和氢气,反应的离子方程式为:2Al+2H O+2OH—
2
=2AlO —+3H ↑;(2)H 是可燃性气体,可燃性气体在点燃前必须进行检纯;(3)在试管中
2 2 2
不要放入大块的Na,避免较多的钠与水反应放出大量的热,使试管内H 与O 的混合气点燃
2 2
而爆炸;(4)钠块表面会附着苯,所以改进后的实验中H 的生成速率减慢;
2
(5)4.6gNa的物质的量为 =0.2mol,8.1gAl的物质的量为 =0.3mol,
先是Na和水反应:2Na + 2H O = 2NaOH + H ↑
2 2
0.2mol 0.2mol 0.1mol
生成n(NaOH)=0.2mol,
再是NaOH和Al反应:2Al + 2NaOH + 2H O = 2NaAlO + 3H ↑
2 2 2
0.3mol(过量) 0.2mol 0.2mol 0.3mol
Al过量,NaOH完全反应,反应后的溶质为0.2molNaAlO ,生成的H 的物质的量为
2 2
0.1mol+0.2mol=0.3mol,标准状况下的体积为0.3mol×22.4L/mol=8.96L;溶液中溶质NaAlO
2
的物质的量浓度是 =1mol/L。
22.(本题14分)某兴趣小组利用下列试剂:铁粉、锌粉、0.1mol/LFeCl 溶液、KSCN溶液、新制氯水,探
2
究Fe2+、Fe3+的氧化性、还原性,并利用实验结论解决一些问题。
(1)用所给试剂写出体现Fe2+具有还原性的反应的离子反应方程式:___。
(2)设计实验方案,完成下列表格。
探究内容 实验方案 实验现象
取少量0.1mol/LFeCl 溶液,往溶液中加入 加入铁粉后,溶液变成___;加入
探究Fe3+的化学性质 3
足量铁粉,再加入少量KSCN溶液 KSCN溶液后,溶液变成___
结论:Fe3+具有___性
(3)该兴趣小组未说明“Fe2+具有氧化性”,提出了向FeCl 溶液中加入锌粉,观察实验现象的方案,该反
2
应的离子方程式为___。
(4)某反应中反应物与生成物有Fe3+、MnO 、HO和一种未知离子X。
2①已知氧化性:MnO >Fe3+,则X离子是___。
②该反应的离子方程式是___。
【答案】
(1)
(2) 浅绿色 无明显现象 氧化
(3)
(4) Mn2+ MnO + 5Fe2++8H+=Mn2++5Fe3++4H O
2
【分析】
(1)
Fe2+具有还原性,可被新制氯水氧化,反应的离子反应方程式: 。
(2)
取少量0.1mol/LFeCl 溶液,往溶液中加入足量铁粉,发生反应: ,Fe3+表现出氧化性,溶
3
液由黄色变成浅绿色,再加入少量KSCN溶液,溶液无明显现象。
(3)
向FeCl 溶液中加入锌粉,锌置换出铁,该反应的离子方程式为 。
2
(4)
根据原子守恒和氧化还原反应规律,推断该反应是MnO 氧化Fe2+得到Fe3+,依题意,该反应的离子方程
式是:MnO + 5Fe2++8H+=Mn2++5Fe3++4H O。
2
①据以上分析,除了Fe3+、MnO 、HO还有Fe2+、H+、Mn2+,未知离子X应是Mn2+;
2
②该反应的离子方程式是:MnO + 5Fe2++8H+=Mn2++5Fe3++4H O。
2关注更新免费领取,淘宝唯一每月更新店铺:知二教育