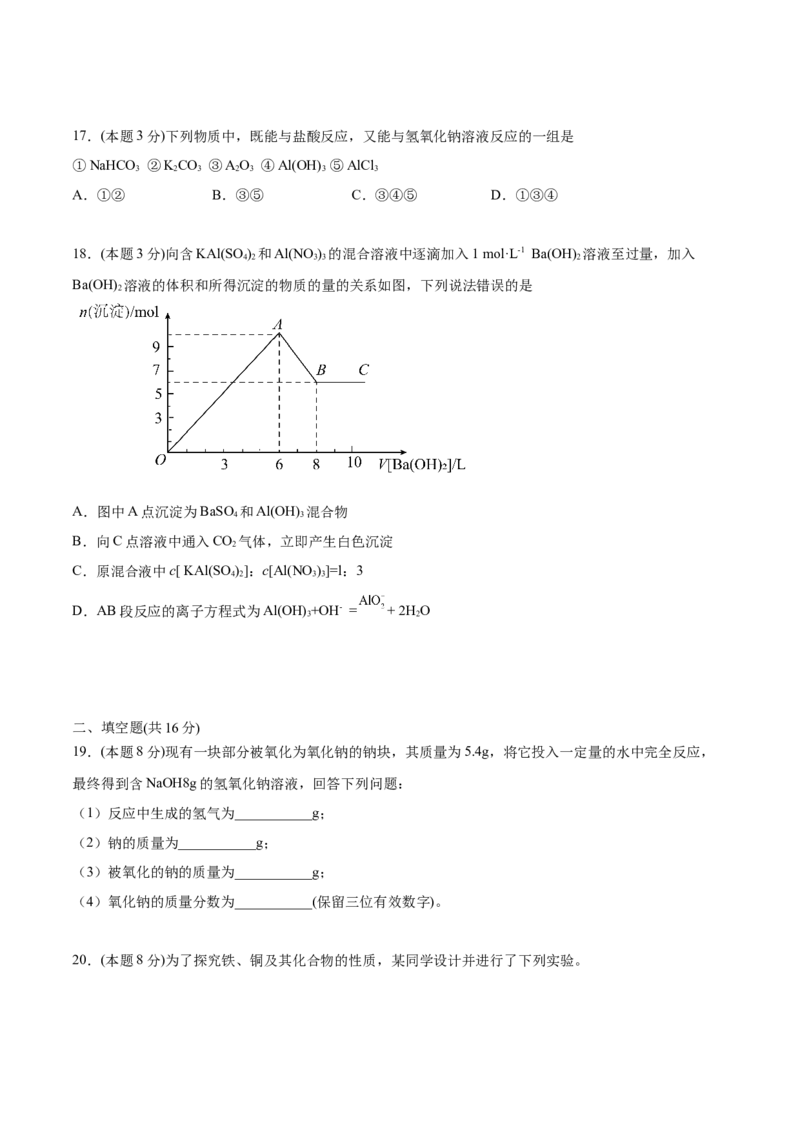文档内容
《铁 金属材料》单元测试(培优提升)
学校:___________姓名:___________班级:___________考号:___________
一、单选题(共54分)
1.(本题3分)我国最早使用的合金
A.生铁 B.青铜 C.硬铝 D.焊锡
2.(本题3分)镁铝合金质优体轻,又不易锈蚀,大量用于航空工业、造船工业、日用化工等领域。下列关
于镁铝合金性质的叙述中正确的是
A.此合金的熔点、硬度比镁和铝的熔点、硬度都高
B.此合金能全部溶解于稀盐酸中
C.此合金能全部溶解于氢氧化钠溶液中
D.此合金不能全部溶解于过量FeCl 溶液中
3
3.(本题3分)我国宋代《开宝本草》中记载了中药材铁华粉的制作方法:“取钢煅作叶,如笏或团,平面
磨错令光、净,以盐水洒之,于醋瓮中阴处埋之一百日,铁上衣生,铁华成矣。”下列说法错误的是
A.“取钢煅作叶,如笏或团”说明金属铁有较好的延展性
B.“平面磨错令光、净”的目的是除去表面的铁锈
C.“铁上衣生”的原因是铁被氧气氧化
D.中药材铁华粉的主要成分是醋酸亚铁
4.(本题3分)下列关于铁及其化合物的说法正确的是 ( )
A.铁是地壳中含量最多的金属元素,因此在日常生活中应用最广
B.FeCl 溶液存放时,在溶液中放入少量的铁粉,目的是防止Fe2+被氧化
2
C.隔绝空气的情况下,FeCl 溶液中加入NaO 后得到白色沉淀Fe(OH)
2 2 2 3
D.FeO、Fe O、Fe O 均为铁的氧化物,并且都是黑色
2 3 3 4
5.(本题3分)下列物质中能由单质直接化合得到的有①NaO ②NaO ③FeCl ④FeCl ⑤Fe O
2 2 2 2 3 3 4
A.①②③⑤ B.②③④⑤ C.①②④⑤ D.①③④⑤
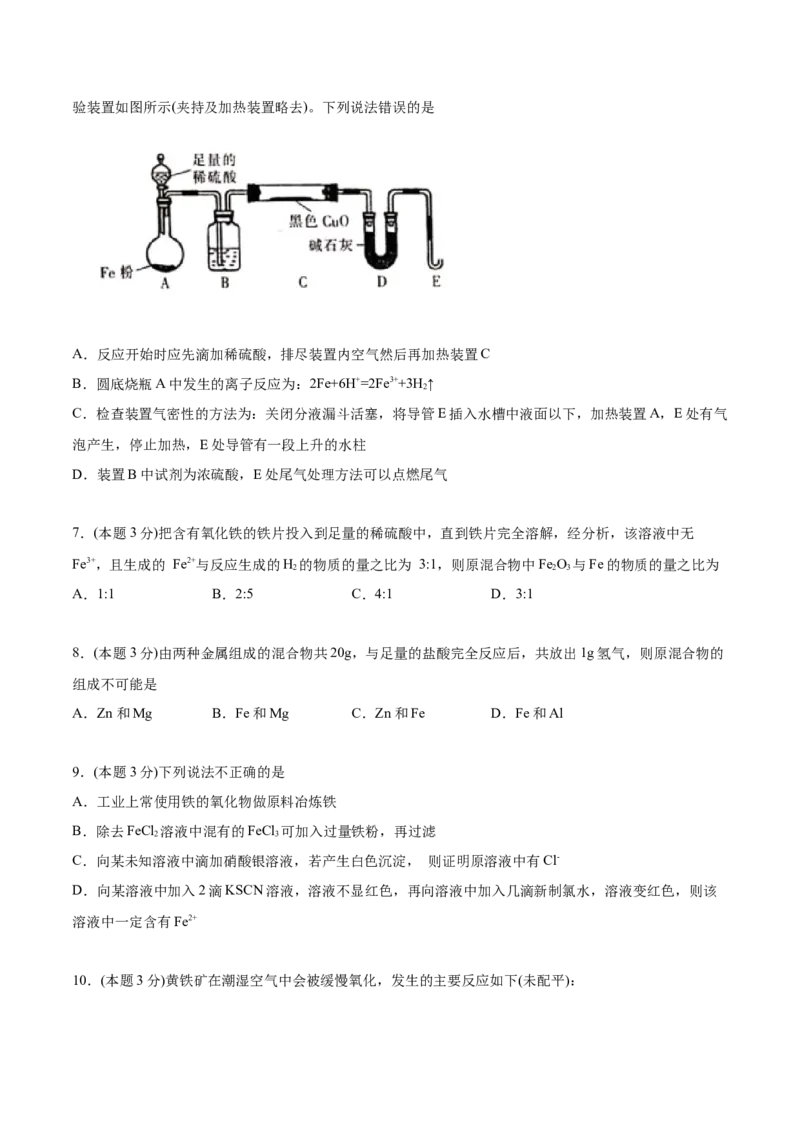
6.(本题3分)某化学小组用5.6 g铁粉与足量的稀硫酸反应,用产生的H 还原足量的CuO制备单质铜,实
2验装置如图所示(夹持及加热装置略去)。下列说法错误的是
A.反应开始时应先滴加稀硫酸,排尽装置内空气然后再加热装置C
B.圆底烧瓶A中发生的离子反应为:2Fe+6H+=2Fe3++3H ↑
2
C.检查装置气密性的方法为:关闭分液漏斗活塞,将导管E插入水槽中液面以下,加热装置A,E处有气
泡产生,停止加热,E处导管有一段上升的水柱
D.装置B中试剂为浓硫酸,E处尾气处理方法可以点燃尾气
7.(本题3分)把含有氧化铁的铁片投入到足量的稀硫酸中,直到铁片完全溶解,经分析,该溶液中无
Fe3+,且生成的 Fe2+与反应生成的H 的物质的量之比为 3:1,则原混合物中Fe O 与Fe的物质的量之比为
2 2 3
A.1:1 B.2:5 C.4:1 D.3:1
8.(本题3分)由两种金属组成的混合物共20g,与足量的盐酸完全反应后,共放出1g氢气,则原混合物的
组成不可能是
A.Zn 和Mg B.Fe和Mg C.Zn 和Fe D.Fe和Al
9.(本题3分)下列说法不正确的是
A.工业上常使用铁的氧化物做原料冶炼铁
B.除去FeCl 溶液中混有的FeCl 可加入过量铁粉,再过滤
2 3
C.向某未知溶液中滴加硝酸银溶液,若产生白色沉淀, 则证明原溶液中有Cl-
D.向某溶液中加入2滴KSCN溶液,溶液不显红色,再向溶液中加入几滴新制氯水,溶液变红色,则该
溶液中一定含有Fe2+
10.(本题3分)黄铁矿在潮湿空气中会被缓慢氧化,发生的主要反应如下(未配平):a: FeS+ O +H O → +Fe2++H+
2 2 2
b: Fe2++H++O →Fe3++ H O
2 2
c: Fe3++FeS + H O→Fe2+ + + H+
2 2
下列说法正确的是
A.a反应中氧化产物只有FeSO
4
B.为了验证b反应后溶液中含Fe2+,可选用KSCN溶液和氯水。
C.c反应中每生成1mol Fe2+转移1mol电子
D.长期盛放黄铁矿的纸箱会被腐蚀而发黑
11.(本题3分)用下列方法均可制得氯气:
①MnO +4HCl(浓) MnCl +Cl↑+2H O
2 2 2 2
②KClO+6HCl(浓)=KC1+3Cl ↑+3H O
3 2 2
③2KMnO +16HCl(浓)=2KCl+2MnCl +5Cl↑+8H O
4 2 2 2
若要制得相同质量的氯气,①②③反应中转移电子数目之比为
A.6:5:6 B.1:3:5
C.15:5:3 D.1:6:10
12.(本题3分)下列有关物质用途的说法中,不正确的是
A.铝制餐具适合于蒸煮和存放碱性食物
B.纯铝的硬度和强度较小,不适合制造机器零部件
C.Ti—Fe合金和La—Ni合金可用作储氢材料
D.铝合金是用来制造飞机和宇宙飞船的理想材料
13.(本题3分)下列除杂方法不合理的是
A.除去Cu固体中少量CuO:加足量盐酸,过滤
B.除去镁粉中的铝粉:加过量氢氧化钠溶液,过滤
C.除去FeCl 溶液中的FeCl :加过量铁粉,过滤
2 3
D.除去NaHCO 溶液中的NaCO:加氯化钙溶液,过滤
3 2 314.(本题3分)解释下列实验现象的离子方程式正确的是
A.硫酸镁溶液与氢氧化钡反应: +Ba2+=BaSO ↓
4
B.FeI 溶液中通入少量Cl 时:2Fe2++Cl=2Fe3++2Cl-
2 2 2
C.金属铝溶于氢氧化钠溶液:Al+2OH-= +H ↑
2
D.碳酸银溶于过量硝酸中:Ag CO+2H+=2Ag++H O+CO↑
2 3 2 2
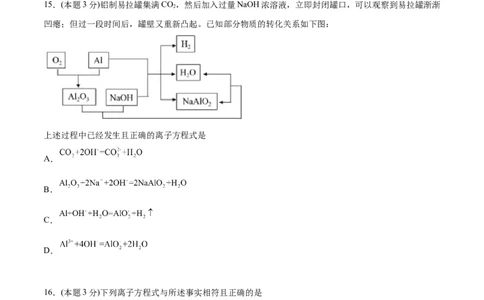
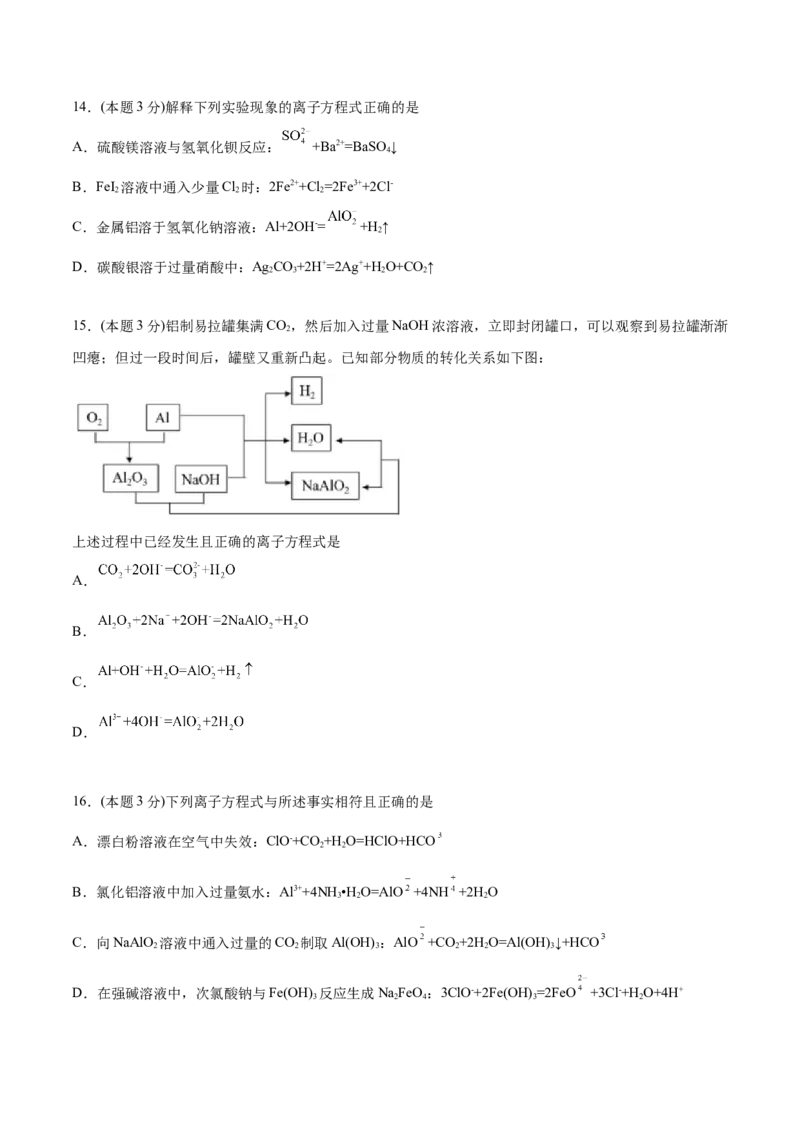
15.(本题3分)铝制易拉罐集满CO,然后加入过量NaOH浓溶液,立即封闭罐口,可以观察到易拉罐渐渐
2
凹瘪;但过一段时间后,罐壁又重新凸起。已知部分物质的转化关系如下图:
上述过程中已经发生且正确的离子方程式是
A.
B.
C.
D.
16.(本题3分)下列离子方程式与所述事实相符且正确的是
A.漂白粉溶液在空气中失效:ClO-+CO +H O=HClO+HCO
2 2
B.氯化铝溶液中加入过量氨水:Al3++4NH•H O=AlO +4NH +2H O
3 2 2
C.向NaAlO 溶液中通入过量的CO 制取Al(OH) :AlO +CO +2H O=Al(OH) ↓+HCO
2 2 3 2 2 3
D.在强碱溶液中,次氯酸钠与Fe(OH) 反应生成NaFeO:3ClO-+2Fe(OH) =2FeO +3Cl-+H O+4H+
3 2 4 3 217.(本题3分)下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的一组是
①NaHCO ②KCO ③AO ④Al(OH) ⑤AlCl
3 2 3 2 3 3 3
A.①② B.③⑤ C.③④⑤ D.①③④
18.(本题3分)向含KAl(SO ) 和Al(NO ) 的混合溶液中逐滴加入1 mol·L-1 Ba(OH) 溶液至过量,加入
4 2 3 3 2
Ba(OH) 溶液的体积和所得沉淀的物质的量的关系如图,下列说法错误的是
2
A.图中A点沉淀为BaSO 和Al(OH) 混合物
4 3
B.向C点溶液中通入CO 气体,立即产生白色沉淀
2
C.原混合液中c[ KAl(SO )]:c[Al(NO )]=l:3
4 2 3 3
D.AB段反应的离子方程式为Al(OH) +OH- = + 2H O
3 2
二、填空题(共16分)
19.(本题8分)现有一块部分被氧化为氧化钠的钠块,其质量为5.4g,将它投入一定量的水中完全反应,
最终得到含NaOH8g的氢氧化钠溶液,回答下列问题:
(1)反应中生成的氢气为___________g;
(2)钠的质量为___________g;
(3)被氧化的钠的质量为___________g;
(4)氧化钠的质量分数为___________(保留三位有效数字)。
20.(本题8分)为了探究铁、铜及其化合物的性质,某同学设计并进行了下列实验。请回答:
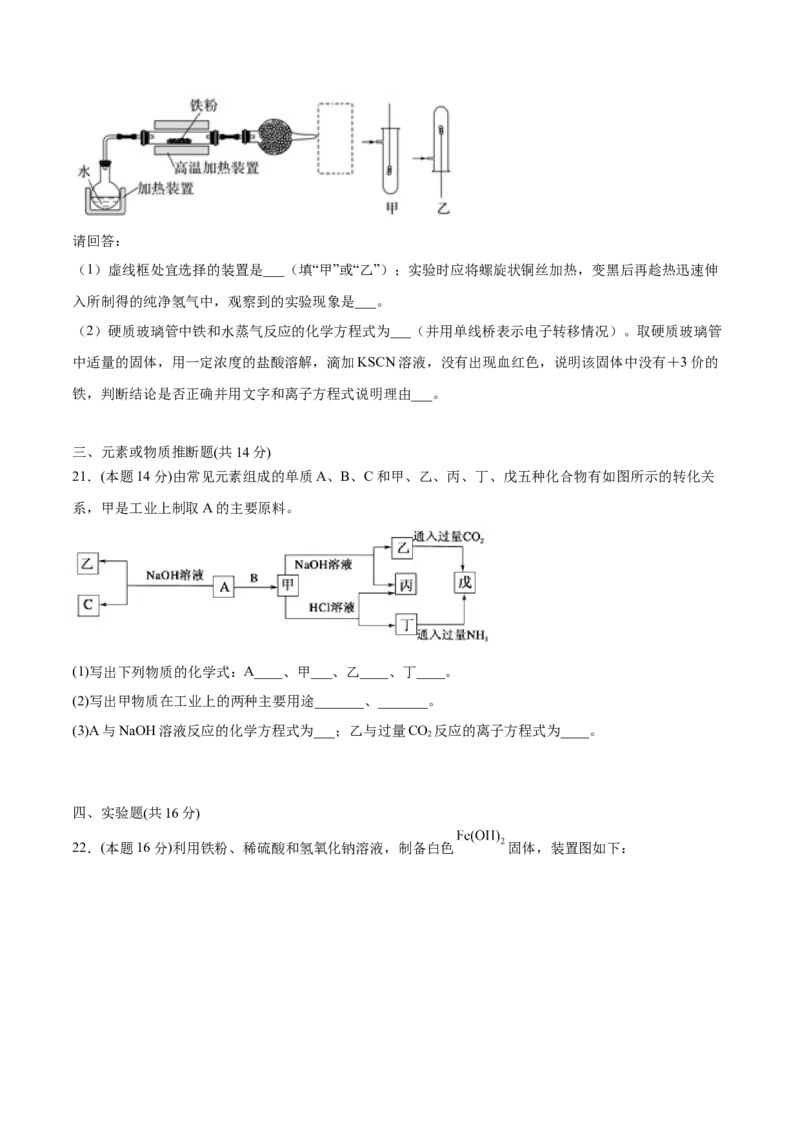
(1)虚线框处宜选择的装置是___(填“甲”或“乙”);实验时应将螺旋状铜丝加热,变黑后再趁热迅速伸
入所制得的纯净氢气中,观察到的实验现象是___。
(2)硬质玻璃管中铁和水蒸气反应的化学方程式为___(并用单线桥表示电子转移情况)。取硬质玻璃管
中适量的固体,用一定浓度的盐酸溶解,滴加KSCN溶液,没有出现血红色,说明该固体中没有+3价的
铁,判断结论是否正确并用文字和离子方程式说明理由___。
三、元素或物质推断题(共14分)
21.(本题14分)由常见元素组成的单质A、B、C和甲、乙、丙、丁、戊五种化合物有如图所示的转化关
系,甲是工业上制取A的主要原料。
(1)写出下列物质的化学式:A____、甲___、乙____、丁____。
(2)写出甲物质在工业上的两种主要用途_______、_______。
(3)A与NaOH溶液反应的化学方程式为___;乙与过量CO 反应的离子方程式为____。
2
四、实验题(共16分)
22.(本题16分)利用铁粉、稀硫酸和氢氧化钠溶液,制备白色 固体,装置图如下:(1)物质B的化学式为___________。
(2)检查装置气密性的方法为D-___________(填编号),分液漏斗水面稳定于某一高度不再下降,气密
性良好。
A.打开开关①和开关② B.观察分液漏斗水面稳定情况
C.用止水夹夹紧小具支试管末端橡皮导管 D.向分液漏斗中尽量加注较多的蒸馏水
E.分液漏斗盖、颈对好孔,然后旋开活塞
(3)铁粉与稀硫酸制备H 的离子方程式为___________,H 的作用有___________(填编号)。
2 2
A.驱赶溶液中的氧气 B.驱赶装置内的空气
C.把物质B压入小具支试管中 D.保护白色 不被空气氧化
(4)实验过程中,用针管吸取大具支试管中的溶液,检验其中是否含有 。方法为:用该针管吸取
___________溶液,用力振荡几次,溶液不变色,把针管中的混合物全部注入干净试管,振荡几次,溶液
慢慢变红色。依据现象得出的结论有___________、___________。
(5)白色 沉淀在___________(填“大具支试管”或“小具支试管”)内生成,经在无氧环境中干
燥处理,得到的白色 粉末是很好的化工___________(填“除酸剂”或“除氧剂”)。关注更新免费领取,淘宝唯一每月更新店铺:知二教育