文档内容
第 26 讲 电解池的原理
知识导航
小杨老师 15521324728 侵权必究
知识精讲
小杨老师 15521324728 侵权必究
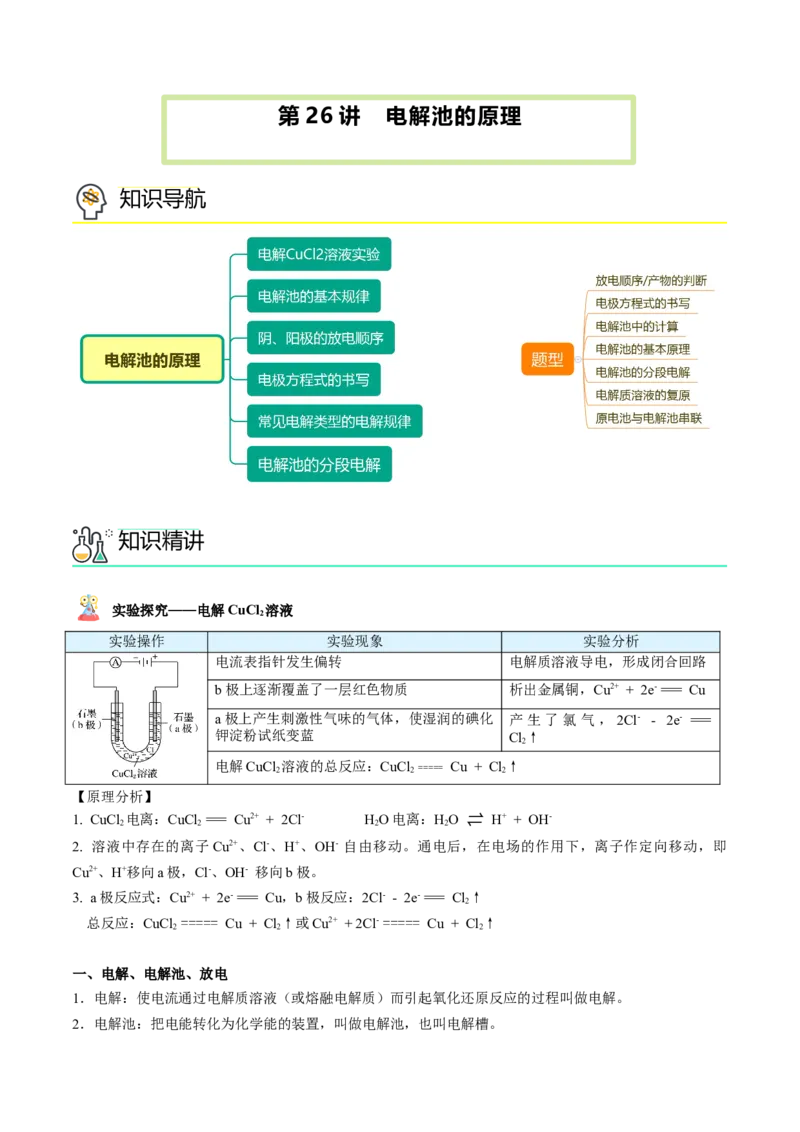
实验探究——电解CuCl 溶液
2
实验操作 实验现象 实验分析
电流表指针发生偏转 电解质溶液导电,形成闭合回路
b极上逐渐覆盖了一层红色物质 析出金属铜,Cu2+ + 2e-=== Cu
a极上产生刺激性气味的气体,使湿润的碘化 产生了氯气 ,2Cl- - 2e- ===
钾淀粉试纸变蓝 Cl↑
2
电解CuCl 2 溶液的总反应:CuCl 2 ===== Cu + Cl 2 ↑
【原理分析】
1. CuCl 电离:CuCl === Cu2+ + 2Cl- HO电离:HO ⇌ H+ + OH-
2 2 2 2
2. 溶液中存在的离子Cu2+、Cl-、H+、OH- 自由移动。通电后,在电场的作用下,离子作定向移动,即
Cu2+、H+移向a极,Cl-、OH- 移向b极。
3. a极反应式:Cu2+ + 2e-=== Cu,b极反应:2Cl- - 2e- === Cl↑
2 杨sir化学,侵权必究
总反应:CuCl ===== Cu + Cl↑或Cu2+ + 2Cl- ===== Cu + Cl↑
2 2 2
一、电解、电解池、放电
1.电解:使电流通过电解质溶液(或熔融电解质)而引起氧化还原反应的过程叫做电解。
2.电解池:把电能转化为化学能的装置,叫做电解池,也叫电解槽。3. 放电:当离子到达电极时,失去/获得电子,发生氧化/还原反应的过程,称为放电。
二、电解池的基本规律
构成条件 ①直流电源;②两个电极;③闭合回路;④电解质溶液或熔融电解质
阳极 与电源_______相连,发生_______反应
电极
阴极 与电源_______相连,发生_______反应
离子流向 阴离子移向______;阳离子移向______
电子流向 电源____极流向电解池____极;电解池____极流向电源____极
【答案】正极 氧化 负极 还原 阳极 阴极 负 阴 阳 正
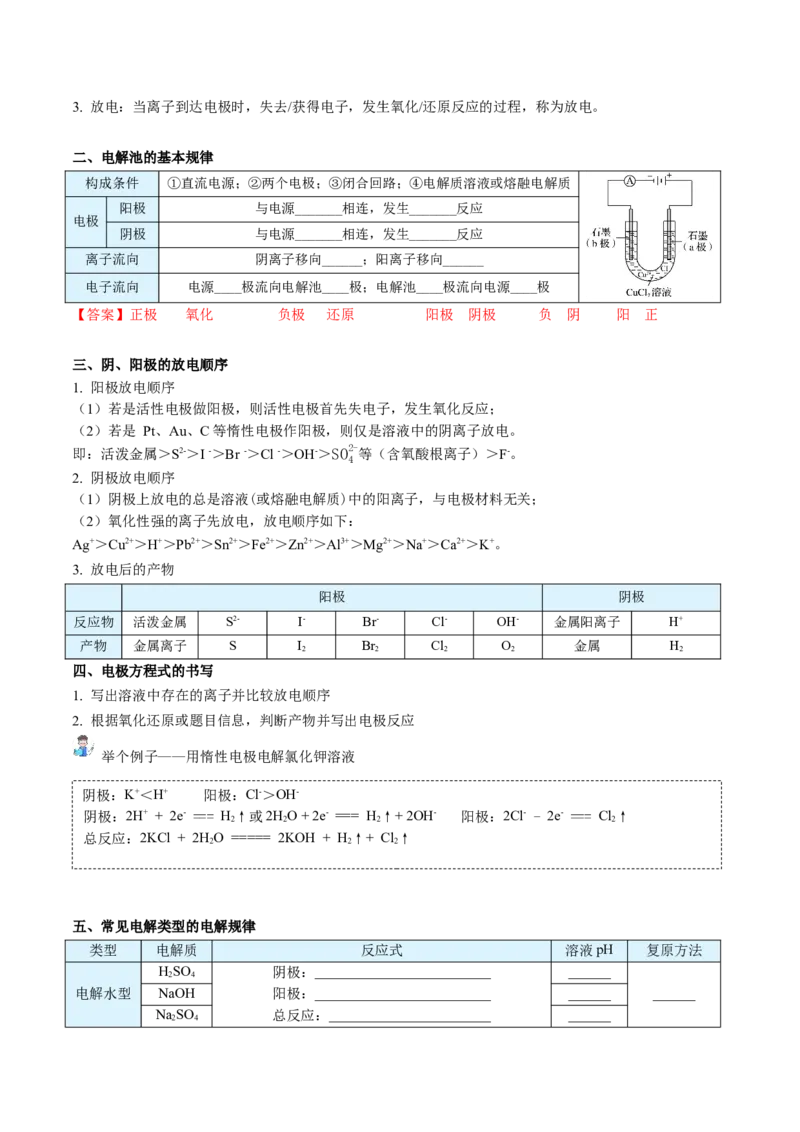
三、阴、阳极的放电顺序
1. 阳极放电顺序
(1)若是活性电极做阳极,则活性电极首先失电子,发生氧化反应;
(2)若是 Pt、Au、C等惰性电极作阳极,则仅是溶液中的阴离子放电。
即:活泼金属>S2->I->Br ->Cl->OH->SO2-等(含氧酸根离子)>F-。
4 杨sir化学,侵权必究
2. 阴极放电顺序
(1)阴极上放电的总是溶液(或熔融电解质)中的阳离子,与电极材料无关;
(2)氧化性强的离子先放电,放电顺序如下:
Ag+>Cu2+>H+>Pb2+>Sn2+>Fe2+>Zn2+>Al3+>Mg2+>Na+>Ca2+>K+。
3. 放电后的产物
阳极 阴极
反应物 活泼金属 S2- I- Br- Cl- OH- 金属阳离子 H+
产物 金属离子 S I Br Cl O 金属 H
2 2 2 2 2
四、电极方程式的书写
1. 写出溶液中存在的离子并比较放电顺序
2. 根据氧化还原或题目信息,判断产物并写出电极反应
举个例子——用惰性电极电解氯化钾溶液
杨sir化学,侵权必究
阴极:K+<H+ 阳极:Cl->OH-
阴极:2H+ + 2e- === H↑或2HO + 2e- === H↑+ 2OH- 阳极:2Cl- - 2e- === Cl ↑
2 2 2 2
总反应:2KCl + 2HO ===== 2KOH + H↑+ Cl↑
2 2 2
五、常见电解类型的电解规律
类型 电解质 反应式 溶液pH 复原方法
HSO 阴极:_________________________ ______
2 4
电解水型 NaOH 阳极:_________________________ ______ ______
NaSO 总反应:_______________________ ______
2 4阴极:_________________________
电解
CuCl 阳极:_________________________ ______ ______
2
电解质型
总反应:_______________________
阴极:_________________________
放H
2
NaCl 阳极:_________________________ ______ ______
生碱型
总反应:_______________________
阴极:_________________________
放O
2
CuSO 阳极:_________________________ ______ ______
4
生酸型
总反应:_______________________
思考与交流:上述各种电解类型中,阴极、阳极附近的pH如何变化?
对点训练
小杨老师 15521324728 侵权必究
题型一:放电顺序与放电产物的判断
杨sir化学,侵权必究
【例1】电解CuCl 与NaCl的混合溶液(惰性电极),阴极上和阳极上最先析出的物质为
2
A.H 和Cl B.Cu和Cl C.H 和O D.Cu和O
2 2 2 2 2 2
【答案】B
【详解】
电解时,溶液中Cu2+、H+、Na+移向阴极,Cu2+先放电得到Cu;Cl-、OH-移向阳极,Cl-先放电得到Cl,
2
阴极上和阳极上最先析出的物质分别为Cu和Cl;
2
故选:B。
【变1】用惰性电极电解等物质的量NaSO 、AgNO、KCl的混合液,最先从阴极和阳极上析出的物质分
2 4 3
别是
A.H 和Cl B.Ag和Cl C.H 和O D.Ag和O
2 2 2 2 2 2
【答案】C
【详解】
用等物质的量的NaSO 、AgNO、KCl的混合液中,首先生成AgCl沉淀,实际电解NaSO 和KNO,相
2 4 3 2 4 3
当于电解水,两极分别生成H 和O,故选C。
2 2
【变2】采用惰性电极从 、 、Cl-、Cu2+、Ba2+、Ag+、H+选出适当离子组成的电解质(非熔融态
下),并电解,
(1)若两极分别放出H 和O,电解质可能为___。
2 2
(2)若阴极析出金属,阳极放出O,电解质可能为___。
2
(3)若两极分别放出气体,且体积比为1:1,电解质可能为___。
杨sir化学,侵权必究
(4)若既无O 也无H 放出,则电解质可能为___。
2 2
【答案】Ba(NO )、HSO 、HNO AgNO、Cu(NO )、CuSO HCl、BaCl CuCl
3 2 2 4 3 3 3 2 4 2 2【分析】
阴极上阳离子放电顺序为Ag+>Cu2+>H+>Ba+,阳极上阴离子放电顺序为Cl->OH-> 、 ,
根据电极产物判断阴阳极放电的离子,从而确定溶液中的电解质。
【详解】
阴极上阳离子放电顺序为Ag+>Cu2+>H+>Ba2+,阳极上阴离子放电顺序为Cl−>OH−>含氧酸根,
(1)当阴极放出H,阳极放出O 时,则阴极H+放电,阳极OH−放电,则溶液中的阴离子为硫酸根或硝酸根,
2 2
阳离子是H+或Ba2+,BaSO 为沉淀,所以电解质是Ba(NO )、HSO 、HNO;
4 3 2 2 4 3
故答案为Ba(NO )、HSO 、HNO;
3 2 2 4 3
(2)当阴极析出金属时,阴极为Cu2+或Ag+放电,阳极放出O,阳极为OH−放电,则溶液中的阴离子为硫酸
2
根或硝酸根,电解质是AgNO、Cu(NO )、CuSO ,
3 3 2 4
故答案为AgNO、Cu(NO )、CuSO ;
3 3 2 4
(3)若两极分别放出气体,且体积比为1:1,则阴极放出H,阳极放出Cl,阴极为H+放电,溶液中的阳
2 2
离子为H+或Ba2+,阴离子为Cl−放电,溶液中的阴离子为Cl−,所以电解质为HCl、BaCl ;
2
故答案为HCl、BaCl ;
2
(4)电解过程中既无O 也无H 放出,则阴极上析出金属,阴极为Cu2+或Ag+放电,阳极上产生氯气,阴离
2 2
子为Cl−放电,AgCl为沉淀,则电解质应为CuCl ;
2
故答案为CuCl 。
2
【点睛】
电解池中阴阳极放电顺序的判断方法:
(1)阴极:阴极上放电的总是溶液中的阳离子,与电极材料无关。金属活动性顺序表中越排在后面的,其
离子的氧化性越强,越易得到电子(注意Fe3+在Cu2+后面)而放电,其放电顺序为:K+ Ca2+ Na+ Al3+ (水
中)H+ Zn2+ Fe2+ Sn4+ Pb2+ H+ Cu2+ Fe3+ Ag+。
(2)阳极:若为活性电极做阳极,则活性电极首先失电子,发生氧化反应;若为惰性电极做阳极,则仅是
溶液中的阴离子放电,其常见的放电顺序为:F- 含氧酸根离子 OH- Cl- Br- I- S2-。
如本题中溶液中的阳离子有H+和Na+,阴极上H+优先放电,得电子得到氢气,氢离子来自水,则同时生成
氢氧化钠;溶液中的阴离子有Cl-和OH-,阳极上Cl-优先放电,失电子得到氯气。
题型二:电极方程式的书写
杨sir化学,侵权必究
【例3】用情性电极电解下列溶液
(1)电解KNO 溶液阳极反应___________
3
(2)电解CuCl 溶液阴极反应___________
2
(3)电解氢氧化钠溶液的总反应___________
(4)电解CuSO 与NaCl混合溶液开始时阳极反应___________,阴极反应___________
4
【答案】
(1)4OH--4e-=O ↑+2H O或2HO-4e-=O ↑+4H+
2 2 2 2
(2)Cu2++2e-=Cu(3)2HO O↑+2H ↑
2 2 2
(4) 2Cl--2e-=Cl↑ Cu2++2e-=Cu
2
【解析】
(1)
惰性电极电解硝酸银溶液时,阳极为水电离出的氢氧根放电生成氧气,电极方程式为4OH--4e-=O ↑+2H O
2 2
或2HO-4e-=O ↑+4H+;
2 2
(2)
惰性电极电解CuCl 溶液时,阴极铜离子放电生成铜单质,电极方程式为Cu2++2e-=Cu;
2
(3)
惰性电极电解NaOH溶液时,阳极氢氧根放电生成氢气,阴极水电离出的氢离子放电生成氢气,实质上是
电解水,总反应为2HO O↑+2H ↑;
2 2 2
(4)
惰性电极电解CuSO 与NaCl混合溶液开始时阳极氯离子放电生成氯气:2Cl--2e-=Cl↑,阴极为铜离子放电
4 2
生成铜单质:Cu2++2e-=Cu。
题型三:电解池中的计算
杨sir化学,侵权必究
【例4】如图所示的A、B两个电解池中的电极均为铂,在A池中加入0.05 mol·L−1的CuCl 溶液,B池中
2
加入0.1 mol·L−1的AgNO 溶液,进行电解。a、b、c、d四个电极上所析出的物质的物质的量之比是
3
A.2∶2∶4∶1 B.1∶1∶2∶1
C.2∶1∶1∶1 D.2∶1∶2∶1
【答案】A
【详解】
a为阴极,铜离子得到电子生成铜,电极反应为Cu2++2e-=Cu;b为阳极,氯离子失去电子生成氯气,电极
反应为2Cl--2e-=Cl↑;c为阴极,银离子得到电子生成银,电极反应为Ag++e-=Ag;d为阳极,氢氧根离子
2
失去电子生成氧气,电极反应为4OH- -4e-=O ↑+2H O;根据电子守恒,四种物质的物质的量关系为
2 2
2:2:4:1。
故选A。
【点睛】掌握串联电路中电流相同,所以通过电子物质的量相等。
题型四:电解池的基本原理
杨sir化学,侵权必究
【例6】在如图所示的装置中,若通直流电5min时,铜电极质量增加2.16g。请回答下列问题:
(1)Y电极为直流电源的___________极。
(2)B中阳极的电极反应式为___________。
(3)C中pH变化:___________(填“增大”、“减小”或“不变”)。
(4)A中反应的方程式为___________。若A中KCl溶液的体积是200mL,电解后,溶液的pH为
___________(设电解前后溶液体积不变)。
【答案】正极 2HO-4e-=O ↑+4H+ 不变 2KCl+2H O Cl↑+H ↑+2KOH 13
2 2 2 2 2
【分析】
用通直流电5min时,铜电极质量增加2.16g,则Cu电极为阴极,因此X为电源的负极,Y电极为直流电
源的正极。A为用惰性电极电解氯化钾溶液,生成氯气、氢气和氢氧化钾;B为用惰性电极电解硫酸铜溶
液,生成铜Cu、O 和HSO ;C中的Ag电极为阳极,银本身放电,据此分析解答。
2 2 4
【详解】
(1)铜电极的质量增加,发生的反应为Ag++e-═Ag,则Cu电极为阴极,Ag为阳极,因此Y为直流电源的正
极,X为直流电源的负极,故答案为:正;
(2)B中的阳极上OH-放电,电极反应式为4OH--4e-═2H O+O↑(或2HO-4e-=O ↑+4H+),故答案为:4OH--4e-
2 2 2 2
═2H O+O↑(或2HO-4e-=O ↑+4H+);
2 2 2 2
(3) C中的Ag电极为阳极,银本身放电,故电极反应为:Ag-e-═Ag+,C中阴极反应为Ag++e-═Ag,因此溶
液pH不变,故答案为:不变;
(4)A为电解KCl溶液,生成KOH、Cl 和H,电解的方程式为2Cl-+2H O Cl↑+H ↑+2OH-(或
2 2 2 2 2
2KCl+2H O Cl↑+H ↑+2KOH);通电5 min时,铜电极的反应式为Ag++e-═Ag,n(Ag)=
2 2 2=0.02mol,电路中通过0.02 mol电子。A中放出0.01 mol H,溶液中生成0.02 mol KOH,c(OH-)=
2
=0.1 mol•L-1,则c(H+)=10-13 mol•L-1,因此pH=-lg c(H+)=13,故答案为:2KCl+2H O
2
Cl↑+H ↑+2KOH(或2Cl-+2H O Cl↑+H ↑+2OH-);13。
2 2 2 2 2
【点睛】
明确Cu电极的质量增加是解答本题的突破口。本题的易错点为(4),要注意溶液pH的计算方法的理解和应
用。
【变7】在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺
方案(原理如图),下列说法不正确的是
A.电源a端为负极
B.Fe3+对总反应起催化作用
C.阳极发生的电极反应式为2HCl-2e-=2H++Cl
2
D.电路中转移1mol电子,需要消耗11.2LO (标准状况)
2
【答案】D
【详解】
A.根据图示,a端, 发生还原反应,所以a端为电源负极,故A正确;
B.根据图示, 、 ,a端总反应为 ,
所以Fe3+对总反应起催化作用,故B正确;
C.根据图示,阳极发生的电极反应式为2HCl-2e-=2H++Cl,故C正确;
2
D.阴极反应为 ,电路中转移1mol电子,根据电子守恒,需要消耗5.6LO (标准状
2
况),故D错误;
选D。
题型五:电解池的分段电解
杨sir化学,侵权必究【例9】用石墨电极电解50mLCuSO 的溶液,两极上均收集到4.48L气体(标准状况),则原混合液中Cu2+
4
物质的量浓度为
A.1mol·L-1 B.2 mol·L-1 C.3mol·L-1 D.4 mol·L-1
【答案】D
【详解】
电解50mLCuSO 的溶液,阳极发生的反应为:4OH--4e-=2H O+O ↑,阴极上发生的电极反应
4 2 2
为:Cu2++2e-=Cu,2H++2e-→H ↑,两极均收集到4.48L(标准状况)气体,即均生成0.2mol
2
的气体,阳极生成0.2mol氧气说明转移了0.8mol电子,而阴极上生成的0.2molH 只得到了
2
0.4mol电子,所以剩余0.4mol电子由铜离子获得,则溶液中有0.2mol铜离子,据c= 得到
铜离子的浓度为: =4mol/L。答案选D。
【变9-3】如图所示的装置,通电一段时间后,测得甲池中某电极质量增加2.16g,乙池中某电极 上析出
6.4g某金属,下列说法正确的是
A.甲池是b极上析出金属银,乙池是c极上析出某金属
B.甲池是a极上析出金属银,乙池是d极上析出某金属
C.某盐溶液可能是CuSO 溶液
4
D.某盐溶液可能是Mg(NO) 溶液
3 2 杨sir化学,侵权必究
【答案】C
【分析】
甲池中a极与电源负极相连为阴极,电极上银离子得电子析出银单质,b电极为阳极,水电离出的氢氧根
放电产生氧气,同时产生氢离子;乙池中c为阴极,d为阳极,乙池电极析出6.4g金属,金属应在c极析
出,说明乙池中含有氧化性比氢离子强的金属阳离子。
【详解】
A.甲池a极上析出金属银,乙池c极上析出某金属,故A错误;
B.甲池a极上析出金属银,乙池c极上析出某金属,故B错误;
C.乙池电极析出6.4g金属,说明乙池中含有氧化性比氢离子强的金属阳离子,Cu2+氧化性强于氢离子,
会先于氢离子放电,则某盐溶液可能是CuSO 溶液,故C正确;
4
D.Mg2+氧化性较弱,电解时在溶液中不能得电子析出金属,所以某盐溶液不能是Mg(NO) 溶液,故D错
3 2
误;故答案为C。
题型六:电解质溶液的复原
杨sir化学,侵权必究
【变10-2】用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示
(气体体积均在相同状况下测定)。欲使溶液恢复到起始状态,向溶液中加入( )
A.0.1 mol CuO B.0.1 mol CuCO
3
C.0.075 mol Cu(OH) D.0.05 mol Cu (OH) CO
2 2 2 3
【答案】D
【分析】
电解CuSO 溶液时,开始发生反应:2CuSO +2H O 2Cu+O ↑+2H SO ,一段时间后,气体体积增大,
4 4 2 2 2 4
说明发生反应:2HO 2H↑+O ↑。结合图象数据分析解答。
2 2 2
【详解】
电解CuSO 溶液时,开始发生反应:2CuSO +2H O 2Cu+O ↑+2H SO ,一段时间后,转移相同电子时
4 4 2 2 2 4
得到气体体积增大,说明发生反应:2HO 2H↑+O ↑。由图可知,第一阶段析出Cu为
2 2 2
=0.1mol,放出的氧气为0.05mol,则需要加入0.1molCuO,第二阶段消耗的水为 =0.05mol,因此恢
复为电解前的浓度需要加入0.1molCuO和0.05molHO。由于CuCO 反应生成二氧化碳,0.1 mol CuCO 相
2 3 3
当于加入0.1 mol CuO,不能恢复为电解前的浓度;Cu(OH) 可以改写为CuO·HO,0.075 mol Cu(OH) 相
2 2 2
当于加入0.075 mol CuO和0.075 molH O,也不能恢复为电解前的浓度;Cu (OH) CO 可以改写为
2 2 2 3
2CuO·HO·CO,0.05 mol Cu (OH) CO 等效为加入0.1molCuO、0.05molHO,溶液可恢复为电解前的浓
2 2 2 2 3 2
度,故选D。
题型七:原电池与电解池串联
杨sir化学,侵权必究
【变11-1】已知某锂离子电池的总反应为LiC+Li CoO C+LiCoO,锂硫电池的总反应为2Li+S LiS
x 1-x 2 2 2
有关上述两种电池说法正确的是A.锂离子电池放电时,Li+向负极迁移
B.锂硫电池充电时,锂电极发生还原反应
C.两种电池的负极材料相同
D.图中表示用锂离子电池给锂硫电池充电
【答案】B
【详解】
A.根据同种电荷相互排斥,异种电荷相互吸引的原则,在原电池中阳离子向负电荷较多的正极移动,则
锂离子电池放电时,Li+向正极迁移,A错误;
B.锂硫电池充电时,锂电极与外接电源的负极相连,锂电极上Li+得电子发生还原反应产生Li单质,B正
确;
C.图中表示锂硫电池给锂离子电池充电,右边电极材料是Li和S,锂负极,硫为正极。左边电极材料是
C和LiCoO ,两种电池的负极材料不相同,C错误;
2
D.图中表示锂硫电池给锂离子电池充电,D错误;
故合理选项是B。
提分特训
小杨老师 15521324728 侵权必究
【题1】用惰性电极电解稀HSO 、Cu(NO )、NaCl的混合液,最初一段时间阴极和阳极上析出的物质分
2 4 3 2
别是
A.H 和Cl B.H 和O C.Cu和Cl D.Cu和O
2 2 2 2 2 2
【答案】C
【详解】
稀HSO 、Cu(NO )、NaCl的混合液,阳离子的放电顺序:Cu2+>H+>Na+,阴离子的放电顺序:Cl->OH-
2 4 3 2
>酸根离子,因此用惰性电极电解稀HSO 、Cu(NO )、NaCl的混合液,阳极Cl-先失电子生成Cl,阴极
2 4 3 2 2
Cu2+先得电子生成Cu,即最初一段时间阴极和阳极上析出的物质分别是Cu和Cl,C满足题意;
2
答案选C。
【题2】如图所示电解池Ⅰ和Ⅱ中,a、b、c、d均为铂电极,在电解过程中b电极有气体逸出,d电极质量
增大。符合上述实验结果的一项是X Y
A AgNO NaCO
3 2 3
B Cu(NO) Pb(NO)
3 2 3 2
C FeSO Al(SO)
4 2 4 3
D MgSO CuSO
4 4
A.A B.B C.C D.D
杨sir化学,侵权必究
【答案】D
【分析】
首先,根据电源正负极可知a、c为阳极,b、d为阴极,然后再根据惰性电极电解时离子的放电顺序,阳
离子放电顺序:
Ag+>Hg2+>Fe3+>Cu2+>H+(指酸电离的)>Pb2+>Sn2+>Fe2+>Zn2+>Al3+>Mg2+>Na+>Ca2+>K+
阴离子的放电顺序
是惰性电极时:S2->I->Br->Cl->OH-> > (含氧酸根离子)
是活性电极时:电极本身溶解放电,即可判断。
【详解】
A.X溶液为AgNO 时,b极为阴极,根据放电顺序可知,是Ag+放电生成固体银,不产生气体,A错误;
3
B.X溶液为Cu(NO ) 时,b极为阴极,根据放电顺序可知,是Cu2+放电生成固体铜,不产生气体,B错误;
3 2
C.Y溶液为Al (SO ) 时,d极为阴极,根据放电顺序可知,H+放电产生氢气,电极质量不增加,C错误;
2 4 3
D.X溶液为MgSO 时,b极为阴极,根据放电顺序可知,H+放电产生氢气,Y溶液为CuSO 时,d极为阴
4 4
极,根据放电顺序可知,是Cu2+放电生成固体铜,电极质量增加,D正确;
【点睛】
电解时阴阳离子的放电顺序的准确记忆是解决这种题目的关键。
【题3】用惰性电极电解下列各组中的三种溶液,电解过程中,溶液中pH依次为减小、不变、增大的是
A.HCl、HNO、KSO B.AgNO、CuCl 、 Cu(NO )
3 2 4 3 2 3 2
C.CaCl 、 KOH、NaNO D.CuSO 、NaSO 、KCl
2 3 4 2 4
【答案】D
【详解】
A.电解HCl生成氯气和氢气,电解本身,电解HNO 时生成氢气和氧气,即电解水型的,电解KSO 时,
3 2 4
时生成氢气和氧气,即电解水型的,溶液的pH依次为升高,降低,不变,故A错误;B.电解AgNO 会生成硝酸、银和氧气,溶液的pH降低;氯化铜溶液呈酸性,电解CuCl 会生成铜和氯气,
3 2
电解后浓度减小,铜离子水解程度减弱,溶液的pH增大;电解Cu(NO ) 时会生成铜、硝酸和氧气,溶
3 2
液的pH降低,故B错误;
C.电解CaCl 时生成氢氧化钙、氯气和氢气,电解KOH时生成氢气和氧气,即电解水型的,电解NaNO
2 3
时,生成氢气和氧气,即电解水型的,溶液的pH依次为升高,升高,不变,故C错误;
D.电解CuSO 时,生成铜和氧气以及硫酸,电解NaSO 生成氢气和氧气,即电解水型的,电解KCl时会
4 2 4
生成氢气、氯气单质和氢氧化钾,溶液中c(H+)依次为升高,不变,降低,pH依次为减小、不变、增大,
故D正确;
故选:D。
【题5】在100 mL H SO 和CuSO 的混合液中,用石墨作电极进行电解,两极上均收集到2.24 L气体(标准
2 4 4
状况下),则原混合液中Cu2+的物质的量浓度为
A.0.1 mol·L-1 B.0.2 mol·L-1 C.1 mol·L-1 D.2 mol·L-1
【答案】C
【详解】
电解0.1LH SO 和CuSO 的混合溶液,阳极发生的反应为:4OH-→2HO+O↑+4e-,阴极上发生的电极反应
2 4 4 2 2
为:Cu2++2e-→Cu,2H++2e-→H↑,两极均收集到2.24L(标况)气体,即均生成0.1mol的气体,阳极生成
2
0.1mol氧气说明转移了0.4mol电子,而阴极上生成的0.1molH 只得到了0.2mol电子,所以剩余0.2mol电
2
子由铜离子获得,且溶液中有0.1mol铜离子,据c= 得到铜离子的浓度为: =1mol/L,故选C。
【题7】如图所示,A、B、C三个装置的烧杯中分别盛有足量的CuCl 溶液。
2
(1)A、B、C三个装置中属于电解池的是__。
(2)A池中Zn是__极,Cu极的电极反应式为__。
(3)B池中Pt棒上的电极反应为__。B池中的总反应化学方程式为__。
(4)C池中Cu极电极反应式为__。
【答案】BC 负 Cu2++2e-=Cu 2Cl--2e-=Cl↑ CuCl Cu+Cl ↑ Cu-2e-=Cu2+
2 2 2
【详解】
(1)A中有自发的氧化还原反应:Zn+CuCl =ZnCl +Cu,所以为原电池,B、C均有外接电源,为电解池;
2 2
(2)A池中总反应为Zn+CuCl =ZnCl +Cu,所以Zn电极失电子发生氧化反应为负极;Cu电极上铜离子得电
2 2
子生成Cu,电极反应式为Cu2++2e-=Cu;
(3)B中Pt电极与电源的正极相连为阳极,溶液中氯离子在阳极失电子被氧化,电极反应式为2Cl--2e-=Cl↑;B中C电极为阴极,铜离子得电子被还原生成铜单质,所以总反应为CuCl Cu+Cl ↑;
2 2 2
(4)C中铜电极与电源正极相连为阳极,铜失电子被氧化成铜离子,电极反应式为Cu-2e-=Cu2+。
【题9】回答下列问题
(1)请你将反应 设计成原电池,并回答下列问题:
①该电池的正极材料可以是___________,也可选用___________等代替。
②画出你所设计的双液原电池的装置图,并标注出电极材料和电解质溶液。___________
③写出电极反应式:负极___________,正极___________。
④该电池负极材料质量减重3.2g,则电路中通过的电子的数目为___________。
(2)从 、 、Na+、Cu2+、Ag+、Cl-等离子中选出适当的离子组成电解质,采用惰性电极对其溶液
进行电解。(注意:请填写满足条件的所有电解质的化学式)
①若两极分别放出H 和O 时,电解质可能为___________(填化学式,下同)。
2 2 杨sir化学,侵权必究
②若阴极析出金属,阳极放出气体,电解质可能为___________。
③若两极分别放出气体,且气体体积比为1∶1时,电解质只能为___________。
【答案】
(1) Ag 石墨(C)或Pt
或
(2) 、 、 、 、 NaCl
【分析】
(1)
①由 可知,Cu失电子发生氧化反应作负极、不如Cu活泼的金属或导电的非金属
作正极,FeCl 溶液为电解质溶液,则该电池的正极材料可以是Ag,也可选用石墨(C)或Pt;答案为Ag;
3
石墨(C)或Pt。
②由 可知,Cu作负极,C棒作正极,电解质溶液为FeCl 溶液和CuSO 溶液,用
3 4盐桥相连接成闭合回路,双液原电池的装置图为 ;答案为
。
③由 可知,该原电池中,负极的电极反应式为 ,正极的电极反应式
为 ;答案为 ; 。
④该电池负极材料质量减重3.2g,则反应的Cu的物质的量为n(Cu)= =0.05mol,由负极的电极反
应式为 可知,电路中通过的电子的数目为0.05×2×N =0.1N 或0.05×2×6.02×1023=6.02×1022;
A A
答案为0.1N 或6.02×1022。
A
(2)
阴极上阳离子放电顺序为Ag+>Cu2+>H+>Na+,阳极上阴离子放电顺序为Cl->OH-> 、
①若两极分别放出H 和O 时,溶液中的电解质不放电,溶液中阳离子为Na+,阴离子为 、 ,所
2 2
以电解质是 或 中的任意一种;答案为 、 。
②当阴极析出金属,则金属离子为Cu2+或Ag+,阳极放出气体时,阴离子为Cl-、 或 ,所以电解质
是 或 或 或 中的任意一种;答案为 、 、 、 。
③当阴极放出H,则阴极为水中H+放电,溶液中的阳离子为Na+,阳极放出Cl,阴离子为Cl-放电,满足
2 2
气体体积比为1:1,所以电解质为NaCl;答案为NaCl。提分作业
小杨老师 15521324728 侵权必究
【练1】用惰性电极电解CuSO 和NaCl 的混合溶液,开始时阴极和阳极上分别
4
析出的物质是
A.H 和Cl B.Cu和Cl C.H 和O D.Cu和O
2 2 2 2 2 2
【答案】B
【详解】
根据电解原理,阳离子放电顺序是Cu2+>H+>Na+,阴离子放电顺序是Cl->OH->SO ,所以开始时阴极
反应式Cu2++2e-=Cu,阳极反应式:2Cl--2e-=Cl↑,故选项B正确。
2
【练2】在某电解质溶液里,用M和N作电极,通电一段时间后,发现M极质量减小,N极质量增大,符
合这一情况的是( )
A.电解质溶液是稀硫酸 B.金属M是阳极,金属N是阴极
C.M和N都是石墨电极 D.M是阴极,N是阳极
【答案】B
【详解】
A.电解稀硫酸溶液,阳极发生氧化反应,质量会减少,即M极质量减小;阴极发生还原反应放出氢气,
N极质量不变,故A不符合题意;
B.由题意可知,M电极溶解,则发生氧化反应,为阳极;N电极质量增加,溶液中的金属阳离子得电子
在N电极上析出,发生还原反应,N为阴极,故B符合题意;
C.如果M和N均是石墨电极,M极质量不会减小,故C不符合题意;
D.由题意可知,M电极溶解,则发生氧化反应,为阳极;N电极质量增加,溶液中的金属阳离子得电子
在N电极上析出,发生还原反应,N为阴极,故D不符合题意;
答案选B。
【练3】用石墨电极电解稀硫酸的过程中,溶液pH的变化情况为
A.逐渐减小 B.逐渐增大 C.不改变 D.先减小,后增大
【答案】A
【详解】
用石墨电极电解稀硫酸,阳极为氢氧根离子失电子发生氧化反应,阴极为氢离子得电子发生还原反应,其
实质为电解水,所以电解过程中,硫酸硫酸浓度越来越大,则溶液pH的变化情况为逐渐减小,故选:A。
【练4】用惰性电极电解饱和食盐水,下列说法正确的是
A.电解过程中, Cl-向阳极方向移动,发生还原反应
B.电解一段时间后,阴极附近溶液pH增大
C.电解池中的总反应为:2H++2Cl-=H↑+Cl↑
2 2
D.欲使电解池中的溶液恢复到电解前状态,应加入适量浓盐酸
【答案】B【解析】
试题分析:A.电解过程中, Cl-向阳极方向移动,发生氧化反应,A错误;B.电解一段时间后,阴极氢
电解
离子放电,产生氢氧根,阴极附近溶液pH增大,B正确;C.电解池中的总反应为:2HO+2Cl-
2
H↑+Cl↑+2OH-,C错误;D.欲使电解池中的溶液恢复到电解前状态,应通入适量氯化氢气体,D错误,
2 2
答案选B。
考点:考查电解饱和食盐水的有关判断
【练5】用石墨作电极完全电解含1 mol溶质X的溶液后,向溶液中加入一定量的物质Y能使电解
液恢复到起始状态是
选项 X溶液 物质Y
A CuCl 1 mol Cu(OH)
2 2
B KOH 1 mol KOH
C NaSO 1 mol HSO
2 4 2 4
D AgNO 0.5 mol AgO
3 2
A.A B.B C.C D.D
杨sir化学,侵权必究
【答案】D
【解析】
A.电解氯化铜,在两极上分别产生金属铜和氯气,电解质复原加入氯化铜即可,故A错误;B.电解氢
氧化钾的实质是电解水,所以电解质复原加入水即可,故B错误;C.电解硫酸钠的实质是电解水,所以
电解质复原加入水即可,故C错误;D.电解硝酸银两极上产生的是金属银和氧气,所以电解质复原加氧
化银即可,电解含1mol溶质硝酸银的溶液,会析出金属银1mol,根据银元素守恒,所以加入0.5mol Ag O
2
后即可复原,故D正确;故选D。
点睛:理解电解池的工作原理以及电解质复原的方法是解题关键,根据电解原确定电解后析出的金属或是
放出的气体,根据:出什么加什么,出多少加多少的原理确定电解质复原加入的物质以及量的多少。
【练6】如图所示,A、B、C三个装置的烧杯中分别盛有足量的CuCl 溶液。
2
(1)A、B、C三个装置中属于电解池的是_______。
(2)A池中Zn是_______极,Cu极的电极反应式为_______。
(3)B池中的总反应化学方程式为_______,若将B池的溶液换成饱和的食盐水,当电路中通过1mol电子时
两极共产生的气体体积为_______(标准状况)。
杨sir化学,侵权必究
(4)C池中Cu极电极反应式为_______。
(5)某化学学习小组在学完原电池后,以Zn+Fe2+=Zn2++Fe为电池总反应设计电池,该电池的正极反应式为_______。
【答案】BC 负 Cu2++2e-=Cu CuCl Cu+Cl ↑ 22.4L Cu-2e-=Cu2+ Fe2++2e-=Fe
2 2
【详解】
(1)A没有外接电源,属于原电池,BC装置都有外接电源,所以是把电能转化为化学能的装置,属于电解
池,
故答案为:BC;
(2)铜、锌、氯化铜原电池中,锌作负极,负极上锌失电子发生氧化反应,电极反应式为:Zn−2e−=Zn2+,
铜离子在正极得电子生成Cu单质,电极反应为:Cu2++2e-=Cu,
故答案为:负;Cu2++2e-=Cu;
(3)该装置是电解池,且阳极是惰性电极,C连接电源负极,所以是阴极,阴极上铜离子得电子发生还原反
应,电极反应式为:Cu2++2e−=Cu,铂连接电源正极,所以铂在阳极,阳极上氯离子失电子发生氧化反
应,电极反应式为:2Cl−−2e−=Cl↑,所以其电池反应式为:CuCl Cu+Cl ↑,若将B池的溶液换成饱
2 2 2
和的食盐水,则电解的总反应为: ,由反应可知转移2mol电子时生
成1mol氢气和1mol氯气,则通过1mol电子时两极共产生的气体的物质的量为1mol,标况下的体积为
22.4L,故答案为:CuCl Cu+Cl ↑;22.4L;
2 2
(4)该装置是电解池,铜是阳极,阳极上铜失电子发生氧化反应,电极反应式为:Cu−2e−=Cu2+,
故答案为:Cu−2e−=Cu2+;
(5)以Zn+Fe2+=Zn2++Fe为电池总反应设计电池,Zn失电子作负极,Fe2+得电子在正极发生反应,电极反应
为:Fe2++2e-=Fe,故答案为:Fe2++2e-=Fe;
【练7】某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时。观察到电流
表的指针发生了偏转。请回答下列问题:
(1)甲池为___________(填“原电池”、“电解池”或“电镀池”),通入 电极的电极反应式为
___________。
(2)乙池中A(石墨)电极的名称为___________(填“正极”、“负极”、“阴极”或“阳极”)。总反应的离子方程
式为___________。
(3)当乙池中B极质量增加21.6g时,甲池中理论上消耗 的体积为___________mL(标准状况下),丙池
中___________极析出___________g铜。
杨sir化学,侵权必究
(4)若丙池中电极不变,将其溶液换成 溶液,电键闭合一段时向后。甲中溶液的pH将
___________(填“增大”“减小”或“不变”);丙中溶液的pH将___________(填“增大”、“减小”或“不变”)。
【答案】
(1) 原电池
(2) 阳极
(3) 1120 D 6.4
(4) 减小 不变
【分析】
由图可知,甲池为燃料电池,通入甲醇的的Pt电极为负极,碱性条件下,甲醇在负极失去电子发生氧化反
应生成碳酸根离子和水,通入氧气的Pt电极为正极,碱性条件下,氧气在正极得到电子发生还原反应生成
氢氧根离子;乙池为电解池,A电极为电解池的阳极,水在阳极失去电子发生氧化反应生成氧气,B电极
为阴极,银离子在阴极得到电子发生还原反应生成银;丙池为电解池,C电极为阳极,氯离子在阳极失去
电子发生氧化反应生成氯气,D电极为阴极,铜离子在阴极得到电子发生还原反应生成铜。
(1)
由分析可知,甲池为原电池;通入甲醇的的Pt电极为负极,碱性条件下,甲醇在负极失去电子发生氧化反
应生成碳酸根离子和水,电极反应式为 ;
(2)
乙池为电解池,A电极为电解池的阳极,水在阳极失去电子发生氧化反应生成氧气,B电极为阴极,银离
子在阴极得到电子发生还原反应生成银,总反应的离子方程式为 ;
(3)
21.6g银的物质的量为 ,由得失电子数目守恒可知,甲池中理论上消耗氧气的体积为0.2mol× ×22.4L/mol×1000=1120mL,丙池中D极析出铜的质量为0.2mol× ×64g/mol=6.4g;
(4)
若丙池中电极不变,将其溶液换成 溶液,电键闭合一段时间后,甲池中的总反应为
2CHOH+3O +4OH-=2CO +6H O,反应中消耗氢氧根离子,溶液的pH将减小;丙池中电解 溶液
3 2 2
的方程式为 ,丙中溶液的pH不变。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育