文档内容
第 26 讲 物质的量在化学方程式计算中的应用
知识导航
知识精讲
一、化学方程式计算的基础
物质是由原子、分子、离子等粒子构成的,物质之间的化学反应也是粒子按照一定的数目关系进行的。
化学方程式中的化学计量系数可以明确表示出化学反应中粒子之间的数目关系。
2Na + 2HO === 2NaOH + H↑
2 2
2 ∶ 2 ∶ 2 ∶ 1
2×6.02×1023∶2×6.02×1023 ∶ 2×6.02×1023 ∶ 1×6.02×1023
2 mol ∶ 2 mol ∶ 2 mol ∶ 1 mol
总结归纳
① 化学方程式中各物质的化学计量数之比等于粒子个数之比,也等于各物质的物质的量之比。
② 对于有气体参与的反应,在同温同压下各气体的化学计量数之比等于体积之比。
二、根据化学方程式计算的一般步骤
三、实例分析举个例子
250 ml 2mol/L的硫酸与足量的铁屑完全反应。计算:
(1)参加反应的铁屑的物质的量;
(2)生成的H 的体积(标准状况)。
2
解:参加反应的HSO 的物质的量为:2mol/L×0.25L=0.50 mol
2 4
(1)设参加反应的铁屑的物质的量为n(Fe)
Fe+HSO ===FeSO+H↑
2 4 4 2
1 1
n(Fe) 0.50 mol
1 n(Fe)
=
1 0.50mol
n(Fe)=0.50 mol
(2)设生成H 的物质的量为V(H )
2 2
Fe+HSO ===FeSO+H↑
2 4 4 2
1mol 22.4L
0.50 mol V(H )
2
1 mol 22.4L
=
0.50mol V(H )
2
V(H )=11.2L
2
答:(1)参加反应的铁屑的物质的量为0.50 mol;(2)生成的H 的体积在标准 状况下为11.2L。
2
经典例题
题型一:单一体系计算
【例2】(2020·新疆·乌鲁木齐市第四中学高一期末)实验室中所用少量氯气 是用MnO 和浓盐酸制取的,
2
用浓盐酸200ml,其密度为1.19g·cm-3,HCl的质量分数为36.5%,跟MnO 恰好完全反应,产生了11.2L
2
(标况)的氯气。试计算:
①浓盐酸的物质的量浓度?___
②求参加反应的HCl的物质的量?___
③被氧化的HCl的质量?___
题型二:单一体系(含不参与反应的杂质)计算
【变3】(2020·贵州铜仁伟才学校高一月考)现有500mL 1 mol·L-1的盐酸与35 g 生铁 样品(杂质不与盐
酸反应)恰好完全反应,则该样品中铁的质量分数是
A.26.7% B.40% C.60% D.80%题型三:单一体系(对比)计算
【变4】(2020·福建·泉州五中高一单元测试)一定量的Na、Mg、Al分别与足量的盐酸反应,放出的氢气
在相同条件下体积比为1:2:3,则Na、Mg、Al三种金属的物质的量之比为( )
A.1:1:1 B.1:2:3 C.1:1:2 D.3:3:4
题型四:混合体系计算
【变6-1】(2020·江西·进贤县第一中学高一月考)由Zn、Cu、Al、Fe四种金属中的两 种组成的混合物
41.5g,与足量的盐酸反应产生的氢气在标况下为22.4升,则混合物中一定含有的金属是
A.Zn B.Fe C.Al D.Cu
【例8】(2013·上海交大附中高一期末)某密闭容器内有6g炭 和14g氧气,在一定条件下完全反应,计
算:
(1)生成的混合气体中CO与CO 各占_____克?
2
(2)生成的混合气体的平均相对分子质量为_____?
【例12】(2016·重庆·高一月考)下图为实验室某浓盐酸试剂瓶标签 上的有关信息,试根据标签上的有关
数据,回答下列问题(一)(二):(计算结果保留一位小数)
(一).(1)浓盐酸中HCl的物质的量浓度为________mol·L-1。
(2) 量取________mL浓盐酸加水稀释就得到500 mL、0.4mol·L-1的稀盐酸。
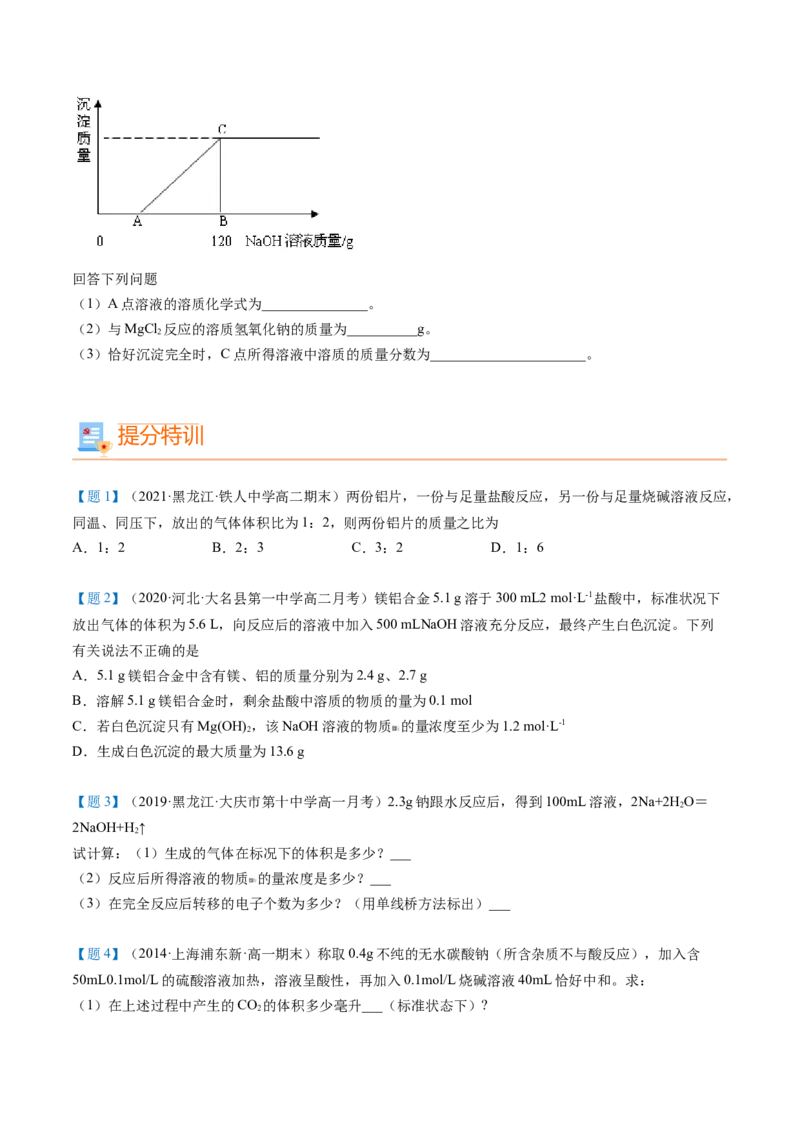
(二).取该浓盐酸10g与某MgCl 溶液90g混合,向混合溶液中逐滴加入10%的NaOH溶液,生成的沉淀的
2
质量与加入的NaOH溶液质量关系如下图所示。回答下列问题
(1)A点溶液的溶质化学式为_______________。
(2)与MgCl 反应的溶质氢氧化钠的质量为__________g。
2
(3)恰好沉淀完全时,C点所得溶液中溶质的质量分数为______________________。
提分特训
【题1】(2021·黑龙江·铁人中学高二期末)两份铝片,一份与足量盐酸反应,另一份与足量烧碱溶液反应,
同温、同压下,放出的气体体积比为1:2,则两份铝片的质量之比为
A.1:2 B.2:3 C.3:2 D.1:6
【题2】(2020·河北·大名县第一中学高二月考)镁铝合金5.1 g溶于300 mL2 mol·L-1盐酸中,标准状况下
放出气体的体积为5.6 L,向反应后的溶液中加入500 mLNaOH溶液充分反应,最终产生白色沉淀。下列
有关说法不正确的是
A.5.1 g镁铝合金中含有镁、铝的质量分别为2.4 g、2.7 g
B.溶解5.1 g镁铝合金时,剩余盐酸中溶质的物质的量为0.1 mol
C.若白色沉淀只有Mg(OH) ,该NaOH溶液的物质 的量浓度至少为1.2 mol·L-1
2
D.生成白色沉淀的最大质量为13.6 g
【题3】(2019·黑龙江·大庆市第十中学高一月考)2.3g钠跟水反应后,得到100mL溶液,2Na+2HO=
2
2NaOH+H ↑
2
试计算:(1)生成的气体在标况下的体积是多少?___
(2)反应后所得溶液的物质 的量浓度是多少?___
(3)在完全反应后转移的电子个数为多少?(用单线桥方法标出)___
【题4】(2014·上海浦东新·高一期末)称取0.4g不纯的无水碳酸钠(所含杂质不与酸反应),加入含
50mL0.1mol/L的硫酸溶液加热,溶液呈酸性,再加入0.1mol/L烧碱溶液40mL恰好中和。求:
(1)在上述过程中产生的CO 的体积多少毫升___(标准状态下)?
2(2)计算无水碳酸钠的纯度___?
【题5】(2011·海南·高一期末)将5.6 g 铁粉放入100 mL CuSO 溶液中,充分反应后,再向溶液中加入足
4
量的稀硫酸,又产生1.12 L气体(标准状况下)。试计算:
(1)最后所得溶液 中FeSO 的物质的量__________;
4
(2)原CuSO 溶液的物质的量浓度__________。
4
【题6】(2021·上海·复旦附中高一期中)液氯储罐中常混有NCl ,当液氯中NCl 的质量分数达到4%以上
3 3
就有爆炸危险。为测定氯气中的NCl 含量,将一定量样品先通过足量盐酸吸收NCl (反应为:
3 3
)。再用400mL6.1mol/L的NaOH溶液( )吸收所有的Cl,测得吸收后
2
NaOH溶液增重56.8g(不考虑盐酸挥发)。经测定NCl 吸收管内 质量为0.270g。
3
(1)计算上述NaOH溶液的质量分数______。
(2)计算该样品中NCl 的质量分数,并判断该样品是否安全______?
3
【题7】(2010·广西·高一竞赛)过氧化钙CaO·nHO中含有部分杂质CaO
2 2
(1)称取0.542g过氧化钙 样品灼烧发生反应:2 CaO ·nHO 2CaO+ O ↑ +2nH O,得到O,氧气在标态下
2 2 2 2 2
的体积为67.2mL,求该样品中CaO 物质的量___________;
2
(2)另取同一样品0.542g溶于适量的稀盐酸中,然后加入足量的NaCO 溶液,将溶液中的Ca2+全部转化为
2 3
CaCO 沉淀,得到干燥的CaCO 0.70g, 计算样品中CaO的质量以及CaO·nHO中n的值___________。
3 3 2 2
【题8】(2020·四川·成都新津为明学校高一月考)(1)如图是某学校实验室从化学试剂商店买回来的氢氧
化钠试剂标签上的部分内容。某同学从该试剂瓶中取出24.0g固体,配成1L溶液,请计算:
氢氧化钠化学纯(CP)
500g
品名:氢氧化钠
化学式:NaOH
相对分子质量:40
所得氢氧化钠溶液的物质的量浓度___________,从所得氢氧化钠溶液中取出200mL于一烧杯中,投入足
量的金属铝,完全反应后,计算产生的气体在标准状况下的体积___________。
(2)Mg、Al混合物共0.4mol,用盐酸将其完全溶解,放出标准状况下11.2L气体,然后再滴入4mol/L的
NaOH溶液,该混合物中Mg、Al的物质的量分别为___________;若该Mg、Al的混合物与盐酸恰好完全
反应,在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积为___________。提分作业
【练1】(2021·四川省安岳中学高一月考)据最新报道,科学 家发现了如下反应:O+PtF =O (PtF),当
2 6 2 6
生成1mol O(PtF)时,消耗O 的体积为
2 6 2
A.11.2L B.22.4L C.不能确定 D.44.8L
【练2】(2021·山东·肥城市教学研究中心高一期中)0.56gCaO正好与20mL盐酸反应,这种盐酸的物质的
量浓度是
A.0.10mol/L B.0.20mol/L C.0.50mol/L D.1.00mol/L
【练3】将7g炭粉与14g氧气在一定条件下完全反生成21g氧化物,则生成物中CO与CO 的物质的量之
2
比为
A.1:1 B.2:1 C.2:3 D.3:1
【练4】(2021·浙江省淳安县汾口中学高一开学考试)将NaCO 和NaHCO 的混合 物加热,生成的气体
2 3 3
(假设无损耗)全部通入足量的石灰水中,得到20.0g白色沉淀,加热后的残留物加入200mL盐酸恰好完全
反应,生成5.60LCO 气体(标准状况下)。试回答下列问题(计算结果均保留3 位有效数字)
2
(1)加热时发生反应的化学方程式为_______。
(2)所加盐酸的物质的量浓度为_______mol/L。
【练5】(2020·湖南常德·高一期末)把5.1 g镁铝合金的粉末放入500 mL1 mol/L盐酸中,恰好完全反应。
试计算:
(1)该合金中镁和铝的物质的量:n(Mg)______________;n(Al)______________
(2)将等质量的该合金投入到足量的氢氧化钠溶液中,求标况下放出气体的体积。__________。
【练6】(2011·福建福州·高一期中)1774年,瑞典化学家舍勒发现软锰矿(主要成分是MnO )和浓盐酸混
2
合加热能制取氯气:MnO +4HCl(浓) MnCl +Cl↑+2H O。现将23.2g含MnO 的质量分数为75%的软
2 2 2 2 2
锰矿石与足量10mol/L浓盐酸完全反应(杂质不参加反应)。把反应后所得溶液稀 释成200ml。计算:
(1)生成的Cl 的体积(标准状况)____________。
2
(2)参加反应的浓盐酸的体积____________。
(3)稀释后溶液中MnCl 的物质的量浓度___________。
2关注更新免费领取,淘宝唯一每月更新店铺:知二教育