文档内容
第 四单元 物质构成的奥秘 测试卷
温馨提示:本卷共三大题,计 25 小题,满分 100 分,考试时间 90分钟。
一、单项选择题:(本题共15小题,每小题3分,满分45分)
1.(A)地壳中含量最多的元素是( )
A. 氧 B. 硅 C. 铝 D. 铁
2.(A)一种元素和另一种元素的区别是( )
A.质子数不同 B.中子数不同
C.相对原子质量不同 D.电子数不同
3.(A)下列关于原子结构的说法中,错误的是( )
A.构成原子核必不可少的粒子是质子
B.原子核都是由质子和中子构成的
C.核电荷数一定等于质子数或核外电子数
D.原子中的质子数不一定等于中子数
4.(A)与元素的化学性质关系最密切的是( )
A.质子数 B.最内层电子数
C.电子层数 D.最外层电子数
5.(A)“神七”太空舱利用NiFe O 做催化剂将宇航员呼出的CO 转化为O ,已知
2 4 2 2
Fe 的化合价为+3,则Ni的化合价为( )
A.+1 B.+2 C.+3 D.+4
6.(A)下列方框中,能表示2N 意义的示意图是( )
2
A B
C D
7.(A)氢是新型清洁能源,但难储运。研究发现,镧和镍的一种合金是储氢材料。
下列有关57号元素镧(La)的说法不正确的是( )
A.该元素为非金属元素 B.该元素原子的核电荷数为57
C.该元素原子的核外电子数为57 D.该元素原子的质子数为57
8.(A)对Fe3+、Fe2+、Fe三种粒子的判断,正确的是 ( )
①核电荷数相同 ②核外电子数相等 ③电子层结构完全相同 ④质量几
1乎相等 ⑤等质量的三种粒子所有的质子数相等
A.①②③④⑤ B.①③⑤
C.①④⑤ D.②③④
9.(A)2009年2月22日2时20分,山西焦煤集团西山煤电公司屯兰煤矿南四采
区发生特别重大瓦斯爆炸事故,造成78人死亡、114人受伤,其中重伤5人。同学
们得知这一消息,开始讨论瓦斯的主要成分CH 的意义,下列四位同学中哪个说
4
法是错误的( )
A B C D
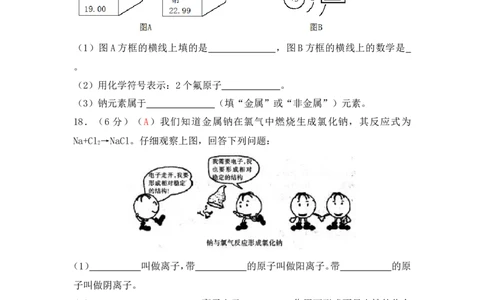
10.(A)下列四种粒子的结构示意图中,说法正确的是( )
+8 2 8 +12 2 8 2 +11 2 8 +12 2 8
① ② ③ ④
A.它们表示四种不同的元素
B.②表示的元素在化合物中通常显+2价
C.①③④表示的元素都是非金属元素
D.①④表示的是阳离子
11.(A)为了防止传染病疫情发生,必须对发生重大自然灾害的地区进行环境消
毒,下列有关常用的消毒剂及对应的化学用语表示正确的是( )
A.Cl 中氯元素的化合价为-1价
2
B.氧化钙中钙元素的化合价为Ca2+
C.过氧化氢(H O )中,氧元素为-1价
2 2
D.漂白精有效成份次氯酸钠(NaClO)中,氯元素为-1价
12.(B)下列有关分子、原子、离子的叙述错误的是( )
A.带电的原子或原子团叫做离子
2B.分子是保持物质化学性质的最小粒子
C.原子是不能再分的最小粒子
D.原子、分子、离子都是构成物质的粒子
13.(B)下列关于耐高温新型陶瓷——氮化硅(Si N )的叙述,正确的是( )
3 4
A.氮化硅中Si、N两种元素的质量比为4:3
B.氮化硅中氮元素的质量分数为60%
C.14g氮化硅中含硅8.4g
D.氮化硅的相对分子质量为l44
14.(B)科学家用单个分子制成了“纳米车”(如右图),它能在人工操纵下运输
药物分子到病源处释放以杀死癌细胞。下列有关“纳米车”的说法正确的是(
)
A.“纳米车”的研制成功说明分子要在人为外力作用下才能运动
B.“纳米车”分子不是由原子构成的
C.“纳米车”运输药物分子的过程是肉眼可以直接看见的
D.“纳米车”研制成功说明在一定条件下人可以控制分子运动
15.(C)在农业科研实验室里,用一定量的NH NO ,和KH PO 。的固体混合物配制无
4 3 2 4
土栽培营养液,已知固体混合物中氮元素的质量分数为28%,则固体混合物中
KH PO 的质量分数为( )
2 4
A.20% B.25% C.85% D.80%
二、填空题(本大题包括7小题,满分35分)
16.(8分)(A)将分子、原子、原子核、质子、中子或电子等词语分别填入有关空格
内:
(1)化学变化中的最小粒子是______。
(2)能直接构成纯净物的是 。
(3)保持物质化学性质的最小粒子是 。
(4)带正电荷的是 。
(5)不显电性的是 。
3(6)决定相对原子质量大小的是 。
(7)在同一原子中数目相等的是 。
⑻质量最小的粒子是 。
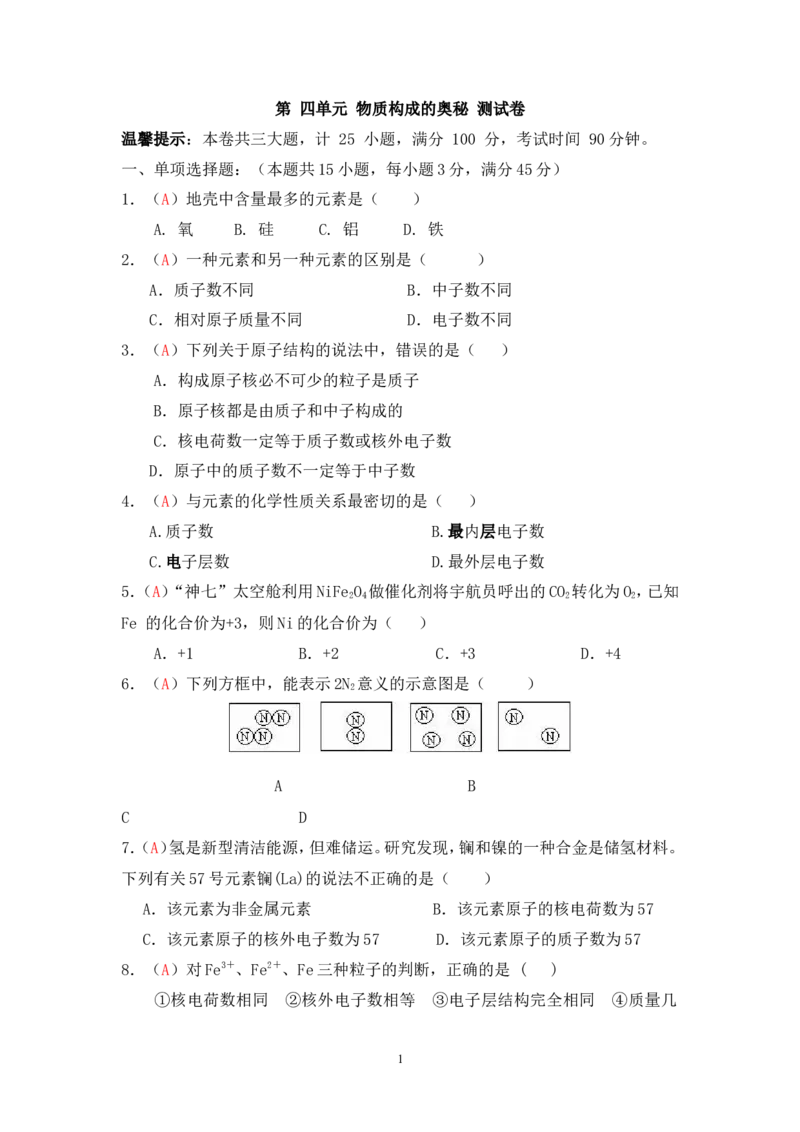
17.(4分)(A)图A是两种元素在元素周期表中的信息,图B是氟原子的原子结构
示意图。
(1)图A方框的横线上填的是 ,图B方框的横线上的数学是
。
(2)用化学符号表示:2个氟原子 。
(3)钠元素属于 (填“金属”或“非金属”)元素。
18.(6 分)(A)我们知道金属钠在氯气中燃烧生成氯化钠,其反应式为
Na+Cl →NaCl。仔细观察上图,回答下列问题:
2
(1) 叫做离子,带 的原子叫做阳离子。带 的原
子叫做阴离子。
(2) 、 离子由于 作用而形成不显电性的化合
物,叫做离子化合物。
19.(3分)(A)A、B两种元素的原子结构示意图
A 中 m=7,则X= ;B中y=12,则n=
4。A、B两种元素形成的化合物的化学式是 。
20.(4分)(B)(1)奇妙的化学王国里,没有生命的阿拉伯数字也变得鲜活起来。
这些数字在化学符号周围不同的位置上,将代表着不同的含义。例如:2N Com SO
bin 2
Zn2+等。请你试着再写出两个带有数字“2”但含义不同的化学符号:
①_________________________;②__________________________。
(2)在一个陌生的星球上充满了一种浅黄绿色的气态单质。科学家研究了该单质
确定其化学式为F ,进一步研究表明:当该元素原子与金属元素原子化合时,只
2
能形成F-。试回答:
①根据上面提供的信息判断,F元素属于____________(填“金属”或“非金
属”)
②科学家在该星球上还发现了另一种元素,确定其元素符号为Al,当Al原子与F
原子化合时Al显+3价,则这种化合物的化学式为_______________
21.(7分)(B)元素周期表是学习化学的重要工具。下面是元素周期表中1~18号
元素原子核外电子排布,我们对它进行研究:
⑴ 第16号元素属于_______元素(填“金属”或“非金属”),它在化学反应中
容易________(填“得”或“失”)电子;
⑵ 元素的化学性质与原子结构中的______________数关系密切;
⑶ 在同一族中,各元素的原子结构呈现的规律有________________
(任写一点);
⑷ 研究表明:第二周期从3~9号元素的原子电子层数相同,核电荷数逐渐增大,
核对核外电子的引力逐渐增大,故原子半径逐渐减小。我分析第三周期从11~17
号元素原子半径变化规律是 _________________________________。
22.(3分)(C)长时间腌制的蔬菜中含有致癌物亚硝酸钠(NaNO ),它是硝酸钠
2
5(NaNO )在一定的条件下反应生成的,现有一包含有硝酸钠的亚硝酸钠样品,测得
3
其中的含氮量为28%,那么含氧量为 。
三、解答题(本大题包括2小题,第23题10分,第24题10分,满分20分)
23.(10分)(B)2008年9月份曝光的引起国人共愤的“结石宝宝”事件,与婴幼
儿服用含有三聚氰胺的奶粉有关。已知三聚氰胺为白色晶体,将它用作食品添加
剂可提高食品中蛋白质的检测值,俗称“蛋白精”, 化学式为C H N 。据此请计算
3 6 6
(1)三聚氰胺中各元素的质量比 ;
(2)三聚氰胺中氮元素的质量分数 。(写出具体的计算过程,结果精确
到0.01%)
(3)某品牌合格奶粉蛋白质含量为18%,含氮量为2.88%(假设奶粉中的含氮量
全部来自蛋白质)。每 100g 奶粉中添加 0.1g 三聚氰胺,理论上能增加
g蛋白质。(写出具体的计算过程,结果精确到0.01g)
24.(10分)(B)莽草酸(化学式:C H O )是制取抗“H1N1流感”药物“达菲”的
7 10 5
原料。
请回答:
(1)莽草酸分子中C、H、O原子个数比为 。
(2)174g莽草酸含氢元素质量为 g。
(3)对1岁以上的儿童推荐按照下列“体重—剂量表”服用“达菲”:
体重 小于等于15千克 15~23千克 23~40千克 大于40千
克
每次用量 30mg 45mg 60mg 60mg
假如患病儿童的体重是35千克,在治疗过程中,需每天服用“达菲”胶囊(每颗
胶囊含“达菲”75mg)2次,一个疗程5天,那么该患儿一个疗程共需服用
颗。
参考答案
一、单项选择题
1.A 考查地壳中元素的含量顺序,可利用谐音“洋闺女铁钙钠”(氧、硅、铝、铁
钙、钠)来记忆。
62.A 解析:本题考查的是对元素概念的理解。元素是具有相同核电荷数(即核
内质子数)的一类原子的总称,即决定元素种类的微粒是质子数。错因会诊:对元
素的概念、元素与原子间的联系与区别不明白,知识残缺乱猜而选B;在学习常见
元素的名称、符号和相对原子质量时,发现不同的元素其原子的相对原子质量不
同而误选C;因在原子中,质子数=核外电子数=核电荷数,没有想到核外电子不稳
定,在化学变化中是可变的而错选D。
3.B 解析:原子核中不一定含有中子,如氢原子的原子核内就没有中子,只有质
子,即构成原子核必不可少的粒子是质子,故A正确,B错误;在同一原子中,核电
荷数一定等于质子数或核外电子数,但不一定等于中子数,故C正确,D不正确。
错因会诊:对知识把握不准,不能确定原子的构成而错选A;没有想到有的氢原子
没有中子而漏选B;原子、离子知识相混淆,认为核外电子数得失了,没有看清该
题是关于原子的结构而错选C。
4.D
5.B 解析:本题考查根据化学式推算化合价,较易。根据的原则是:化合物中正
负化合价的代数和等于0。设NiFe O 中,Ni的化合价为x。Fe为+3价,O为-2价,
2 4
则:x+(+3)×2+(-2)×4=0, x=+2,B为正确选项,A、C、D均为错项。
6.A
7.A 解析:金属元素汉字用“钅”旁表示(汞除外),通常非金属有三种状态,
“气”字头的表示是气态非金属,如氧元素;有“氵”旁的是液态非金属,如溴
元素;有“石”字旁的表示固态非金属元素,如硫元素。
8.C
9.D
10.B 解析:①的质子数<核外电子总数,是阴离子,其原子的最外层电子数多于
4个(为6个),是非金属元素,②的质子数=核外电子总数,是原子,其最外层有
2个电子,易失去2个电子,在化合物中通常显+2价,③④的质子数>核外电子总
数,是阳离子,其原子的最外层电子数均少于4个(分别为1个、2个),是金属元
素,故B为正确选项,C、D为错项;元素的种类决定于质子数,②④的核内质子数
相同,表示同种元素,则它们表示三种不同的元素,A为错项。
11.C 解析:本题联系生活中的实际问题考查化合价的知识。Cl 为单质,其中氯
2
元素的化合价为0,故A错;B选项将化合价与离子符号相混淆,元素的化合价应
7标在元素符号的正上方(化合价为1时,不能省略。“+、一”放在数字前),离子
所带电荷应标在元素符号右上角(电荷为1时,省略。“ +、一”放在数字后);次
氯酸钠(NaClO)中,Na元素为+1价,O元素为-2价,根据化合物里元素正负化合价
代数和等于零的原则可求出氯元素为+1价。错因会诊:错选A是因为只想到氯元
素主要显-1价,没有考虑到在单质中元素的化合价为0;错选B是由于没有把离
子符号的标注与化合价相分开,二者混淆而错选;漏选C是因为氧元素在通常情
况下显-2价;错选D是由于氯元素在一般情况下显-1价,没有根据化合价代数
和为零的原则进行计算。
12.C
13.C 解析:Si N 中Si、N两种元素的质量比为28×3:14×4=3:2,A为错项;
3 4
Si N 的相对分子质量为28×3+14×4=140,D为错项;Si N 中氮元素的质量分数
3 4 3 4
为14×4/140×100%=40%,B为错项;14g氮化硅中含硅的质量为:14g×(1-40%)
=8.4g,C为正确选项。
14.D 解析:从题中信息可知,“纳米车” 能在人工操纵下运输药物分子到病
源处释放以杀死癌细胞,说明在一定条件下人可以控制分子运动。
15.A 解析:NH NO 中含氮元素而KH PO 中没有氮元素,NH NO 中氮元素的质量分
4 3 2 4 4 3
数为:,设混合物的质量为m,则氮元素的质量为28%·m,的质量:,则KH PO 的
2 4
质量分数:(m__ )m×100%=20%。
二、填空题
16.(每空1分,共8分)16.(1)原子 (2)分子、原子 (3)分子 (4)原子核、质
子 (5)分子、原子、中子 (6)质子和中子 (7)质子、电子 ⑻电子
17.(每空1分,共4分)17.(1)Na, 7 (2)2F (3)金属
18.(每空1分,共6分)18.(1)带电的原子 正电荷 负电荷 (2)阴、阳
相互 解析:这是一道看图回答题。途中有趣的卡通图画体现了该题的直观性,
也是近年来中考的方向。根据心理科学,图、表等比文字更容易让人理解和记住。
自己也可以设计这样的题目来练习一下。点拨:对于离子化合物的形成应该了解。
19. (每空1分,共3分)7 2 BA 解析:利用原子中,核电荷数=质子数=核
2
外电子数的关系,求得X与n。再据元素的常见化合价与原子的最外层电子数的
关系,A原子最外层电子数为7,易得到1个电子,A元素呈-1价,B原子最外层电
子数为2个电子,易失去2个电子,B元素呈+2价,则由此可利用交叉法,得BA 。
2
820. (每空1分,共4分)(1)2H+、2CO;(2)非金属;AlF 解析:与金属化合时形
3
成F-,说明原子的最外层电子数为7,所以为非金属元素。
21. (每空1分,最后两空各2分,共7分)⑴ 非金属 ;得 ; ⑵ 最外层电子 ;
⑶ 电子层数递增或最外层电子数相等或从上到下核电荷数增大等(只要合理均
可)⑷ 逐渐减小
解析:(1)由元素周期表可以看出,第16号元素是S,原子最外层电子数为6,大
于4,属于非金属元素,在化学反应中容易得电子而使最外层达到8电子稳定结
构;(2) 元素的化学性质与原子结构中的最外层电子数关系密切;(3)这是一个
开放性试题。在同一族中,各元素的原子结构呈现的规律有:电子层数递增、最外
层电子数相等、从上到下核电荷数增大。
22. (每空3分,共3分)22.49%
三、计算解答题
23. (共10分)(1)C︰H︰N=6︰1︰14 (3分) (2)N%=66.67% (3分)(3)奶
粉中蛋白质的质量=100×18%=18g,奶粉中N的质量=100×2.88%=2.88g
蛋白质的含氮量=2.88/18×100%=16%
蛋白质的质量=(0.1×66.67%)÷16%==0.42 g (4分)
解析:(1)C H N 中C︰H︰N=12×3:1×6:14×6=6︰1︰14;(2)C H N 的相对分子
3 6 6 3 6 6
146
质量为:12×3+1×6+14×6=126,C H N 中N%= 100% 66.67%;(3)100g
3 6 6
126
奶粉中蛋白质的质量=100g×18%=18g,含N的质量=100g×2.88%=2.88g,则蛋
白质的含氮量=2.88g/18g×100%=16% ,0.1g三聚氰胺中的含氮的质量为:
0.1g×66.67%=0.0667g,则每100g奶粉中添加0.1g三聚氰胺,理论上能增加蛋
白质的质量为:0.0667g÷16%==0.42 g 。
24. (共10分)(1) 7︰10︰5 (3分) (2) l0 (3分)(3) 8 (4分) 解析:本
题主要考查有关化学式的计算。依据莽草酸的化学式(C H O )可直观得出莽草酸
7 10 5
分子中C、H、O原子个数比为7:10:5;174g莽草酸含氢元素质量为:174g×
110
=10g;若患病儿童的体重是35千克,按照表中要求,他每次
127110165
服用“达菲”的量是60mg,则该患儿一个疗程服用“达菲”的量是
5×2×60mg=600 mg,需服用“达菲”胶囊的颗数为:600 mg÷75mg/颗=8颗。
910