文档内容
第 24 讲 铝
知识导航
知识精讲
一、铝的结构、存在、物理性质及用途
1.结构:铝的原子结构示意图为____________。
2. 存在:铝是地壳中含量最多的金属元素,自然界中的铝全部以___________存在。
3. 物理性质:_______色有金属光泽的固体,有良好的延展性、导电性和传热性等,密度较小,质地柔软。
4. 用途:① 纯铝用作导线;②铝合金用于制造汽车、飞机、生活用品等。
【答案】 化合态 银白
二、铝的化学性质
1.铝与氧气的反应
① 常温:铝与空气中的氧气反应,化学方程式为___________________________。表面生成一层______的
氧化铝薄膜,对内部金属起着_________作用,所以铝在空气中稳定存在,具有很强的抗腐蚀性能。
② 点 燃 : 铝 在 氧 气 中 点 燃 , 放 出 大 量 的 热 和 耀 眼 的 白 光 , 化 学 方 程 式 为
_____________________________。
【答案】(1)致密 保护 4Al+3O===2AlO (2) 4Al + 3O ===== 2Al O
2 2 3 2 2 3
2. 铝与(非氧化性)酸的反应实验操作
实验现象 铝片_________,有_________冒出,将点燃的木条放在试管口_________
实验原理
【答案】逐渐溶解 气泡 有爆鸣声
2Al+6HCl===2AlCl +3H↑ Al+6H+===2Al3++3H↑
3 2 2
3. 铝与碱的反应
实验操作
实验现象 铝片_________,有_________冒出,将点燃的木条放在试管口_________
实验原理
【答案】逐渐溶解 气泡 有爆鸣声
2Al+2HO+2NaOH===2NaAlO+3H↑ 2Al+2OH-+2HO===2AlO+3H↑
2 2 2 2 2
三、氧化铝
1.物理性质
白色固体,难溶于水,硬度大,熔点很高,是优良耐火材料。
2. 化学性质
氧化铝既能与 酸反应生成盐和水,又能与碱反应生成盐和水,这类氧化物叫做两性氧化物。
①与酸反应:_________________________________________________________
②与碱反应:_________________________________________________________
3. 用途
制造耐火、耐高温器材、工业冶炼铝、可以制作各种宝石。
【答案】Al O+6HCl===2AlCl +3HO Al O+6H+===2Al3++3HO
2 3 3 2 2 3 2
Al O+2NaOH===2NaAlO+HO Al O+2OH- ===2AlO-+HO
2 3 2 2 2 3 2 2
对点训练
题型一:铝的应用
【变1-2】(2020·湖南·娄底市春元中学高一月考) 下列用途或说法主要体现铝的物理性质的是
①家用铝锅 ②铝具有还原性 ③制导线 ④铝锅不能长期贮存碱液 ⑤制包装铝箔 ⑥做防锈油漆 ⑦
制成合金作制造飞机的材料
A.①②③④ B.②⑤⑥⑦C.①③⑤⑦ D.②④⑤⑥
【答案】C
【详解】
①铝可用于制作家用铝锅利用了铝的导热性,利用了物理性质;
②铝具有还原性,还原性是化学性质;
③制导线利用了铝的导电性,导电性为物理性质;
④铝锅不能长期贮存碱液是因为铝能与碱溶液反应,该性质为化学性质;
⑤制包装铝箔利用了铝的延展性,利用了铝的物理性质;
⑥做防锈油漆是因为铝易与空气中的氧气反应产生致密的氧化铝薄膜,体现了化学性质;
⑦制成合金作制造飞机的材料是铝合金密度小、硬度大,利用了物理性质;
综上所述,①③⑤⑦符合题意;
答案选C。
题型二:铝的性质
【变2-1】(2021·云南丽江·高一期末)下列关于铝的说 法中,正确的是
A.铝的化学性质不活泼 B.铝很活泼
C.自然界中存在单质铝 D.铝不与碱反应
【答案】B
【详解】
A.在金属活动顺序表中铝在氢之前,性质活泼,在化学反应中容易失去电子,表现还原性,故A错误;
B.铝原子最外层电子数较少,容易失去电子,具有较强的还原性,属于活泼金属,故B正确;
C.因为铝的化学性质活泼,在自然界中以化合态形式存在,故C错误;
D.铝可以与强碱反应,如和氢氧化钠溶液反应生成偏铝酸钠和氢气,故D错误;
故选:B。
【变3】(2021·全国·高一专题练习)有关Al与NaOH溶液反应的说法中, 正确的是
A.Al是还原剂,NaOH及HO均是氧化剂
2
B.还原产物是H,且由HO还原所得的H 与NaOH还原所得的H 物质的量之比为2 : 1
2 2 2 2
C.反应中1molAl失去 mol电子
D.此反应中,只有水是氧化剂,NaOH既不是氧化剂也不是还原剂
【答案】D
【分析】
铝与氢氧化钠溶液发生反应的实质为2Al+6HO=2Al(OH) +3H↑、NaOH+Al(OH) =NaAlO+2HO,据此
2 3 2 3 2 2
回答;
【详解】
A.根据反应实质,Al的化合价升高,Al作还原剂,HO作氧化剂,NaOH既不是氧化剂也不是还原剂,
2故A错误;
B.根据铝与氢氧化钠溶液反应实质,NaOH既不是氧化剂也不是还原剂,氢气只来自于HO,故B错误;
2
C.反应Al的化合价由0价→+3价,因此1molAl参与反应失去3mol电子,故C错误;
D.根据上述分析,水是氧化剂,NaOH既不是氧化剂也不是还原剂,故D正确;
答案选D。
题型三:铝热反应
【例5】(2021·安徽·蒙城第一中学高一期末)铝热反应常用于焊接钢轨 ,其焊接速度快,设备简易,适
用于野外作业。实验室采用如图装置进行铝热反应,下列说法错误的是
A.该反应的实质是金属的置换反应
B.该反应是放热反应,Fe O 和铝粉的混合物被称为铝热剂
2 3
C.铝单质很活泼,通常表面附着层致密的氧化铝薄膜
D.铝热反应只能用于冶炼铁、锰、铬、镁等熔点较高的金属
【答案】D
【详解】
A.该反应为2Al+Fe O Al O+2Fe,反应特点是单质与化合物反应产生新的单质和新的化合物,故实
2 3 2 3
质上是金属的置换反应,A正确;
B.作为铝热剂重要组成的金属氧化物,铝热剂应为Al和过渡元素的氧化物所形成的混合物,B正确;
C.铝单质很活泼,容易被空气中的氧气氧化为氧化铝,氧化铝非常致密,对内层金属起保护作用,因此
在金属铝表面通常附着一层致密的氧化铝薄膜,C正确;
D.铝热反应是金属铝和金属氧化物之间的置换反应,反应放出大量的热,使产生的金属以液态形式存在。
利用铝热反应可以冶炼还原性比Al弱,但是熔点较高的金属,如金属铁、锰、铬等金属,但镁还原性比铝
强,不能用铝热反应制取,D错误;
故合理选项是D。
题型四:铝的相关计算
【变6】(2021·全国·高二课时练习)称取两份铝粉,第一份加足量的浓氢氧化钠溶液,第二份加足量的盐
酸,充分反应后产生了等体积的气体(同温同压),则两份铝粉的质量比是A.1:1 B.1:3 C.3:1 D.1:2
【答案】A
【详解】
称取两份铝粉,第一份加足量的浓氢氧化钠溶液,第二份加足量的盐酸,充分反应后产生了等体积的气体
(同温同压),根据2Al~2NaOH~3H 与2Al~6HCl~3H,说明两份铝粉物质的量等及质量相等,质量比
2 2
是1:1,故A符合题意。
综上所述,答案为A。
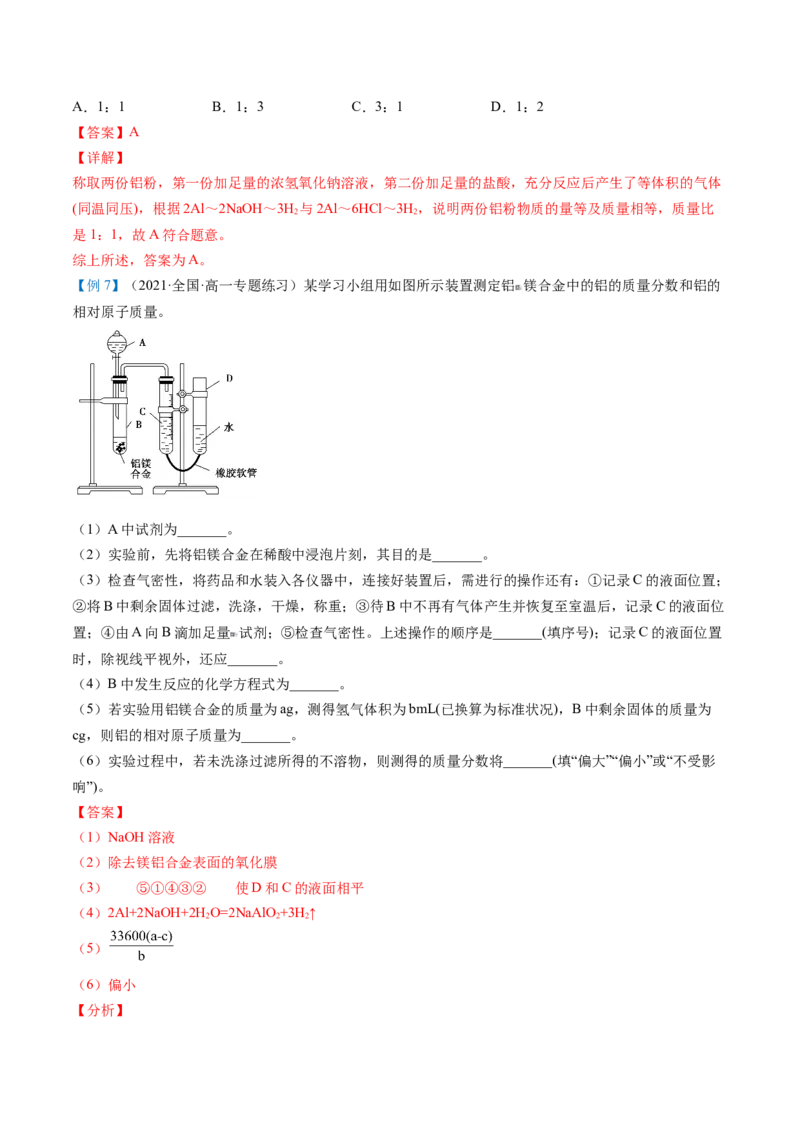
【例7】(2021·全国·高一专题练习)某学习小组用如图所示装置测定铝 镁合金中的铝的质量分数和铝的
相对原子质量。
(1)A中试剂为_______。
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是_______。
(3)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:①记录C的液面位置;
②将B中剩余固体过滤,洗涤,干燥,称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位
置;④由A向B滴加足量 试剂;⑤检查气密性。上述操作的顺序是_______(填序号);记录C的液面位置
时,除视线平视外,还应_______。
(4)B中发生反应的化学方程式为_______。
(5)若实验用铝镁合金的质量为ag,测得氢气体积为bmL(已换算为标准状况),B中剩余固体的质量为
cg,则铝的相对原子质量为_______。
(6)实验过程中,若未洗涤过滤所得的不溶物,则测得的质量分数将_______(填“偏大”“偏小”或“不受影
响”)。
【答案】
(1)NaOH溶液
(2)除去镁铝合金表面的氧化膜
(3) ⑤①④③② 使D和C的液面相平
(4)2Al+2NaOH+2H O=2NaAlO +3H ↑
2 2 2
(5)
(6)偏小
【分析】(1)
观察实验装置图可知是用量气法完成实验目的,故A中应盛NaOH溶液,在B中发生
2Al+2NaOH+2H O=2NaAlO +3H ↑的反应,故答案:NaOH溶液。
2 2 2
(2)
铝镁属于活泼金属,在空气中易被氧气氧化生成一层氧化膜,所以实验前,先将铝镁合金在稀酸中浸泡片
刻,除去铝镁合金表面的氧化膜,故答案:除去镁铝合金表面的氧化膜。
(3)
要完成该实验应先检查气密性,然后在记录C的液面位置,再由A向B滴加足量试剂,待B中不再有气体
产生并恢复至室温后,记录C的液面位置,在将将B中剩余固体过滤,洗涤,干燥,称重,所以正确顺序
应为⑤①④③②;为使C中气体的压强相等,还应使D与C液面相平,故答案:⑤①④③②;使D和C的
液面相平。
(4)
观察实验装置图可知是用量气法完成实验目的,在A中应盛NaOH溶液,在B中发生
2Al+2NaOH+2H O=2NaAlO +3H ↑的反应,故答案:2Al+2NaOH+2H O=2NaAlO +3H ↑。
2 2 2 2 2 2
(5)
据铝镁合金的质量为ag,测得氢气体积为bmL(已换算为标准状况),B中剩余固体为镁,其质量为cg,根
据2 mol Al~3 mol H 得铝的相对原子质量M(Al)= ,故答案: 。
2
(6)
据w(Al)= ×100%的计算公式可知,未洗涤不溶物可能会附着一些杂质,导致C的质量增加, Al的
质量分数偏小,故答案:偏小。
提分特训
【题1】(2021·云南高一期末)下列关于铝的 说法中,正确的是( )
A.铝的化学性质不活泼 B.铝很活泼
C.自然界中存在单质铝 D.铝不与碱反应
【答案】B
【解析】A项,在金属活动顺序表中铝在氢之前,性质活泼,在化学反应中容易失去电子,表现还原性,
故A错误;B项,铝原子最外层电子数较少,容易失去电子,具有较强的还原性,属于活泼金属,故B正
确;C项,因为铝的化学性质活泼,在自然界中以化合态形式存在,故C错误;D项,铝可以与强碱反应,
如和氢氧化钠溶液反应生成偏铝酸钠和氢气,故D错误;故选B。
【题2】(2021·陕西·蒲城县教学研究室高三期中)我国铝材工业水平处于世界领先行列。下列说法不正确
的是A.铝制餐具不宜长时间盛放酸性、碱性或咸的食物
B.常温下,铝制品耐腐蚀是因为铝不活泼
C.铝合金密度小、强度高,广泛应用于航空领域
D.工业上常用NaOH溶液去除铝表面的氧化膜
【答案】B
【详解】
A.酸、碱、盐等可直接侵蚀铝的氧化物且铝与酸、碱都能发生反应,所以铝制餐具不宜长时间盛放酸性、
碱性或咸的食物,故A正确;
B.常温下,铝制品耐腐蚀是因为铝表面被氧化后形成一层致密的氧化物薄膜,阻止金属继续被腐蚀,而
不是因为铝不活泼,故B错误;
C.合金的硬度大于其成分金属,铝合金密度小、强度高,广泛应用于航空领域,故C正确;
D.氧化铝为两性氧化物,能够与NaOH反应生成偏铝酸钠和水,工业上常用NaOH溶液去除铝表面的氧
化膜,故D正确;
答案选B。
【题3】(2020·河南·临颍县南街高级中学高一月考)铝箔在空 气中加热,金属熔化而不滴落的原因是(
)
A.熔化的金属铝非常黏稠 B.铝的密度小,所受重力也小
C.大部分铝已经被氧化 D.氧化膜的熔点比铝高,兜住了熔化的铝
【答案】D
【详解】
铝的失电子能力较强,容易被空气中的氧气氧化,在铝的表面形成一层致密的氧化薄膜,而氧化铝的熔点
远远高于金属铝,故铝箔在空气中加热,金属熔化而不滴落的,综上所述,答案为D。
【题4】(2021·新疆乌市八中高一月考)有关Al与NaOH溶液反应的说法中,正确的是( )
A.Al是还原剂,NaOH及HO均是氧化剂
2
B.还原产物是H,且由HO还原所得的H 与NaOH还原所得的H 物质的量之比为2 : 1
2 2 2 2
C.反应中1molAl失去 mol电子
D.此反应中,只有水是氧化剂,NaOH既不是氧化剂也不是还原剂
【答案】D
【解析】铝与氢氧化钠溶液发生反应的实质为2Al+6HO=2Al(OH) +3H↑、NaOH+Al(OH) =NaAlO+
2 3 2 3 2
2HO。A项,根据反应实质,Al的化合价升高,Al作还原剂,HO作氧化剂,NaOH既不是氧化剂也不是
2 2
还原剂,故A错误;B项,根据铝与氢氧化钠溶液反应实质,NaOH既不是氧化剂也不是还原剂,氢气只
来自于HO,故B错误;C项,反应Al的化合价由0价→+3价,因此1molAl参与反应失去3mol电子,
2
故C错误;D项,根据上述分析,水是氧化剂,NaOH既不是氧化剂也不是还原剂,故D正确;故选D。
【题5】(2021·浙江·高一月考)下列物质的用途错误的是
A.镁铝合金:制作门窗 B.过氧化钠:供氧剂
C.四氧化三铁:红色油漆 D.硫酸亚铁:食品抗氧化剂【答案】C
【详解】
A.镁铝合金硬度大,密度小,适合做门框,故A正确;
B.过氧化钠与水反应生成氧气,即2NaO+2H O=4NaOH+O ↑,适合作供氧剂,故B正确;
2 2 2 2
C.四氧化三铁为黑色物质,三氧化二铁为红棕色物质,可以制造红色油漆,故C错误;
D.硫酸亚铁中亚铁离子具有还原性,可以作为食品抗氧化剂,故D正确;
答案为C。
【题6】(2021·甘肃·金昌市第二中学高一期中)下列离子方程式书写正确的是
A.钠和冷水反应:Na+2HO=Na++2OH+H↑
2 2
B.氯气通入烧碱溶液:Cl+2OH-=Cl-+ClO-+H O
2 2
C.Al O 粉末溶于NaOH溶液中:Al O+OH-=AlO +H O
2 3 2 3 2
D.FeCl 溶液通入足量的Cl 反应:Fe2++Cl=Fe3++2Cl-
2 2 2
【答案】B
【详解】
A.钠与水反应生成氢氧化钠和氢气,反应的离子方程式是2Na+2HO=2Na++2OH-+H↑,故A错误;
2 2
B.Cl 通入NaOH溶液中生成氯化钠、次氯酸钠、水,反应的离子方程式是Cl+2OH-=Cl-+ClO-+HO,
2 2 2
故B正确;
C.Al O 溶于NaOH溶液生成偏铝酸钠和水,反应的离子方程式是Al O+2OH-=2AlO +HO,故C错误;
2 3 2 3 2
D.FeCl 溶液通入足量的Cl 反应,Fe2+被氧化为Fe3+,反应的离子方程式是2Fe2++Cl=2Fe3++2Cl-,故D
2 2 2
错误;
选B。
【题7】(2020·黑龙江·伊美区第二中学高一期末)已知A为淡黄色固体,T、R为两种常见的用途很广的
金属单质,D是具有磁性的黑色晶体,C是无色无味的气体, H是白色沉淀,且在潮湿空气中迅速变为灰
绿色,最终变为红褐色固体。
(1)写出下列物质的化学式:A:_______,D:_______,R:_______。
(2)按要求写下列反应方程式:
①A和水反应生成B、C的化学方程式_______;
②B和R反应生成N的离子方程式_______;③D与盐酸反应的离子方程式_______。
(3)检验气体C的方法_______
【答案】NaO Fe O Al 2NaO+2H O=4NaOH+O ↑
2 2 3 4 2 2 2 2
2Al+2OH-+2H O=2 +3H ↑ Fe O+8H+=Fe2++2Fe3++4H O 用带火星的木条伸入试管口,若带
2 2 3 4 2
火星的木条复燃,说明有氧气生成
【分析】
A为淡黄色固体,A能与水反应,推出A为NaO,C为无色无味的气体,则C为O,B为NaOH,D是具
2 2 2
有磁性的黑色晶体,推出D为Fe O,T为金属单质,推出T为Fe,H是白色沉淀,且在潮湿空气中迅速
3 4
变为灰绿色,最终变为红褐色固体,推出H为Fe(OH) ,M为Fe(OH) ,氢氧化铁与盐酸反应生成FeCl 和
2 3 3
HO,即W为FeCl ,R为金属,且能与NaOH溶液发生反应,推出R为Al,Q为Al O,N为NaAlO ,E
2 3 2 3 2
为FeCl ,据此分析;
2
【详解】
(1)根据上述分析,A为NaO,D为Fe O,R为Al;故答案为NaO;Fe O;Al;
2 2 3 4 2 2 3 4
(2)①NaO 与水反应的化学方程式为2NaO+2HO=4NaOH+O↑;故答案为2NaO+2HO=4NaOH+
2 2 2 2 2 2 2 2 2
O↑;
2
②Al与NaOH溶液反应的离子方程式为2Al+2OH-+2HO=2 +3H↑;故答案为2Al+2OH-+
2 2
2HO=2 +3H↑;
2 2
③D为Fe O,有 的+2价Fe, 的+3价Fe,与盐酸反应的离子方程式为Fe O+8H+=Fe2++2Fe3++4H O;
3 4 3 4 2
故答案为Fe O+8H+=Fe2++2Fe3++4H O;
3 4 2
(3)气体C为氧气,检验氧气的方法是用带火星的木条伸入试管口,若带火星的木条复燃,说明有氧气生成;
故答案为用带火星的木条伸入试管口,若带火星的木条复燃,说明有氧气生成。
【题8】(2021·全国·高一专题练习)如图为铝热反应的实验装置,请回答下列问题:
(1)该实验装置中还缺___,在试剂使用正确且符合要求的情况下引发铝热反应的操作为___,写出铝热反应
的化学方程式:___。
(2)若将氧化铁换成氧化镁,该反应___(填“能”或“不能”)发生,理由是___。
(3)若将所得产品置于足量的NaOH溶液中, 可能看到的现象是__,写出铝热反应的一种主要用途:___。
(4)假设铝足量且反应充分,设计一种实验方案,证明本实验中有单质铁生成:___。【答案】镁条 在混合物中间插一根用砂纸打磨过的镁条,然后点燃镁条 Fe O+2Al Al O+2Fe
2 3 2 3
不能 镁比铝活泼,铝不能置换出镁 部分固体溶解,有气泡产生 焊接钢轨或冶炼某些熔点高的
金属 取适量反应后的固体混合物,先用NaOH溶液除去铝,再加入稀硫酸,有气泡冒出,说明有铁生
成;或用磁铁靠近固体,有固体可被磁铁吸引,说明有铁生成
【详解】
(1)观察装置图知,缺少引燃剂镁条,故应在混合物中插入适当长度用砂纸打磨过的镁条,点燃镁条可引发
铝热反应,铝热反应的化学方程式:Fe O+2Al Al O+2Fe;
2 3 2 3
(2)Mg比Al活泼,Al不能从MgO中置换出Mg;
(3)若铝过量,剩余的铝及反应生成的氧化铝与NaOH溶液反应,可看到部分固体溶解,且溶液中有气泡产
生;
(4)可取适量反应后的固体混合物,先用NaOH溶液除去铝,再加入盐酸或稀硫酸,根据有气泡冒出确定有
铁生成;也可用磁铁靠近固体,根据固体可被磁铁吸引判断有铁生成。
提分作业
【练1】Al在空气中能够稳定存在的原因是( )
A.Al的活泼性差 B.Al表面有致密的氧化膜
C.Al与氧气不反应 D.Al的还原性差
【答案】B
【解析】A项,铝是一种比较活泼的金属,A错误;B项,铝能与空气中的氧气迅速反应,在表面形成一
层致密的氧化物保护薄膜,这是铝在空气中能稳定存在的主要原因,B正确;C项,常温下,铝在空气中
易与氧气反应生成氧化铝,C错误;D项,铝最外层有三个电子,易失电子,还原性很强,D错误;故选
B。
【练2】下列关于铝和铝合金的叙述错误的是( )
A.铝是地壳里含量最多的金属元素 B.铝的金属性比钠、镁都弱
C.铝能与强碱溶液反应放出氢气 D.硬铝比纯铝的硬度低
【答案】D
【解析】A项,铝是地壳里含量最多的金属元素,A正确;B项,铝的金属性比钠、镁都弱,B正确;C项,
铝能与强碱溶液反应放出氢气,同时还生成偏铝酸钠,C正确;D项,硬铝属于合金,比纯铝的硬度大,
D错误,故选D。
【练3】(2021·全国高一专题练习)有关铝制餐具下 列使用较为合理的是( )A.盛放烧碱 B.烧煮开水
C.用金属丝擦洗表面的污垢 D.用碱水洗涤
【答案】B
【解析】A项,铝及其表面的氧化膜(氧化铝)都可以与NaOH反应,所以铝制仪器不能用于盛放烧碱 ,
故A错误;B项,铝及其表面的氧化膜(氧化铝)与热水很难反应,所以可用铝制仪器烧煮开水,故B正确;
C项,铝制品表面有一层致密的氧化薄膜,可以起到保护作用,若用金属丝擦表面的污垢,会破坏保护膜,
故C错误;D项,铝及其表面的氧化膜(氧化铝)都可以与碱性溶液反应,所以铝制仪器不能用碱液洗涤污
垢,故D错误。故选B。
【练4】(2020·全国·高一课时练习)下列关于金属铝及氧化铝的说法不正确的是
A.铝是地壳中含量最多的元素
B.铝在自然界中通常以化合态形式存在
C.金属铝在空气中有良好的抗腐蚀性
D.氧化铝是一种高硬度﹑高熔沸点的化合物,红宝石、蓝宝石的主要成分均是氧化铝
【答案】A
【详解】
A.铝是地壳中含量最多的金属元素,故A错误;
B.铝的化学性质活泼,在自然界中通常以化合态形式存在,故B正确;
C.常温下,金属铝能被空气中的氧气氧化,表面生成一层致密的氧化铝薄膜,这层薄膜能阻止内部金属
继续与 生反应,故金属铝在空气中有良好的抗腐蚀性,故C正确;
D.氧化铝是一种高硬度、高熔沸点的化合物,红宝石、蓝宝石的主要成分均是氧化铝,故D正确。
故选A。
【练5】(2021·浙江·镇海中学高一期末)关于铁铝及其合金的说法不正确的是
A.生铁的含碳量为2%~4.3%
B.稀土金属可以用于生产合金
C.铝是一种活泼金属,铝表面的保护膜和铝均能与盐酸发生反应
D.向装有氢氧化钠溶液的试管中放入未打磨的铝片,一直观察不到气泡
【答案】D
【详解】
A.生铁和钢均属于铁碳合金,生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%,A正确;
B.稀土金属添加到合金中,可以改善合金的物理或化学性能,因此稀土金属在冶金工业上应用广泛,可
以用于生产合金,B正确;
C.Al和Al O 均为两性物质,都能与盐酸反应,C正确;
2 3
D.当铝表面的氧化膜被NaOH溶液溶解后,里面的铝与NaOH溶液反应能产生氢气,D错误;
故答案选D。
【练6】(2022·浙江高三专题练习)下列关于铝单质的叙述中,正确的是( )
A.不能用铝制的器皿来盛放酸梅汤或碱水是因为铝会和酸或碱反应B.铝制品在空气中有很强的抗腐蚀性是因为铝的化学性质很稳定
C.铝和NaOH溶液反应:Al+2OH-+2HO=[Al(OH) ]-+H↑
2 4 2
D.用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝会滴落下来,是因为
金属铝的熔点较低
【答案】A
【解析】A项,无论是铝还是其氧化物都能与酸或碱反应,A项正确;B项,铝制品在空气,其表面形成
致密的氧化膜,铝的化学性质不稳定,B项错误;C项,电荷、电子均不守恒,正确的离子方程式为2Al+
2OH-+6HO===2[Al(OH) ]-+3H↑,C项错误;D项,打磨后的铝箔在酒精灯上灼烧表面生成Al O,高熔
2 4 2 2 3
点的Al O 兜住了熔融的液态铝,不会滴落,D项错误;故选A。
2 3
【练7】(2021·云南·玉龙纳西族自治县田家炳民族中学高一月考)下列离子方程式中正确的是
A.向氯化亚铁溶液中通入氯气:2Fe2++Cl=2Fe3++2Cl-
2
B.Na与水反应:2Na+HO=2Na++OH-+H ↑
2 2
C.氧化亚铁与稀盐酸:FeO+2H+=Fe3++H O
2
D.氧化铝与氢氧化钠:Al O+6OH-=2Al(OH) +3H O
2 3 3 2
【答案】A
【详解】
A.Fe2+与Cl 反应生成Fe3+和Cl-,离子方程式为2Fe2++Cl=2Fe3++2Cl-,A正确;
2 2
B.Na与HO反应生成NaOH和H,离子方程式为2Na+2HO=2Na++2OH-+H ↑,B错误;
2 2 2 2
C.FeO与HCl反应生成Fe2+和HO,离子方程式为FeO+2H+=Fe2++H O,C错误;
2 2
D.Al O 与NaOH反应生成NaAlO 和HO,离子方程式为Al O+2OH-=2 +HO,D错误;
2 3 2 2 2 3 2
故选A。
【练8】(2020·湖南·娄底市春元中学高一月考)(1)选择填空:将铝 的用途与性质搭配起来(每个选项只选
用一次)。
A.质轻 B.延展性好 C.易传热 D.易导电
①太阳能热水器:________;②飞机:________;③电缆:________;④:铝箔:________。
(2)佛山是有色金属之乡,其中铝合金材料的产量约占全国的一半。铝合金材料属于________(填“纯净物”
“混合物”或“单质”)。
【答案】C A D B 混合物
【详解】
(1)①太阳能热水器利用了铝易传热的性质,选C;
②铝及其合金密度小,即质氢,可用作飞机的材料,选A;
③铝有良好的导电性,易导电,可用来制作电缆,选D;
④铝有良好的延长性,易制成薄片,如铝箔,选B;
(2)合金是由金属和金属或非金属在一定温度下熔合而成具有金属特性的混合物,因此铝合金材料也属于混
合物。关注更新免费领取,淘宝唯一每月更新店铺:知二教育