文档内容
广东省中山市 2013 年初中化学竞赛试题
考试时间: 9:30----11:30
竞赛时间2小时。迟到超过半小时者不能进考场。开始考试后1小时内不得离场。时间到,把试卷(背面
朝上)放在桌面上,立即起立撤离考场。
试卷装订成册,不得拆散。所有解答(包括选择题)必须写在答题卡指定的方框内,不得用铅笔填写。
姓名、考生号和所属学校必须写在答题卡首页左侧指定位置,写在其他地方者按废卷论处。
可能用到的原子量
Na Mg Ca Ba Cu N H C S O
23 24 40 137 64 14 1 12 32 16
一、选择题(15题×2分=30分,每题有1到2个正确选项,选对得2分,错选得0分,漏选得1分)
1、18世纪时,通过实验得出空气是由氮气和氧气组成的结论的科学家是
A.瑞典化学家舍勒 B.英国化学家普利斯特里
C.法国化学家拉瓦锡 D.意大利科学家阿伏伽德罗
2、某新产品磨牙器能有效帮助去除牙齿表面的牙垢,磨牙器磨头采用50%橡胶与50%的金刚砂(主要成
分为碳化硅)特制而成。已知碳化硅中碳元素显-4价,硅元素显+4价,则碳化硅的化学式为
A.SiC B.Si C C.Si C D.SiC
2 3 3 2 2
3、实验表明,不能用块状大理石与稀硫酸制取CO 气体,而能用大理石粉末与稀硫酸制取CO 气体。由此
2 2
得出的合理结论是
A.能发生反应的物质之间是否发生反应,与反应条件有关
B.反应物之间接触面积越大,越有利于反应的进行
C.块状大理石与大理石粉末的化学性质不同
D.块状大理石与大理石粉末中各元素原子间的结合状况不同
4、已知:NaHCO + HCl = NaCl + H O + CO ↑。某种混合气体中可能含有N、HCl、 CO,将混合气体
3 2 2 2
依次通过NaHCO 溶液和灼热的CuO,气体体积无变化但是有红色物质生成;再通过NaOH溶液,气
3
体体积明显减小;将燃着的木条伸入装有剩余气体的集气瓶中,木条熄灭(假设每步反应都是完全的),
则下列说法中正确的是
A.一定有CO和HCl,肯定无N B.一定有CO和N,可能有HCl
2 2
C.一定有CO和HCl,可能有N D.一定有CO和N,肯定无HCl
2 2
5、氯气和氧气都是活泼的非金属单质,在一定条件下它们都能跟甲烷反应。已知O 与CH 充分反应后
2 4
的生成物是CO 和HO,以此类推,Cl 和CH 充分反应后的生成物是
2 2 2 4
A.CCl 和HCl B.CCl 和Cl
4 4 2
C.CHCl 和H D.C和HCl
2 2 2
6、已知NaHS、MgSO 和NaHSO 由组成的混合物中硫元素的质量分数为a%,则氧元素的质量分数为
4 3
A.1.75a% B.1.25a% C.1-1.75a% D.无法计算
7、科学家用单个分子制成了“纳米车”,它能在人工操纵下运输药物分子到病源处释放以杀死癌细胞。下列
有关“纳米车”的说法正确的是
A.“纳米车”的研制成功说明分子要在人为外力作用下才能运动
B.“纳米车”分子不是由原子构成的
C.“纳米车”运输药物分子的过程是肉眼不能直接看见的
D.“纳米车”研制成功说明在一定条件下人可以控制分子运动
8、往装有25mL盐酸的锥形瓶中逐滴加入NaOH溶液〔用V (NaOH)代表加入NaOH溶液的体积〕,在表
示此变化过程的下列图像中,合理的是
19、20世纪70年代末,由于高压技术的发展,一些实验室让氢气在 -268.8oC 、1.013×107万帕下,变成能导
电的固态“金属氢”,关于氢的下列说法中错误的是
A.氢是地壳中含量最高的元素 B.同一条件下,氢气是密度最小的气体
C.氢是无污染的新型能源 D.气态氢不能导电,故能导电的固态氢的气化过程属于化学变化
10、下列“家庭小实验”不能达到预期目的的是
A.用柠檬酸、果汁、白糖、水、小苏打等制汽水
B.用空塑料瓶、小卵石、石英沙、活性炭、膨松棉等制作简易净水器
C.向洗净的碎鸡蛋壳中加入食盐水可制二氧化碳
D.用酒精浸泡捣烂的某些植物的花瓣可制酸碱指示剂
11、要除去下列物质中混有的少量杂质(括号内为杂质),所用的试剂和操作都正确的是
A.CaCl 固体(CaCO)---加入足量的稀盐酸、过滤、洗涤、干燥
2 3
B.NaCl固体(KCO)---加入足量的稀盐酸,蒸发、结晶
2 3
C.Fe粉(Al)---加入足量盐酸,蒸发、结晶
D.MnO 固体中(KCl)---加入足量水,过滤、洗涤、干燥
2
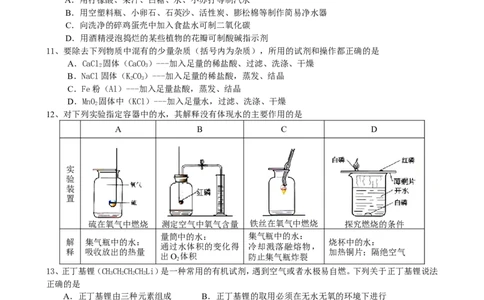
12、对下列实验指定容器中的水,其解释没有体现水的主要作用的是
A B C D
实
验
装
置
硫在氧气中燃烧 测定空气中氧气含量 铁丝在氧气中燃烧 探究燃烧的条件
量筒中的水: 集气瓶中的水:
解 集气瓶中的水: 烧杯中的水:
通过水体积的变化得 冷却溅落融熔物,
释 吸收放出的热量 加热铜片;隔绝空气
出O 体积 防止集气瓶炸裂
2
13、正丁基锂(CHCHCHCHLi)是一种常用的有机试剂,遇到空气或者水极易自燃。下列关于正丁基锂说法
3 2 2 2
正确的是
A.正丁基锂由三种元素组成 B.正丁基锂的取用必须在无水无氧的环境下进行
C.正丁基锂着火时可以用水扑灭 D.正丁基锂可以存放很长时间不会变质
14、根据下表中pH的数据判断,下列说法正确的是
物质 盐酸 硫酸铜溶液 氯化钠溶液 水 碳酸钠溶液 氢氧化钠溶液
pH <7 <7 =7 =7 >7 >7
A.pH<7的溶液一定是酸溶液 B. 盐溶液可能显酸性、碱性或中性
C.pH=7的一定是水 D.pH>7的溶液一定是碱溶液
15、对下列各主题知识的整理完全正确的是
2二、填空题(39分)
16、(4分)中山市倡导“135”出行,即1公里以内步行,3公里以内骑自行车,5公里乘坐公共交通工具,提
倡“低碳城市”、“绿色出行”。回答下列问题:
(1)“低碳城市”的建设减少了 (填化学式)气体的排放,能减缓气候变暖的速率。
(2)法国化学家PaulSabatier采用“组合转化”技术使CO 和H 在催化剂作用下生成CH 和HO。试写出
2 2 4 2
该反应的化学方程式 。
(3)请你写出一种日常生活中符合“低碳经济”理念的做法: 。
17、(4分)铁元素在化合物中常显+2、+3价,FeO 按照氧化物的形式可表示为FeO•FeO;铅元素常见化合
3 4 2 3
价为+2、+4价。
(1)试对Pb O 用上述形式表示组成,其氧化物的形式应为( )
3 4
A.PbO•Pb
2
O
3
B.2PbO•PbO
2
C.Pb•2PbO
2
D.Pb(PbO
2
)
2
(2)根据FeO 氧化物的形式可表示为FeO•FeO,试写出FeO 与盐酸发生反应的化学方程式
3 4 2 3 3 4
____________________________________________________________________________________
18、(7分)汽车给人们生活带来巨大便利的同时也带来了严重的空气污染;汽车发动机是将空气与汽油(设
汽油主要成分为:C H )以一定的比例混合成良好的混合气,被吸入汽缸,经压缩后由高压放电点火燃烧而
8 18
产生热能,高温高压的气体作用于活塞顶部,推动活塞作往复运动,从而产生动力,发动机再将燃烧后的废
气排出;经过研究发现,汽车尾气中含有NO、CO等有害气体。试着回答下列问题:
(1) 尾气中的NO是在发动机中高压放电或者高温的时候经过化合反应产生,试写出该反应的方程式:
_______________________________________________________
CO是由汽油不完全燃烧产生的,试写出该反应可能的方程式:__________________________________
(2)汽车尾气中的CO在四氧化三钴(Co O)纳米棒的催化作用下,低温即与O 反应生成CO.下列关于
3 4 2 2
该反应的说法中,不正确的是( )
A.反应类型为化合反应 B.可降低汽车尾气对大气的污染
C.反应前后Co O 质量改变 D.反应前后碳元素的化合价改变
3 4
(3)汽车尾气中的NO可以在催化剂的作用下,使CO与NO发生化学反应,生成一种单质和一种化合物,其
中单质为组成大气最多的一种成分,试写出该反应的化学方程式:________________________________
19、(4分)有机物的命名与它的组成相关(如下表所示),
则C H 的名称为 ;丁烷的化学式为 。
3 8
名称 甲烷 乙烷 丁烷 戊烷
化学式 CH C H C H C H
4 2 6 3 8 5 12
20、(4分)某种炸药的化学式为C NO ,是迄今为止最烈性的非核爆炸品之一,爆炸生成两种非常稳
8 8 16
定的气体。
(1)该炸药C、N、O三种元素质量之比为: 。
(2)写出它的爆炸反应方程式: 。
21、(6分)侯德榜是在中国化学工业史上一位杰出的科学家,他为祖国的化学工业事业奋斗终生,并以独创
的制碱工艺闻名于世界,以下是侯德榜先生制碱工业的简要流程:
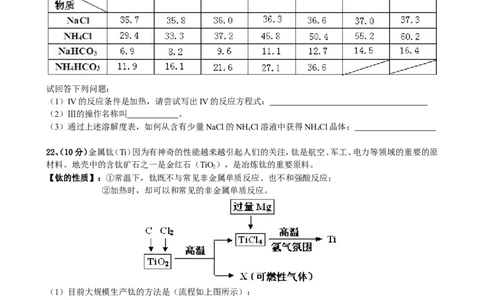
3下表是四种物质在100g水中不同温度的溶解度,其中NH HCO 水溶液呈碱性,性质不稳定,36℃时开始分
4 3
解为二氧化碳、氨和水,60℃可以分解完。
试回答下列问题:
(1)IV的反应条件是加热,请尝试写出IV的反应方程式:
(2)Ⅲ的操作名称叫 。
(3)通过上述溶解度表,如何从含有少量NaCl的NH Cl溶液中获得NH Cl晶体:
4 4
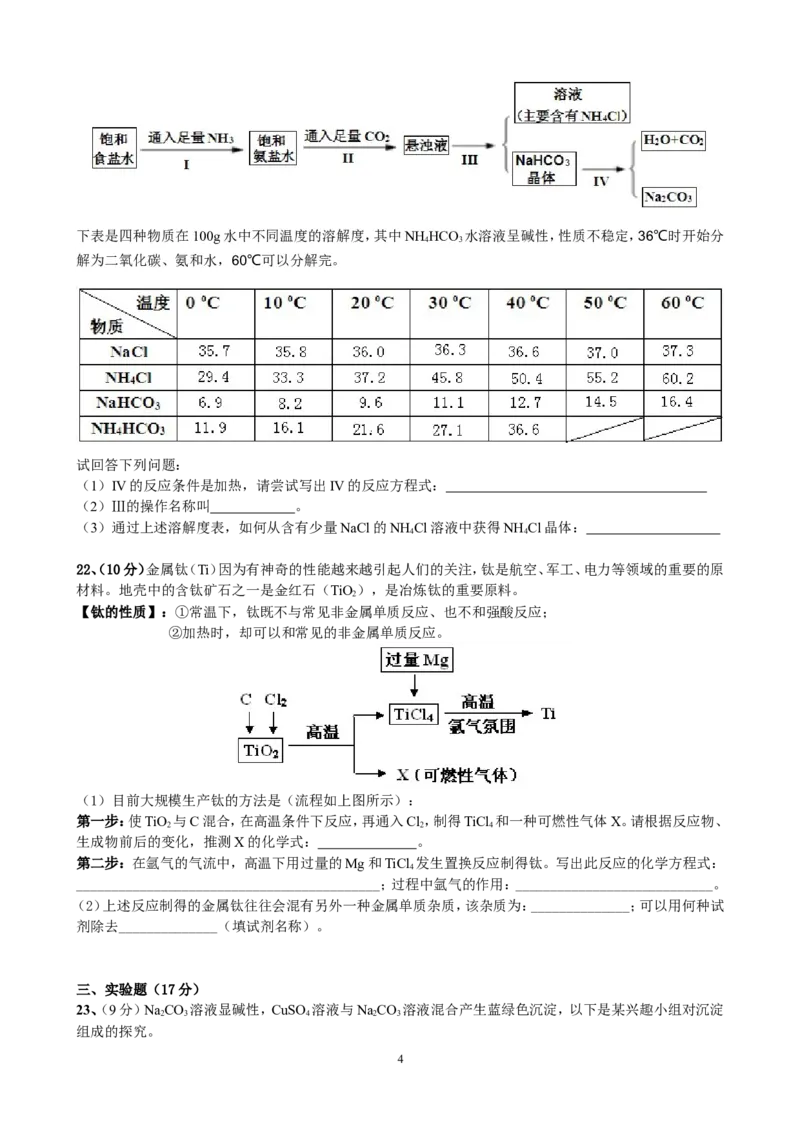
22、(10分)金属钛(Ti)因为有神奇的性能越来越引起人们的关注,钛是航空、军工、电力等领域的重要的原
材料。地壳中的含钛矿石之一是金红石(TiO),是冶炼钛的重要原料。
2
【钛的性质】:①常温下,钛既不与常见非金属单质反应、也不和强酸反应;
②加热时,却可以和常见的非金属单质反应。
(1)目前大规模生产钛的方法是(流程如上图所示):
第一步:使TiO 与C混合,在高温条件下反应,再通入Cl,制得TiCl 和一种可燃性气体X。请根据反应物、
2 2 4
生成物前后的变化,推测X的化学式: 。
第二步:在氩气的气流中,高温下用过量的Mg和TiCl 发生置换反应制得钛。写出此反应的化学方程式:
4
___________________________________________;过程中氩气的作用:____________________________。
(2)上述反应制得的金属钛往往会混有另外一种金属单质杂质,该杂质为:______________;可以用何种试
剂除去______________(填试剂名称)。
三、实验题(17分)
23、(9分)NaCO 溶液显碱性,CuSO 溶液与NaCO 溶液混合产生蓝绿色沉淀,以下是某兴趣小组对沉淀
2 3 4 2 3
组成的探究。
4【提出假设】
假设1:沉淀为Cu (OH)
2
假设2:沉淀为
假设3:沉淀为碱式碳酸铜[化学式可表示为nCuCO·mCu (OH) ]
3 2
【查阅资料】无论是哪一种沉淀受热均易分解(假设均不含结晶水)。
【物质成分探究】
步骤1:将所得悬浊液过滤,洗涤滤渣后晾干;
步骤2:甲同学取一定量上述蓝绿色固体,用如下装置(气密性良好)进行定性实验;
已知: nCuCO·mCu (OH) 受热易分解,生成CuO、CO、HO。
3 2 2 2
蓝绿色固体
K
N
2
碱石灰
无 水 澄清石灰水
A CaCl B C D
2
(1)若反应后A中蓝绿色固体变黑,C中无明显现象,证明假设 成立。
(2)乙同学认为只要将上图中B装置的试剂改用下列某试剂后,仅凭肉眼观察到的现象便可验证上
述所有假设,该试剂是 (填代号)。
A.浓硫酸 B.无水CuSO C.碱石灰 D.PO
4 2 5
(3)乙同学验证假设3成立的实验现象是 。
【物质含量探究】
(4)乙同学进一步探究假设3中固体的组成,用上述装置进行实验:
若所取蓝绿色固体样品质量为54.2 g置于A装置中,实验结束后装置B的质量增加5.4 g,C中的
产生沉淀的质量为20g。则该蓝绿色固体的化学式为 ;
24、(8分)某兴趣小组对Zn、Ni( 镍)、Cu的金属活动性顺序展开了探究。
【提出假设】对三种金属的活动性顺序提出可能的假设①Zn >Ni>Cu;②Zn >Cu >Ni;你觉得还有其他的可
能性吗?请任写一种假设:③__________________________
【查阅资料】小红同学查阅了部分含镍化合物的溶解性如下表,且得知镍能与酸反应。
OH- NO - SO 2- Cl-
3 4
Ni2+ 不溶 可溶 可溶 可溶
【设计实验】同温下,取大小、厚度相同的这三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观
察现象。
【记录现象】请帮助小红用实验现象填写完整下表:
Ni Zn Cu
与盐酸反应的现象 气体产生缓慢 气体产生激烈
金属逐渐溶解 金属迅速溶解
【得出结论】原假设中正确的是____________________(填序号)。
写出镍与盐酸反应的化学方程式___________________________________ ;
【结论应用】
根据以上实验结果,请选择另一类别的一种试剂设计实验,也同样达到一次验证上述假设的正确与
否,写出你选择试剂的化学式___________________.
5五、计算题(14分)
25、(7分)有一瓶NaCO 和NaSO 的药品混合物,某同学欲测定该药品NaSO 的纯度,进行如下分析:取
2 3 2 4 2 4
试样x g,用适量的蒸馏水配成溶液,加入足量的BaCl 溶液使沉淀完全。滤出的沉淀经洗涤、干燥后,质量
2
为 y g。将沉淀用足量盐酸洗涤后过滤,取沉淀洗涤、干燥得到z g固体。
(1)y的取值范围为 。(用含有x的式子表示)
(2)求NaSO 的质量分数。
2 4
26、(7分)广州--中山--珠海城际轻轨的开通大大促进了沿线城市经济的发展。石灰石是主要修路材料之
一。某兴趣小组用修路材料石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将
反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的NaCO 溶液,他们决定利用该废液,测
2 3
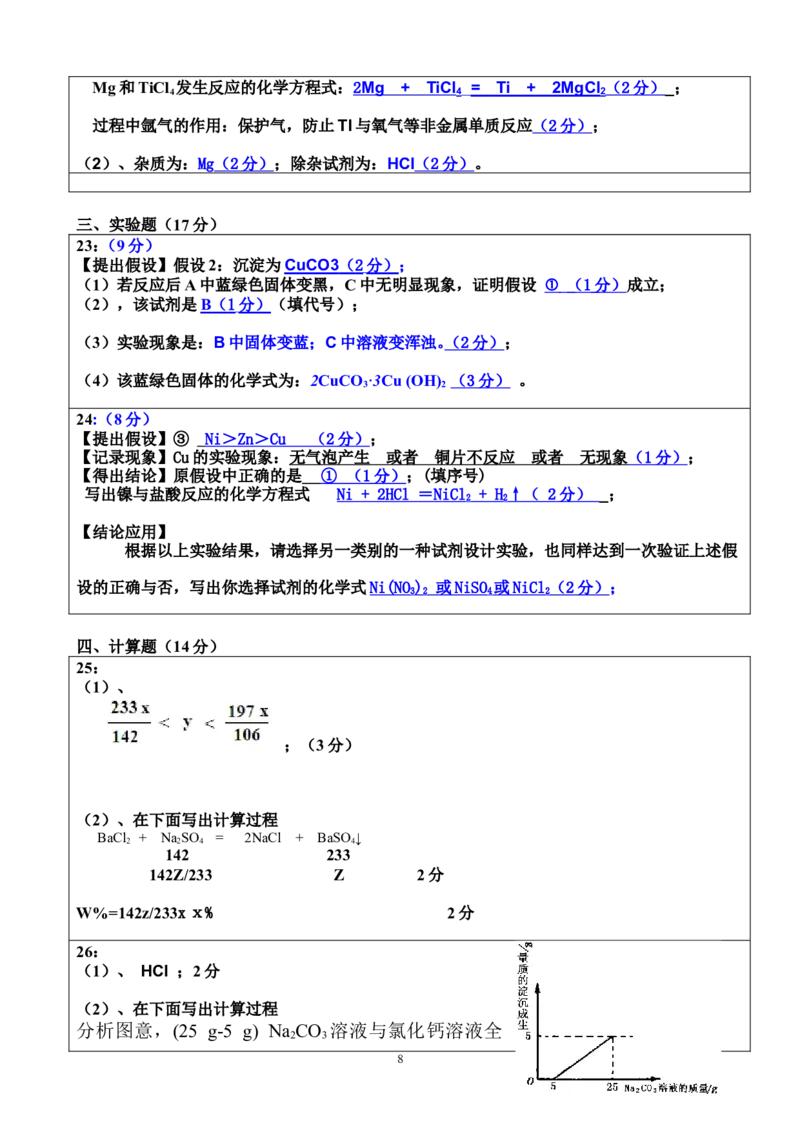
定这瓶NaCO 溶液中溶质的质量分数。他们将废液过滤,然后向废液中慢慢滴加 NaCO 溶液,加入
2 3 2 3
NaCO 溶液的质量与生成沉淀质量的关系如下图所示。
2 3
(1)在加入NaCO 溶液的过程中,开始时没有发现沉淀生成,说明滤液中的溶质除含有CaCl 外,还含有
2 3 2
______________________;
(2)计算NaCO 溶液中溶质的质量分数。(计算结果精确到0.1%)
2 3
广东省中山市 2013 年初中化学竞赛答题卡
一、选择题(15题×2分=30分,每题有1到2个正确选项,选对得2分,错选得0分,漏选得1分)
61 2 3 4 5 6 7 8 9 10
C A AB B A C CD D AD C
11 12 13 14 15
D A AB B D
二、填空题(39分)
16:
(1 ) 、 C O ( 1 分 ) ;
2
(2) (2 分 )
(3 ) 提倡骑自行车、步行、乘公交等( 1 分、其他合理答案同样给分)
17:
(1)、 B (2分)
(2)、Fe O +8HCl=2FeCl +FeCl (2分)
3 4 3 2
18:
5、、
(每
个2分)
(2)、 C (1分);
催化剂
2CO + 2NO = 2CO + N (2分)
2 2
19:
(1)、丙烷(2分);
(2)、C H (2分)。
4 10
20:
(1)、6:7:16(2分);
(2)、C N O = 8CO +4N (2分)。
8 8 16 2 2
21:
Δ
(1)、2NaHCO =Na CO +H O+CO ↑ ( 2 分 ) ;
3 2 3 2 2
(2)、过滤 ( 1 分) ;
(3)、蒸发浓缩、冷却结晶、过滤 ( 3 分) ;
22:
(1)、X的化学式为 CO ( 2 分) _;
7Mg和TiCl 发生反应的化学方程式: 2 Mg + TiC l = T i + 2MgC l ( 2 分) _;
4 4 2
过程中氩气的作用:保护气,防止TI与氧气等非金属单质反应 ( 2 分) ;
(2)、杂质为:Mg ( 2 分) ;除杂试剂为:HCl ( 2 分) 。
三、实验题(17分)
23:(9分)
【提出假设】假设2:沉淀为 CuCO3 ( 2 分) ;
(1)若反应后A中蓝绿色固体变黑,C中无明显现象,证明假设 ( 1 分 )成立;
(2),该试剂是 B ( 1 分) (填代号);
(3)实验现象是:B中固体变蓝;C中溶液变浑浊。 ( 2 分) ;
(4)该蓝绿色固体的化学式为:2CuCO ·3Cu (OH) ( 3 分) 。
3 2
24:(8分)
【提出假设】③ N i > Z n > Cu ( 2 分) ;
【记录现象】Cu的实验现象: 无气泡产生 或者 铜片不反应 或者 无现象 ( 1 分) ;
【得出结论】原假设中正确的是 ① ( 1 分) ;(填序号)
写出镍与盐酸反应的化学方程式 Ni + 2HCl = NiC l + H ↑ ( 2 分) _;
2 2
【结论应用】
根据以上实验结果,请选择另一类别的一种试剂设计实验,也同样达到一次验证上述假
设的正确与否,写出你选择试剂的化学式Ni(NO ) 或 NiS O 或 NiC l ( 2 分) ;
3 2 4 2
四、计算题(14分)
25:
(1)、
;(3分)
(2)、在下面写出计算过程
BaCl + NaSO = 2NaCl + BaSO↓
2 2 4 4
142 233
142Z/233 Z 2分
W%=142z/233xⅹ% 2分
26:
(1)、 HCl ;2分
(2)、在下面写出计算过程
分析图意,(25 g-5 g) Na CO 溶液与氯化钙溶液全
2 3
8部反应,生成5 g碳酸钙沉淀(1分)
设:20gNa CO 溶液中溶质的质量为x
2 3
Na CO +CaCl = CaCO ↓+2NaCl (1分)
2 3 2 3
106 100
x 5g
106:100=x:5g x=5.3g (2分)
5.3g
该Na CO 溶液中溶质的质量分数为 ×100%=26.5% (1分)
2 3 25g5g
9