文档内容
第 27 讲 电解原理的应用
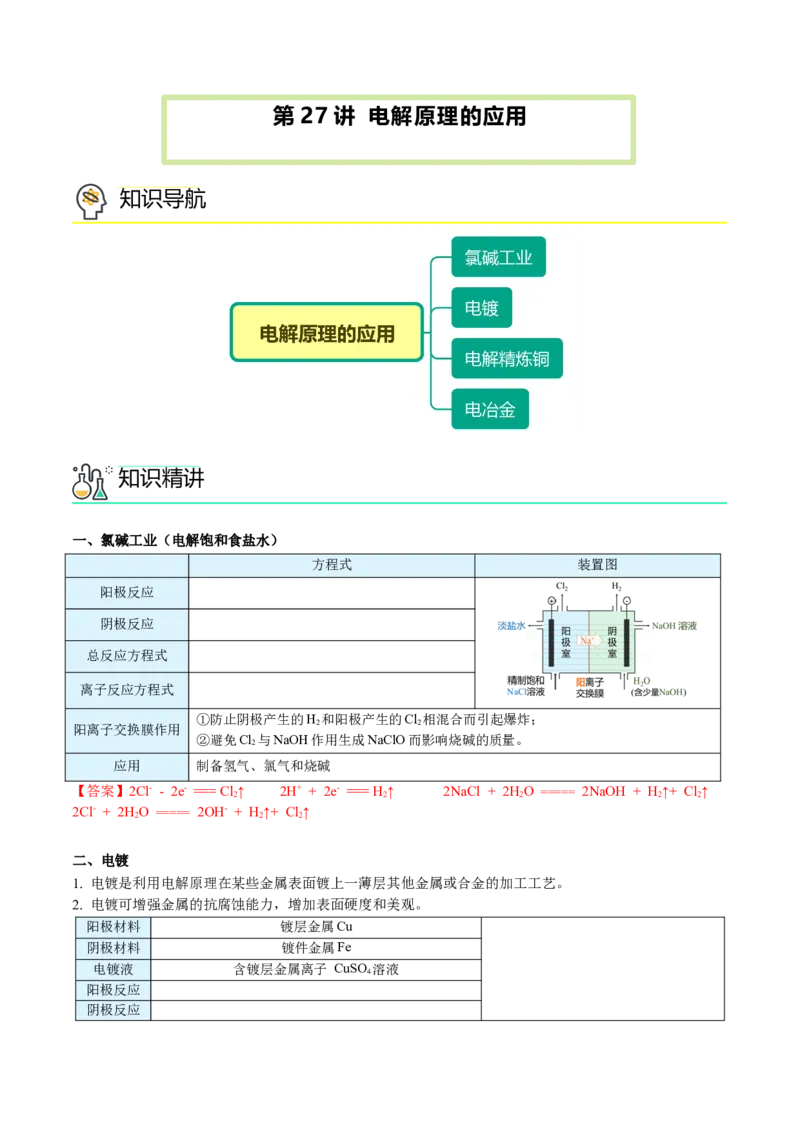
知识导航
小杨老师 15521324728 侵权必究
知识精讲
小杨老师 15521324728 侵权必究
一、氯碱工业(电解饱和食盐水)
方程式 装置图
阳极反应
阴极反应
总反应方程式
离子反应方程式
①防止阴极产生的H 和阳极产生的Cl 相混合而引起爆炸;
2 2
阳离子交换膜作用
②避免Cl 与NaOH作用生成NaClO而影响烧碱的质量。
2
应用 制备氢气、氯气和烧碱
杨sir化学,侵权必究
【答案】2Cl- - 2e- === Cl ↑ 2H+ + 2e- === H ↑ 2NaCl + 2HO ===== 2NaOH + H↑+ Cl↑
2 2 2 2 2
2Cl- + 2HO ===== 2OH- + H↑+ Cl↑
2 2 2
二、电镀
1. 电镀是利用电解原理在某些金属表面镀上一薄层其他金属或合金的加工工艺。
2. 电镀可增强金属的抗腐蚀能力,增加表面硬度和美观。
杨sir化学,侵权必究
阳极材料 镀层金属Cu
阴极材料 镀件金属Fe
电镀液 含镀层金属离子 CuSO 溶液
4
阳极反应
阴极反应溶液变化 电解质溶液的浓度__________
【答案】Cu - 2e- ===Cu2+ Cu2+ + 2e- === Cu 保持不变
三、电解精炼铜
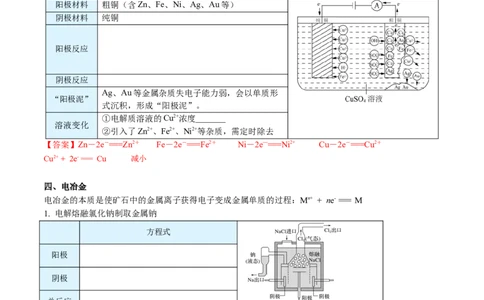
电解精炼粗铜时,以待精炼的铜(含Zn、Fe、Ni、Ag、Au等)作阳极,用CuSO 溶液作电解质溶液,可
4
得含铜量为99.95%~99.98%的电解铜。
杨sir化学,侵权必究
阳极材料 粗铜(含Zn、Fe、Ni、Ag、Au等)
阴极材料 纯铜
阳极反应
阴极反应
Ag、Au等金属杂质失电子能力弱,会以单质形
“阳极泥”
式沉积,形成“阳极泥”。
①电解质溶液的Cu2+浓度_______
溶液变化
②引入了Zn2+、Fe2+、Ni2+等杂质,需定时除去
【答案】Zn-2e-===Zn2+ Fe-2e-===Fe2+ Ni-2e—===Ni2+ Cu-2e-===Cu2+
Cu2+ + 2e- === Cu 减小
四、电冶金
电冶金的本质是使矿石中的金属离子获得电子变成金属单质的过程:Mn+ + ne- === M
1. 电解熔融氯化钠制取金属钠
方程式
阳极
阴极
总反应
【答案】2Cl--2e-===Cl↑ 2Na++2e-===2Na 2NaCl(熔融)===== 2Na + Cl↑
2 2
2.电解熔融的氯化镁制金属镁:MgCl (熔融)===== Mg + Cl↑
2 2
3.电解熔融的氧化铝制金属铝:2Al O(熔融)===== 4Al + 3O↑
2 3 2
对点训练
小杨老师 15521324728 侵权必究
题型一:氯碱工业
杨sir化学,侵权必究
【例1】如图用碳棒电解饱和食盐水的示意图,已知Na+向c极方向移动,则A.a极为正极 B.c极附近溶液pH变大
C.d极产生可燃性气体 D.电解后n(Na+)变大
【答案】B
【分析】
根据题干信息,Na+向c极方向移动,则c为阴极,电极反应式为:2H++2e-=H ,d为阴极,电极反应式为:
2
2Cl--2e-=Cl,因此a为电源负极,b为电源正极,据此分析解答。
2
【详解】
A.根据上述分析可知,a为负极,A错误;
B.c为阴极,电极反应式为:2H++2e-=H ,氢离子浓度减小,pH增大,B正确;
2
C.d为阴极,电极反应式为:2Cl--2e-=Cl,Cl 为不可燃气体,C错误;
2 2
D.电解过程中,Na+不参与反应,Na+的物质的量不变,D错误;
答案选B。
【变2】"84"消毒液(主要成分为NaClO)广泛应用于杀菌消毒。某化学演习小组用甲烷燃料电池电解饱
和食盐水制备"84"消毒液,装置如图 所示,a、b、c、d均为惰性电极,下列说法正确的是( )
A.c是阳极
B.甲烷发生的电极反应方程式为:CH-8e-+8OH−= CO↑+6H O
4 2 2
C.消耗2.24L(标准状况)甲烷,K+通过交换膜向左室移动0.8mol
D.电解装置中的总反应为:NaCl +HO NaClO+H ↑
2 2
【答案】D
【分析】
用甲烷燃料电池电解饱和食盐水制备“84”消毒液,a、b、c、d均为惰性电极,电解饱和食盐水阳极生成
Cl,阴极生成H 和NaOH,为保证Cl 与NaOH充分反应制备NaClO,则d电极为阳极生成Cl,c电极为
2 2 2 2
阴极;则a为甲烷燃料电池的负极,b为甲烷燃料电池的正极;以此分析作答。
【详解】
A.根据分析,c为阴极,A错误;B.甲烷燃料电池中所用电解质溶液为KOH溶液,则CH 发生失电子的氧化反应生成 ,甲烷发生的
4
电极反应方程式为CH-8e-+10OH-= +7H O,B错误;
4 2
C.根据分析,a为甲烷燃料电池的负极,b为甲烷燃料电池的正极,原电池中阳离子向正极移动,故K+通
过阳离子交换膜向右室移动,C错误;
D.电解装置中发生的反应为2NaCl+2H O 2NaOH+H ↑+Cl↑、Cl+2NaOH=NaCl+NaClO+H O,则电解
2 2 2 2 2
装置中的总反应为NaCl+H O NaClO+H ↑,D正确;
2 2
答案选D。
题型二:电镀
杨sir化学,侵权必究
【变3】餐具表面镀银可达到增强抗腐蚀性、提升美观等目的。下列关于铁表面镀银的说法不正确的是
A.电路中每通过1mole-,阴极析出1mol银
B.铁电极应与电源负极相连
C.阳极电极反应式为Ag﹣e- = Ag+
D.电镀液需要不断更换
【答案】D
【详解】
A.阴极发生反应Ag++e-=Ag,故每通过1mole-析出1mol银,A正确;
B.铁为镀件,应与电源负极相连,故B正确;
C.阳极为镀层金属,电极反应式为Ag﹣e- = Ag+,故C正确;
D.阳极发生反应为Ag﹣e- = Ag+,阴极发生反应Ag++e-=Ag,电镀液浓度不变,不需要更换,故D错误;
故选D。
题型三:电解精炼铜
杨sir化学,侵权必究
【例4】粗铜中含有 、 、 等杂质,用下图装置精炼铜。下列有关说法正确的是A. 是粗铜、 是纯铜
B.反应前后 电解液的浓度保持不变
C.阴极电极反应为:
D.电解过程中, 、 两极质量的变化量一直相等
【答案】C
【详解】
A.电解精炼铜时,粗铜为阳极,精铜为阴极,b为阳极,a为阴极,A错误;
B.电解精炼铜时,粗铜为阳极,比金属铜活泼的金属锌、铁、镍会先于金属铜失电子,精铜为阴极,电
极反应为:Cu2+ + 2e- = Cu,所以电解液的浓度降低,B错误;
C.精铜为阴极,电极反应为:Cu2+ + 2e- = Cu,C正确;
D.电解精炼铜时,粗铜为阳极,比金属铜活泼的金属锌、铁、镍会先于金属铜失电子,精铜为阴极,电
极反应为:Cu2+ + 2e- = Cu,阳极质量的减少与阴明极质量的增加不等,阳极质量减少的多,D错误;
答案选C。
题型四:电冶金
杨sir化学,侵权必究
【变5-1】下列有关金属冶炼的原理,错误的是
A. B.
C.Fe O+3CO 2Fe+3CO D.2NaCl(熔融) 2Na+Cl ↑
2 3 2 2
【答案】B
【详解】
A.Hg活动性比较弱,采用热分解方法制取,故符合Hg的冶炼方法,A正确;
B.Al是活泼金属,采用电解方法冶炼,方程式方法不符合反应事实,B错误;
C.Fe是比较活泼的金属,采用热还原方法冶炼,该方法符合Fe的冶炼方法,C正确;
D.Na是活泼金属,采用电解方法冶炼,该方法符合Na的冶炼方法,D正确;
故合理选项是B。
题型五:电解法制备物质
杨sir化学,侵权必究
【变6-1】如图所示,以 为主要原料制备 (已知: ),下列说
法正确的是A. 在阴极室产生
B.每有 生成时导线中有4mol电子通过
C.电解过程中,阳极无气体生成
D.为提高制备 的效率,应选用阳离子交换膜
杨sir化学,侵权必究
【答案】D
【分析】
由电解原理可知,电解过程中实质是电解水,阳极上水失去电子生成H+和O,阴极上水得到电子生成H
2 2
和OH-,由 可知,Cr O 在氢离子浓度较大的电极室中制得,即 在
2
阳极室产生;为提高制备 的效率,CrO 通过离子交换膜移向阳极。
【详解】
A.由分析而可知, 在阳极室产生,故A错误;
B.根据 反应可知,每有 生成时,消耗2molH+,根据阳极反应
式为: ,通过4mol电子,产生4mol氢离子,现消耗2molH+,则导线中有2mol电子
通过,故B错误;
C.电解过程中,阳极产生氧气,故C错误;
D.为提高制备 的效率,CrO 通过离子交换膜移向阳极,故应选用阳离子交换膜,故D正确;
故选D。
【变6-3】回答下列问题:
(1)某同学根据漂白粉的制备原理和电解原理制作了一种家用环保型消毒液发生器(如图所示,没有使用离
子交换膜),用石墨作电极电解饱和氯化钠溶液。通电时,为使Cl 被完全吸收,制得有较强杀菌能力的消
2
毒液,则:①利用Cl 与石灰乳反应可以制取漂白粉,反应的化学方程式为_____。
2
②L极区的电极反应式为_______。
杨sir化学,侵权必究
(2)电解法可以提纯粗镓,具体原理如图所示。镓在阳极溶解生成的Ga3+与NaOH溶液反应生成GaO ,
GaO 在阴极放电的电极反应式_______。
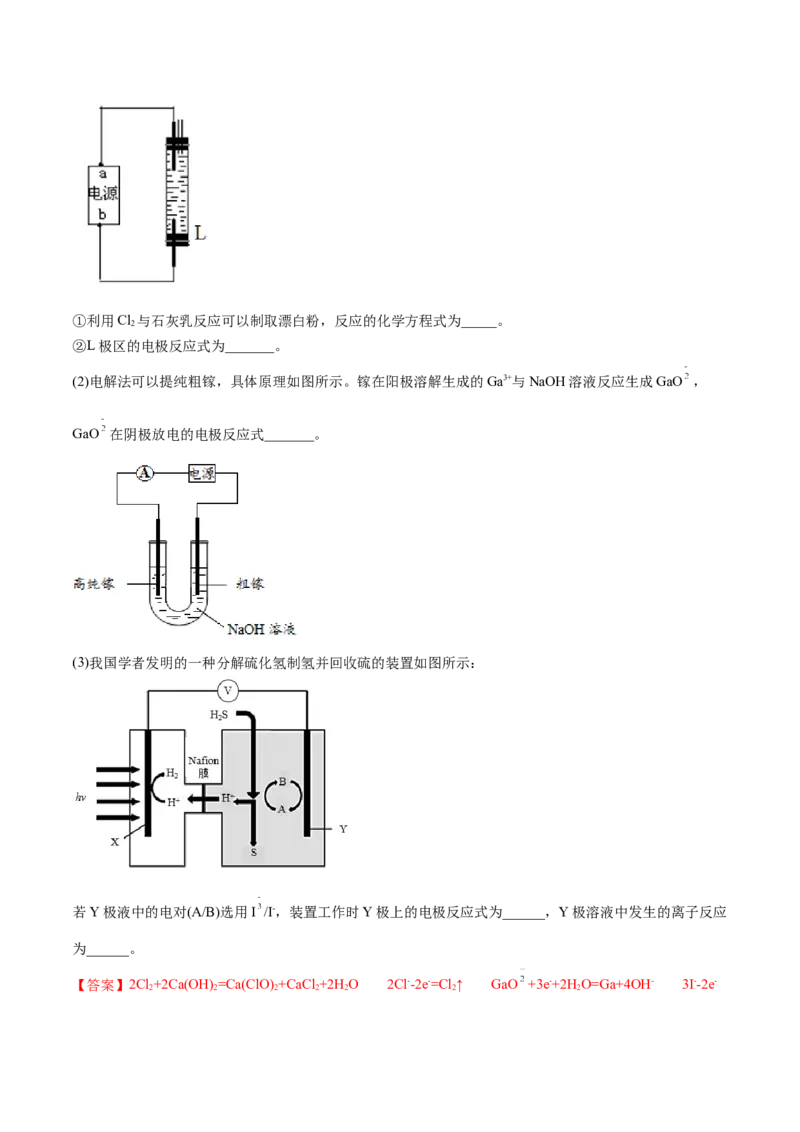
(3)我国学者发明的一种分解硫化氢制氢并回收硫的装置如图所示:
若Y极液中的电对(A/B)选用I /I-,装置工作时Y极上的电极反应式为______,Y极溶液中发生的离子反应
为______。
【答案】2Cl+2Ca(OH) =Ca(ClO) +CaCl +2H O 2Cl--2e-=Cl↑ GaO +3e-+2H O=Ga+4OH- 3I--2e-
2 2 2 2 2 2 2=I I +H S=S↓+2H++3I-
2
【详解】
(1)①利用Cl 与石灰乳反应可以制取漂白粉,反应的化学方程式为2Cl+2Ca(OH) =CaCl +Ca(ClO) +2H O;
2 2 2 2 2 2
②通电时,为使Cl 被完全吸收,该装置的下端生成氯气,则L极区的电极反应式为2Cl--2e-=Cl↑;
2 2
(2)电解法可以提纯粗镓,则高纯镓作阴极,粗镓作阳极,阳极上Ga失去电子变为Ga3+,生成的Ga3+与
NaOH溶液反应生成GaO ,GaO 在阴极放电生成Ga,电极反应式GaO +3e-+2H O=Ga+4OH-;
2
(3)根据图示,该装置是将光能转变为化学能和电能,X电极将H+转化为H,化合价降低,发生还原反应,
2
则Y电极发生氧化反应,若Y极液中的电对(A/B)选用I /I-,则电极反应为3I--2e-= I ,Y电极溶液中含有
H2S,具有还原性,而I 具有氧化性,二者发生氧化还原反应S单质、碘离子和氢离子,离子反应为:I
+H S=S↓+2H++3I-;
2
题型六:电解原理的应用综合
杨sir化学,侵权必究
【变7-1】关于下列各图的说法(其中①③④中均为情性电极)中正确的是
A.①装置中阴极处产生的气体能够使湿润KI淀粉试纸变蓝
B.②装置中待镀铁制品应与电源正极相连
C.③装置中电子由b极流向a极
杨sir化学,侵权必究
D.④装置中的阳离子交换膜可以避免生成的Cl 与NaOH溶液反应
2
【答案】D
【详解】
A.①装置为电解池,电解CuCl 溶液,在阴极处产生Cu,阳极处产生的Cl 能够使湿润KI淀粉试纸变蓝,
2 2
A不正确;
B.②装置中,在待镀铁制品表面镀铜,铜片应作阳极,待镀铁制品应作阴极,与电源负极相连,B不正
确;
C.③装置中,a电极为负极,b电极为正极,电子由负极沿导线流向正极,所以电子由a极流向b极,C
不正确;
D.④装置中,阳极生成Cl,阴极生成H 和NaOH,Cl 与H、NaOH都会发生反应,阳离子交换膜可以
2 2 2 2避免生成的Cl 与NaOH溶液反应,D正确;
2
故选D。
【例8】电解池在生产中有广泛的应用。
(1)精炼银:如图为电解精炼银的示意图___________,(填“a”或“b”)极为含有杂质的粗银,b的电极
反应式___________,若b极有少量红棕色气体产生,则生成该气体的电极反应式为___________。
(2)氯碱工业:用离子交换膜法电解饱和食盐水的装置如图所示,①口有刺激性气味的气体逸出,则A
为外电源的___________极,与B相连的电极的电极反应式___________。为了获得产品,选用
___________(填“阴”或“阳”)离子交换膜。
(3)若以惰性电极电解氯化铝溶液,总反应的离子方程式为___________。
【答案】
(1) a Ag++e-=Ag NO +e-+2H+═NO ↑+H O
2 2
(2) 正 2H++e-= H ↑ 阳
2
(3)2Al3++6Cl-+6H O 3Cl↑+3H ↑+2Al(OH) ↓
2 2 2 3
【解析】
(1)
电解精炼银时,粗银作阳极发生氧化反应,与电源正极相连的是电解池的阳极,所以a极为含有杂质的粗
银;b极与电源负极相连是电解池的阴极,b的电极反应式Ag++e-=Ag;电解质溶液中含硝酸根,b极有少
量红棕色气体应是二氧化氮,生成该气体的电极反应为:NO +e-+2H+═NO ↑+H O;
2 2
(2)
由①口有刺激性气味的气体逸出,可知①口产生氯气,为氯离子失电子得到,则A为外电源的正极,与B相连的电极做电解池的阴极,电极反应式为2H++e-= H ↑;为了得到NaOH产品,需要在Na+移到阴极区,
2
应选用阳离子交换膜;
(3)
惰性电极电解氯化铝溶液,由失电子能力Cl->OH-,阳极为氯离子失电子得到氯气,得电子能力H+>Al3+,
阴极为水中氢离子失电子生成氢气,则电解氯化铝溶液生成氢氧化铝沉淀、氢气、氯气,离子反应为2Al3+
+6Cl-+6H O 3Cl↑+3H ↑+2Al(OH) ↓。
2 2 2 3
提分特训
小杨老师 15521324728 侵权必究
【题1】下列叙述正确的是
A.电镀时,通常把待镀的金属制品作阳极
B.氢氧燃料电池(酸性电解质)中O 通入正极,电极反应为O+4H++4e-= 2H O
2 2 2
C.氯碱工业是电解熔融的NaCl,在阳极能得到Cl
2
D.电解熔融的氧化铝制取金属铝,用铁作阳极
【答案】B
【详解】
A. 电镀时,通常把待镀的金属制品作阴极,镀层金属作阳极,故A错误;
B. 氢氧燃料电池(酸性电解质)中O 通入正极,由于是酸性环境,故电极反应为O+4H++4e-= 2H O,故
2 2 2
B正确;
C. 氯碱工业是电解饱和NaCl溶液,在阳极能得到Cl,阴极得到氢气和氢氧化钠,故C错误;
2
D. 铁作阳极时,铁将放电生成Fe2+,开始时阴极还能析出少量铝,后来就变成电镀铁了,同时用铁作阳
极,阳极放电的是金属铁,电极被损耗,不符合生产实际,应用石墨作阳极,故D错误;
故选B。
【题2】某小组用如图装置模拟电镀铜和精炼铜。下列说法不正确的是
A.电镀铜和精炼铜时,Y上的电极反应都是:Cu2++2e-=Cu
B.电镀铜时,Y 电极为待镀的金属制品
C.精炼铜时,X 电极是粗铜,比铜活泼的金属最终变成阳极泥
D.电镀铜时,X 电极是铜,溶液中的Cu2+浓度保持不变
【答案】C
【分析】电镀铜时,阳极X为Cu,发生的电极反应为:Cu-2e-=Cu2+,阴极Y为待镀金属,发生的电极反应为:Cu2+
+2e-= Cu;
精炼铜时,阳极X为粗Cu,发生的电极反应为:Cu-2e-=Cu2+,阴极Y为纯Cu,发生的电极反应为:Cu2+
+2e-= Cu。
【详解】
A.由分析可知,电镀铜和精炼铜时,Y上的电极反应都是:Cu2++2e-=Cu,A正确;
B.由分析可知,电镀铜时,Y电极为待镀的金属制品,B正确;
C.精炼铜时,X电极是粗铜,比Cu活泼的金属在Cu之前失电子,以离子形式进入溶液中,没有Cu活泼
的金属不失电子,以金属形式进入阳极附近的溶液中成为阳极泥,C错误;
D.电镀铜时,阳极X为Cu,发生的电极反应为:Cu-2e-=Cu2+,阴极Y为待镀金属,发生的电极反应为:
Cu2+ +2e-= Cu,由此可知:电镀时,溶液中Cu2+浓度保持不变,D正确。
答案选C
【题4】铝是应用广泛的金属。以铝土矿(主要成分为Al O,含SiO 和Fe O 等杂质)为原料制备铝的一种
2 3 2 2 3
工艺流程如图:
注:SiO 在“碱溶”时转化为铝硅酸钠沉淀。
2
(1)“碱溶”时生成偏铝酸钠的离子方程式为_______
(2)“电解Ⅰ”是电解熔融Al O,写出阳极的电极反应式_______。
2 3
(3)“电解Ⅱ”是电解NaCO 溶液,原理如图所示。阳极的电极反应式为_______。
2 3
【答案】Al O+2OH-=2 +H O 2O2--4e-=O ↑ 4 +2H O-4e-=4 +O ↑
2 3 2 2 2 2
【详解】
铝土矿在碱溶时,其中的Al O 和SiO 可与NaOH溶液反应,二氧化硅反应后转化为铝硅酸钠沉淀,氧化
2 3 2
铝和氢氧化钠反应后得到可溶于水的偏铝酸钠,Fe O 与氢氧化钠溶液不反应,则滤渣为铝硅酸钠和
2 3
Fe O;过滤后,滤液中的NaAlO 与NaHCO 反应生成氢氧化铝沉淀和NaCO,氢氧化铝经灼烧后得到
2 3 2 3 2 3
Al O,最后电解熔融的Al O 得到铝;NaCO 溶液经电解后可以再生成NaHCO 和NaOH进行循环利用。
2 3 2 3 2 3 3(1)“碱溶”时,铝土矿中的Al O 和SiO 能够与氢氧化钠反应,其中生成偏铝酸钠的离子方程式为
2 3 2
Al O+2OH-=2 +H O;
2 3 2
(2)“电解Ⅰ”是电解熔融Al O,电解过程中,阳极上生成氧气,能够氧化石墨生成二氧化碳,因此阳极
2 3
的电极反应式为2O2--4e-=O ↑;
2
(3)“电解Ⅱ”是电解NaCO 溶液,阳极上是溶液中的水失电子生成氧气,产生的氢离子与碳酸根离子反
2 3
应生成碳酸氢根离子,电极反应式为4 +2H O-4e-=4 +O ↑。
2 2
【题6】(1)利用LiOH和钴氧化物可制备锂离子电池正极材料。LiOH可由电解法制备,钴氧化物可通
过处理钴渣获得。利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。B极区电解液
为________溶液(填化学式),阳极电极反应式为_________________,电解过程中Li+向________电极迁移
(填“A”或“B”)。
(2)用NaOH溶液吸收烟气中的SO ,将所得的NaSO 溶液进行电解,可循环再生NaOH,同时得到
2 2 3
HSO ,其原理如下图所示(电极材料为石墨)。图中a极要连接电源的________(填“正”或“负”)极,C口流出
2 4
的物质是________,SO 放电的电极反应式为______________,电解过程中阴极区碱性明显增强,用平衡
移动原理解释原因:_______________。
杨sir化学,侵权必究
【答案】LiOH 2Cl--2e-=Cl↑ B 负 硫酸 -2e-+HO= +2H+ HO H+
2 2 2
+OH-,在阴极H+放电生成H,c(H+)减小,水的电离平衡正向移动,碱性增强
2
【详解】
(1)由图可知,B极区生成H,同时会生成LiOH,则B极区电解液为LiOH溶液;电极A为阳极,在阳
2
极区LiCl溶液中Cl-放电,电极反应式为2Cl--2e-===Cl ↑;在电解过程中Li+(阳离子)向B电极(阴极区)
2
迁移,故答案为:LiOH;2Cl--2e-=Cl↑;B;
2(2)根据Na+、SO 的移动方向可知,Na+移向阴极区,a极应接电源负极,b极应接电源正极,阳极上
亚硫酸根离子失去电子发生氧化反应生成硫酸根,电极反应式为SO -2e-+HO=SO +2H+,阴极上水
2
电离出的氢离子得到电子发生还原反应生成氢气,电极反应式为2HO+2e-=H ↑+2OH-,则从C口流出
2 2
的是HSO ,在阴极区,H+放电破坏水的电离平衡,c(H+)减小,c(OH-)增大,生成NaOH,溶液碱性增强,
2 4
从B口流出的是浓度较大的NaOH溶液,故答案为:负;硫酸; -2e-+HO= +2H+;HO H
2 2
++OH-,在阴极H+放电生成H,c(H+)减小,水的电离平衡正向移动,碱性增强。
2
提分作业
小杨老师 15521324728 侵权必究
【练1】用铁棒和铜棒做电极,模拟在铁棒上镀铜,实验装置如图所示,下列判断正确的是
A.溶液中阳离子移向b极发生还原反应
B.铜棒的材质必须用纯铜
C.电解一段时间后加Cu(OH) 固体使溶液恢复原来的浓度
2
D.该实验过程中电解质溶液的pH会不断减小
【答案】A
【分析】
用电解原理模拟在铁棒上镀铜,则铁为阴极,铜为阳极,即a电极为Cu,b电极为Fe,阴极上铜离子得电
子析出铜单质,电解质溶液可为氯化铜、硫酸铜溶液等。
【详解】
A.电解过程中,a为阳极、b为阴极,溶液中阳离子移向b极发生还原反应生成铜,故A正确;
B.镀时镀层金属作阳极,即b电极常常用纯铜,但也可用混有活泼性大于Cu的金属的铜合金或用混有活
泼性小于Ag的金属的铜合金等,故B错误;
C.电镀铜时,铜在阳极失去电子进入溶液中,溶液中的铜离子在阴极得电子生成铜,理论上溶液中各离
子的种类和浓度不变,电解一段时间后不需要加Cu(OH) 固体使溶液恢复原来的浓度,故C错误;
2
D.该实验过程中铜在阳极失去电子进入溶液中,溶液中的铜离子在阴极得电子生成铜,溶液中的各离子
的浓度不变,pH不变,故D错误;
故选A。
【练2】工业上冶炼钠、银、铁,常采用的方法分别是A.电解法、热还原法、热分解法 B.电解法、 热分解法、热还原法
C.热分解法、热还原法、电解法 D.热还原法、热分解法、电解法
【答案】B
【详解】
金属钠是特别活泼的金属,采用电解方法冶炼;银是不活泼的金属,采用热分解方法冶炼;铁是比较活泼
的金属,采用热还原方法冶炼,故合理选项是B。
【练3】某学生想制作一种家用环保型消毒液发生器,用石墨作电极解饱和氯化钠溶液,通电时,为使Cl
2
被完成吸收投篮有较强杀菌能力的消毒液,设计了如图所示的装置,以下对电源电极名称和消毒液和主要
成分判断正确的是( )
A.a为正极,b为负极:NaClO和NaCl
B.a为负极,b为正极:NaClO和NaCl
C.a为阳极,b为阴极:HClO和NaCl
D.a为阴极,b为阳极:HClO和NaCl
杨sir化学,侵权必究
【答案】B
【分析】
电解池中,阳极是阴离子放电,阴极是阳离子放电,氯气能和氢氧化钠反应生成次氯酸钠,可以制得有较
强杀菌能力的消毒液.
【详解】
电解氯化钠溶液时,阳极是氯离子失电子生成氯气的过程,阴极是氢离子的电子生成氢气的过程,为使Cl
2
被完全吸收,制得有较强杀菌能力的消毒液,所以一定要让氯气在d电极产生,所以d电极是阳极,c电
极是阴极,即a为负极,b为正极,氯气和氢氧化钠反应生成的是氯化钠和次氯酸钠。
故选B。
【练4】关于图中电化学装置,有关叙述正确的是A.装置①的石墨电极上会析出金属钠
B.装置②中随着电解的进行左边电极会产生红色的铜
C.装置③中的离子交换膜为阴离子交换膜
D.装置④的待镀铁制品应与电源正极相连
【答案】B
【详解】
A.装置①中阴极上金属离子放电生成单质,即金属单质在铁电极上生成,故A错误;
B.装置②中铜离子在阴极得电子,则随着电解的进行左边电极会产生红色的铜,故B正确;
C.装置③中右边得到浓氢氧化钠溶液,左边得到淡盐水,故钠离子向右移动,所以离子交换膜为阳离子
交换膜,故C错误;
D.装置④中,电镀池中,镀层作电解池阳极,待镀金属作阴极,则待镀铁制品应与电源负极相连,故D
错误;
故答案为B。
【练5】某科研实验小组用EIS膜池构型的电渗析装置电解磷酸钠和硫酸制备磷酸二氢钠,装置如图所示,
下列有关说法错误的是
A.电极电势:a