文档内容
第10单元 知识点汇总
一、酸、碱、盐的组成
1、酸是由氢元素和酸根组成的化合物 如:硫酸(HSO )、盐酸(HCl)、硝酸(HNO)
2 4 3
2、碱是由金属元素和氢氧根组成的化合物 如:氢氧化钠、氢氧化钙、氨水(NH ·H O)
3 2
3、盐是由金属元素元素(或铵根)和酸根组成的化合物 如:氯化钠、碳酸钠
注:酸、碱、盐的水溶液可以导电(原因:溶于水时离解形成自由移动的阴、阳离子)
二、酸
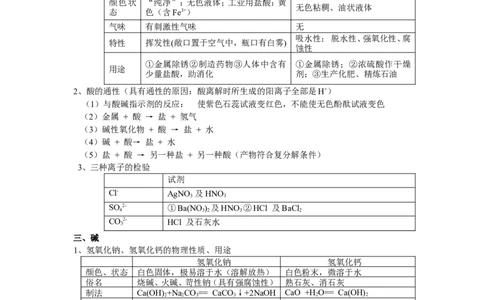
1、浓盐酸、浓硫酸的物理性质、特性、用途
浓盐酸 浓硫酸
颜色状 “纯净”:无色液体;工业用盐酸:黄
无色粘稠、油状液体
态 色(含Fe3+)
气味 有刺激性气味 无
吸水性; 脱水性、强氧化性、腐
特性 挥发性(敞口置于空气中,瓶口有白雾)
蚀性
①金属除锈②制造药物③人体中含有 ①金属除锈;②浓硫酸作干燥
用途
少量盐酸,助消化 剂;③生产化肥、精炼石油
2、酸的通性(具有通性的原因:酸离解时所生成的阳离子全部是H+)
(1)与酸碱指示剂的反应: 使紫色石蕊试液变红色,不能使无色酚酞试液变色
(2)金属 + 酸 → 盐 + 氢气
(3)碱性氧化物 + 酸 → 盐 + 水
(4)碱 + 酸→ 盐 + 水
(5)盐 + 酸 → 另一种盐 + 另一种酸(产物符合复分解条件)
3、三种离子的检验
试剂
Cl- AgNO 及HNO
3 3
SO 2- ①Ba(NO ) 及HNO ②HCl 及BaCl
4 3 2 3 2
CO2- HCl 及石灰水
3
三、碱
1、氢氧化钠、氢氧化钙的物理性质、用途
氢氧化钠 氢氧化钙
颜色、状态 白色固体,极易溶于水(溶解放热) 白色粉末,微溶于水
俗名 烧碱、火碱、苛性钠(具有强腐蚀性) 熟石灰、消石灰
制法 Ca(OH) +Na CO== CaCO ↓+2NaOH CaO +H O== Ca(OH)
2 2 3 3 2 2
①氢氧化钠固体作干燥剂 ①工业:制漂白粉
②化工原料:制肥皂、造纸 ②农业:改良酸性土壤、配波尔多
用途
③去除油污:炉具清洁剂中含氢氧化 液
钠 ③建筑:
2、碱的通性(具有通性的原因:离解时所生成的阴离子全部是OH-)
(1)碱溶液与酸碱指示剂的反应: 使紫色石蕊试液变蓝色,使无色酚酞试液变红色
(2)酸性氧化物+碱 → 盐+水
(3)酸+碱 → 盐+水
(4)盐+碱→ 另一种盐+另一种碱(反应物均可溶,产物符合复分解条件)
注:①难溶性碱受热易分解(不属于碱的通性)
如Cu(OH) ΔCuO +H O
2 2
12Fe(OH) ΔFe O+3H O
3 2 3 2
②常见沉淀:AgCl↓ BaSO↓ Cu(OH) ↓ F e(OH) ↓ Mg(OH) ↓ BaCO ↓
4 2 3 2 3
CaCO ↓
3
③复分解反应的条件:当两种化合物互相交换成分,生成物中有沉淀或有气体或有水生
成时,复分解反应才可以发生。
五、酸性氧化物与碱性氧化物
酸性氧化物 碱性氧化物
凡能与碱反应生成盐和水的氧化物 凡能与酸反应生成盐和水的氧化物
定
大多数非金属氧化物是酸性氧化物 大多数金属氧化物是碱性氧化物
义
大多数酸性氧化物是非金属氧化物 所有碱性氧化物是金属氧化物
(1)大多数可与水反应生成酸 (1)少数可与水反应生成碱
CO+H O== HCO NaO +H O== 2NaOH
2 2 2 3 2 2
化 SO +H O== HSO KO +H O== 2KOH
2 2 2 3 2 2
学 SO +H O== HSO BaO +H O== Ba(OH)
3 2 2 4 2 2
性 CaO +H O== Ca(OH)
2 2
质 (2) 酸性氧化物+碱 → 盐+水 (2) 碱性氧化物+酸 → 盐+水
CO +Ca(OH) == CaCO ↓+H O Fe O+6HCl== 2FeCl +3H O
2 2 3 2 2 3 3 2
(不是复分解反应)
四、中和反应 溶液酸碱度的表示法——pH
1、定义:酸与碱作用生成盐和水的反应
2、应用:(1)改变土壤的酸碱性;(2)处理工厂的废水;(3)用于医药。
3、溶液酸碱度的表示法——pH
(1)0 7 14
酸性增强 中性 碱性增强
(2)pH的测定:最简单的方法是使用pH试纸
用玻璃棒(或滴管)蘸取待测试液少许,滴在pH试纸上,显色后与标准比色卡对照,读
出溶液的pH(读数为整数)。
(3)酸雨:正常雨水的pH约为5.6(因为溶有CO);pH<5.6的雨水为酸雨
2
2