文档内容
《铁 金属材料》单元测试(基础巩固)
学校:___________姓名:___________班级:___________考号:___________
一、单选题(共54分)
1.(本题3分)铁的下列性质中不属于纯铁的物理性质是
A.质软 B.银白色 C.能导电 D.易生锈
2.(本题3分)下列有关铁及其化合物的说法错误的是
A.陨铁中存在游离态的铁
B.铁能与水蒸气反应,生成氧化铁和氢气
C.铁的氧化物都不溶于水,也不与水反应
D.氢氧化亚铁在空气中易被氧化成氢氧化铁
3.(本题3分)一些高档茶叶、点心等食品的包装盒中有一个小袋,将小袋打开,可以看到黑色粉末,部分
已变成棕褐色。将上述粉末溶于稀盐酸,取上层清液,滴入几滴氯水,再滴加KSCN溶液,溶液立即变为
红色。下列说法不正确的是
A.小袋中原来装有氧化铁 B.小袋中原来装有铁粉
C.该黑色粉末不可食用 D.该黑色粉末做抗氧化剂
4.(本题3分)下列溶液能溶解铁且无新的固体和气体产生的是
A.CuSO 溶液 B.稀硫酸 C.FeCl 溶液 D.AgNO 溶液
4 3 3
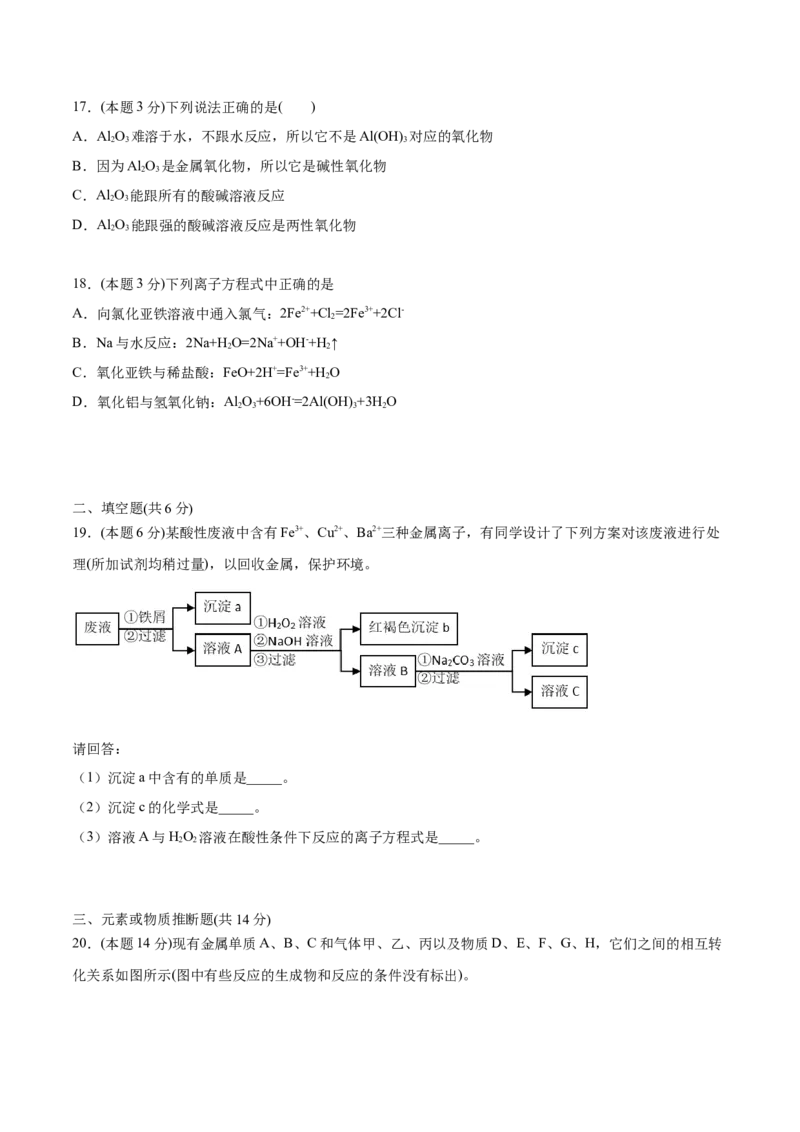
5.(本题3分)某学习小组进行了如图所示的实验,实验后组员之间的交流不合理的是
A.甲同学认为试管b中收集到的气体可点燃,且产生淡蓝色火焰B.乙同学认为试管a中生成的黑色固体可能为四氧化三铁
C.丙同学认为将少量还原性铁粉放入试管中,加适量的水,加热也可实现该反应
D.丁同学认为用盐酸溶解生成固体所得溶液有颜色
6.(本题3分)将1.12 g铁粉加入25mL2molL-1氯化铁溶液中充分反应(忽略溶液体积变化),下列分析正确
的是 ⋅
A.铁粉有剩余
B.Cl-浓度减小
C.向溶液中滴入无色KSCN溶液,溶液不变红
D.反应液质量增加1.12 g
7.(本题3分)下列有关铁、铁矿石与铁的氧化物的说法正确的是
A.赤铁矿的主要成分是Fe O,磁铁矿的主要成分是Fe O,Fe O 俗称铁红
2 3 3 4 2 3
B.在自然界中,不可能有游离态的铁存在
C.能通过化合反应制得Fe(OH) ,但不能通过化合反应制得FeCl
3 2
D.铁的氧化物能与酸反应生成盐和水,因此Fe O、Fe O、FeO都是碱性氧化物
3 4 2 3
8.(本题3分)下列反应的离子方程式正确的是
A.铁钉放入硫酸铜溶液中:
B.硫酸铜溶液与Ca(OH) 溶液混合:
2
C.钠与水反应:
D.氧化铁与稀盐酸混合:
9.(本题3分)要除去FeCl 溶液中少量的FeCl ,可行的方法是
2 3
A.滴入KSCN溶液
B.通入氯气
C.加入适量铜粉并过滤
D.加入适量铁粉并过滤10.(本题3分)已知2Fe3++Fe=3Fe2+,将适量铁粉放入FeCl 溶液中,完全反应后,溶液中的Fe2+和Fe3+个数
3
相等,则已反应的Fe3+和未反应的Fe3+的个数之比是
A.2:3 B.3:2 C.1:2 D.1:1
11.(本题3分)我国铝材工业水平处于世界领先行列。下列说法不正确的是
A.铝制餐具不宜长时间盛放酸性、碱性或咸的食物
B.常温下,铝制品耐腐蚀是因为铝不活泼
C.铝合金密度小、强度高,广泛应用于航空领域
D.工业上常用NaOH溶液去除铝表面的氧化膜
12.(本题3分)下列物质中,不是既能跟盐酸反应,又能跟NaOH反应的是
A.NaHCO B.Al C.Al O D.Fe O
3 2 3 2 3
13.(本题3分)下列对金属和金属材料的认识中,不正确的是( )
A.生铁和钢的性能完全相同
B.铁在潮湿的空气中容易生锈
C.赤铁矿的主要成分是氧化铁
D.回收废旧金属有利于节约金属资源
14.(本题3分)一定质量的铝片分别和足量的氢氧化钠溶液和盐酸反应,相同情况下放出氢气的质量
A.一样多 B.与酸更多 C.与碱更多 D.无法确定
15.(本题3分)区别镁铝,最好采用的方法是
A.投入沸水中 B.投入冷水中
C.投入盐酸中 D.投入烧碱溶液中
16.(本题3分)下列关于铁铝的性质叙述错误的是
A.补血剂中含有铁元素,人体缺铁,会引起贫血
B.铝是人体中一种微量元素,如果摄入过多,会患老年痴呆
C.铝的导热性比铁强,因而用铝锅煮食物比铁锅好
D.硬铝是一种合金,硬度比纯铝大17.(本题3分)下列说法正确的是( )
A.Al O 难溶于水,不跟水反应,所以它不是Al(OH) 对应的氧化物
2 3 3
B.因为Al O 是金属氧化物,所以它是碱性氧化物
2 3
C.Al O 能跟所有的酸碱溶液反应
2 3
D.Al O 能跟强的酸碱溶液反应是两性氧化物
2 3
18.(本题3分)下列离子方程式中正确的是
A.向氯化亚铁溶液中通入氯气:2Fe2++Cl=2Fe3++2Cl-
2
B.Na与水反应:2Na+HO=2Na++OH-+H ↑
2 2
C.氧化亚铁与稀盐酸:FeO+2H+=Fe3++H O
2
D.氧化铝与氢氧化钠:Al O+6OH-=2Al(OH) +3H O
2 3 3 2
二、填空题(共6分)
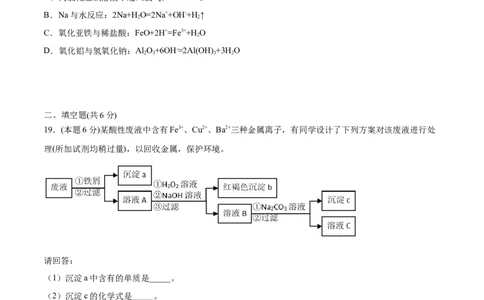
19.(本题6分)某酸性废液中含有Fe3+、Cu2+、Ba2+三种金属离子,有同学设计了下列方案对该废液进行处
理(所加试剂均稍过量),以回收金属,保护环境。
请回答:
(1)沉淀a中含有的单质是_____。
(2)沉淀c的化学式是_____。
(3)溶液A与HO 溶液在酸性条件下反应的离子方程式是_____。
2 2
三、元素或物质推断题(共14分)
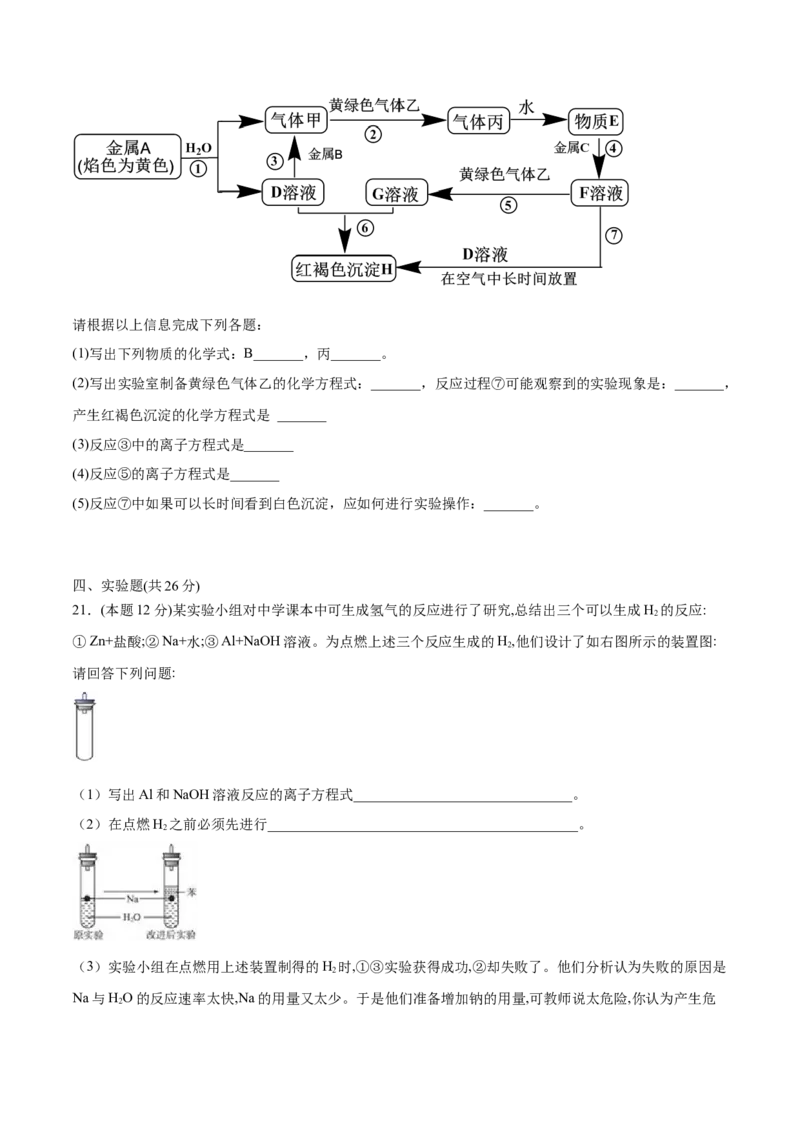
20.(本题14分)现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转
化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。请根据以上信息完成下列各题:
(1)写出下列物质的化学式:B_______,丙_______。
(2)写出实验室制备黄绿色气体乙的化学方程式:_______,反应过程⑦可能观察到的实验现象是:_______,
产生红褐色沉淀的化学方程式是 _______
(3)反应③中的离子方程式是_______
(4)反应⑤的离子方程式是_______
(5)反应⑦中如果可以长时间看到白色沉淀,应如何进行实验操作:_______。
四、实验题(共26分)
21.(本题12分)某实验小组对中学课本中可生成氢气的反应进行了研究,总结出三个可以生成H 的反应:
2
①Zn+盐酸;②Na+水;③Al+NaOH溶液。为点燃上述三个反应生成的H,他们设计了如右图所示的装置图:
2
请回答下列问题:
(1)写出Al和NaOH溶液反应的离子方程式_______________________________。
(2)在点燃H 之前必须先进行____________________________________________。
2
(3)实验小组在点燃用上述装置制得的H 时,①③实验获得成功,②却失败了。他们分析认为失败的原因是
2
Na与HO的反应速率太快,Na的用量又太少。于是他们准备增加钠的用量,可教师说太危险,你认为产生危
2险的原因是___________________________。
(4)实验小组查阅钠、苯(一种不溶于水的液态有机物)、水的密度分别为0.97 g·mL-1、0.88 g·mL-1、1.00
g·mL-1,并据此对实验进行了改进。在改进后的实验中H 的生成速率____________。(填“减慢”或“加快”)
2
(5)将4.6gNa和8.1gAl投入到足量的水中,所得溶液的体积为200mL,则生成标准状况下的H 的体积是
2
___________?该溶液中溶质的物质的量浓度是__________________?
22.(本题14分)某兴趣小组利用下列试剂:铁粉、锌粉、0.1mol/LFeCl 溶液、KSCN溶液、新制氯水,探
2
究Fe2+、Fe3+的氧化性、还原性,并利用实验结论解决一些问题。
(1)用所给试剂写出体现Fe2+具有还原性的反应的离子反应方程式:___。
(2)设计实验方案,完成下列表格。
探究内容 实验方案 实验现象
取少量0.1mol/LFeCl 溶液,往溶液中加入 加入铁粉后,溶液变成___;加入
探究Fe3+的化学性质 3
足量铁粉,再加入少量KSCN溶液 KSCN溶液后,溶液变成___
结论:Fe3+具有___性
(3)该兴趣小组未说明“Fe2+具有氧化性”,提出了向FeCl 溶液中加入锌粉,观察实验现象的方案,该反
2
应的离子方程式为___。
(4)某反应中反应物与生成物有Fe3+、MnO 、HO和一种未知离子X。
2
①已知氧化性:MnO >Fe3+,则X离子是___。
②该反应的离子方程式是___。关注更新免费领取,淘宝唯一每月更新店铺:知二教育