文档内容
第 28 讲 金属的腐蚀与防护
知识导航
小杨老师 15521324728 侵权必究
知识精讲
小杨老师 15521324728 侵权必究
一、金属的腐蚀
1.概念:金属与周围的气体或液体物质发生氧化还原反应而引起损耗的现象。
2.实质:金属失电子变成阳离子,被氧化,其反应为:M - ne- === Mn+(M为金属元素)。
杨sir化学,侵权必究
3.分类:
分类 化学腐蚀 电化学腐蚀
金属与其表面接触的一些物质(如O、Cl、 不纯的金属或合金与电解质溶液接触,
条件 2 2
SO 2 等)直接反应 形成原电池
现象 无电流产生 有微弱电流产生
本质 金属被氧化 较活泼的金属被氧化
联系 化学腐蚀和电化学腐蚀往往同时发生,但电化学腐蚀更普遍,速率更快
二、钢铁的析氢腐蚀与吸氧腐蚀
析氢腐蚀 吸氧腐蚀
图示条件 水膜呈较强酸性(pH≤4.3) 水膜呈弱酸性、中性或碱性
负极反应
正极反应
总反应式
Fe2+ + 2OH- === Fe(OH) ↓
2
其他反应 4Fe(OH) +2HO + O === 4Fe(OH)
2 2 2 3
2Fe(OH) === Fe O·xHO + (3﹣x)H O
3 2 3 2 2
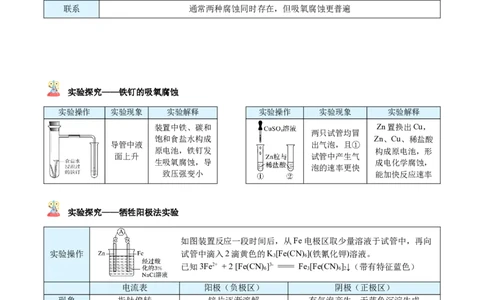
联系 通常两种腐蚀同时存在,但吸氧腐蚀更普遍
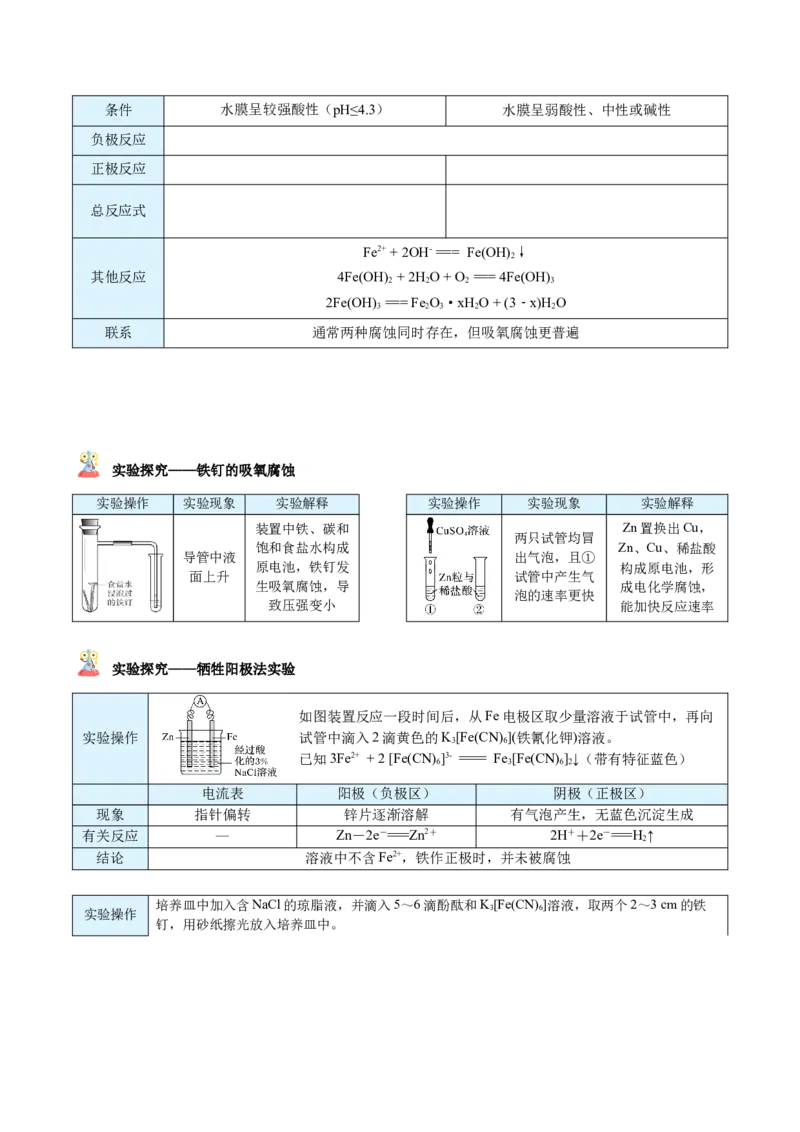
实验探究——铁钉的吸氧腐蚀
杨sir化学,侵权必究
实验操作 实验现象 实验解释 实验操作 实验现象 实验解释
装置中铁、碳和 Zn置换出Cu,
两只试管均冒
饱和食盐水构成 Zn、Cu、稀盐酸
导管中液 出气泡,且①
原电池,铁钉发 构成原电池,形
面上升 试管中产生气
生吸氧腐蚀,导 成电化学腐蚀,
泡的速率更快
致压强变小 能加快反应速率
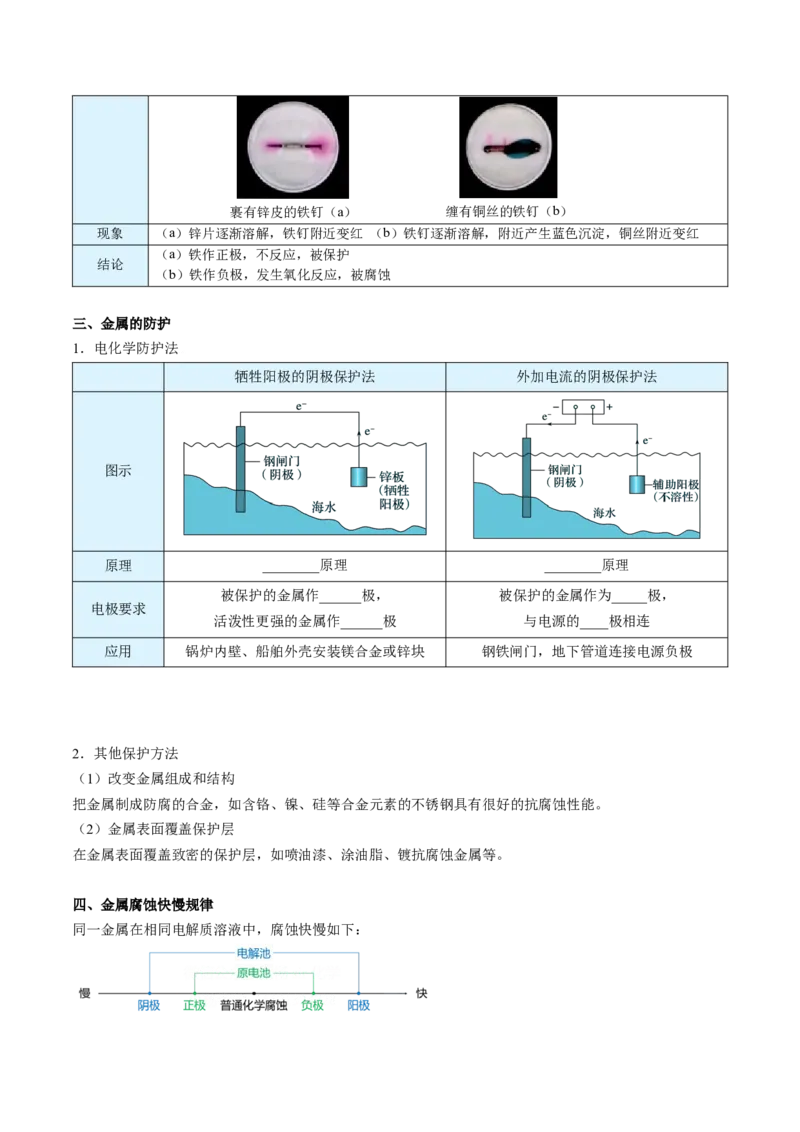
实验探究——牺牲阳极法实验
如图装置反应一段时间后,从Fe电极区取少量溶液于试管中,再向
实验操作 试管中滴入2滴黄色的K[Fe(CN) ](铁氰化钾)溶液。
3 6
已知3Fe2+ + 2 [Fe(CN) ]3- ==== Fe [Fe(CN) ]↓(带有特征蓝色)
6 3 6 2
电流表 阳极(负极区) 阴极(正极区)
现象 指针偏转 锌片逐渐溶解 有气泡产生,无蓝色沉淀生成
有关反应 — Zn-2e-===Zn2+ 2H++2e-===H↑
2
结论 溶液中不含Fe2+,铁作正极时,并未被腐蚀
培养皿中加入含NaCl的琼脂液,并滴入5~6滴酚酞和K[Fe(CN)]溶液,取两个2~3 cm的铁
实验操作 3 6
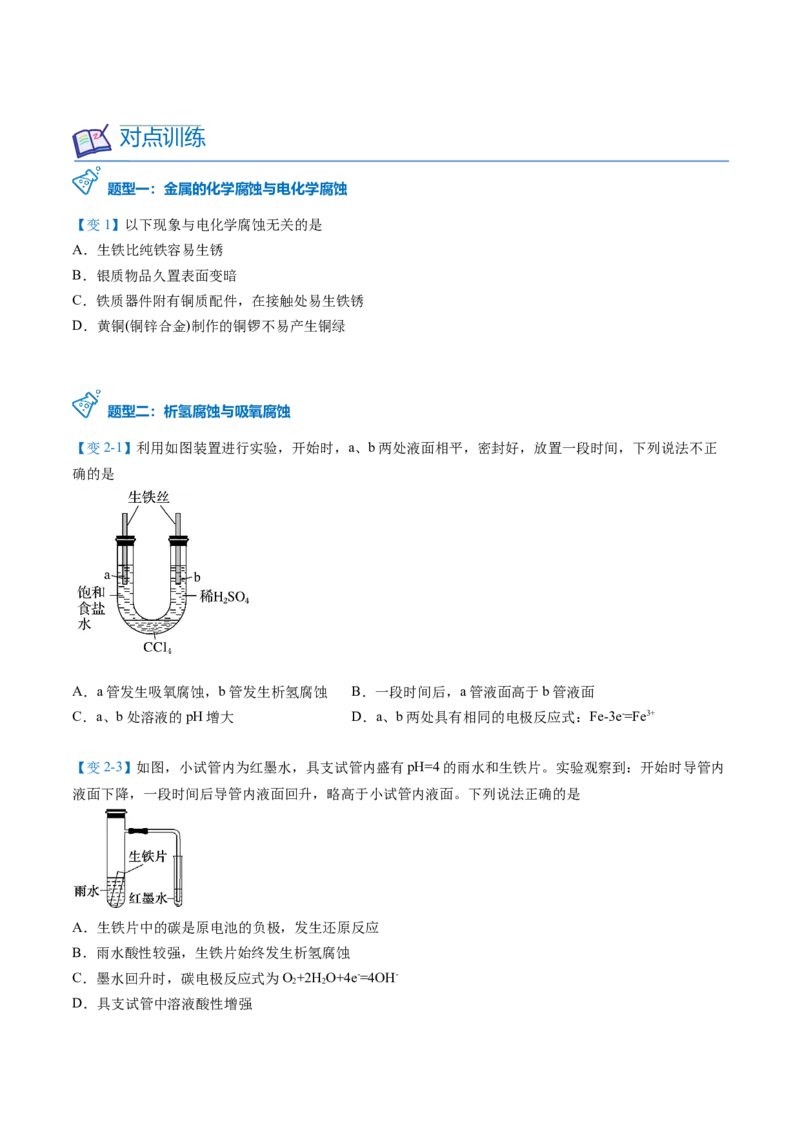
钉,用砂纸擦光放入培养皿中。裹有锌皮的铁钉(a) 缠有铜丝的铁钉(b)
现象 (a)锌片逐渐溶解,铁钉附近变红 (b)铁钉逐渐溶解,附近产生蓝色沉淀,铜丝附近变红
(a)铁作正极,不反应,被保护
结论
(b)铁作负极,发生氧化反应,被腐蚀
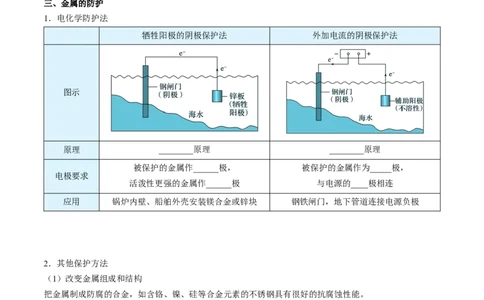
三、金属的防护
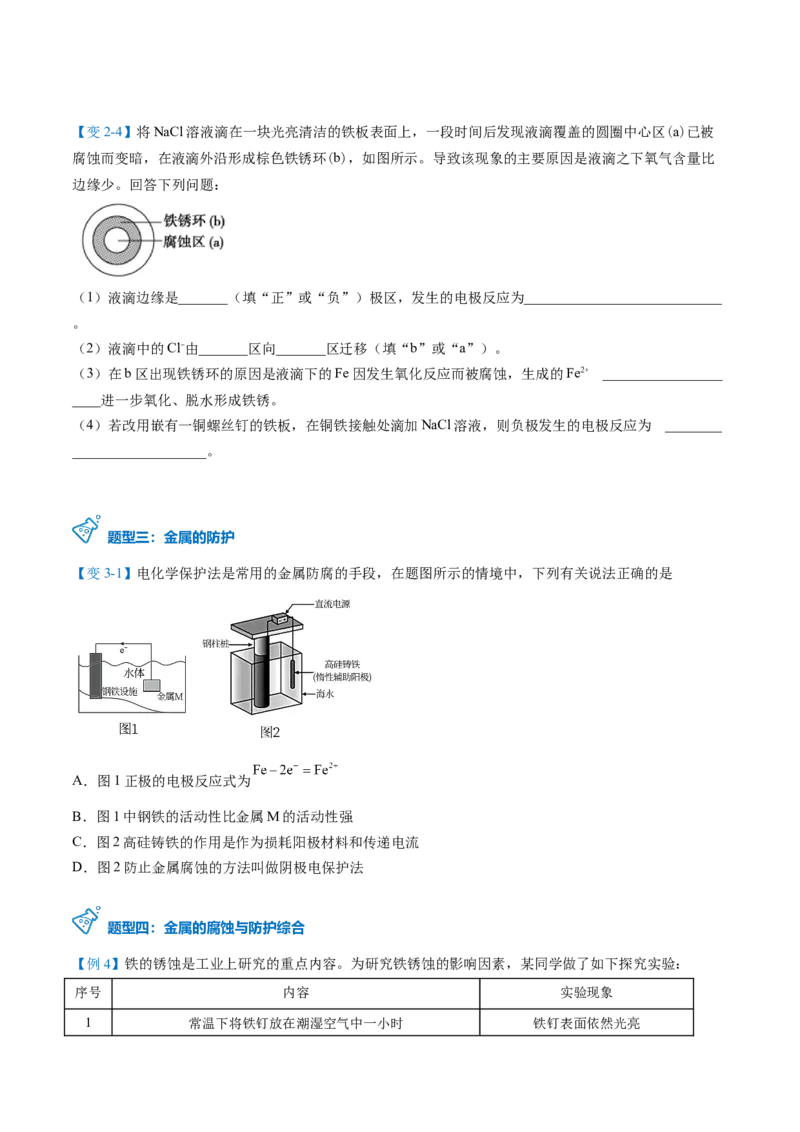
1.电化学防护法
杨sir化学,侵权必究
牺牲阳极的阴极保护法 外加电流的阴极保护法
图示
原理 ________原理 ________原理
被保护的金属作______极, 被保护的金属作为_____极,
电极要求
活泼性更强的金属作______极 与电源的____极相连
应用 锅炉内壁、船舶外壳安装镁合金或锌块 钢铁闸门,地下管道连接电源负极
2.其他保护方法
(1)改变金属组成和结构
把金属制成防腐的合金,如含铬、镍、硅等合金元素的不锈钢具有很好的抗腐蚀性能。
(2)金属表面覆盖保护层
在金属表面覆盖致密的保护层,如喷油漆、涂油脂、镀抗腐蚀金属等。
杨sir化学,侵权必究
四、金属腐蚀快慢规律
同一金属在相同电解质溶液中,腐蚀快慢如下:对点训练
小杨老师 15521324728 侵权必究
题型一:金属的化学腐蚀与电化学腐蚀
杨sir化学,侵权必究
【变1】以下现象与电化学腐蚀无关的是
A.生铁比纯铁容易生锈
B.银质物品久置表面变暗
C.铁质器件附有铜质配件,在接触处易生铁锈
D.黄铜(铜锌合金)制作的铜锣不易产生铜绿
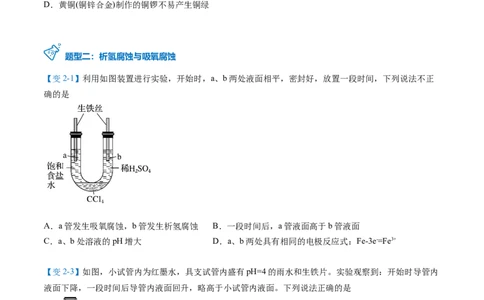
题型二:析氢腐蚀与吸氧腐蚀
杨sir化学,侵权必究
【变2-1】利用如图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间,下列说法不正
确的是
A.a管发生吸氧腐蚀,b管发生析氢腐蚀 B.一段时间后,a管液面高于b管液面
C.a、b处溶液的pH增大 D.a、b两处具有相同的电极反应式:Fe-3e-=Fe3+
【变2-3】如图,小试管内为红墨水,具支试管内盛有pH=4的雨水和生铁片。实验观察到:开始时导管内
液面下降,一段时间后导管内液面回升,略高于小试管内液面。下列说法正确的是
A.生铁片中的碳是原电池的负极,发生还原反应
B.雨水酸性较强,生铁片始终发生析氢腐蚀
C.墨水回升时,碳电极反应式为O+2H O+4e-=4OH-
2 2
D.具支试管中溶液酸性增强【变2-4】将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆圈中心区(a)已被
腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比
边缘少。回答下列问题:
(1)液滴边缘是_______(填“正”或“负”)极区,发生的电极反应为____________________________
。
(2)液滴中的Cl-由_______区向_______区迁移(填“b”或“a”)。
(3)在b区出现铁锈环的原因是液滴下的Fe因发生氧化反应而被腐蚀,生成的Fe2+ _________________
____进一步氧化、脱水形成铁锈。
杨sir化学,侵权必究
(4)若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为 ________
___________________。
题型三:金属的防护
杨sir化学,侵权必究
【变3-1】电化学保护法是常用的金属防腐的手段,在题图所示的情境中,下列有关说法正确的是
A.图1正极的电极反应式为
B.图1中钢铁的活动性比金属M的活动性强
C.图2高硅铸铁的作用是作为损耗阳极材料和传递电流
D.图2防止金属腐蚀的方法叫做阴极电保护法
杨sir化学,侵权必究
题型四:金属的腐蚀与防护综合
杨sir化学,侵权必究
【例4】铁的锈蚀是工业上研究的重点内容。为研究铁锈蚀的影响因素,某同学做了如下探究实验:
序号 内容 实验现象
1 常温下将铁钉放在潮湿空气中一小时 铁钉表面依然光亮2 常温下将铁钉放在潮湿的空气中一个月 铁钉表面已变得灰暗
3 常温下将铁钉放在干燥空气中一个月 干燥的铁钉表面依然光亮
4 将潮湿的铁钉放在常温的氧气流中一小时 铁钉表面略显灰暗
5 将潮湿的铁钉放在高于常温的氧气流中一小时 铁钉表面已变得灰暗
6 将铁钉放在燃煤的厨房中一个月 铁钉表面已变得灰暗
7 将浸过氯化钠溶液的铁钉放在高于常温的氧气流中一小时 铁钉表面灰暗程度比实验5严重
(1)上述实验中发生了吸氧腐蚀的是___________(根据实验现象填序号,下同),正极反应式是
___________;
(2)发生的腐蚀是析氢腐蚀的是___________(填序号)负极反应式是___________。
(3)由该实验可知,可以影响铁锈蚀速率的因素有_____(填两项);
(4)为防止铁的锈蚀,地下埋的水管可采用外加电流的阴极保护法,请列举工业上普遍采用的其它方法
是___________(答两种方法)。
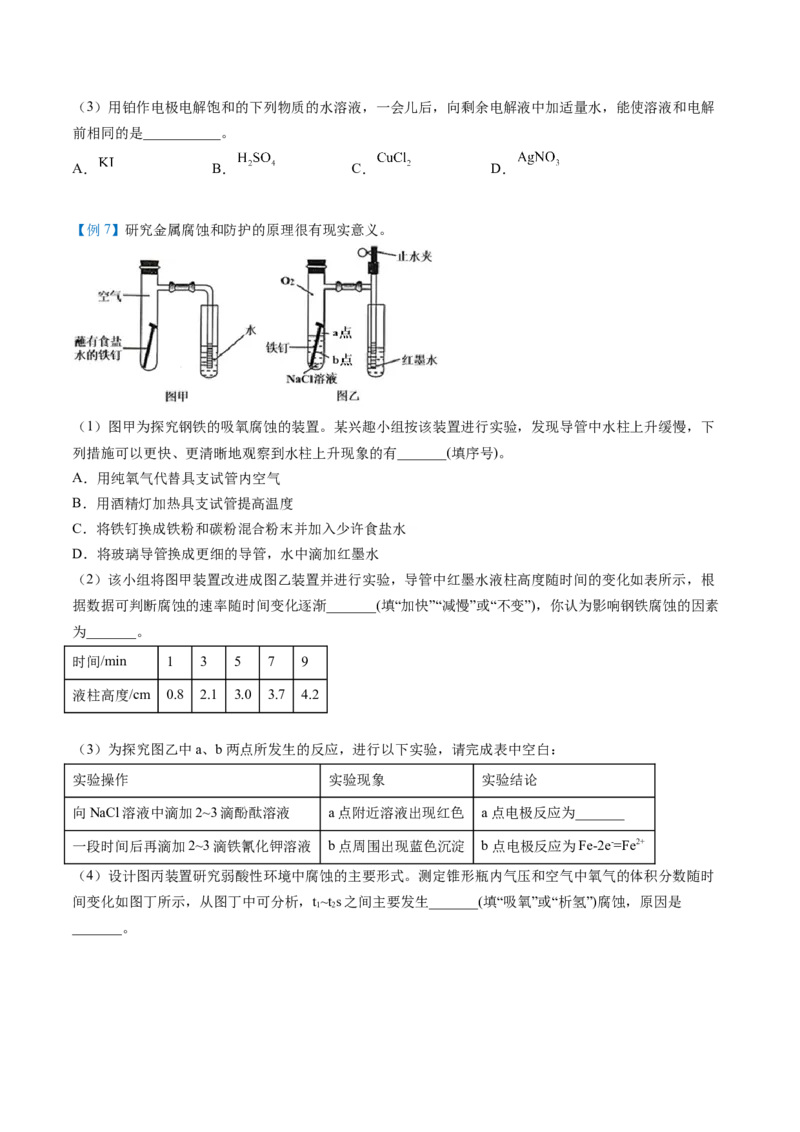
【例5】如图所示,甲、乙两装置电极材料都是铁棒与碳棒,请回答下列问题:
(1)若两装置中均为 溶液,反应一段时间后:
①有红色物质析出的是甲装置中的___________棒,乙装置中的___________棒;
②乙装置的电化学防护法称为___________,其中碳极的电极反应式是:___________。
③取少量甲装置中负极附近溶液加入2滴 溶液,现象为___________,生成沉淀的化学式为
___________。
(2)若两装置中均为饱和 溶液:
①写出乙装置中总反应的离子方程式:___________。
②将湿润的淀粉 试纸放在乙装置碳极附近,发现试纸变蓝,解释其原因___________(3)用铂作电极电解饱和的下列物质的水溶液,一会儿后,向剩余电解液中加适量水,能使溶液和电解
前相同的是___________。
A. B. C. D.
杨sir化学,侵权必究
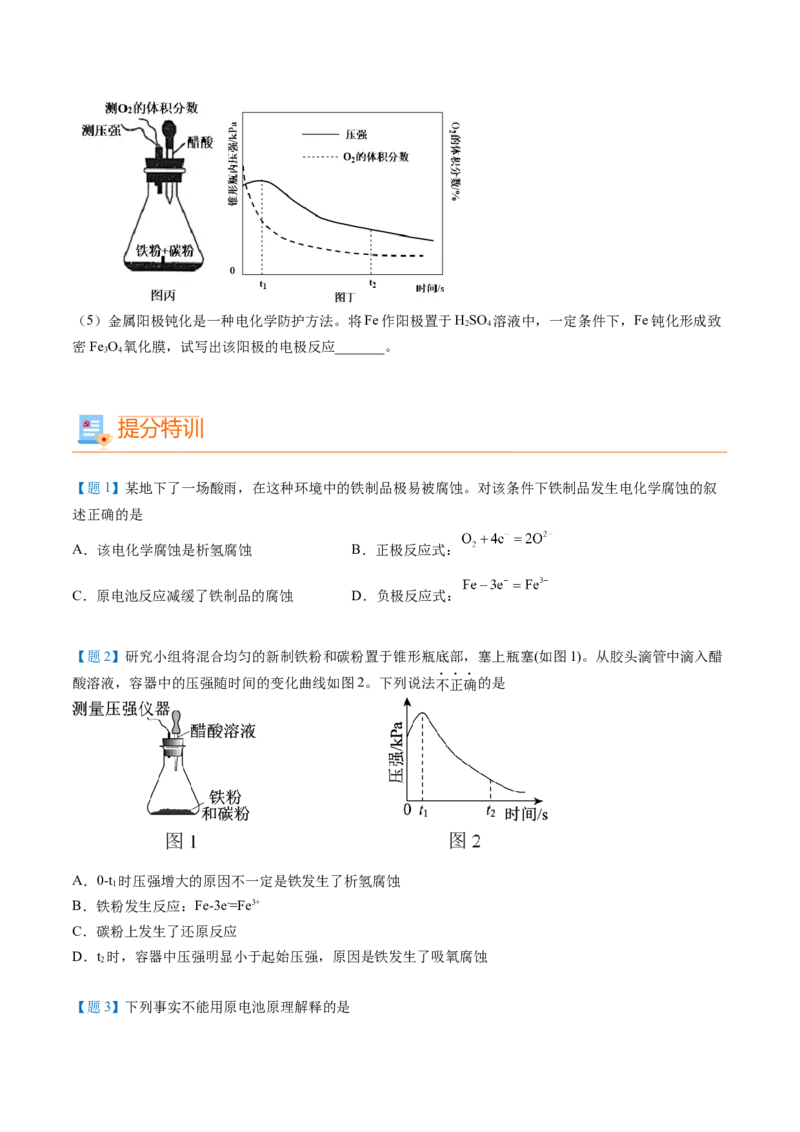
【例7】研究金属腐蚀和防护的原理很有现实意义。
(1)图甲为探究钢铁的吸氧腐蚀的装置。某兴趣小组按该装置进行实验,发现导管中水柱上升缓慢,下
列措施可以更快、更清晰地观察到水柱上升现象的有_______(填序号)。
A.用纯氧气代替具支试管内空气
B.用酒精灯加热具支试管提高温度
C.将铁钉换成铁粉和碳粉混合粉末并加入少许食盐水
杨sir化学,侵权必究
D.将玻璃导管换成更细的导管,水中滴加红墨水
(2)该小组将图甲装置改进成图乙装置并进行实验,导管中红墨水液柱高度随时间的变化如表所示,根
据数据可判断腐蚀的速率随时间变化逐渐_______(填“加快”“减慢”或“不变”),你认为影响钢铁腐蚀的因素
为_______。
时间/min 1 3 5 7 9
液柱高度/cm 0.8 2.1 3.0 3.7 4.2
(3)为探究图乙中a、b两点所发生的反应,进行以下实验,请完成表中空白:
实验操作 实验现象 实验结论
向NaCl溶液中滴加2~3滴酚酞溶液 a点附近溶液出现红色 a点电极反应为_______
一段时间后再滴加2~3滴铁氰化钾溶液 b点周围出现蓝色沉淀 b点电极反应为Fe-2e-=Fe2+
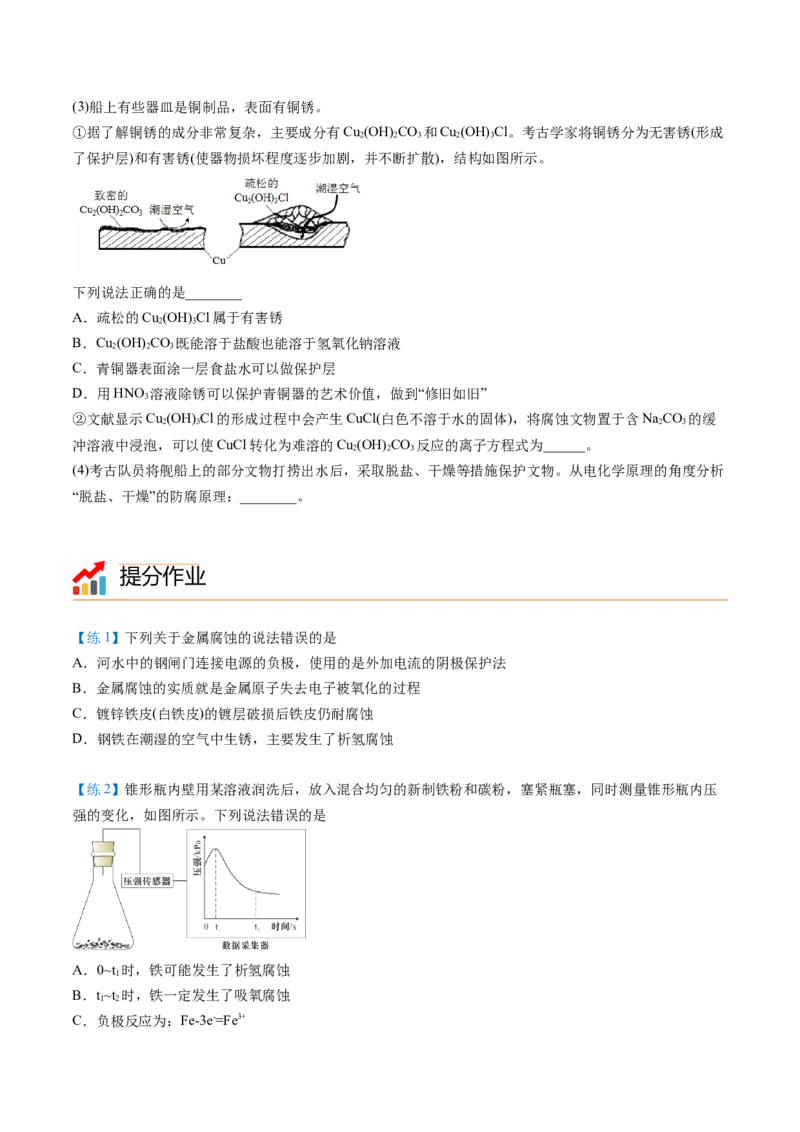
(4)设计图丙装置研究弱酸性环境中腐蚀的主要形式。测定锥形瓶内气压和空气中氧气的体积分数随时
间变化如图丁所示,从图丁中可分析,t~ts之间主要发生_______(填“吸氧”或“析氢”)腐蚀,原因是
1 2
_______。(5)金属阳极钝化是一种电化学防护方法。将Fe作阳极置于HSO 溶液中,一定条件下,Fe钝化形成致
2 4
密Fe O 氧化膜,试写出该阳极的电极反应_______。
3 4
提分特训
小杨老师 15521324728 侵权必究
【题1】某地下了一场酸雨,在这种环境中的铁制品极易被腐蚀。对该条件下铁制品发生电化学腐蚀的叙
述正确的是
A.该电化学腐蚀是析氢腐蚀 B.正极反应式:
C.原电池反应减缓了铁制品的腐蚀 D.负极反应式:
【题2】研究小组将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图1)。从胶头滴管中滴入醋
酸溶液,容器中的压强随时间的变化曲线如图2。下列说法不正确的是
A.0-t 时压强增大的原因不一定是铁发生了析氢腐蚀
1
B.铁粉发生反应:Fe-3e-=Fe3+
C.碳粉上发生了还原反应
D.t 时,容器中压强明显小于起始压强,原因是铁发生了吸氧腐蚀
2
【题3】下列事实不能用原电池原理解释的是A.白铁(镀锌)制品比一般铁器耐腐蚀
B.铁片、铝片在冷的浓硫酸中钝化
C.工程施工队在铁制水管外刷一层“银粉”
杨sir化学,侵权必究
D.纯锌与稀硫酸反应时,滴入少量 溶液后反应速率加快
【题5】深埋在潮湿土壤中的铁管道,在硫酸盐还原菌(一种厌氧微生物,适宜pH为7~8)的作用下,能被
硫酸根离子腐蚀,原理如图。下列有关说法正确的是
A.腐蚀过程中,土壤酸性逐渐增强
B.输送暖气铁管道温度越高,越易发生此类腐蚀
C.正极反应为
杨sir化学,侵权必究
D.管道壁镶嵌锌块或锡块都可保护管道不易被腐蚀
【题7】2018年7月至9月,国家文物局在辽宁开展水下考古,搜寻、发现并确认了甲午海战北洋水师沉
舰——经远舰。已知:正常海水呈弱碱性。
(1)经远舰在海底“沉睡”124年后,钢铁制成的舰体腐蚀严重。舰体发生电化学腐蚀时,负极的电极反应式
为_______。
(2)为了保护文物,考古队员采用“牺牲阳极的阴极保护法”对舰船进行了处理。
①下列说法不正确的是________。
A.锌块发生氧化反应:Zn-2e-=Zn2+
B.舰体有电子流入,可以有效减缓腐蚀
杨sir化学,侵权必究
C.若通过外加电源保护舰体,应将舰体与电源正极相连
D.地下钢铁管道用导线连接锌块与该种舰体保护法原理相同
②采用“牺牲阳极的阴极保护法”后,舰体上正极的电极反应式为_________。(3)船上有些器皿是铜制品,表面有铜锈。
①据了解铜锈的成分非常复杂,主要成分有Cu (OH) CO 和Cu (OH) Cl。考古学家将铜锈分为无害锈(形成
2 2 3 2 3
了保护层)和有害锈(使器物损坏程度逐步加剧,并不断扩散),结构如图所示。
下列说法正确的是________
A.疏松的Cu (OH) Cl属于有害锈
2 3
B.Cu (OH) CO 既能溶于盐酸也能溶于氢氧化钠溶液
2 2 3
C.青铜器表面涂一层食盐水可以做保护层
D.用HNO 溶液除锈可以保护青铜器的艺术价值,做到“修旧如旧”
3
②文献显示Cu (OH) Cl的形成过程中会产生CuCl(白色不溶于水的固体),将腐蚀文物置于含NaCO 的缓
2 3 2 3
冲溶液中浸泡,可以使CuCl转化为难溶的Cu (OH) CO 反应的离子方程式为______。
2 2 3
(4)考古队员将舰船上的部分文物打捞出水后,采取脱盐、干燥等措施保护文物。从电化学原理的角度分析
“脱盐、干燥”的防腐原理:________。
提分作业
小杨老师 15521324728 侵权必究
【练1】下列关于金属腐蚀的说法错误的是
A.河水中的钢闸门连接电源的负极,使用的是外加电流的阴极保护法
B.金属腐蚀的实质就是金属原子失去电子被氧化的过程
C.镀锌铁皮(白铁皮)的镀层破损后铁皮仍耐腐蚀
D.钢铁在潮湿的空气中生锈,主要发生了析氢腐蚀
【练2】锥形瓶内壁用某溶液润洗后,放入混合均匀的新制铁粉和碳粉,塞紧瓶塞,同时测量锥形瓶内压
强的变化,如图所示。下列说法错误的是
A.0~t 时,铁可能发生了析氢腐蚀
1
B.t~t 时,铁一定发生了吸氧腐蚀
1 2
C.负极反应为:Fe-3e-=Fe3+D.用于润洗锥形瓶的溶液一定显酸性
【练3】一定条件下,碳钢腐蚀与溶液pH的关系如下:
pH 2 4 6 6.5 8 13.5 14
腐蚀快慢 较快 慢 较快
主要产物 Fe2+ FeO FeO FeO
3 4 2 3
下列说法不正确的是
A.在pH<4的溶液中,碳钢腐蚀的负极反应式为Fe-2e-=Fe2+
B.在pH>6的溶液中,碳钢主要发生吸氧腐蚀
C.在pH>14的溶液中,碳钢腐蚀的正极反应式为O+4OH-+4e-=2H O
2 2
D.在煮沸除氧气后的碱性溶液中,碳钢腐蚀速率会减慢
杨sir化学,侵权必究
【练4】如图装置中,U形管内为红墨水,a、b试管内分别盛有食盐水和稀醋酸溶液,各加入生铁块,放
置一段时间,下列有关描述错误的是
A.生铁块中的碳是原电池的正极
B.红墨水柱两边的液面为左低右高
C.两试管中相同的电极反应式是: Fe- 2e-=Fe2+
D.a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀
【练5】下列不能有效防止钢铁锈蚀的措施是
A.将钢铁与锌板相连 B.将钢铁置于潮湿的空气中
C.在钢铁表面喷油漆 D.将钢铁与直流电源负极相连
【练6】下列关于电化学腐蚀及防护的说法不正确的是
A.“牺牲阳极的阴极保护法”就是将被保护的钢铁设备连接到外接直流电源的负极
杨sir化学,侵权必究
B.白铁皮是在薄钢板表面镀锌,即便镀层破损,仍然可以保护钢板不被腐蚀
C.在钢铁制品表面喷漆、涂油、镀铬或覆盖搪瓷、塑料都可以避免钢铁腐蚀
D.钢铁表面吸附的溶有氧气的水膜酸性很弱时,仍然以吸氧腐蚀为主
【练7】如图, 水槽中试管内有一枚铁钉,放置数天观察:(1)若液面上升,则溶液呈______性,发生______腐蚀,电极反应式为:负极:______________,正极:
___________________。
(2)若液面下降,则溶液呈________性,发生_________腐蚀,电极反应式为:负极:______________;正
极:__________________。
【练8】金属腐蚀的电化学原理可用下图模拟。
请写出有关电极反应式:
①铁棒上的电极反应式:_______________________
碳棒上的电极反应式:_________________________
(2)该图所表示的是_________________________(填“析氢”或“吸氧”)腐蚀。
(3)若将O 撤走,并将NaCl溶液改为稀HSO 溶液,则此图可表示__________(填“析氢”或“吸氧”)腐蚀原理;
2 2 4
若用牺牲阳极法来保护铁棒不被腐蚀溶解,即可将碳棒改为_________棒。
杨sir化学,侵权必究
【练9】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。
I.如图装置中,U 形管内为红墨水,a、b 试管内分别盛有氯化铵(显酸性)溶液和食盐水,各加入生铁
块,放置一段时间均被腐蚀,这两种腐蚀都属于____腐蚀。
(1)红墨水柱两边的液面变为左低右高,则_____(填“a”或“b”)边盛有食盐水。
(2)b 试管中铁发生的是_____腐蚀。
II.下面两个图都是金属防护的例子。(3)为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材
料R 可以采用_______(从下面选项中选择),此方法叫做_____保护法。 A.铜 B.钠 C.
锌 D.石墨
(4)图乙方案也可以降低铁闸门腐蚀的速率,其中铁闸门应该连接在直流电源的______极。
(5)采取以上两种方法,_________(填“甲”或“乙”)种能使铁闸门保护得更好。
杨sir化学,侵权必究倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育