文档内容
第 22 讲 沉淀溶解平衡的应用
知识导航
小杨老师 15521324728 侵权必究
知识精讲
小杨老师 15521324728 侵权必究
一、沉淀的生成
1.应用
在无机物的制备和提纯、废水处理等领域,常利用生成沉淀来达到分离或除去某些离子的目的。
杨sir化学,侵权必究
2.方法
方法 实例 操作及原理
除去NHCl中的FeCl
溶于水,加氨水调节pH:Fe3++3NH·HO===Fe(OH)↓+3NH+
4 3 3 2 3 4
调节pH法
加入Cu(OH) 或CuO,①Fe3+ + 3HO ⇌ Fe(OH) + 3H+
2 2 3
除去CuCl 中的FeCl
2 3
②Cu(OH) + 2H+ === Cu2+ + 2HO CuO+ 2H+ === Cu2+ + 2HO
2 2 2
除去废水中的Hg2+ 加入NaS:S2- + Hg2+ === HgS↓
2
沉淀剂法
除去废水中的Cu2+ 通入HS:HS + Cu2+=== CuS↓ + 2H+
2 2
二、沉淀的溶解
1.原理
根据平衡移动原理,对于在水中难溶的电解质,如果能设法不断地移去平衡体系中的相应离子,使平衡向
沉淀溶解的方向移动,就可以使沉淀溶解。如:2.Mg(OH) 沉淀溶解实验
2 杨sir化学,侵权必究
实验操作
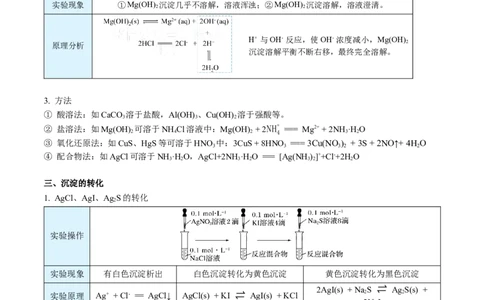
实验现象 ①Mg(OH) 沉淀几乎不溶解,溶液浑浊;②Mg(OH) 沉淀溶解,溶液澄清。
2 2
H+ 与OH- 反应,使OH- 浓度减小,Mg(OH)
原理分析 2
沉淀溶解平衡不断右移,最终完全溶解。
3. 方法
① 酸溶法:如CaCO 溶于盐酸,Al(OH) 、Cu(OH) 溶于强酸等。
3 3 2
② 盐溶法:如Mg(OH) 可溶于NH Cl溶液中:Mg(OH) + 2NH+ === Mg2+ + 2NH ·H O
2 4 2 4 3 2
③ 氧化还原法:如CuS、HgS等可溶于HNO 中:3CuS + 8HNO === 3Cu(NO ) + 3S + 2NO↑+ 4H O
3 3 3 2 2
④ 配合物法:如AgCl可溶于NH ·H O,AgCl+2NH·H O === [Ag(NH)]++Cl-+2H O
3 2 3 2 3 2 2
三、沉淀的转化
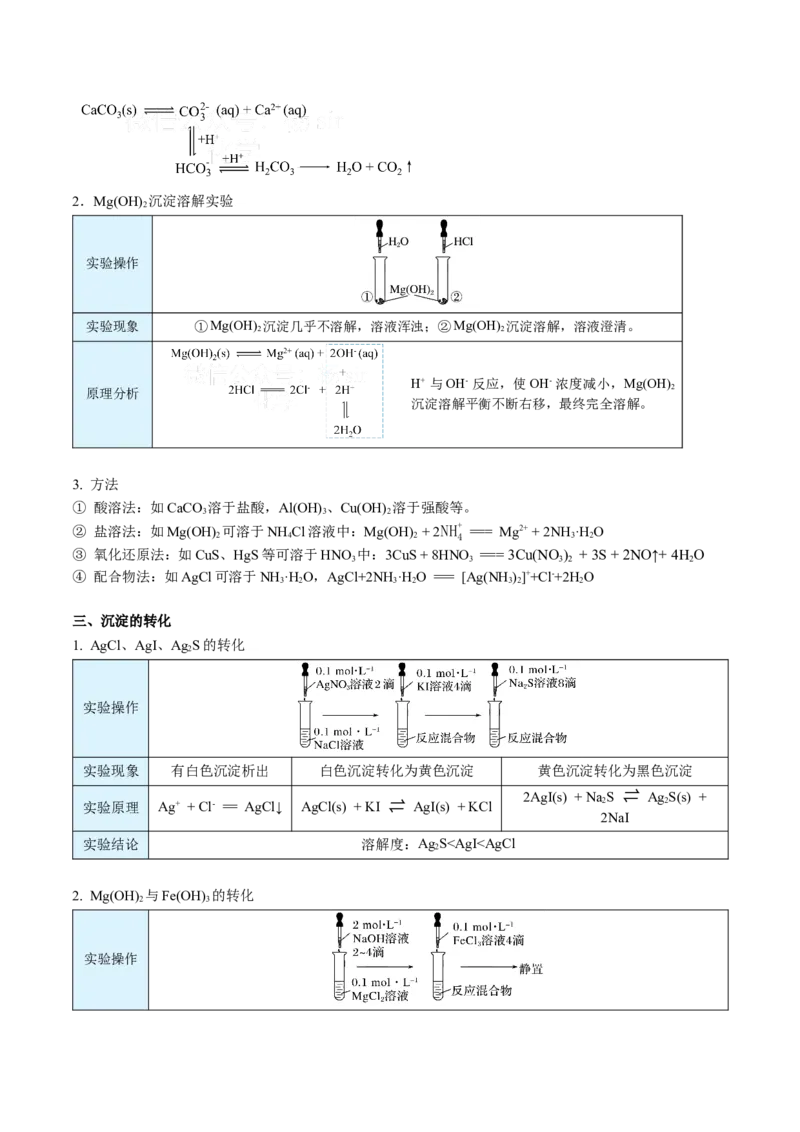
1. AgCl、AgI、Ag S的转化
2 杨sir化学,侵权必究
实验操作
实验现象 有白色沉淀析出 白色沉淀转化为黄色沉淀 黄色沉淀转化为黑色沉淀
2AgI(s) + Na S ⇌ Ag S(s) +
实验原理 Ag+ + Cl- == AgCl↓ AgCl(s) + KI ⇌ AgI(s) + KCl 2 2
2NaI
实验结论 溶解度:Ag SK (CuS)>K (HgS),因此
sp sp sp sp sp
先沉淀,故答案为C。
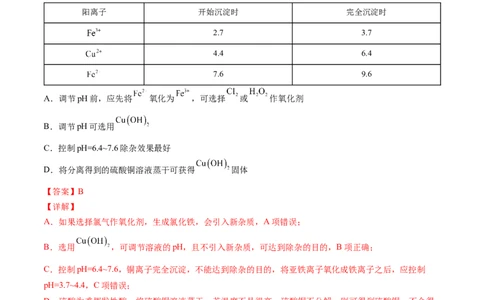
【例2】利用调节pH的方法,可以除去硫酸铜溶液中的亚铁离子(已知:在一定条件下,某些常见阳离子
沉淀时对应的pH如表所示),下列说法正确的是
阳离子 开始沉淀时 完全沉淀时
2.7 3.7
4.4 6.4
7.6 9.6
A.调节pH前,应先将 氧化为 ,可选择 或 作氧化剂
B.调节pH可选用
C.控制pH=6.4~7.6除杂效果最好
D.将分离得到的硫酸铜溶液蒸干可获得 固体
【答案】B
【详解】
A.如果选择氯气作氧化剂,生成氯化铁,会引入新杂质,A项错误;
B.选用 ,可调节溶液的pH,且不引入新杂质,可达到除杂的目的,B项正确;
C.控制pH=6.4~7.6,铜离子完全沉淀,不能达到除杂的目的,将亚铁离子氧化成铁离子之后,应控制
pH=3.7~4.4,C项错误;
D.硫酸为难挥发性酸,将硫酸铜溶液蒸干,若温度不是很高,硫酸铜不分解,则可得到硫酸铜,不会得
到 ,D项错误;
故选B。
【变2-2】钴在硬质高温合金、催化剂等高新技术领域有广泛应用。从某炼锌厂的废渣(含Zn、Co、Fe、
ZnO、SiO 等)中回收钴的一种工艺流程如图:
2相关金属离子[Co(Mn+ )=0.1mol·L-1]形成氢氧化物沉淀的pH范围如表:
金属离子 Co2+ Fe2+ Fe3+ Zn2+
开始沉淀的pH 7.15 6.3 1.5 6.2
沉淀完全的pH 9.15 8.3 2.8 8.2
(1)若无氧化步骤,对实验的影响是_____。试剂X可以为下列物质中的_____。
A.KOH B.Zn(OH) C.ZnO D.NaCO
2 2 3
(2)常温下,已知Co(OH) 的溶度积常数为K ,则Co3+完全沉淀时[c(Co3+)<10-5mol·L-1],溶液的pH至少
3 sp
为_____(用含K 的式子表示)。
sp
【答案】
(1) 无法有效除铁 BC
(2)14+lg
【分析】
废渣(含Zn、Co、Fe、ZnO、SiO 等)其中二氧化硅不溶于酸,滤渣1为SiO,溶液中含有锌离子,亚铁离
2 2
子,钻离子,经双氧水氧化后,亚铁离子转化为三价铁离子,调节pH 值使三价铁离子转化为氢氧化铁沉
淀,加入有机溶剂经过萃取分液,水相中为钴离子,有机相为锌离子,操作2是蒸发浓缩、冷却结晶、过
滤、洗涤,干燥,据此分析解题;
(1)
若无氧化步骤,亚铁离子不能转化为三价铁离子,对实验的影响是无法有效除铁;加入试剂X的目的调节
pH,三价铁离子转化为氢氧化铁沉淀,但是不能引入杂质,产物中与硫酸锌生成,可以加入含锌,能消耗
氢离子的,可以是氧化锌和氢氧化锌,故选BC;
(2)
常温下,Co(OH) 的溶度积常数为K ,则Co3+完全沉淀时[c(Co3+)<10-5mol·L-1],溶液的c(OH-)=
3 sp
,pH至少为14+1g ;
题型二:沉淀的转化
杨sir化学,侵权必究【变3-1】已知: 时, 的溶度积分别为 .下列说法正确
的是
A.可溶性硫化物可作为处理上述金属离子的沉淀剂
B.上述三种物质溶解度最小的是
杨sir化学,侵权必究
C.在硫化铜悬浊液中滴加几滴 溶液,会生成 沉淀
D.向含 均为 的溶液中通入 气体,产生沉淀的顺序依次为
【答案】A
【详解】
A.硫化钠能够与Hg2+、Cu2+、Pb2+离子反应生成难溶物CuS、PbS、HgS,所以硫化钠是处理废水中含上
述金属离子的沉淀剂,A正确;
B.CuS、PbS、HgS为相同类型的难溶物,可通过它们的溶度积直接判断溶解度大小,根据题干信息可知,
溶解度最小的、最难溶的为HgS,B错误;
C.K (PbS)>K (CuS),所以CuS比PbS更难溶,在硫化铜悬浊液中滴几滴硝酸铅溶液,不一定会
sp sp
转化为PbS,需要浓度较大才能发生转化,C错误;
D.CuS、PbS、HgS为相同类型的难溶物,可通过它们的溶度积直接判断溶解度大小,根据题干信息可知,
溶解度最小的、最难溶的为HgS,溶度积最大、最后生成沉淀的为PbS,所以产生沉淀的顺序依次为
HgS、CuS、PbS,D错误;
故答案为:A。
题型三:沉淀转化的应用
杨sir化学,侵权必究
【变4-1】不法分子曾用含有可溶性钡盐的工业废盐腌制咸鸭蛋而引发了钡盐中毒事件。根据资料得知,
当胃液中Ba2+浓度小于10-4mol·Lˉ1时,可以达到解毒目的。已知:K (BaSO)=1.1×10-10、
sp 4
K (BaCO )=2.6×10-9。下列有关说法错误的是( )
sp 3
A.可溶性钡盐使人体蛋白质变性引起中毒
B.误食碳酸钡不会引起中毒
C.医学上用0.38mol·Lˉ1的硫酸钠溶液给患者洗胃,可以达到有效解毒效果
D.BaSO 在一定条件下也可以转化为BaCO
4 3
【答案】B
【解析】A项,钡离子属于重金属离子,可使蛋白质变性而引发中毒,则可溶性钡盐能使人体蛋白质变性
引起中毒,故A正确;B项,人体胃酸的成分是盐酸,误食碳酸钡会与胃酸反应转化为可溶性的氯化钡,
能使人体蛋白质变性引起中毒,故B错误;C项, ,=2.9×10-10mol/L<10-4mol·Lˉ1,则医学上用0.38mol·Lˉ1的硫酸钠溶液
给患者洗胃,可以达到有效解毒效果,故C正确;D项,根据溶度积常数可知,BaSO 比BaCO 跟难溶,
4 3
但在饱和的碳酸钠溶液中,硫酸钡溶解在水中的钡离子可与碳酸根离子结合形成碳酸钡沉淀,则在一定条
件下BaSO 也可以转化为BaCO ,故D正确;故选B。
4 3
【变4-2】自然界地表层原生铜的硫化物经氧化、淋滤作用后变成CuSO 溶液,向地下深层渗透,遇到难
4
溶的ZnS或PbS,慢慢转变为铜蓝(CuS)。下列分析正确的是
A.CuS的溶解度大于PbS的溶解度
B.原生铜的硫化物具有还原性,而铜蓝没有还原性
C.CuSO 与ZnS反应的离子方程式是Cu2++S2-=CuS↓
4
D.整个过程涉及的反应类型有氧化还原反应和复分解反应
杨sir化学,侵权必究
【答案】D
【详解】
A.难溶性物质在水溶液中存在沉淀溶解平衡,PbS(s) Pb2+(aq)+S2-(aq),当向该溶液中加入含有Cu2+的
物质时,由于K (CuS)<K (PbS),所以会形成CuS沉淀,发生沉淀的转化,由难溶解的向更难溶解的物质
sp sp
转化。由于二者的化学组成相似,所以CuS的溶解度小于PbS的溶解度,A项错误;
B.自然界地表层原生铜的硫化物被氧化、淋滤作用后变成CuSO 溶液,说明原生铜的硫化物具有还原性,
4
在CuS中S是-2价,也具有还原性,B项错误;
C.ZnS难溶于水,因此CuSO 与ZnS反应的离子方程式是Cu2++ZnS=CuS+Zn2+,C项错误;
4
D.在整个过程中既有电子转移的氧化还原反应,也有沉淀转化的复分解反应,D项正确;
故选D。
【例6】锂被誉为“高能金属”,废旧锂离子电池的正极材料主要含有LiCoO 及少量Al、Fe等,处理该
2
废料的一种工艺流程如图所示:
已知:① ,LiCoO 难溶于水,具有强氧化性(且氧化性强于KMnO );
2 4
②相关金属离子形成氢氧化物沉淀的pH值如表所示:
杨sir化学,侵权必究
金属离子 Al3+ Fe3+ Fe2+ Co2+
开始沉淀的pH 4.0 2.7 7.6 7.0
沉淀完全的pH 5.2 3.7 9.6 9.0回答下列问题::
(1)写出“碱溶”时发生主要反应的化学方程式:___________。
(2)为提高“酸溶”的浸出速率,可采取的措施有___________(任写一种)。
(3)“酸溶”时,LiCoO 能将HO 氧化,其离子方程式为___________;若用浓盐酸代替HSO 和HO
2 2 2 2 4 2 2
的混合液,缺点是___________。
(4)用氨水调节pH的范围为___________。
(5)该流程涉及多次过滤,实验室中过滤后洗涤沉淀的操作为___________。
(6)写出“沉钴”过程中发生反应的离子方程式:___________。
【答案】
(1)2Al+2NaOH+2H O=2Na AlO +3H
2 2 2
(2)升高温度(增大双氧水的浓度)
(3) 2LiCoO + H O+6H+=2Li++2Co2++4H O+ O ↑ Cl-易被氧化成Cl,污染空气
2 2 2 2 2 2
(4)3.7 pH<7.0
(5)沿玻璃棒向漏斗中注入少量蒸馏水,使水面没过沉淀物,待水滤去后,再加水蒸馏洗涤,连续洗2
3次
(6)Co2++2HCO =CoCO ↓+CO ↑+H O
3 2 2
【解析】
(1)
废旧锂离子电池的正极材料主要含有LiCoO 及少量Al、Fe等,加碱时Al发生反应,其反应的化学方程式:
2
2Al+2NaOH+2H O=2Na AlO +3H ,故答案:2Al+2NaOH+2H O=2Na AlO +3H
2 2 2 2 2 2
(2)
为提高“酸溶”的浸出速率,可增大双氧水的浓度,或者升高温度,故答案:升高温度(增大双氧水的浓
度)。
(3)
通过题给信息可知:LiCoO 难溶于水,具有强氧化性,且氧化性强于KMnO ,所以酸溶时LiCoO 能将
2 4 2
HO 氧化,其离子方程式为2LiCoO + H O+6H+=2Li++2Co2++4H O+ O ↑。若用浓盐酸代替HSO 和HO 的
2 2 2 2 2 2 2 2 4 2 2
混合液,Cl-易被氧化成Cl,污染空气。故答案:2LiCoO + H O+6H+=2Li++2Co2++4H O+ O ↑;Cl-易被氧化
2 2 2 2 2 2
成Cl,污染空气。
2
(4)
用氨水调节pH值,是为了除去铁离子,留下钴离子,根据相关金属离子形成氢氧化物沉淀的pH值表可知,
沉淀完全时的pH就是3.7 pH<7.0,故答案:3.7 pH<7.0。
(5)
沉淀的洗涤操作是:沿玻璃棒向漏斗中注入少量蒸馏水,使水面没过沉淀物,待水滤去后,再加水蒸馏洗
涤,连续洗2 3次,直至沉淀物洗净为止。故答案:沿玻璃棒向漏斗中注入少量蒸馏水,使水面没过沉淀物,待水滤去后,再加水蒸馏洗涤,连续洗2 3次。
(6)
在浸液中通入氨气除去铁离子,在加入碳酸氢铵,沉钴过程中是CoSO 与NH HCO 反应,得到CoCO 沉
4 4 3 3
淀,根据原子守恒,该反应的离子方程式为:Co2++2HCO =CoCO ↓+CO ↑+H O。故答案:Co2++2HCO
3 2 2
=CoCO ↓+CO ↑+H O。
3 2 2
提分特训
小杨老师 15521324728 侵权必究
【题1】在1L0.01mol·L-1MgCl 溶液中,加入1mL0.01mol·L-1的NaCO 溶液,下列说法正确的是(已知
2 2 3
MgCO 的K =6.8×10-6mol2·L-2) ( )
3 sp
A.有MgCO 沉淀析出 B.无MgCO 沉淀析出
3 3
C.无法确定 D.有沉淀但不是MgCO
3
【答案】B
【解析】在1L 0.01mol·L-1 MgCl 溶液中,加入1mL 0.01mol·L-1的NaCO 溶液,混合溶液体积可近似为
2 2 3
1L,所得溶液中c(Mg2+)=0.01 mol·L-1,c(CO2-)= =1×10-5 mol·L-1,c(Mg2+)× c(CO2-)=
3 3
0.01 mol·L-1×1×10-5 mol·L-1=1×10-7 mol2·L-2<K [Mg(OH) ],所以无沉淀析出,故选B。
sp 2
【题2】往锅炉注入NaCO 溶液浸泡,将水垢中的CaSO 转化为CaCO ,再用盐酸去除,下列叙述中正确
2 3 4 3
的是( )
A.温度升高,NaCO 溶液的K 和c(H+)均会增大
2 3 w
B.CaSO 能转化为CaCO ,说明K (CaCO)>K (CaSO)
4 3 sp 3 sp 4
C.CaCO 溶解于盐酸而CaSO 不溶,是因为硫酸酸性强于盐酸
3 4
D.沉淀转化的离子方程式为CO(aq)+CaSO(s) CaCO (s)+SO(aq)
4 3
【答案】D
【解析】温度升高,水的电离平衡正向移动,K 增大;温度升高,NaCO 的水解平衡正向移动,[OH-]增
w 2 3
大,[H+]减小,A项错误;K (CaCO)<K (CaSO),B项错误;CaCO 与盐酸反应生成可溶性的氯化钙、
sp 3 sp 4 3
水和二氧化碳,CaSO 与盐酸不满足复分解反应发生的条件,与酸性强、弱无关,C项错误;硫酸钙较为
4
致密,可转化为较为疏松且溶解度更小的碳酸钙,反应的离子方程式为 CaSO(s)+CO(aq) CaCO (s)
4 3
+SO(aq),D项正确。
【题3】已知,Fe2+结合S2-的能力大于结合OH-的能力,而Al3+则正好相反。在Fe (SO ) 和AlCl 的混合溶
2 4 3 3
液中,先加入过量的KI溶液,再加入足量的NaS与氨水的混合溶液,所得沉淀是
2
A.Al S、FeS和S B.FeS和Al(OH) C.Fe S 和Al(OH) D.FeS、Al(OH) 和S
2 3 3 2 3 3 3
【答案】D
【详解】
在Fe (SO ) 和AlCl 的混合溶液中加过量KI,先是Fe (SO ) 与KI发生氧化还原反应:2Fe3++2I-=2Fe2+
2 4 3 3 2 4 3
+I,反应完后溶液中含大量Fe2+、Al3+、I,再加入NaS与氨水的混合溶液后,溶液有大量S2-、OH-,依
2 2 2题意知,Fe2+结合S2-能力强,两盐发生复分解反应,形成FeS沉淀,Al3+结合OH-能力强,但由于I 的存在
2
发生:I+S2-=S↓+2I-,所以最终得到的沉淀是FeS、Al(OH) 和S的混合物。
2 3
故选D。
【题4】已知表数据:
物质 Fe(OH) Cu(OH) Fe(OH)
2 2 3
K (25℃) 8.0×10-16 2.2×10-20 4.0×10-38
sp
完全沉淀时的pH 9.6 6.4 3.4
对含等物质的量的CuSO 、FeSO 、Fe (SO ) 的混合溶液的说法,不正确的是
4 4 2 4 3
A.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
B.该溶液中c(SO ):[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5:4
杨sir化学,侵权必究
C.向该溶液中加入适量氯水,并调节pH到3.4后过滤,可获得纯净的CuSO 溶液
4
D.在pH=5的溶液中Fe3+不能大量存在
【答案】C
【详解】
A.从表格中可以看出,Fe(OH) 的Ksp是最小的,所以它最先出现沉淀,故A正确;
3
B.因为Cu2+、Fe2+、 Fe3+对应的碱全是弱碱,所以这三种离子在溶液中都会发生水解,因此它们的物质的
量会减少,故B正确;
C.加入氯水,可以把亚铁离子全氧化成三价,但它的还原产物Cl-肯定还在溶液中,而且在调节pH时加
入的试剂也会在溶液中有所保留,所以得到的溶液中不可能只含CuSO 一种溶质,故C错误;
4
D.在pH = 5的溶液中c(H+)= 10-5moL/L,c(Fe3+)=. ,Fe3+不能大量存在,
故D正确;
故答案:C。
【题5】向盛有硝酸银溶液的试管中加入氨水,首先形成难溶物,继续滴加氨水,难溶物溶解得到无色透
明溶液,下列说法正确的是
A.反应后溶液中没有沉淀,所以反应前后 的浓度不变
B.沉淀溶解后,生成的 难电离
C.在 中, 给出孤对电子, 提供空轨道
D.该实验能证明 比 稳定
【答案】D【分析】
氨水呈碱性,向盛有硝酸银水溶液的试管里加入氨水,首先形成难溶物,Ag++OH-=AgOH↓,继续添加氨
水,难溶物溶解得到无色的透明溶液,发生:AgOH+2NH=[Ag(NH )]++OH-,据此分析判断。
3 3 2
【详解】
A.反应后形成[Ag(NH)]+络离子,该离子较稳定难电离,所以Ag+的浓度减小,故A错误;
3 2
B.[Ag(NH)]OH为强电解质,完全电离[Ag(NH)]OH=[Ag(NH )]++OH-,故B错误;
3 2 3 2 3 2
C.在配合离子[Ag(NH)]+ 中,Ag+提供空轨道,NH 提供孤电子对,形成配位键,故C错误;
3 2 3
D.氨水呈碱性,向盛有硝酸银水溶液的试管里加入氨水,首先形成难溶物,Ag++OH-=AgOH↓,继续添加
氨水,难溶物溶解得到无色的透明溶液,发生:AgOH+2NH=[Ag(NH )]++OH-,氢氧化银沉淀能转化为络
3 3 2
合物离子[Ag(NH)]+,说明[Ag(NH)]+比氢氧化银稳定,故D正确;
3 2 3 2
故选D。
【题7】(2021·广东广州市质检)根据化学平衡理论,请回答下列几个问题:
(1)某温度(t℃)时,水中c(H+)和c(OH-)的关系如图所示,a点水的离子积K =___________。该温度下,
w
pH=12的NaOH溶液与pH=2的HSO 溶液等体积混合,溶液显___________(填“酸”或“碱”或“中”)性。
2 4
(2)向含有酚酞的0.1mol·L−1的氨水中加入少量NH Cl固体,观察到的现象是___________,请结合离子方程
4
式分析产生该现象的主要原因是:___________。
(3)将体积相等的NaOH稀溶液和CHCOOH溶液混合,若溶液呈中性,则溶液中c(Na+)______c(CHCOO-)
3 3
(填“>”“<”或“=”),则混合前c(NaOH)_______c(CHCOOH)(填“>”“<”或“=”)。
3 杨sir化学,侵权必究
(4)为配制SbCl 溶液,取少量SbCl 固体溶于2~3mL水中,观察到有白色沉淀生成,为避免出现该现象,
3 3
配制SbCl 溶液的正确方法是___________。
3
(5)25℃时,已知K [Cu(OH) ]=2×10−20,要使c(Cu2+)=0.2mol·L−1溶液中的Cu2+沉淀较完全[残留在溶液中的
sp 2
c(Cu2+)降低到2×10−4mol·L−1],则应加入NaOH溶液调节pH为___________。
【答案】(1)1×10−12 碱 (2)红色的溶液颜色变浅 NH ·H O NH ++OH-;加入NH Cl固体,
3 2 4 4
c(NH +)增大,平衡向左移动,c(OH-)减小,因此溶液颜色由红色变浅
4
(3)= <
(4)先将SbCl 固体溶解在较浓的盐酸中,再加水稀释到所需浓度 (5)6
3
【解析】(1)根据图中信息得到某温度(t℃)时a点水的离子积
。该温度下,pH=12的NaOH溶液即氢氧根物质的量
浓度c(OH-)=1.0mol∙L−1,pH=2的HSO 溶液即氢离子物质的量浓度为c(H+)=1.0×10−2mol∙L−1,pH=12的
2 4NaOH溶液与pH=2的HSO 溶液等体积混合,则氢氧根的物质的量大于氢离子物质的量,因此溶液显碱性;
2 4
(2)向含有酚酞的0.1mol·L−1的氨水中加入少量NH Cl固体,铵根离子浓度增大,氨水电离平衡逆向移动,
4
氢氧根浓度减小,因此观察到的现象是红色的溶液颜色变浅,请结合离子方程式分析产生该现象的主要原
因是:NH ·H O NH ++OH-;加入NH Cl固体,c(NH +)增大,平衡向左移动,c(OH-)减小,因此溶
3 2 4 4 4
液颜色由红色变浅;故答案为:NH ·H O NH ++OH-;加入NH Cl固体,c(NH +)增大,平衡向左移动,
3 2 4 4 4
c(OH-)减小,因此溶液颜色由红色变浅。(3)将体积相等的NaOH稀溶液和CHCOOH溶液混合,混合后溶
3
液呈中性,再根据电荷守恒得到溶液中c(Na+)=c(CHCOO-);若浓度相等、体积相等混合,则生成醋酸钠,
3
醋酸钠中醋酸根水解显碱性,而要使混合溶液呈中性,则还需加酸,由于体积相等,因此混合前c(NaOH)
<c(CHCOOH)。(4)根据题意为配制SbCl 溶液,避免出现有白色沉淀生成,主要是加盐酸来抑制SbCl 水
3 3 3
解,因此配制SbCl 溶液的正确方法是先将SbCl 固体溶解在较浓的盐酸中,再加水稀释到所需浓度;(5)根
3 3
据题意得出 ,
, ,则pH=6。
提分作业
小杨老师 15521324728 侵权必究
【练1】工业上向锅炉里注入NaCO 溶液浸泡,将水垢中的CaSO 转化为CaCO ,而后用盐酸去除。下列
2 3 4 3
叙述不正确的是( )
A.温度升高,NaCO 溶液的K 和c(OH-)均会增大
2 3 w
B.沉淀转化的离子方程式为CO2- (aq)+CaSO (s) CaCO (s)+SO 2- (aq)
3 4 3 4
C.盐酸溶液中,CaCO 的溶解性大于CaSO
3 4
D.NaCO 溶液遇CO 后,阴离子浓度均减小
2 3 2
【答案】D
【解析】A项,温度升高,K 增大,温度升高促进碳酸钠溶液水解,c(OH-)增大,A正确;B项,加入碳
w
酸钠溶液,把硫酸钙转化为碳酸钙:CO2- (aq)+CaSO (s) CaCO (s)+SO 2- (aq),B正确;C项,因
3 4 3 4
为碳酸钙与盐酸反应,而硫酸钙不与盐酸反应,所以在盐酸溶液中碳酸钙的溶解性大于硫酸钙,C正确;
D项,根据CO2-+CO +H O=2HCO -知,阴离子HCO -的浓度增大,D错误;故选D。
3 2 2 3 3
【练2】下列应用或现象主要体现的是沉淀溶解平衡原理的是
①可用FeS除去废水中的Cu2+
②溶洞的形成
③误将钡盐[BaCl 、Ba(NO )]当作食盐食用后,常用0.5%的NaSO 溶液解毒
2 3 2 2 4
④碳酸钡不能作“钡餐”而硫酸钡能
杨sir化学,侵权必究
⑤泡沫灭火器灭火
A.①③④ B.②③⑤ C.③④⑤ D.①②③④
【答案】D【详解】
①因CuS比FeS更难溶于水,所以在含有Cu2+的废水中,加入FeS,Cu2+和S2-会生成更难溶的CuS沉淀,
促进了FeS的溶解,此过程存在沉淀溶解平衡,故①符合题意。
②形成溶洞的地貌中岩石的主要成分是碳酸钙,遇到溶有二氧化碳的水,碳酸根离子会和二氧化碳和水生
成碳酸氢根离子,从而促进碳酸钙溶解,此过程存在沉淀溶解平衡,故②符合题意。
③钡离子和硫酸根离子反应生成不溶于酸和水的硫酸钡,即易溶性的物质能向难溶性的物质转化,所以可
以用沉淀溶解平衡原理来解释,故③符合题意。
④胃酸的成分是盐酸,硫酸钡和盐酸不反应,但盐酸能使碳酸钡转化为可溶的氯化钡,此过程存在沉淀溶
解平衡,故④符合题意。
⑤泡沫灭火器所装试剂是碳酸氢钠和硫酸铝,,碳酸氢钠和硫酸铝相互促进水解,从而迅速产生二氧化碳,
所以可以用盐类水解原理来解释泡沫灭火器灭火的原理,故⑤不符合题意。
综上所述,①②③④符合题意,本题答案D
【练3】某炼铁废渣中含有大量CuS及少量铁的化合物,工业上以该废渣为原料生产CuCl ▪2H O晶体的工
2 2
艺流程如图,下列说法错误的是
A.焙烧后的废气能使酸性高锰酸钾溶液褪色
B.氧化步骤中,用双氧水代替氯气会更好
C.调节pH选用的试剂可以是CuO固体
D.CuCl ▪2H O晶体直接加热可制得CuCl 固体
2 2 2
【答案】D
【详解】
A. 焙烧后的废气中含有二氧化硫,能与酸性高锰酸钾溶液发生氧化还原反应而使之褪色,A正确;
B. 由图知,氧化的目的是把亚铁离子氧化为铁离子,而双氧水的还原产物为水,且过量的双氧水也不会
污染环境,所以用双氧水代替氯气会更好,B正确;
C. 调节pH选用的试剂应该可以和氢离子反应,且不引入新的杂质,可以用氧化铜、氢氧化铜或碳酸铜,
C正确;
D.将CuC1 ▪2H O晶体加热,铜离子会发生水解,所以应该在氯化氢气氛中加热才能得到CuCl 固体, D
2 2 2
错误;
答案选D。
【练4】已知常温下 , ,下列有关说法正确的是
A.常温下, 在纯水中的 比在 溶液中的 大B.向 与 的悬浊液中加入几滴浓 溶液, 不变
C.在 的饱和溶液中通入 ,有 析出,且溶液中
杨sir化学,侵权必究
D.向 、 的混合溶液中滴入几滴 溶液,出现黄色沉淀,此现象可验证
【答案】B
【详解】
A. 只随温度的改变而改变,所以二者 相等,A项错误;
B. 与 的悬浊液在滴入几滴浓 溶液后,仍是二者的饱和浴液
,温度不变, 、 不变,故 不变,B项正确;
C.在 的饱和溶液中通入 , 增大, 的沉淀溶解平衡向左移动,
有 析出,溶液中 增大, 减小, 、 不再相等,C项错误;
D.向 、 的混合溶液中滴入几滴 溶液,出现黄色沉淀,证明发生了反应: ,
但由于不知道溶液中 、 的浓度大小,不能确定 和 溶度积大小关系,故D项错误。
故选B。
【练5】已知:工业生产中可用ZnS作为沉淀剂除去工业废水中的Cu2+,可表示为Cu2+(aq)+ZnS(s) Zn2+
(aq)+CuS(s)。下列说法不正确的是
A.反应达平衡时,c(Cu2+)=c(Zn2+)
B.过量的ZnS可通过过滤除去
C.该反应平衡常数K=
D.相同温度时,溶解度:S(ZnS)>S(CuS)
【答案】A
【详解】
A.溶解度S(ZnS)>S(CuS),所以达到反应平衡时c(Cu2+)<c(Zn2+),A错误;
B.工业生产中可用ZnS作为沉淀剂,过量的ZnS可通过过滤除去,B正确;C.Cu2+(aq)+ZnS(s) Zn2+(aq)+CuS(s)平衡常数K= ,C正确;
D.溶解度小的沉淀转化能转化为溶解度更小的沉淀,ZnS能转化为CuS,则溶解度S(ZnS)>S(CuS),D正
确;
答案选A。
【练6】(2021·河南高二期末)孔雀石主要含碱式碳酸铜[Cu (OH) CO],还含少量Fe、Si的化合物。
2 2 3
实验室以孔雀石为原料制备CuSO 及CaCO ,首先将其溶于稀硫酸中,得到的溶液中含有Cu2+、Fe2+、Fe3
4 3
+。从下列所给试剂中选择:
A.KMnO B.(NH )S C.HO D.KSCN
4 4 2 2 2
(1)检验溶液中Fe3+的最佳试剂为______(填代号)。
(2)为使Fe2+、Fe3+一起沉淀,需先加____(填代号),此时发生反应的离子方程式为________。
(3)然后再加_______(填化学式)调整溶液的pH只生成Fe(OH) 沉淀。
3
【答案】(1)D (2) C 2Fe2++H O+2H+=2Fe3++2H O
2 2 2
(3)CuO或CuCO
3
【解析】(1)KSCN溶液可以和Fe3+反应使溶液变成血红色,故选D;(2)为使Fe2+、Fe3+一起沉淀,应先加
入氧化剂将Fe2+氧化为Fe3+,同时不能引入新的杂质,所以应选用C.HO,发生的反应为2Fe2+
2 2
+H O+2H+=2Fe3++2H O;(3)加入的物质应能与氢离子反应,且不引入新的阳离子杂质,所以可以选用
2 2 2
CuO或CuCO。
3
【练7】(2021·内蒙古集宁一中高二月考)(1)在25℃下,向浓度均为0.1 mol∙L−1的MgCl 和CuCl 混合溶液
2 2
中逐滴加入氨水,先生成_______沉淀(填化学式),生成该沉淀的离子方程式为_______。(已知25℃时,
K [Mg(OH) ]=1.8×10−11,K [Cu(OH) ]=2.2×10−20)
sp 2 sp 2
(2)相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol∙L−1盐酸、③0.1 mol∙L−1氯化
镁溶液、④0.1 mol∙L−1硝酸银溶液中,c(Ag+)由大到小的顺序为:_______
(3)已知:K (AgBr)=5.4×10−13,K (AgCl)=1.8×10−10,向BaCl 溶液中加入AgNO 和KBr,当两种沉淀共存
sp sp 2 3
时, =_______。
杨sir化学,侵权必究
(4)已知在25℃时,K [Mg(OH) ]=3.2×10−11。25℃时,向0.02 mol∙L−1的MgCl 溶液中加入NaOH固体,如
sp 2 2
要生成Mg(OH) 沉淀,应使溶液中的c(OH-)最小为_______mol∙L−1。
2
(5)某温度时,BaSO 在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是_______
4A.加入NaSO 可使溶液由a点变到b点
2 4
B.通过蒸发可以使溶液由d点变到c点
C.b点有BaSO 沉淀生成
4
D.a点对应的K 大于c点对应的K
sp sp
【答案】(1)Cu(OH) 2NH ·H O+Cu2+ =Cu(OH) ↓+2NH+
2 3 2 2 4
(2)④>①>②>③ (3)3×10−3 (4)4×10−5 (5)C
【解析】(1)在25℃下,向浓度均为0.1 mol∙L−1的MgCl 和CuCl 混合溶液中逐滴加入氨水,沉淀镁离子需
2 2
要的氢氧根浓度 ,沉淀铜离子需要的氢氧根浓度
,氢氧根浓度最先满足沉淀铜离子所需浓度,
因此先生成Cu(OH) 沉淀,生成该沉淀的离子方程式为2NH ·H O+Cu2+ =Cu(OH) ↓+2NH+;(2)相同温度下,
2 3 2 2 4
氯化银溶解平衡AgCl(s) Ag+(aq)+Cl-(aq),将足量氯化银固体分别放入相同体积的①蒸馏水,平衡
正向移动,但银离子浓度不变;②0.1 mol∙L−1盐酸,氯离子浓度增大,平衡逆向移动;③0.1 mol∙L−1氯化
镁溶液,氯离子浓度增大,比②中氯离子浓度大,平衡逆向移动比②更多,银离子浓度比②中银离子浓度
小;④0.1 mol∙L−1硝酸银溶液,平衡逆向移动,但银离子浓度比原来大,因此c(Ag+)由大到小的顺序为:
④>①>②>③;(3)已知:K (AgBr)=5.4×10−13,K (AgCl)=1.8×10−10,向BaCl 溶液中加入AgNO 和
sp sp 2 3
KBr,当两种沉淀共存时, ;(4)已知在
25℃时,K [Mg(OH) ]=3.2×10−11。25℃时,向0.02 mol∙L−1的MgCl 溶液中加入NaOH固体,如要生成
sp 2 2
Mg(OH) 沉淀,应使溶液中的c(OH-)最小 ,则c(OH-)=
2
4×10−5mol∙L−1;(5)A项,加入NaSO ,硫酸根浓度增大,硫酸钡溶解平衡逆向移动,钡离子浓度减小,曲
2 4
线从a点往c点移动,故A错误;B项,d点蒸发溶剂,溶液体积减小,钡离子浓度、硫酸根浓度同时增大,c点与b点硫酸根浓度不变,钡离子浓度增大,因此蒸发溶液不可能由d点变到c点,故B错误;C项,b
点浓度积大于K ,因此有BaSO 沉淀生成,故C正确;D项,ac曲线是硫酸钡的溶度积常数变化曲线,因
sp 4
此a点对应的K 等于c点对应的K ,故D错误;故选C。
sp sp倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育