文档内容
课题2:金属的化学性质
教学目标:
1、知识与技能:
(1) 知道铁、铝、铜等常见金属与氧气反应,与稀盐酸、稀硫酸的置换反应;与盐溶液的反
应。
(2) 掌握常见金属活动性顺序表,并学会利用金属活动性顺序解决一些实际问题。
2、过程与方法:
(1)通过对旧知的回忆、家庭小实验及录像 发生猜想(金属活动性顺序)
设计实验 验证金属活动性顺序存在和用途 1 猜想金属活动性顺序的用
途2 设计实验 验证金属活动性顺序的用途2
(2)通过对金属与氧气、稀硫酸(稀盐酸)、盐溶液反应的三步实验探究,逐步完善金属活动
性顺序表,使学生感到水到渠成,易于接受。
3、情感态度与价值观:
通过家庭小实验,引导学生主动参与知识的获取过程;通过对金属活动性研究的过程,学
习科学探究的方法,培养学生进行科学探究的能力;通过实验和游戏,培养学生团队合作
精神。
课前准备:
教师准备:布置家庭小实验(见下)
学生准备:把镁条、铝片、铁片、铜片(先用砂纸除去表面氧化膜)和黄金饰品(自备)挂
在家中(干燥的空气中)观察现象并记录到下表中。
提示:重点观察各金属表面的金属光泽是否有变化
第一天 第二天 第三天 第四天 第五天
Mg
Al
Fe
Cu
Au
教学过程:
第一课时
师生活动 设计意图
[引入]: 通 过 家 庭
通过上节课的学习,我们知道金属的用途不仅与它们的物理性质有 小 实 验 让
关,而且还与他们的化学性质有密切的关系。今天我们来重点研究它们的 学 生 感 知
化学性质。 生 活 中 的
[投影]家庭小实验表格。每小组汇报交流。 化学,激发
学 生 的 探
究欲望。
[录象回顾] Fe、Cu、Au在氧气中加热的实验 回 顾 旧 知
[交流与讨论] 感 悟 金 属
[话题1] 金属为什么会失去光泽? 的活动性,
[话题2] 为什么在相同条件下,不同金属失去光泽的顺序有差异? 进行猜想。
[ 猜 想 ] 结 合 上 述 实 验 , 请 你 对 五 种 金 属 的 排 序 是
______________________________。
[小结与归纳]
根据Mg、Fe、Cu、Au与氧气反应的难易程度我们看出,镁、铝比较活
泼,铁、铜次之,金最不活泼。(真金不怕火炼)
[过渡] 镁与锌,铁与铜到底谁更活泼些呢?
我们能否设计一个实验,来解决上述问题呢?
[启发]资料(图片资料锌与酸反应)
1小组讨论: 使 学 生 学
①设计实验方案; ②汇报交流 会 通 过 小
③教师根据学生交流情况,探讨推荐学生设计方案; 组 合 作 分
[活动与探究](见表一) 析、解决问
一、 三组用稀盐酸,二、四组用稀硫酸。 题。进一步
[汇报交流] 熟 悉 实 验
能 与 盐 酸 、 稀 硫 酸 发 生 反 应 的 金 属 有 : 探 究 的 步
__________________________ ; 骤,让学生
不能与盐酸、稀硫酸发生反应的金属有: ________________________。 形成:进行
根据反应发生的剧烈程度,将以上金属按活泼性排序: 实 验 — —
_____________。 分 析 现 象
由上述探究也可以得出: — — 寻 找
___________的金属活动性比_____强,它能置换出盐酸或稀硫酸中的氢; 规 律 — —
的金属活动性比_____弱,它不能置换出盐酸或稀硫酸中的氢。 得 出 结 论
关 于 金 属 与 酸 溶 液 反 应 , 你 得 出 的 结 论 是 : 的 实 验 思
___________________________________ 路。
[归纳]
Mg > Zn > Fe > (H) > Cu
金属活动性由强到弱
[演示](补充实验 ) 铜和稀硫酸
银和稀硫酸
[问题]怎么确定铜和银哪个更活泼?
[资料]铁和硫酸铜反应 回顾旧知,
讨论猜想规律; 猜 想 和 运
[活动与探究](见表二) 用 已 学 规
结论: 律
通过上述实验,你得出铝、铜、银的金属活动性顺序为:
________________
关于金属与盐溶液的反应,你得出的结论是:
____________________ ____ ____
介 绍 金 属
的 活 动 性
顺序,
[总结] 使 学 生 体
会 知 识 的
经过许多类似的实验探究,我们归纳出常见金属在水溶液中的活动 形成过程,
性顺序 把 学 生 在
K > Ca > Na > Mg > Al > Zn > Fe > Sn > Pb > (H) Cu > Hg > Ag 实 验 中 获
>Pt > Au 得 的 零 乱
金属活动性由强减弱 知 识 形 成
[记忆]比一比,赛一赛 体系。
[交流与小结]
本节课你学到了什么?
通过对铁、铝、铜等常见金属与氧气反应,与稀盐酸、稀硫酸的反应;与盐
溶液的反应的探究,归纳出金属活动性顺序。
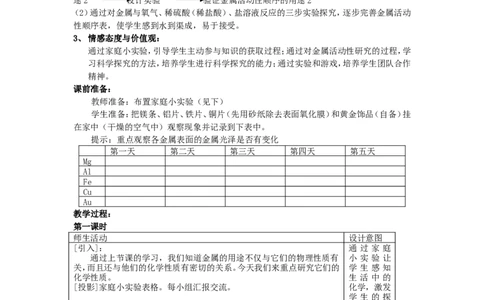
课堂练习:
21、金属活动性大于铁,小于铝的是 ( )
A.Zn B.K C.Cu D.Mg
2、某同学为判断A、B、C三种金属的活动性大小,设计了下列四个实验:
(1)将金属B放入C的盐溶液中,看能否置换出C
(2)将金属B放入酸中,看能否置换出酸中的氢
(3)将金属A放入B的盐溶液,看能否置换出B
(4)将金属C放入A的盐溶液中,看能否置换出A
你认为上述可以不做的实验是( )
A、(1) B、(2) C、(3) D、(4)
3、《教与学》P21 12
(2改成B是常见的金属,请写出它的化学式_________________)
4、我们常说的“真金不怕火炼”的原因是 ( )
A.金的熔点高 B.金的硬度大
C.金的密度大 D.金不活泼,高温时也不与氧气反应
5《教与学》P20 1、2
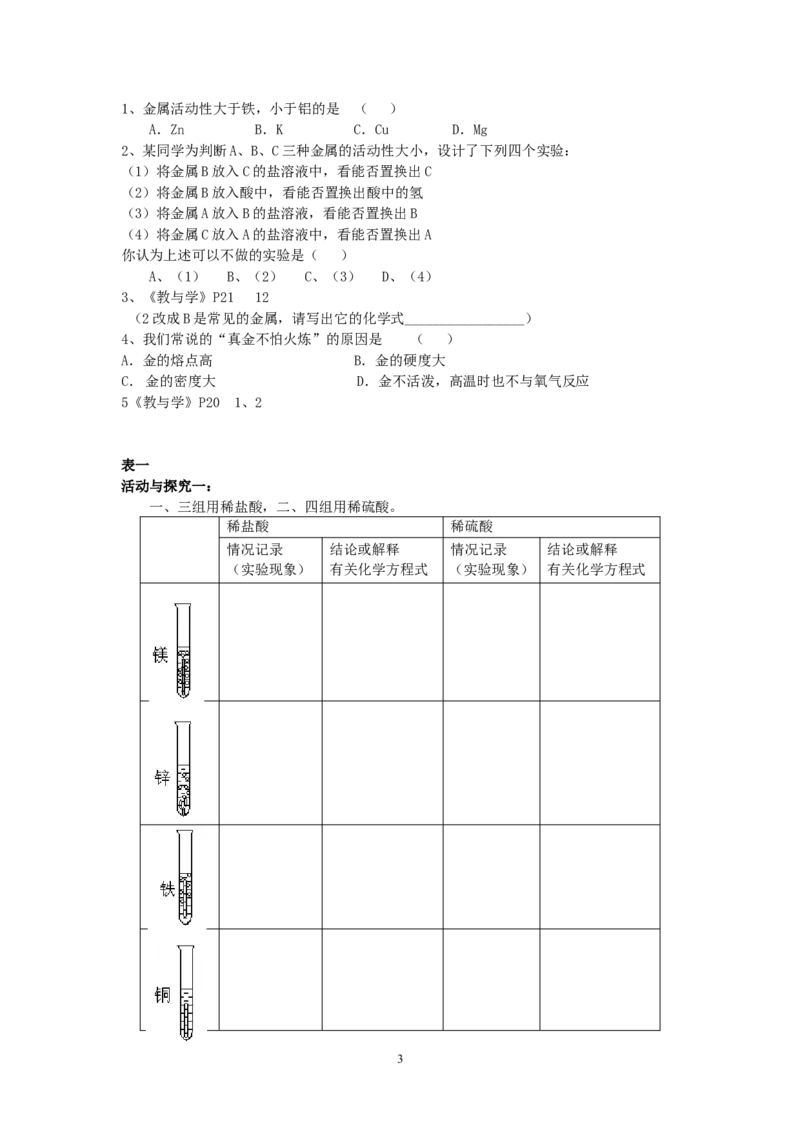
表一
活动与探究一:
一、三组用稀盐酸,二、四组用稀硫酸。
稀盐酸 稀硫酸
情况记录 结论或解释 情况记录 结论或解释
(实验现象) 有关化学方程式 (实验现象) 有关化学方程式
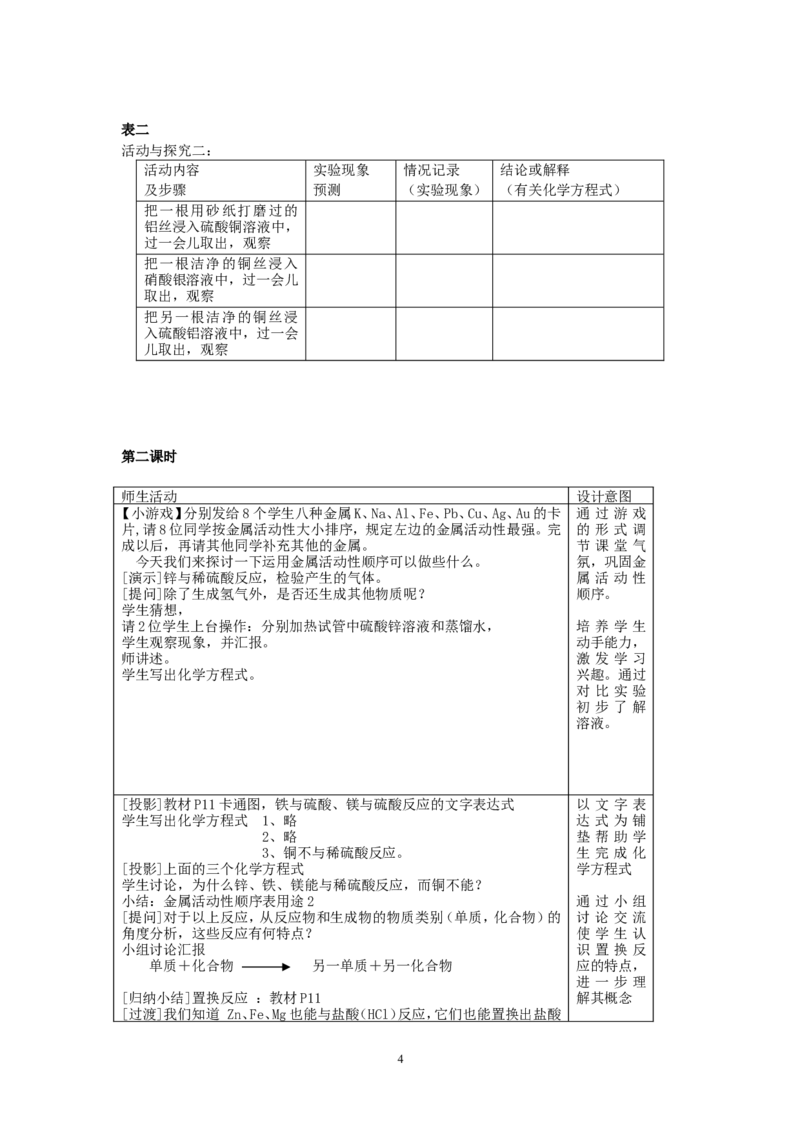
3表二
活动与探究二:
活动内容 实验现象 情况记录 结论或解释
及步骤 预测 (实验现象) (有关化学方程式)
把一根用砂纸打磨过的
铝丝浸入硫酸铜溶液中,
过一会儿取出,观察
把一根洁净的铜丝浸入
硝酸银溶液中,过一会儿
取出,观察
把另一根洁净的铜丝浸
入硫酸铝溶液中,过一会
儿取出,观察
第二课时
师生活动 设计意图
【小游戏】分别发给8个学生八种金属K、Na、Al、Fe、Pb、Cu、Ag、Au的卡 通 过 游 戏
片,请8位同学按金属活动性大小排序,规定左边的金属活动性最强。完 的 形 式 调
成以后,再请其他同学补充其他的金属。 节 课 堂 气
今天我们来探讨一下运用金属活动性顺序可以做些什么。 氛,巩固金
[演示]锌与稀硫酸反应,检验产生的气体。 属 活 动 性
[提问]除了生成氢气外,是否还生成其他物质呢? 顺序。
学生猜想,
请2位学生上台操作:分别加热试管中硫酸锌溶液和蒸馏水, 培 养 学 生
学生观察现象,并汇报。 动手能力,
师讲述。 激 发 学 习
学生写出化学方程式。 兴趣。通过
对 比 实 验
初 步 了 解
溶液。
[投影]教材P11卡通图,铁与硫酸、镁与硫酸反应的文字表达式 以 文 字 表
学生写出化学方程式 1、略 达 式 为 铺
2、略 垫 帮 助 学
3、铜不与稀硫酸反应。 生 完 成 化
[投影]上面的三个化学方程式 学方程式
学生讨论,为什么锌、铁、镁能与稀硫酸反应,而铜不能?
小结:金属活动性顺序表用途2 通 过 小 组
[提问]对于以上反应,从反应物和生成物的物质类别(单质,化合物)的 讨 论 交 流
角度分析,这些反应有何特点? 使 学 生 认
小组讨论汇报 识 置 换 反
单质+化合物 另一单质+另一化合物 应的特点,
进 一 步 理
[归纳小结]置换反应 :教材P11 解其概念
[过渡]我们知道 Zn、Fe、Mg也能与盐酸(HCl)反应,它们也能置换出盐酸
4中氢
[投影]文字表达式:
铁+盐酸 氯化亚铁+氢气
镁+盐酸 氯化镁+氢气
锌+盐酸 氯化锌+氢气
学生写化学方程式并讨论现象
[演示]P11铝和硫酸铜
铜和硝酸银
铜和硫酸铝
学生观察现象,能反应的写出其化学方程式,并写出反应基本类型。
(提示):
铝+硫酸铜 铜+硫酸铝
铜+硝酸银 银+硝酸铜
铜和硫酸铝不反应
学生讨论:
为什么铝能置换出硫酸铜中的铜,而铜不能置换出硫酸铝中的铝?
小结:金属活动性顺序表的用途。
1、归纳:常见的金属活动性顺序表的应用1、2、3
[本节小结]
1、置换反应
2、学习书写两类置换反应的化学方程式,并巩固对这两类置换反应能
否发生的判断依据。
课堂练习:
《教与学》P21 7、6、5、4、8
教学反思
5