文档内容
优秀领先 飞翔梦
想
2015-2016学年广西贵港市港南区校级九年级(上)联考
化学试卷(二)
一、选择题(共12小题,每小题3分,共36分,每小题只有一个选项符合题意)
1.下列变化属于物理变化的是( )
A.碳酸氢铵分解B.钢铁生锈 C.干冰升华 D.羊毛燃烧
2.建立宏观与微观的联系是化学学科特有的思维方式.下列对于宏观现象的微观解释中,错
误的是( )
A.水通直流电分解,是因为水分子被破坏,形成新的分子
B.“酒香不怕巷子深”,说明了分子在不断运动
C.一氧化碳和二氧化碳具有不同的化学性质,是因为构成它们的分子不同
D.20mL水与 20mL酒精混合后体积小于40mL,是因为分子数目减少
3.下列实验现象叙述错误的是( )
A.硫在空气中燃烧发出淡蓝色的火焰
B.木炭在氧气中燃烧发出淡蓝色的火焰
C.铁丝在氧气中燃烧火星四射
D.磷在空气中燃烧放出大量白烟
4.根据如图的有关信息判断,下列说法正确的是( )
A.镁离子(Mg2+)核内有12个质子
B.镁的相对原子质量为24.31g
C.在化学反应中,氯原子容易失去1个电子
D.镁离子(Mg2+)与氯离子(Cl﹣)的最外层电子数不相等
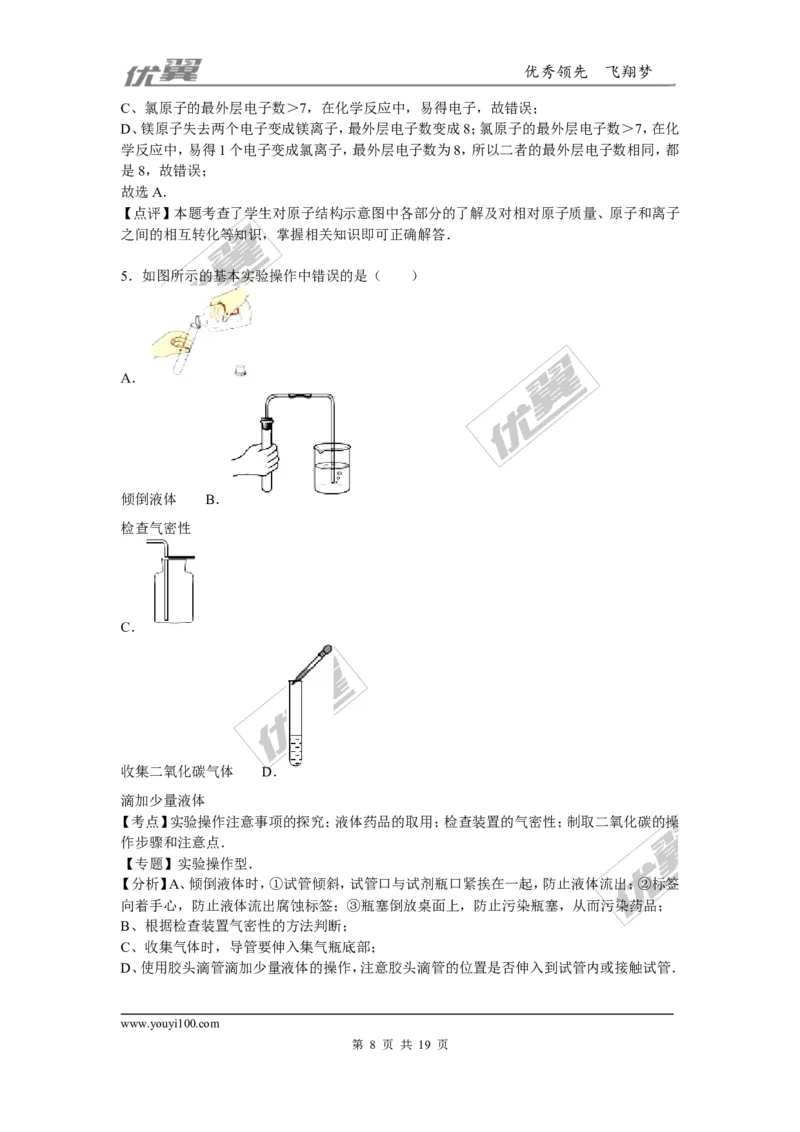
5.如图所示的基本实验操作中错误的是( )
A.
www.youyi100.com
第 1 页 共 19 页优秀领先 飞翔梦
想
倾倒液体 B.
检查气密性
C.
收集二氧化碳气体 D.
滴加少量液体
6.下列说法正确的是( )
A.铝的金属活动性比铁强,则铝制品比铁制品更容易锈蚀
B.单质是由同种元素组成的,但同种元素组成的物质不一定是单质
C.生石灰与烧碱分别放入水中都有热量放出,不能用加水的方法鉴别二者
D.纯碱和火碱的溶液都呈碱性,所以,它们都属于碱
7.烟台是座美丽的城市.下列对海洋化学资源利用的有关叙述错误的是( )
A.利用多级闪急蒸馏法淡化海水
B.利用蒸发结晶的方法从海水中提取食盐
C.利用像海水或卤水中加入石灰乳的方法将海水中的Mg2+富集沉淀出来
D.利用海底蕴藏的大量“可燃冰”作燃料,以它为燃料不会加剧温室效应
8.下列知识整理的内容不完全正确的一组是( )
A 化学与安全 B 化学与生活
稀酸溅入眼睛﹣﹣用大量水冲洗 除去餐具上的油污﹣﹣用洗洁精乳化
进入矿井﹣﹣先做灯火实验 人体需要适量补碘﹣﹣防止患甲状腺疾病
C 化学与能源 D 化学与环保
化石燃料﹣﹣煤、石油和天然气 减少汽车尾气污染﹣﹣提倡使用公共交通等
清洁能源﹣﹣太阳能、风能等 减少温室气体排放﹣﹣利用水力、核能发电
A.A B.BC.CD.D
9.如图是甲,乙,丙三种物质(均不含结晶水)的溶解曲线图.现有t ℃时甲,乙,丙三种物质
2
的饱和溶液(无固体存在),下列说法正确的是( )
www.youyi100.com
第 2 页 共 19 页优秀领先 飞翔梦
想
A.将温度由t ℃降到t ℃时,析出甲的质量比乙多
2 1
B.将温度由t ℃降到t ℃,所得溶液中溶质的质量分数由大到小的顺序为:乙>丙>甲
2 1
C.若甲中含有少量杂质乙,可采用降温结晶的方法进行提纯
D.三种物质溶解度大小依次为:乙>丙>甲
10.将一定质量的Zn粒放入AgNO 与Cu(NO )的混合溶液中,充分反应后发现,溶液底部
3 3 2
有少量固体;过滤后在滤渣和滤液中分别加入适量稀盐酸,滤渣中有无色气体产生,滤液中
无沉淀产生.结合实验现象判断,下列结论中,正确的是( )
A.滤渣中可能含有单质锌B.滤液中一定没有银离子
C.滤渣中一定没有单质铜 D.滤液的颜色可能为蓝色
11.下面除去混合物中少量杂质(括号内为杂质)的方案中,不合理的 是
混合物 思路方法 选用物质
A CO (CO) 点燃 空气
2
B NaOH(Na CO ) 沉淀、过滤 石灰乳[Ca(OH)
2 3 2
C FeCl (CuCl ) 置换、过滤 铁粉
2 2
D NaCl(MgCl ) 沉淀、过滤 NaOH ]
2
A.A B.BC.CD.D
12.分别将下列各组物质同时加入到水中,最终能得到无色、透明溶液的是( )
A.BaCl 、NaOH、H SO B.KCl、NaOH、CuSO
2 2 4 4
C.HNO 、NaCl、K SO D.FeCl 、Na SO 、KCl
3 2 4 3 2 4
二、我会填空题(共16分,除化学方程式每空2分外,其余每空1分)
13.用化学用语填空:
(1)亚铁离子 ;(2)2个氮气分子 ;
(3)碳酸钠中的阴离子 ;(4)地壳中含量最多的金属元素 .
14.水与人类的生活和生产密切相关,2010年“中国水周”的宣传主题是“严格水资源管理,
保障可持续发展”.为相应这一主题,某中学环保小组的同学配合环保部门.定期对流经我
市的河水进行取样测试.请根据某日采集的水样回答以下问题:
(1)在白瓷板上放一小片pH试纸,用玻璃棒蘸取少量(1)中所得到的液体,测得其pH大于
7,则说明该水样显 性;
(2)由上述数据分析,该河水的主要污染物可能是(填序号) ;
①带有酸臭味的城市生活污水 ②化工厂排放的污水
(3)为了保护河水的水质,下列做法合理的是(填序号) .
①抑制水中所有动、植物的生长②不任意排放工业废水
www.youyi100.com
第 3 页 共 19 页优秀领先 飞翔梦
想
③禁止使用农药和化肥④生活污水经过净化处理后再排放.
15.豆腐是人们喜爱的食物,其主要成分如表所示.请回答下列问题:
豆腐的主要成分
物质 每100g含有
水 89.30g
蛋白质 4.70g
油脂 1.30g
糖类 2.80g
维生素B 0.06mg
1
维生素B 0.03mg
2
钙 0.24g
铁 1.40g
其它
(1)其中的铁、钙是指 (填序号);
①分子 ②原子 ③元素
(2)当人体缺钙时,可能引起的疾病是 (填序号);
①骨质疏松症 ②贫血症 ③夜盲症
(3)豆腐中除了蛋白质、油脂、糖类、无机盐、水之外,还包括的营养物质是 ;
(4)豆腐常用塑料袋包装,请指出使用塑料袋包装的利与弊(各答一条).
利: ;弊: .
16.我国著名的化学家侯德榜先生发明的制碱原理为: 、 ,用
的方法可以把NaHCO 晶体从混合物中分离出来,在制取NaHCO 时,先向饱和的NaCl溶液
3 3
中通入较多的NH ,再通入足量的CO 的目的是 .
3 2
三、我会回答(共18分,化学方程式每空3分,其余每空2分)
17.高铁的出现使交通运输业水平又上升到一个新的层次.高铁建设工程技术人员常利用点
燃铝热剂的方法来焊接钢轨.铝热剂是铝粉和氧化铁粉末的混合物,燃烧生成铁和氧化铝.
(1)钢轨属于 (填“单质”、“合金”、“氧化物”之一).
(2)点燃铝热剂反应的化学方程式为: .反应类型为 .(填“分
解”、“化合”、“置换”、“复分解”之一)
(3)某同学回忆起一氧化碳与氧化铁反应时,一氧化碳是还原剂,他推理得出上述反应中还
原剂是 (选填“铝”或“氧化铁”).在铝热剂中元素化合价为零的物质是
.
18.如图是有关物质转化关系的示意图,其中A是含有碳元素的化合物,D是一种含有钠元
素的化合物,请回答下列问题:
(1)写出下列物质的化学式:A: G:
(2)写出B和F反应的化学方程式: .
www.youyi100.com
第 4 页 共 19 页优秀领先 飞翔梦
想
四、我会实验(共22分,除19(1)每空1分,其余每空2分)
19.以下是我们熟悉的实验室制取气体的发生装置、收集装置,请回答下列问题:
(1)写出图1装置中有标号仪器的名称:a ;b .
(2)利用上述A、D装置的组合可以制取的一种气体是 ,写出实验室制取该气
体的化学方程式 ,检验该气体是否收集满的方法是 .
(3)若用B装置作为制取气体的发生装置,应满足的条件是 .
(4)若用图2所示的装置,收集一瓶难溶于水的气体,实验前将该装置装满水正放,则气体应
从
(填“c”或“d”)端进入.将该装置装满水倒放,则气体应从 (填
“c”或“d”)端进入.
20.氢化钙固体是登山运动员常用的能源提供剂.某探究小组的同学通过查阅资料得知,氢
化钙(CaH )遇水反应生成氢氧化钙和氢气.探究小组的同学把一定量的CaH 加入Na CO
2 2 2 3
溶液中,充分反应后过滤,得到滤渣和滤液,经检验,滤渣的成分是碳酸钙.
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】
猜想一:NaOH 猜想二: .
猜想三:NaOH和Na CO 猜想四:NaOH、Na CO 和Ca(OH)
2 3 2 3 2
经过讨论,大家一致认为猜想四不合理,其原因是 .
【实验验证】
实验 现象 结论
实验一:取滤液,向其中滴入少量碳酸无明显现象
钠溶液 不成立
实验二:另取滤液,向其中加入足量稀 猜想三成立
盐酸
实验二中发生明显现象的化学方程式是 .
【反思与拓展】登山运动员常用CaH 作为能源提供剂,与氢气相比的优点是 .
2
五、计算题(共8分)
21.盐水选种是我国古代劳动人民发明的一种巧妙的挑选种子的方法.农业生产上常用质量
分数为15%﹣20%的氯化钠溶液来选种.
(1)要配制150kg16%的氯化钠,计算应称取氯化钠的质量.
(2)选种进行一段时间后,农技员估计溶液和溶质质量分数都有所减少,他取出50g氯化钠
溶液,加入过量的AgNO 溶液,得到沉淀14.35g,计算氯化钠溶液中溶质的质量分数.
3
www.youyi100.com
第 5 页 共 19 页优秀领先 飞翔梦
想
2015-2016 学年广西贵港市港南区校级九年级(上)联考
化学试卷(二)
参考答案与试题解析
一、选择题(共12小题,每小题3分,共36分,每小题只有一个选项符合题意)
1.下列变化属于物理变化的是( )
A.碳酸氢铵分解B.钢铁生锈 C.干冰升华 D.羊毛燃烧
【考点】化学变化和物理变化的判别 .
【专题】物质的变化与性质.
【分析】本题考查学生对物理变化和化学变化的确定.判断一个变化是物理变化还是化学变
化,要依据在变化过程中有没有生成其他物质,生成其他物质的是化学变化,没有生成其他
物质的是物理变化
【解答】解:A、碳酸氢铵分解生成氨气、水、二氧化碳,属于化学变化,故A错;
B、钢铁生锈生成了主要成分是氧化铁的新物质,属于化学变化,故B错;
C、干冰升华是由固态直接变为气态,只是状态的变化,没有新物质生成,属于物理变化,故C
正确;
D、羊毛燃烧有烧焦羽毛气味,有新物质生成,属于化学变化,故D错.
故选C.
【点评】搞清楚物理变化和化学变化的本质区别是解答本类习题的关键.判断的标准是看在
变化中有没有生成其他物质.一般地,物理变化有物质的固、液、气三态变化和物质形状的变
化.
2.建立宏观与微观的联系是化学学科特有的思维方式.下列对于宏观现象的微观解释中,错
误的是( )
A.水通直流电分解,是因为水分子被破坏,形成新的分子
B.“酒香不怕巷子深”,说明了分子在不断运动
C.一氧化碳和二氧化碳具有不同的化学性质,是因为构成它们的分子不同
D.20mL水与 20mL酒精混合后体积小于40mL,是因为分子数目减少
【考点】利用分子与原子的性质分析和解决问题.
【专题】物质的微观构成与物质的宏观组成.
【分析】A、根据分子在化学变化中可再分分析;
B、根据分子是在不断运动的特性进行分析;
C、根据一氧化碳和二氧化碳的分子构成进行分析;
D、根据分子之间有间隔的特性进行分析.
【解答】解:A、分子在化学变化中可再分,所以,水通直流电分解,是因为水分子被破坏,形成
新的分子,故A正确;
B、由于酒精的分子通过运动扩散到空气中,能闻到酒香,故B正确;
C、由于一氧化碳和二氧化碳的分子构成不同,结构决定性质,所以,一氧化碳和二氧化碳具
有不同的化学性质,故C正确;
D、20mL水与 20mL酒精混合后体积小于40mL,是因为分子间有间隔,故D错误.
www.youyi100.com
第 6 页 共 19 页优秀领先 飞翔梦
想
故选:D.
【点评】本题难度不大,掌握利用分子的基本性质分析和解决问题的方法、物质的结构决定物
质的性质是解答此类题的关键.
3.下列实验现象叙述错误的是( )
A.硫在空气中燃烧发出淡蓝色的火焰
B.木炭在氧气中燃烧发出淡蓝色的火焰
C.铁丝在氧气中燃烧火星四射
D.磷在空气中燃烧放出大量白烟
【考点】氧气与碳、磷、硫、铁等物质的反应现象.
【专题】实验现象的观察和记录.
【分析】A、根据硫在空气中燃烧的现象进行分析判断.
B、根据木炭在氧气中燃烧的现象进行分析判断.
C、根据铁丝在氧气中燃烧的现象进行分析判断.
D、根据磷在空气中燃烧的现象进行分析判断.
【解答】解:A、硫在空气中燃烧,发出淡蓝色的火焰,故选项说法正确.
B、木炭在氧气中燃烧,发出白光,故选项说法错误.
C、铁丝在氧气中剧烈燃烧,火星四射,故选项说法正确.
D、磷在空气中燃烧,产生大量的白烟,故选项说法正确.
故选:B.
【点评】本题难度不大,掌握常见物质燃烧的现象即可正确解答;在描述物质燃烧的现象时,
需要注意光和火焰、烟和雾的区别.
4.根据如图的有关信息判断,下列说法正确的是( )
A.镁离子(Mg2+)核内有12个质子
B.镁的相对原子质量为24.31g
C.在化学反应中,氯原子容易失去1个电子
D.镁离子(Mg2+)与氯离子(Cl﹣)的最外层电子数不相等
【考点】原子结构示意图与离子结构示意图;元素周期表的特点及其应用.
【专题】压轴实验题;化学用语和质量守恒定律.
【分析】A、圆圈内的数字表示原子核内的质子数;
B、相对原子质量的单位是1,通常省略不写;
C、氯原子的最外层电子数>7,在化学反应中,易得电子;
D、分析镁离子和氯离子的结构示意图并进行比较.
【解答】解:A、圆圈内的数字表示原子核内的质子数,原子变成离子,得失的是核外电子,质
子数不变;故镁离子(Mg2+)核内有12个质子,正确;
B、镁的相对原子质量为24.31g,相对原子质量的单位是1,不是克,故错误;
www.youyi100.com
第 7 页 共 19 页优秀领先 飞翔梦
想
C、氯原子的最外层电子数>7,在化学反应中,易得电子,故错误;
D、镁原子失去两个电子变成镁离子,最外层电子数变成8;氯原子的最外层电子数>7,在化
学反应中,易得1个电子变成氯离子,最外层电子数为8,所以二者的最外层电子数相同,都
是8,故错误;
故选A.
【点评】本题考查了学生对原子结构示意图中各部分的了解及对相对原子质量、原子和离子
之间的相互转化等知识,掌握相关知识即可正确解答.
5.如图所示的基本实验操作中错误的是( )
A.
倾倒液体 B.
检查气密性
C.
收集二氧化碳气体 D.
滴加少量液体
【考点】实验操作注意事项的探究;液体药品的取用;检查装置的气密性;制取二氧化碳的操
作步骤和注意点.
【专题】实验操作型.
【分析】A、倾倒液体时,①试管倾斜,试管口与试剂瓶口紧挨在一起,防止液体流出;②标签
向着手心,防止液体流出腐蚀标签;③瓶塞倒放桌面上,防止污染瓶塞,从而污染药品;
B、根据检查装置气密性的方法判断;
C、收集气体时,导管要伸入集气瓶底部;
D、使用胶头滴管滴加少量液体的操作,注意胶头滴管的位置是否伸入到试管内或接触试管.
www.youyi100.com
第 8 页 共 19 页优秀领先 飞翔梦
想
【解答】解:A、取用液体时:注意瓶口、标签的位置,瓶塞的放置;标签应向着手心,瓶塞倒放;
图中操作正确;
B、检查气密性时,手要紧握试管外壁,导管伸入水中,看是否有气泡冒出,图中操作正确;
C、收集二氧化碳气体要用向上排空气法,导管伸入集气瓶底部,图中操作正确;
D、胶头滴管伸入试管内或接触试管,会造成药品的污染,图中操作错误.
故选:D.
【点评】准确读取图中的信息,联系化学实验基本操作的内容,是正确解答此类题的基础.
6.下列说法正确的是( )
A.铝的金属活动性比铁强,则铝制品比铁制品更容易锈蚀
B.单质是由同种元素组成的,但同种元素组成的物质不一定是单质
C.生石灰与烧碱分别放入水中都有热量放出,不能用加水的方法鉴别二者
D.纯碱和火碱的溶液都呈碱性,所以,它们都属于碱
【考点】金属的化学性质;酸、碱、盐的鉴别;单质和化合物的概念;常见的氧化物、酸、碱和盐
的判别.
【专题】物质的鉴别题;化学物质的分类思想;物质的分类;金属与金属材料.
【分析】A、根据金属的化学性质进行分析判断.
B、根据单质是由同种元素组成的纯净物,进行分析判断.
C、根据生石灰能与水反应放出大量的热,烧碱溶于水放出大量的热,进行分析判断.
D、纯碱和火碱分别是碳酸钠、氢氧化钠的俗称,据此进行分析判断.
【解答】解:A、铝的金属活动性比铁强,但铝制品空气中氧气反应在其表面生成一层致密的
氧化铝薄膜,防止内部的铝进一步被氧化,因此铝制品抗腐蚀性强,故选项说法错误.
B、单质是由同种元素组成的,但同种元素组成的物质不一定是单质,如氧气、臭氧是由同种
元素组成的物质,属于混合物,故选项说法正确.
C、生石灰能与水反应放出大量的热,烧碱溶于水放出大量的热,但生石灰溶于水生成的氢氧
化钙微溶于水,氢氧化钠易溶于水,能用加水的方法鉴别二者,故选项说法错误.
D、纯碱和火碱分别是碳酸钠、氢氧化钠的俗称,都呈碱性,碳酸钠是由钠离子和碳酸根离子
构成的化合物,属于盐,故选项说法错误.
故选:B.
【点评】本题难度不大,掌握金属的化学性质、单质的特征、生石灰的化学性质、碱与盐的特征
等是正确解答本题的关键.
7.烟台是座美丽的城市.下列对海洋化学资源利用的有关叙述错误的是( )
A.利用多级闪急蒸馏法淡化海水
B.利用蒸发结晶的方法从海水中提取食盐
C.利用像海水或卤水中加入石灰乳的方法将海水中的Mg2+富集沉淀出来
D.利用海底蕴藏的大量“可燃冰”作燃料,以它为燃料不会加剧温室效应
【考点】对海洋资源的合理开发与利用;常用燃料的使用与其对环境的影响.
【专题】课本知识同类信息.
【分析】根据已有的知识进行分析,A淡化海水最常用的方法是蒸馏法,B食盐的溶解度随温
度变化不大,可以使用蒸发结晶的方法提取食盐,C要将镁离子富集可以使用加入氢氧化钙
的方法,D可燃冰燃烧生成二氧化碳.
【解答】解:A、淡化海水最常用的方法是多级闪急蒸馏法,故A叙述正确;
www.youyi100.com
第 9 页 共 19 页优秀领先 飞翔梦
想
B、食盐的溶解度随温度变化不大,可以使用蒸发结晶的方法提取食盐,故B叙述正确;
C、要将镁离子富集可以使用加入氢氧化钙的方法,故C叙述正确;
D、可燃冰燃烧生成二氧化碳,会加剧温室效应,故D叙述错误;
故选D.
【点评】本题考查了对海洋资源的利用,完成此题,可以依据选项的叙述具体进行分析即可.
8.下列知识整理的内容不完全正确的一组是( )
A 化学与安全 B 化学与生活
稀酸溅入眼睛﹣﹣用大量水冲洗 除去餐具上的油污﹣﹣用洗洁精乳化
进入矿井﹣﹣先做灯火实验 人体需要适量补碘﹣﹣防止患甲状腺疾病
C 化学与能源 D 化学与环保
化石燃料﹣﹣煤、石油和天然气 减少汽车尾气污染﹣﹣提倡使用公共交通等
清洁能源﹣﹣太阳能、风能等 减少温室气体排放﹣﹣利用水力、核能发电
A.A B.BC.CD.D
【考点】常见的意外事故的处理方法;防治空气污染的措施;乳化现象与乳化作用;防范爆炸
的措施;化石燃料及其综合利用;资源综合利用和新能源开发;人体的元素组成与元素对人
体健康的重要作用.
【专题】化学与环境保护;化学与能源;化学与生活.
【分析】A、依据实验室事故处理方法方法判断稀酸入眼的急救;依据可燃性气体点燃易爆炸
解答;
B、依据洗洁精的去油污原理分析判断;从缺钙导致的病症判断病症;
C、依据化石燃料的种类以及清洁能源的种类分析判断;
D、从环境污染的角度分析即可.
【解答】解:
A、稀酸入眼的急救方式是首先用大量的水冲洗眼部;矿井中有可燃性气体,可燃性气体点燃
易爆炸,进入矿井不能做灯火实验;错误.
B、洗洁精的去油污是发生乳化作用;人体需要适量补碘,防止患甲状腺疾病;正确.
C、三大化石燃料是煤、石油和天然气,它们的过度使用对环境质量下降影响较大,而太阳能、
风能等使用时不会对环境造成危害,所以是相对清洁的能源;正确.
D、汽车尾气的污染是空气质量下降的主要原因,所以提倡使用公共交通少开私家车,是减少
减少汽车尾气污染的有效途径;温室气体的排放与化石燃料的使用有直接关系,用利用水力、
核能发电减小了化石燃料的燃烧,从而减少温室气体排放;正确.
故选A.
【点评】此题是一道多点知识考查题,与生活学习相关,强调了平时学习中的归纳总结,对比
和联想,只有这样才能更利于知识的理解和应用.
9.如图是甲,乙,丙三种物质(均不含结晶水)的溶解曲线图.现有t ℃时甲,乙,丙三种物质
2
的饱和溶液(无固体存在),下列说法正确的是( )
A.将温度由t ℃降到t ℃时,析出甲的质量比乙多
2 1
www.youyi100.com
第 10 页 共 19 页优秀领先 飞翔梦
想
B.将温度由t ℃降到t ℃,所得溶液中溶质的质量分数由大到小的顺序为:乙>丙>甲
2 1
C.若甲中含有少量杂质乙,可采用降温结晶的方法进行提纯
D.三种物质溶解度大小依次为:乙>丙>甲
【考点】固体溶解度曲线及其作用;结晶的原理、方法及其应用;晶体和结晶的概念与现象;溶
质的质量分数、溶解性和溶解度的关系.
【专题】溶液、浊液与溶解度.
【分析】A、不知饱和溶液的质量多少,无法判断降温析出晶体的质量多少;
B、据物质的溶解度随温度变化情况及饱和溶液中溶质的质量分数计算解答;
C、据甲乙的溶解度受温度影响情况分析提纯物质的方法;
D、比较物质的溶解度大小须确定温度.
【解答】解:A、不知饱和溶液的质量多少,无法判断降温析出晶体的质量多少,故错误;
B、将温度由t ℃降到t ℃,甲乙的溶解度减小析出晶体,溶液中溶质质量减小、溶剂的质量
2 1
不变,则溶质的质量分数减小,丙的溶解度变大,溶液中溶质、溶剂的质量不变,溶质的质量
分数不变;饱和溶液中溶质的质量分数= ×100%,即溶解度大则溶质的质量分
数大,而t ℃时乙的溶解度大于甲的溶解度大于丙的溶解度,故所得溶液中溶质的质量分数
1
由大到小的顺序为:乙>甲>丙,故错误;
C、甲的溶解度受温度影响较大,乙的溶解度受温度影响较小,所以若甲中含有少量杂质乙,
可采用降温结晶的方法进行提纯,正确;
D、比较三种物质溶解度大小未确定温度,所以无法比较其大小,故错误;
故选:C.
【点评】了解溶解度概念四要素、溶解度曲线的意义,饱和溶液中溶解度大则溶质的质量分数
大等知识,才能结合题意正确分析解答.
10.将一定质量的Zn粒放入AgNO 与Cu(NO )的混合溶液中,充分反应后发现,溶液底部
3 3 2
有少量固体;过滤后在滤渣和滤液中分别加入适量稀盐酸,滤渣中有无色气体产生,滤液中
无沉淀产生.结合实验现象判断,下列结论中,正确的是( )
A.滤渣中可能含有单质锌B.滤液中一定没有银离子
C.滤渣中一定没有单质铜 D.滤液的颜色可能为蓝色
【考点】金属的化学性质.
【专题】金属与金属材料.
【分析】在金属活动性顺序中,Zn>H>Cu>Ag,氢前的金属能与酸反应生成氢气,位置在前
的金属能将位于其后的金属从其盐溶液中置换出来.
【解答】解:
A、过滤、洗涤后往滤渣中加入稀盐酸,有气泡产生,说明滤渣中有金属锌,故A错误;
B、根据“在滤渣和滤液中分别加入适量稀盐酸,滤渣中有无色气体产生,滤液中无沉淀产
生”,则可知:一定有锌,一定无AgNO ,故B正确;
3
C、由于加入的锌的量过量,故滤渣中一定有单质铜,故C错误;
D、在AgNO 和Cu(NO )的混合溶液中加入一定量的锌粉,锌与硝酸银反应生成硝酸锌和
3 3 2
银,和硝酸铜反应生成硝酸锌和铜,生成的铜会与硝酸银反应生成硝酸铜和银;而锌过量,硝
酸铜会全被反应掉,则滤液的颜色不可能为蓝色,故D错误.
故选:B.
【点评】本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序的意义进行.
www.youyi100.com
第 11 页 共 19 页优秀领先 飞翔梦
想
11.下面除去混合物中少量杂质(括号内为杂质)的方案中,不合理的 是
混合物 思路方法 选用物质
A CO (CO) 点燃 空气
2
B NaOH(Na CO ) 沉淀、过滤 石灰乳[Ca(OH)
2 3 2
C FeCl (CuCl ) 置换、过滤 铁粉
2 2
D NaCl(MgCl ) 沉淀、过滤 NaOH ]
2
A.A B.BC.CD.D
【考点】物质除杂或净化的探究;常见气体的检验与除杂方法;盐的化学性质.
【专题】物质的分离、除杂、提纯与共存问题.
【分析】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去
杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质
反应,不能与原物质反应;②反应后不能引入新的杂质.
【解答】解:A、除去二氧化碳中的一氧化碳不能够点燃,这是因为当二氧化碳(不能燃烧、不
能支持燃烧)大量存在时,少量的一氧化碳是不会燃烧的;且除去气体中的气体杂质不能使
用气体,否则会引入新的气体杂质,故选项所采取的方法错误.
B、Na CO 能与石灰乳反应生成碳酸钙和氢氧化钠,再过滤除去不溶物,能除去杂质且没有
2 3
引入新的杂质,符合除杂原则,故选项所采取的方法正确.
C、CuCl 能与铁粉反应生成氯化亚铁和铜,在过滤除去不溶物,能除去杂质且没有引入新的
2
杂质,符合除杂原则,故选项所采取的方法正确.
D、MgCl 能与NaOH溶液反应生成氢氧化镁沉淀和氯化钠,在过滤除去不溶物,能除去杂质
2
且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选A.
【点评】物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条
件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.
12.分别将下列各组物质同时加入到水中,最终能得到无色、透明溶液的是( )
A.BaCl 、NaOH、H SO B.KCl、NaOH、CuSO
2 2 4 4
C.HNO 、NaCl、K SO D.FeCl 、Na SO 、KCl
3 2 4 3 2 4
【考点】离子或物质的共存问题.
【专题】物质的分离、除杂、提纯与共存问题.
【分析】A、根据氯化钡和硫酸会生成白色的硫酸钡沉淀进行分析;
B、根据硫酸铜在溶液中显蓝色进行分析;
C、根据所有的钾盐、钠盐都溶于水进行分析;
D、根据铁离子在溶液中显黄色进行分析.
【解答】解:A、氯化钡和硫酸会生成白色的硫酸钡沉淀,而题中要求的是无色、透明溶液,所
以三种物质不能共存,故A错误;
B、硫酸铜在溶液中显蓝色,而题中要求的是无色、透明溶液,所以三种物质放入水中得到的
溶液不满足题意,故B错误;
C、所有的钾盐、钠盐都溶于水,三种物质都溶于水,形成的溶液都是无色的,满足题意,故C
正确;
D、铁离子在溶液中显黄色,而题中要求的是无色、透明溶液,所以三种物质放入水中得到的
溶液不满足题意,故D错误;
www.youyi100.com
第 12 页 共 19 页优秀领先 飞翔梦
想
故选:C.
【点评】在解此类题时,首先分析选项中物质的性质,只要会生成沉淀、气体、水中的一种,就
不能共存.
二、我会填空题(共16分,除化学方程式每空2分外,其余每空1分)
13.用化学用语填空:
(1)亚铁离子 F e 2 + ;(2)2个氮气分子 2N ;
2
(3)碳酸钠中的阴离子 CO 2﹣ ;(4)地壳中含量最多的金属元素 A l .
3
【考点】化学符号及其周围数字的意义.
【专题】化学用语和质量守恒定律.
【分析】(1)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷
数,数字在前,正负符号在后,带1个电荷时,1要省略.
(2)分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应
的数字.
(3)碳酸钠中的阴离子是碳酸根离子,写出其离子符号即可.
(4)地壳中含量最多的金属元素是铝元素,写出其元素符号即可.
【解答】解:(1)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正
负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.故亚铁离子可表示为:Fe2+.
(2)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相
应的数字,则2个氮气分子可表示为:2N .
2
(3)碳酸钠中的阴离子是碳酸根离子,其离子符号为:CO 2﹣.
3
(4)地壳中含量最多的金属元素是铝元素,其元素符号为:Al.
故答案为:(1)Fe2+;(2)2N ;(3)CO 2﹣;(4)Al.
2 3
【点评】本题难度不大,掌握常见化学用语(元素符号、分子符号、离子符号等)的书写方法是
正确解答此类题的关键.
14.水与人类的生活和生产密切相关,2010年“中国水周”的宣传主题是“严格水资源管理,
保障可持续发展”.为相应这一主题,某中学环保小组的同学配合环保部门.定期对流经我
市的河水进行取样测试.请根据某日采集的水样回答以下问题:
(1)在白瓷板上放一小片pH试纸,用玻璃棒蘸取少量(1)中所得到的液体,测得其pH大于
7,则说明该水样显 碱 性;
(2)由上述数据分析,该河水的主要污染物可能是(填序号) ② ;
①带有酸臭味的城市生活污水 ②化工厂排放的污水
(3)为了保护河水的水质,下列做法合理的是(填序号) ②③ .
①抑制水中所有动、植物的生长②不任意排放工业废水
③禁止使用农药和化肥④生活污水经过净化处理后再排放.
【考点】水资源的污染与防治;溶液的酸碱度测定;保护水资源和节约用水.
【专题】空气与水.
【分析】(1)根据酸碱和PH值的关系进行分析解答,
(2)根据排放的污水的酸碱性和待测液体的酸碱性分析,
(3)根据水污染的来源分析并判断.
【解答】解:(1)碱性溶液的pH值大于7,酸性溶液的pH值小于7,故答案为:碱,
(2)根据(2)可知溶液显碱性,而生活污水显酸性,可以排除①,故答案为:②,
www.youyi100.com
第 13 页 共 19 页优秀领先 飞翔梦
想
(3)①水中的动植物还可以净化水,不能抑制其生长,故错误,
②工业生产中的废水会造成工业污染,经过处理再排放,则能避免水污染,所以正确,
③农药和化肥可以提高农作物的产量,要合理使用,故错误,
④城市生活污水会造成生活污染,经过处理再排放,则能避免水污染,所以正确;
故答案为:
(1)碱;
(2)②;
(3)②④.
【点评】水资源缺乏的危机日益严重,要保护水资源首先要了解水体污染的来源.
15.豆腐是人们喜爱的食物,其主要成分如表所示.请回答下列问题:
豆腐的主要成分
物质 每100g含有
水 89.30g
蛋白质 4.70g
油脂 1.30g
糖类 2.80g
维生素B 0.06mg
1
维生素B 0.03mg
2
钙 0.24g
铁 1.40g
其它
(1)其中的铁、钙是指 ③ (填序号);
①分子 ②原子 ③元素
(2)当人体缺钙时,可能引起的疾病是 ① (填序号);
①骨质疏松症 ②贫血症 ③夜盲症
(3)豆腐中除了蛋白质、油脂、糖类、无机盐、水之外,还包括的营养物质是 维生素 ;
(4)豆腐常用塑料袋包装,请指出使用塑料袋包装的利与弊(各答一条).
利: 使用方便 ;弊: 造成白色污染 .
【考点】生命活动与六大营养素;元素的概念;白色污染与防治;人体的元素组成与元素对人
体健康的重要作用.
【专题】压轴实验题;化学与生活健康.
【分析】(1)豆腐中的铁、钙指的是元素;
(2)人体缺钙时,可能引起的疾病是骨质疏松;
(3)六大营养元素是指蛋白质、油脂、糖类、无机盐、水和维生素;
(4)结合塑料的成分、性质和在现实生活中的应用来回答.
【解答】解:(1)豆腐中的铁、钙指的是元素;
故选③.
(2)人体缺钙时,可能引起的疾病是骨质疏松;
故选①.
(3)六大营养元素是指蛋白质、油脂、糖类、无机盐、水和维生素;
故答案为:维生素.
(4)从现实生活中的应用和其成分得出答案,人们购物,放置物品等方面提供了方便,但是各
类生活塑料制品使用后被弃置成为固体废物,由于随意乱丢乱扔,难于降解处理,以致造成
城市环境严重污染的现象.
www.youyi100.com
第 14 页 共 19 页优秀领先 飞翔梦
想
故答案为:利:使用方便;弊:造成白色污染.
【点评】本题考查六大营养元素的种类和作用,属于基础知识,容易做好.
16.我国著名的化学家侯德榜先生发明的制碱原理为:
NH +CO +H O+NaCl═NH Cl+NaHCO 、 2NaHCO Na CO +H O+CO ↑ ,用
3 2 2 4 3 3 2 3 2 2
过滤 的方法可以把NaHCO 晶体从混合物中分离出来,在制取NaHCO 时,先向饱和的
3 3
NaCl溶液中通入较多的NH ,再通入足量的CO 的目的是 使 CO 更易被吸收 .
3 2 2
【考点】纯碱的制取;书写化学方程式、文字表达式、电离方程式.
【专题】元素与化合物;常见的盐 化学肥料.
【分析】我国著名化学家侯德榜发明的联合制碱法,主要原理是:向浓氨水(NH •H O)中通入
3 2
足量的CO ,然后加入食盐充分搅拌,反应生成氯化铵和碳酸氢钠,由于碳酸氢钠的溶解度
2
很小,以晶体形式析出,将析出的碳酸氢钠加热得碳酸钠、二氧化碳和水,写出反应的化学方
程式即可.
二氧化碳与水反应形成不稳定的碳酸,使水吸收二氧化碳量较少,而把二氧化碳通入溶有氨
气而呈碱性的水中,会使生成的碳酸与氨水发生反应,而增大二氧化碳气体的吸收.
【解答】解:我国著名化学家侯德榜发明的联合制碱法,主要原理是:向浓氨水(NH •H O)中
3 2
通入足量的CO ,然后加入食盐充分搅拌,反应生成氯化铵和碳酸氢钠,反应的化学方程式
2
为:NH +CO +H O+NaCl═NH Cl+NaHCO .由于碳酸氢钠的溶解度很小,以晶体形式析出,
3 2 2 4 3
进行过滤,将析出的碳酸氢钠加热得碳酸钠、二氧化碳和水,反应的化学方程式为:2NaHCO
3
Na CO +H O+CO ↑.
2 3 2 2
在制取NaHCO 时,先向饱和的NaCl溶液中通入较多的NH ,再通入足量的CO 的目的是
3 3 2
先通入氨气,氨气与水形成呈碱性的氨水可与二氧化碳与水生成的碳酸发生反应,更有利于
二氧化碳气体的吸收.
故答案为:NH +CO +H O+NaCl═NH Cl+NaHCO ;2NaHCO Na CO +H O+CO ↑;过
3 2 2 4 3 3 2 3 2 2
滤;使CO 更易被吸收.
2
【点评】本题难度不大,了解侯德榜先生发明的制碱原理、化学方程式的书写方法等是正确解
答本题的关键.
三、我会回答(共18分,化学方程式每空3分,其余每空2分)
17.高铁的出现使交通运输业水平又上升到一个新的层次.高铁建设工程技术人员常利用点
燃铝热剂的方法来焊接钢轨.铝热剂是铝粉和氧化铁粉末的混合物,燃烧生成铁和氧化铝.
(1)钢轨属于 合金 (填“单质”、“合金”、“氧化物”之一).
(2)点燃铝热剂反应的化学方程式为: F e O +2Al Al O +2Fe .反应类型为 置换
2 3 2 3
反应 .(填“分解”、“化合”、“置换”、“复分解”之一)
(3)某同学回忆起一氧化碳与氧化铁反应时,一氧化碳是还原剂,他推理得出上述反应中还
原剂是 铝 (选填“铝”或“氧化铁”).在铝热剂中元素化合价为零的物质是 铝 .
【考点】金属材料及其应用;反应类型的判定;书写化学方程式、文字表达式、电离方程式.
【专题】化学用语和质量守恒定律;物质的分类;金属与金属材料.
【分析】(1)依据钢的组成分析解答;
www.youyi100.com
第 15 页 共 19 页优秀领先 飞翔梦
想
(2)依据关于该反应的叙述结合化学方程式的书写规则书写即可,并依据反应前后物质的种
类判断反应的基本类型;
(3)依据还原剂得氧被氧化,单质的化合价为零分析判断;
【解答】解:(1)钢属于铁的一种合金,不是铁的氧化物和单质;
(2)依据叙述可知该反应的反应物是铝和氧化铁,生成物是氧化铝和铁,其反应的方程式为:
Fe O +2Al Al O +2Fe,该反应的反应物和生成物均是一种单质与一种化合物,所以
2 3 2 3
是置换反应.
(3)由于该反应中铝得到氧被氧化所以铝是该反应的还原剂,因为单质中元素的化合价为零,
所以在铝热剂中元素化合价为零的物质是铝;
故答案为:(1)合金;(2)Fe O +2Al Al O +2Fe;置换反应;(3)铝;铝;
2 3 2 3
【点评】此题是有关金属的基础知识考查,解题时只要抓住铝热反应的特点以及氧化还原反
应的实质就可顺利解题.
18.如图是有关物质转化关系的示意图,其中A是含有碳元素的化合物,D是一种含有钠元
素的化合物,请回答下列问题:
(1)写出下列物质的化学式:A: CaCO G: H O
3 2
(2)写出B和F反应的化学方程式: 2NaOH+CO ═Na CO +H O .
2 2 3 2
【考点】物质的鉴别、推断;书写化学方程式、文字表达式、电离方程式.
【专题】框图型推断题;物质的检验、鉴别与推断.
【分析】高温条件下,碳酸钙分解生成氧化钙和二氧化碳,氧化钙和水反应生成氢氧化钙,二
氧化碳和氢氧化钠反应生成碳酸钠和水,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化
钠.
【解答】解:高温条件下,碳酸钙分解生成氧化钙和二氧化碳,氧化钙和水反应生成氢氧化钙,
二氧化碳和氢氧化钠反应生成碳酸钠和水,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧
化钠,因此ABCDEFG分别是碳酸钙、二氧化碳、氧化钙、碳酸钠、氢氧化钙、氢氧化钠和水;
(1)A是碳酸钙,G是水,化学式分别是CaCO 、H O.
3 2
故填:CaCO ;H O.
3 2
(2)B和F分别是二氧化碳和氢氧化钠,二氧化碳和氢氧化钠反应生成碳酸钠和水,反应的
化学方程式为:2NaOH+CO ═Na CO +H O.
2 2 3 2
故填:2NaOH+CO ═Na CO +H O.
2 2 3 2
【点评】本题主要考查物质的性质,只有掌握了各种物质的性质,才能够判断物质之间相互转
化时的反应物和生成物,从而可以进行各方面的判断.
四、我会实验(共22分,除19(1)每空1分,其余每空2分)
19.以下是我们熟悉的实验室制取气体的发生装置、收集装置,请回答下列问题:
www.youyi100.com
第 16 页 共 19 页优秀领先 飞翔梦
想
(1)写出图1装置中有标号仪器的名称:a 酒精灯 ;b 集气瓶 .
(2)利用上述A、D装置的组合可以制取的一种气体是 二氧化碳(或氧气) ,写出实验室
制取该气体的化学方程式 CaCO +2HCl=CaCl +H O+CO ↑ 或 2H O 2H O+O ↑ ,
3 2 2 2 2 2 2 2
检验该气体是否收集满的方法是 将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了
(或将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了) .
(3)若用B装置作为制取气体的发生装置,应满足的条件是 要加热 .
(4)若用图2所示的装置,收集一瓶难溶于水的气体,实验前将该装置装满水正放,则气体应
从 d (填“c”或“d”)端进入.将该装置装满水倒放,则气体应从 c (填“c”或“d”)端
进入.
【考点】常用气体的发生装置和收集装置与选取方法;实验室制取气体的思路;实验室制取氧
气的反应原理;二氧化碳的实验室制法;书写化学方程式、文字表达式、电离方程式.
【专题】常见气体的实验室制法、检验、干燥与净化.
【分析】酒精灯是常用的加热仪器,集气瓶是收集气体的仪器;制取装置包括加热和不需加热
两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需
要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;氧
气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了.实验室制取
CO ,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化
2
钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用
向上排空气法收集.二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,
证明满了.若用图2所示的装置,收集一瓶难溶于水的气体,实验前将该装置装满水正放,则
气体应从短管进入,因为气体的密度比水小;将该装置装满水倒放,则气体应从短管进入.
【解答】解:(1)酒精灯是常用的加热仪器,集气瓶是收集气体的仪器;故答案为:酒精灯;集
气瓶;(2)利用上述A、D装置的组合可以制取的一种气体是:二氧化碳(或氧气);二氧化碳
的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;氧气的验满方法是:
将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;故答案为:氧气或二氧化碳;
CaCO +2HCl=CaCl +H O+CO ↑或2H O 2H O+O ↑;将一根燃着的木条平放在集气
3 2 2 2 2 2 2 2
瓶口,木条熄灭,证明满了(或将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了);
(3)若用B装置作为制取气体的发生装置,应满足的条件是要加热,故答案为:要加热;
(4)若用图2所示的装置,收集一瓶难溶于水的气体,实验前将该装置装满水正放,则气体应
从短管进入,因为气体的密度比水小;将该装置装满水倒放,则气体应从短管进入;故答案为:
d;c;
【点评】本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化
学方程式的书写和气体的验满等,综合性比较强.气体的制取装置的选择与反应物的状态和
www.youyi100.com
第 17 页 共 19 页优秀领先 飞翔梦
想
反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要
考点之一,主要出现在实验题中.
20.氢化钙固体是登山运动员常用的能源提供剂.某探究小组的同学通过查阅资料得知,氢
化钙(CaH )遇水反应生成氢氧化钙和氢气.探究小组的同学把一定量的CaH 加入Na CO
2 2 2 3
溶液中,充分反应后过滤,得到滤渣和滤液,经检验,滤渣的成分是碳酸钙.
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】
猜想一:NaOH 猜想二: NaOH 和 C a ( OH ) .
2
猜想三:NaOH和Na CO 猜想四:NaOH、Na CO 和Ca(OH)
2 3 2 3 2
经过讨论,大家一致认为猜想四不合理,其原因是 N a CO +Ca( OH ) ═CaCO ↓+2NaOH .
2 3 2 3
【实验验证】
实验 现象 结论
实验一:取滤液,向其中滴入少量碳酸无明显现象
钠溶液 猜想二 不成立
实验二:另取滤液,向其中加入足量稀 猜想三成立
盐酸 先无变化后产生气泡
实验二中发生明显现象的化学方程式是 N a CO +2HCl═2NaCl+H O+CO ↑ .
2 3 2 2
【反思与拓展】登山运动员常用CaH 作为能源提供剂,与氢气相比的优点是 携带安全 .
2
【考点】实验探究物质的组成成分以及含量;碱的化学性质;盐的化学性质;书写化学方程式、
文字表达式、电离方程式.
【专题】科学探究.
【分析】由题目的信息可知:氢氧化钙和碳酸钠反应时,可能恰好完全反应,这时的滤液中含
有的溶质是氢氧化钠;如果氢氧化钙过量时,滤液中含有的溶质是氢氧化钠和氢氧化钙;如
果碳酸钠过量时,滤液中含有的溶质是氢氧化钠和碳酸钠,猜想三应是氢氧化钠和碳酸钠;
另外由题目的信息可知:猜想四是不合理的,因为碳酸钠与氢氧化钙不能共存,碳酸钠与氢
氧化钙反应生成碳酸钙白色沉淀和氢氧化钠,配平即可;
在实验一中,取滤液,向其中滴入少量碳酸钠溶液,无明显现象,说明没有氢氧化钙,即猜想
二不成立;
实验二:另取滤液,向其中加入足量稀盐酸,观察到先无变化后产生气泡的现象时,说明滤液
中含有氢氧化钠和碳酸钠,即猜想三成立;若向NH Cl的溶液中加一定量CaH ,充分反应,
4 2
产生的气体是氧气、氨气,因为氢化钙(CaH )与水反应生成氢氧化钙和氢气,氯化铵和氢氧
2
化钙反应生成氯化钙和水和氨气;登山运动员常用CaH 作为能源提供剂,与氢气相比,其优
2
点是携带安全.
【解答】解:【猜想与假设】
由题目的信息可知:氢氧化钙和碳酸钠反应时,可能恰好完全反应,这时的滤液中含有的溶
质是氢氧化钠;如果氢氧化钙过量时,滤液中含有的溶质是氢氧化钠和氢氧化钙;如果碳酸
钠过量时,滤液中含有的溶质是氢氧化钠和碳酸钠,猜想二应是氢氧化钠和碳酸钠;
由题目的信息可知:猜想四是不合理的,因为碳酸钠与氢氧化钙不能共存,碳酸钠与氢氧化
钙反应生成碳酸钙白色沉淀和氢氧化钠,配平即可;故答案为:Na CO +Ca(OH)
2 3
=CaCO ↓+2NaOH.
2 3
【实验证明】
实验一,取滤液,向其中滴入少量碳酸钠溶液,没有产生沉淀,说明没有氢氧化钙,即猜想二
不成立;
www.youyi100.com
第 18 页 共 19 页优秀领先 飞翔梦
想
实验二:另取滤液,向其中加入足量稀盐酸,观察到先无变化后产生气泡的现象时,说明滤液
中含有氢氧化钠和碳酸钠,即猜想三成立;
碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:
Na CO +2HCl═2NaCl+H O+CO ↑.
2 3 2 2
【反思与拓展】
登山运动员常用CaH 作为能源提供剂,与氢气相比,其优点是携带安全;
2
故答案为:
【猜想与假设】NaOH和Ca(OH) ;Na CO +Ca(OH) ═CaCO ↓+2NaOH.
2 2 3 2 3
【实验证明】实验一:猜想二;实验二:先无变化后产生气泡.
Na CO +2HCl═2NaCl+H O+CO ↑.
2 3 2 2
【反思与拓展】携带安全.
【点评】本题既考查了实验步骤的设计,又考查了化学方程式的书写,还对实验进行了评价,
综合性比较强.实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验
结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性
探究.同学们要具体分析,综合掌握.
五、计算题(共8分)
21.盐水选种是我国古代劳动人民发明的一种巧妙的挑选种子的方法.农业生产上常用质量
分数为15%﹣20%的氯化钠溶液来选种.
(1)要配制150kg16%的氯化钠,计算应称取氯化钠的质量.
(2)选种进行一段时间后,农技员估计溶液和溶质质量分数都有所减少,他取出50g氯化钠
溶液,加入过量的AgNO 溶液,得到沉淀14.35g,计算氯化钠溶液中溶质的质量分数.
3
【考点】根据化学反应方程式的计算;有关溶质质量分数的简单计算.
【专题】溶质质量分数与化学方程式相结合的计算;有关化学方程式的计算.
【分析】(1)根据氯化钠的质量=氯化钠溶液×溶液溶质质量分数进行解答;
(2)根据氯化银的质量求出氯化钠的质量再求出氯化钠溶液中溶质的质量分数;
【解答】解:(1)氯化钠的质量:150kg×16%=24kg
(2)设溶液中氯化钠的物质的量为x,
AgNO +NaCl=AgCl↓+NaNO
3 3
58.5 143.5
x 14.35g
x=5.85g
氯化钠溶液中溶质的质量分数= ×100%=11.7%
故答案:(1)应称取氯化钠的质量为24kg.
(2)氯化钠溶液中溶质的质量分数为11.7%.
【点评】本题主要考查了根据化学方程式计算有关物质的质量和有关溶质质量分数的计算,
培养学生的分析问题、解决问题的能力,难度较大.
www.youyi100.com
第 19 页 共 19 页