文档内容
《化学反应与电能》单元测试(基础巩固)
学校:___________姓名:___________班级:___________考号:___________
一、单选题(共54分)
1.(本题3分)一般情况下,两种活泼性不同的金属在潮湿的环境中接触时,活泼性强的金属首先被腐蚀。
为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌的金属是
A.锌板 B.银板 C.铜板 D.铅板
2.(本题3分) 原电池的电极反应式不仅与电极材料的性质有关,也与电解质溶液有关。下列说法错误的
是
A.由金属Al、Cu和浓硝酸组成的原电池,经过一段时间后负极反应式为:
B.由金属Al、Cu和稀硫酸组成的原电池,负极反应式为:
C.由Al、Mg、NaOH溶液组成的原电池,负极反应式为
D.由Fe、Cu、 溶液组成的原电池,负极反应式为:
3.(本题3分)关于铅蓄电池的说法正确的是
A.在放电时,电池的正极材料是铅板
B.在放电时,电池的负极材料质量减小
C.在放电时, 向正极迁移
D.在放电时,正极发生的反应是:4.(本题3分)微型银—锌电池可用作电子仪器的电源,其电极分别是Ag/Ag O和Zn,电解质为KOH溶液,
2
电池总反应为 ,下列说法正确的是
A.电池工作过程中,KOH溶液浓度降低
B.电池工作过程中,电解液中 向正极迁移
C.负极发生反应
D.正极发生反应
杨sir化学,侵权必究
5.(本题3分)根据甲醇在酸性电解质溶液中与氧气作用生成二氧化碳和水的反应,设计一种燃料电池。该
燃料电池工作时,负极上发生的反应为。
A.
B.
C.
D.
6.(本题3分) 银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示为:
。下列说法不正确的是
A.该电池属于二次电池和碱性电池
B. 电极是电池的负极,发生氧化反应
C.电池工作过程中,电解质溶液的浓度保持不变
D.充电时,电池的正极应与电源的正极相连
7.(本题3分)下列有关电化学的说法正确的是
A.原电池的金属负极质量一定减小 B.待充电电池的负极应与电源正极相连
杨sir化学,侵权必究
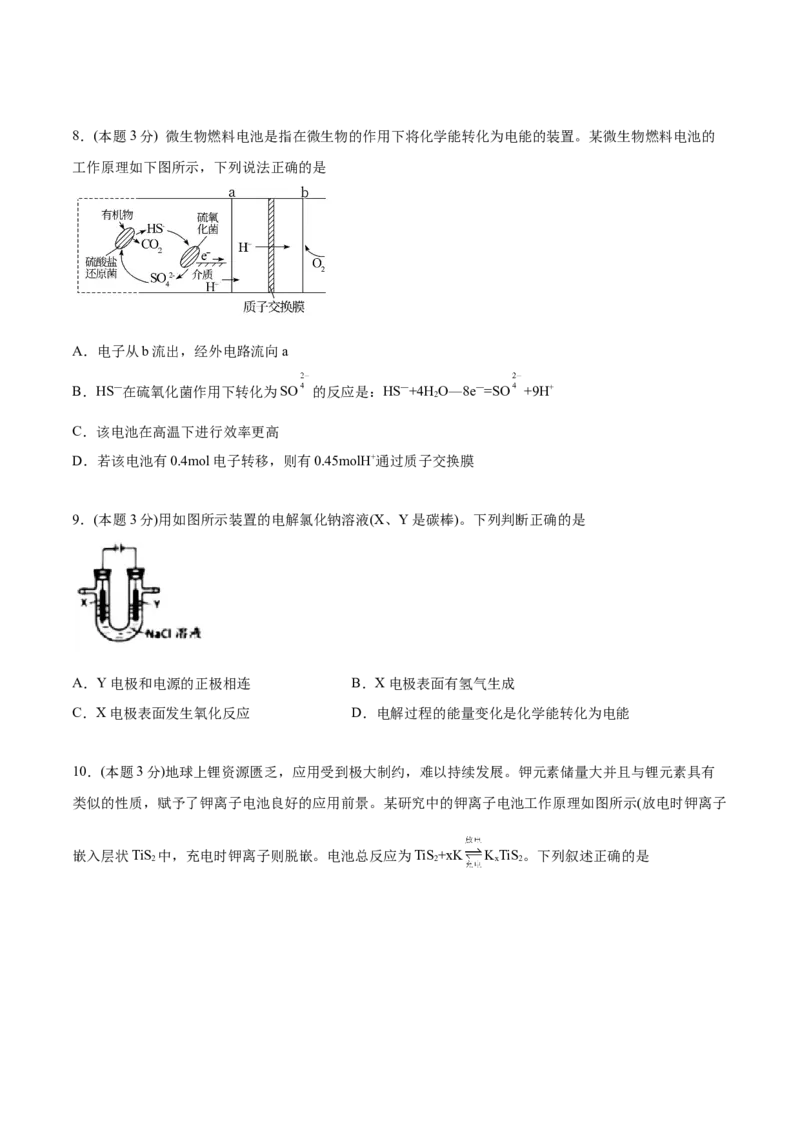
C.电解池的电解质溶液质量一定减小 D.原电池工作时在溶液中电流由负极到正极8.(本题3分) 微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的
工作原理如下图所示,下列说法正确的是
A.电子从b流出,经外电路流向a
B.HS—在硫氧化菌作用下转化为SO 的反应是:HS—+4H O—8e—=SO +9H+
2
C.该电池在高温下进行效率更高
杨sir化学,侵权必究
D.若该电池有0.4mol电子转移,则有0.45molH+通过质子交换膜
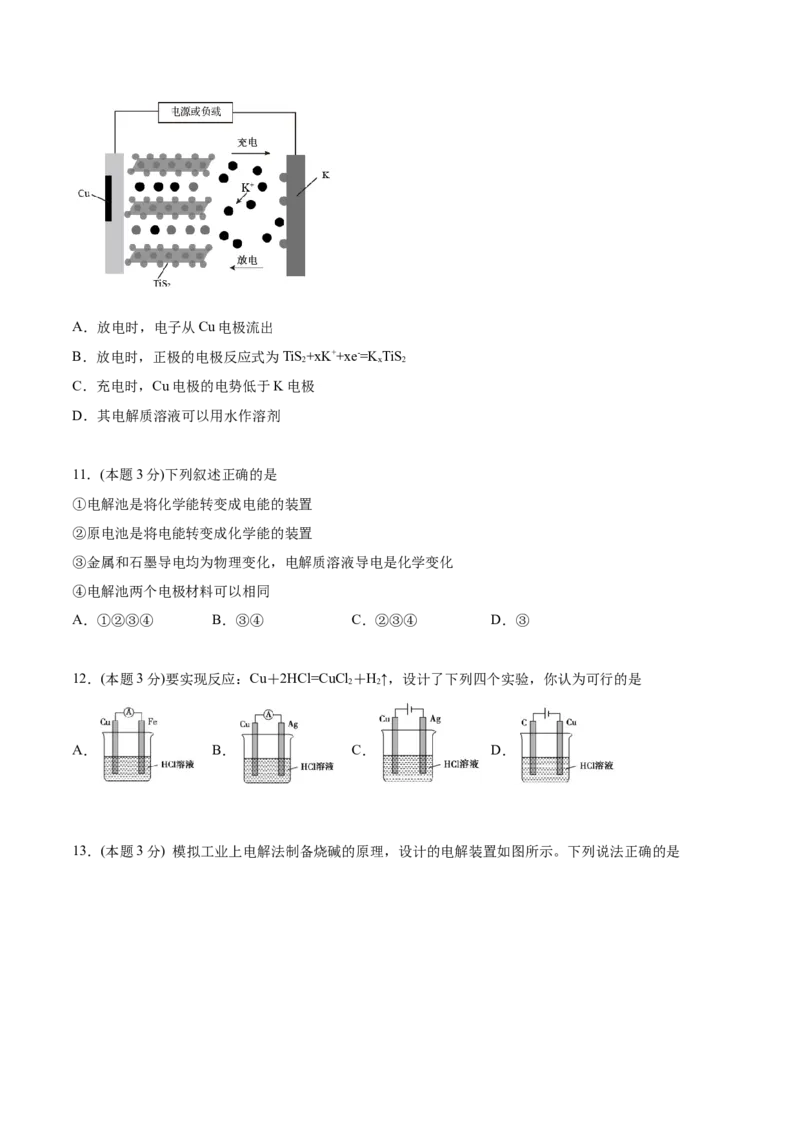
9.(本题3分)用如图所示装置的电解氯化钠溶液(X、Y是碳棒)。下列判断正确的是
A.Y电极和电源的正极相连 B.X电极表面有氢气生成
C.X电极表面发生氧化反应 D.电解过程的能量变化是化学能转化为电能
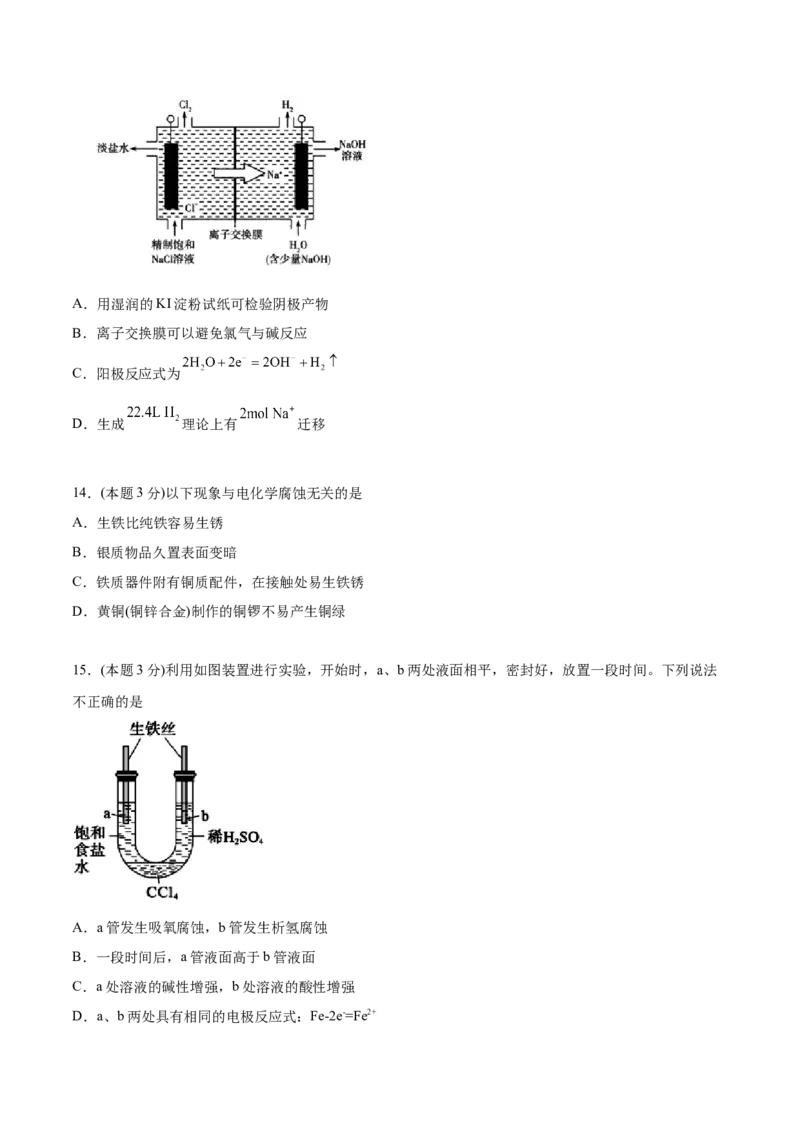
10.(本题3分)地球上锂资源匮乏,应用受到极大制约,难以持续发展。钾元素储量大并且与锂元素具有
类似的性质,赋予了钾离子电池良好的应用前景。某研究中的钾离子电池工作原理如图所示(放电时钾离子
嵌入层状TiS 中,充电时钾离子则脱嵌。电池总反应为TiS +xK KTiS 。下列叙述正确的是
2 2 x 2A.放电时,电子从Cu电极流出
B.放电时,正极的电极反应式为TiS +xK++xe-=K TiS
2 x 2
C.充电时,Cu电极的电势低于K电极
杨sir化学,侵权必究
D.其电解质溶液可以用水作溶剂
11.(本题3分)下列叙述正确的是
①电解池是将化学能转变成电能的装置
②原电池是将电能转变成化学能的装置
③金属和石墨导电均为物理变化,电解质溶液导电是化学变化
④电解池两个电极材料可以相同
A.①②③④ B.③④ C.②③④ D.③
12.(本题3分)要实现反应:Cu+2HCl=CuCl +H↑,设计了下列四个实验,你认为可行的是
2 2
A. B. C. D.
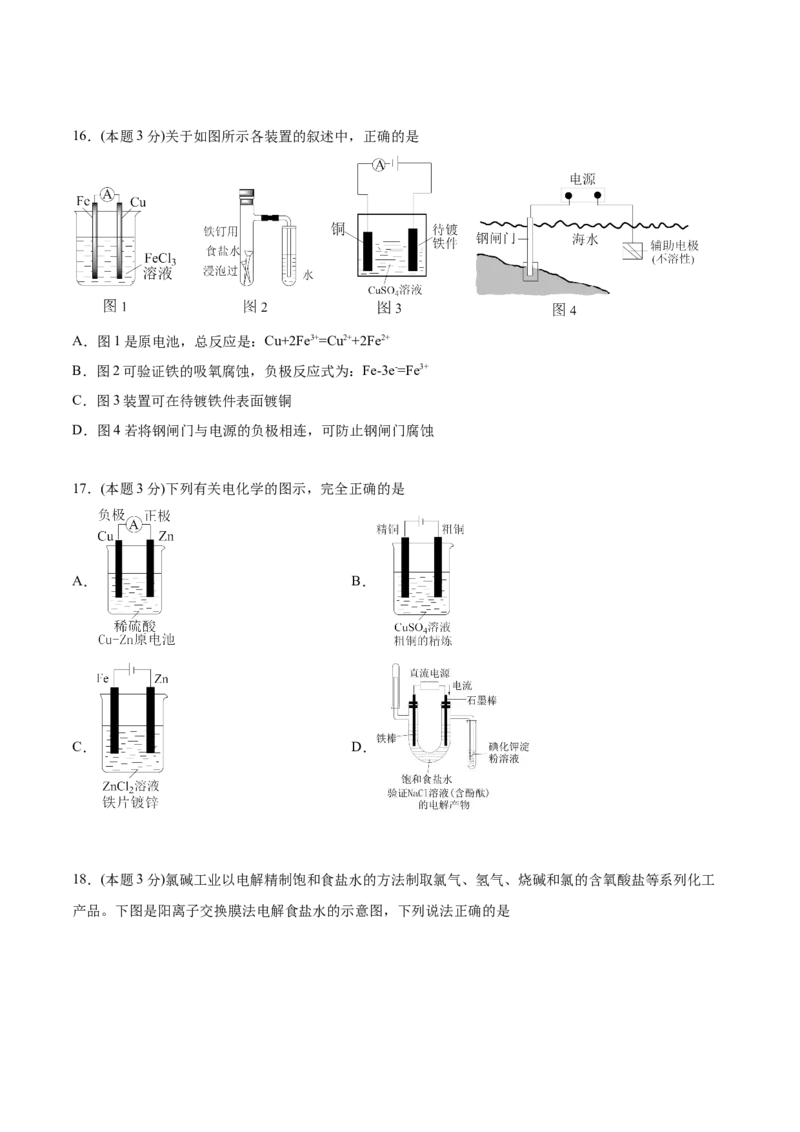
13.(本题3分) 模拟工业上电解法制备烧碱的原理,设计的电解装置如图所示。下列说法正确的是A.用湿润的KI淀粉试纸可检验阴极产物
B.离子交换膜可以避免氯气与碱反应
C.阳极反应式为
D.生成 理论上有 迁移
杨sir化学,侵权必究
14.(本题3分)以下现象与电化学腐蚀无关的是
A.生铁比纯铁容易生锈
B.银质物品久置表面变暗
C.铁质器件附有铜质配件,在接触处易生铁锈
D.黄铜(铜锌合金)制作的铜锣不易产生铜绿
15.(本题3分)利用如图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间。下列说法
不正确的是
A.a管发生吸氧腐蚀,b管发生析氢腐蚀
B.一段时间后,a管液面高于b管液面
C.a处溶液的碱性增强,b处溶液的酸性增强
D.a、b两处具有相同的电极反应式:Fe-2e-=Fe2+
杨sir化学,侵权必究16.(本题3分)关于如图所示各装置的叙述中,正确的是
A.图1是原电池,总反应是:Cu+2Fe3+=Cu2++2Fe2+
B.图2可验证铁的吸氧腐蚀,负极反应式为:Fe-3e-=Fe3+
C.图3装置可在待镀铁件表面镀铜
D.图4若将钢闸门与电源的负极相连,可防止钢闸门腐蚀
17.(本题3分)下列有关电化学的图示,完全正确的是
A. B.
C. D.
杨sir化学,侵权必究
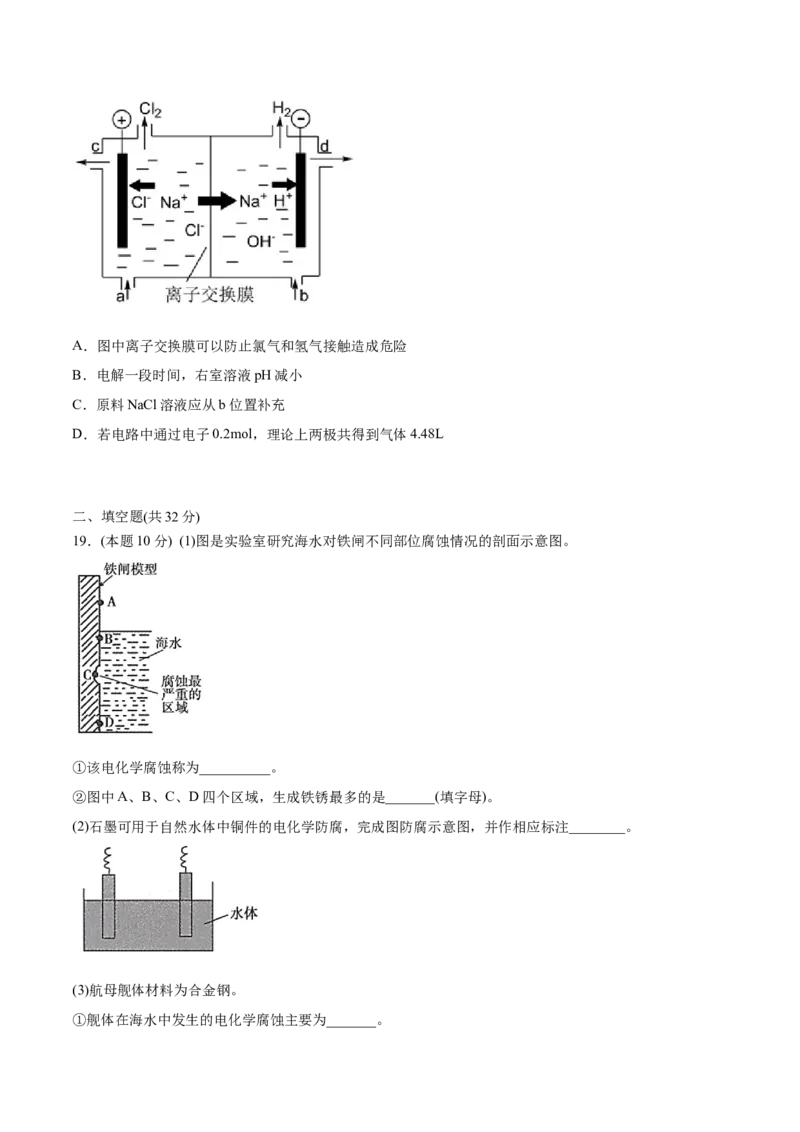
18.(本题3分)氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工
产品。下图是阳离子交换膜法电解食盐水的示意图,下列说法正确的是A.图中离子交换膜可以防止氯气和氢气接触造成危险
B.电解一段时间,右室溶液pH减小
C.原料NaCl溶液应从b位置补充
D.若电路中通过电子0.2mol,理论上两极共得到气体4.48L
杨sir化学,侵权必究
二、填空题(共32分)
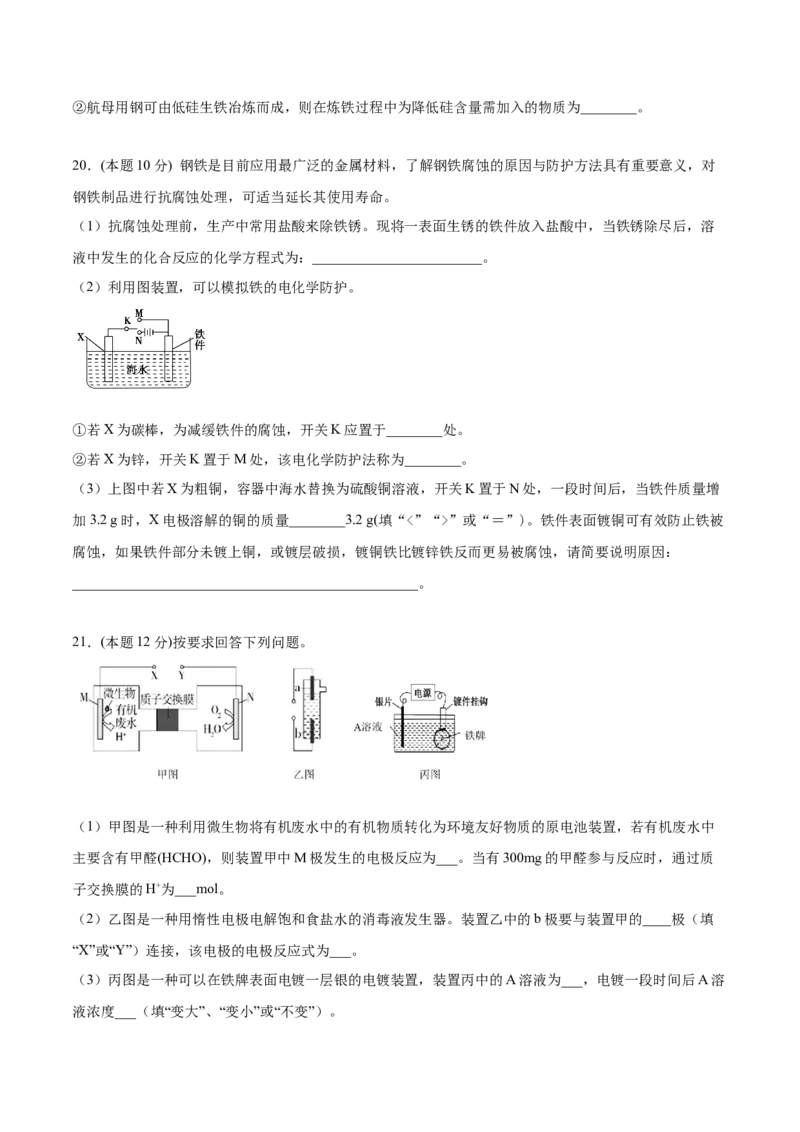
19.(本题10分) (1)图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。
①该电化学腐蚀称为__________。
②图中A、B、C、D四个区域,生成铁锈最多的是_______(填字母)。
(2)石墨可用于自然水体中铜件的电化学防腐,完成图防腐示意图,并作相应标注________。
(3)航母舰体材料为合金钢。
①舰体在海水中发生的电化学腐蚀主要为_______。
杨sir化学,侵权必究②航母用钢可由低硅生铁冶炼而成,则在炼铁过程中为降低硅含量需加入的物质为________。
20.(本题10分) 钢铁是目前应用最广泛的金属材料,了解钢铁腐蚀的原因与防护方法具有重要意义,对
钢铁制品进行抗腐蚀处理,可适当延长其使用寿命。
(1)抗腐蚀处理前,生产中常用盐酸来除铁锈。现将一表面生锈的铁件放入盐酸中,当铁锈除尽后,溶
液中发生的化合反应的化学方程式为:________________________。
(2)利用图装置,可以模拟铁的电化学防护。
杨sir化学,侵权必究
①若X为碳棒,为减缓铁件的腐蚀,开关K应置于________处。
②若X为锌,开关K置于M处,该电化学防护法称为________。
(3)上图中若X为粗铜,容器中海水替换为硫酸铜溶液,开关K置于N处,一段时间后,当铁件质量增
加3.2 g时,X电极溶解的铜的质量________3.2 g(填“<”“>”或“=”)。铁件表面镀铜可有效防止铁被
腐蚀,如果铁件部分未镀上铜,或镀层破损,镀铜铁比镀锌铁反而更易被腐蚀,请简要说明原因:
_________________________________________________。
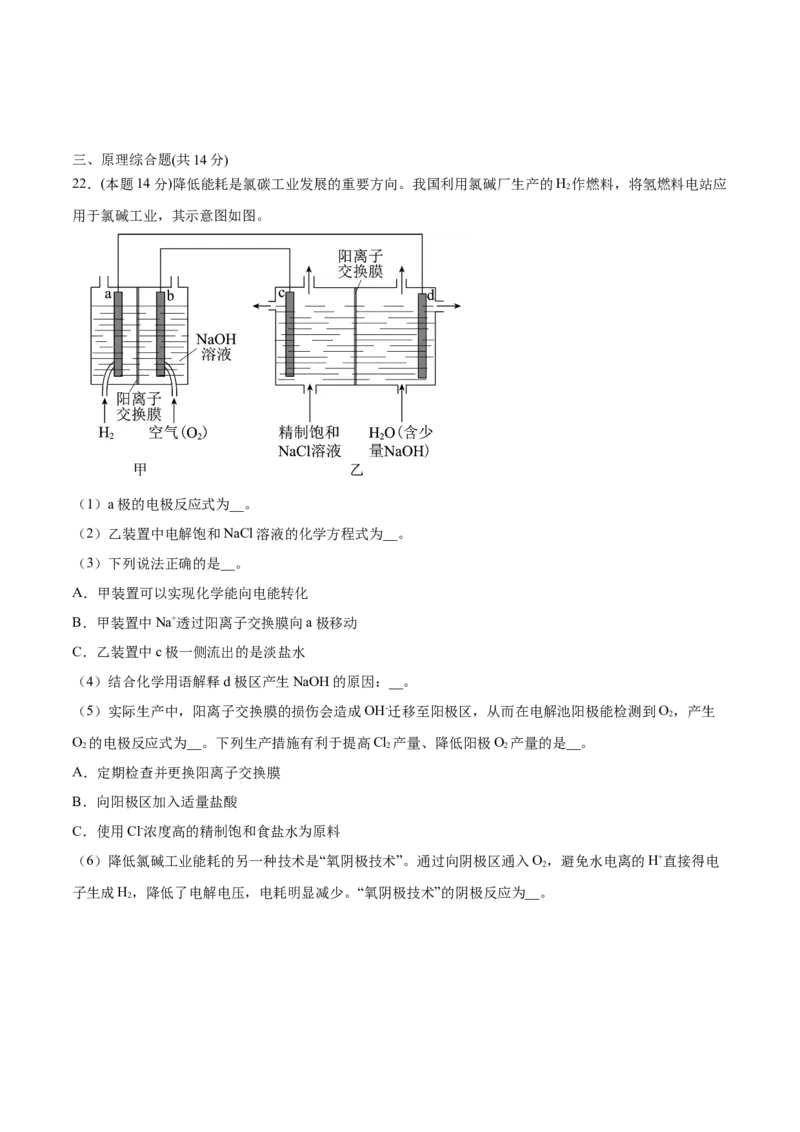
21.(本题12分)按要求回答下列问题。
(1)甲图是一种利用微生物将有机废水中的有机物质转化为环境友好物质的原电池装置,若有机废水中
主要含有甲醛(HCHO),则装置甲中M极发生的电极反应为___。当有300mg的甲醛参与反应时,通过质
子交换膜的H+为___mol。
(2)乙图是一种用惰性电极电解饱和食盐水的消毒液发生器。装置乙中的b极要与装置甲的____极(填
“X”或“Y”)连接,该电极的电极反应式为___。
(3)丙图是一种可以在铁牌表面电镀一层银的电镀装置,装置丙中的A溶液为___,电镀一段时间后A溶
液浓度___(填“变大”、“变小”或“不变”)。
杨sir化学,侵权必究三、原理综合题(共14分)
22.(本题14分)降低能耗是氯碳工业发展的重要方向。我国利用氯碱厂生产的H 作燃料,将氢燃料电站应
2
用于氯碱工业,其示意图如图。
(1)a极的电极反应式为__。
(2)乙装置中电解饱和NaCl溶液的化学方程式为__。
(3)下列说法正确的是__。
A.甲装置可以实现化学能向电能转化
B.甲装置中Na+透过阳离子交换膜向a极移动
C.乙装置中c极一侧流出的是淡盐水
(4)结合化学用语解释d极区产生NaOH的原因:__。
(5)实际生产中,阳离子交换膜的损伤会造成OH-迁移至阳极区,从而在电解池阳极能检测到O,产生
2
O 的电极反应式为__。下列生产措施有利于提高Cl 产量、降低阳极O 产量的是__。
2 2 2
A.定期检查并更换阳离子交换膜
杨sir化学,侵权必究
B.向阳极区加入适量盐酸
C.使用Cl-浓度高的精制饱和食盐水为原料
(6)降低氯碱工业能耗的另一种技术是“氧阴极技术”。通过向阴极区通入O,避免水电离的H+直接得电
2
子生成H,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为__。
2倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育