文档内容
《化学反应与电能》单元测试(培优提升)
学校:___________姓名:___________班级:___________考号:___________
一、单选题(共45分)
1.(本题3分)下列叙述正确的是
①电解池是将化学能转变成电能的装置
②原电池是将电能转变成化学能的装置
③金属和石墨导电均为物理变化,电解质溶液导电是化学变化
④电解池两个电极材料可以相同
杨sir化学,侵权必究
A.①②③④ B.③④ C.②③④ D.③
2.(本题3分) 铜锌原电池为电化学建构认识模型奠定了重要的基础,懂得原理才能真正做到举一反三,
应用到其他复杂的电池分析中。盐桥中装有琼脂凝胶,内含氯化钾。下面两种原电池说法错误的是
A.原电池Ⅰ和Ⅱ的反应原理都是Zn+Cu2+=Zn2++Cu
B.电池工作时,导线中电子流向为Zn→Cu
C.正极反应为Zn-2e-=Zn2+,发生还原反应
D.电池工作时,盐桥中的K+向右侧烧杯移动,Cl-向左侧烧杯移动
杨sir化学,侵权必究
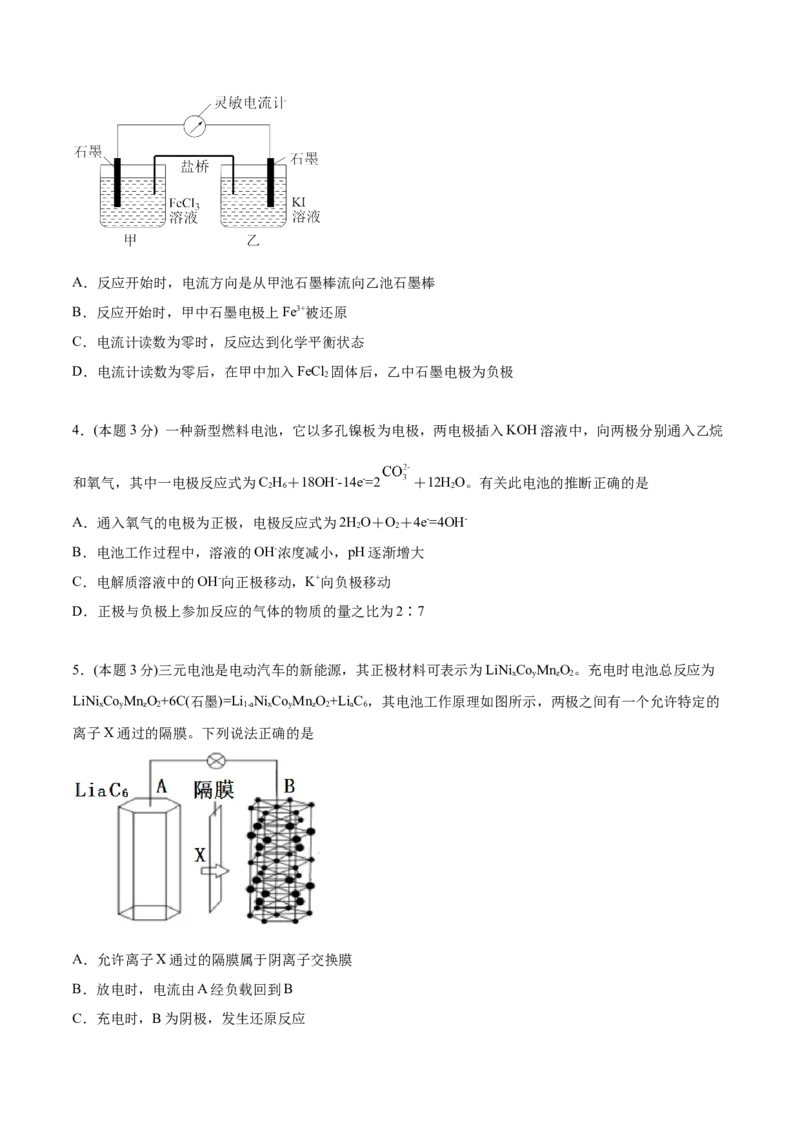
3.(本题3分)控制合适的条件,将反应2Fe3++ 2I- 2Fe2++ I 设计成如图所示原电池(甲池为FeCl 溶液,
2 3
乙池为KI溶液,盐桥的作用是形成闭合回路),下列判断不正确的是A.反应开始时,电流方向是从甲池石墨棒流向乙池石墨棒
B.反应开始时,甲中石墨电极上Fe3+被还原
C.电流计读数为零时,反应达到化学平衡状态
D.电流计读数为零后,在甲中加入FeCl 固体后,乙中石墨电极为负极
2 杨sir化学,侵权必究
4.(本题3分) 一种新型燃料电池,它以多孔镍板为电极,两电极插入KOH溶液中,向两极分别通入乙烷
和氧气,其中一电极反应式为C H+18OH--14e-=2 +12HO。有关此电池的推断正确的是
2 6 2
A.通入氧气的电极为正极,电极反应式为2HO+O+4e-=4OH-
2 2
B.电池工作过程中,溶液的OH-浓度减小,pH逐渐增大
C.电解质溶液中的OH-向正极移动,K+向负极移动
D.正极与负极上参加反应的气体的物质的量之比为2∶7
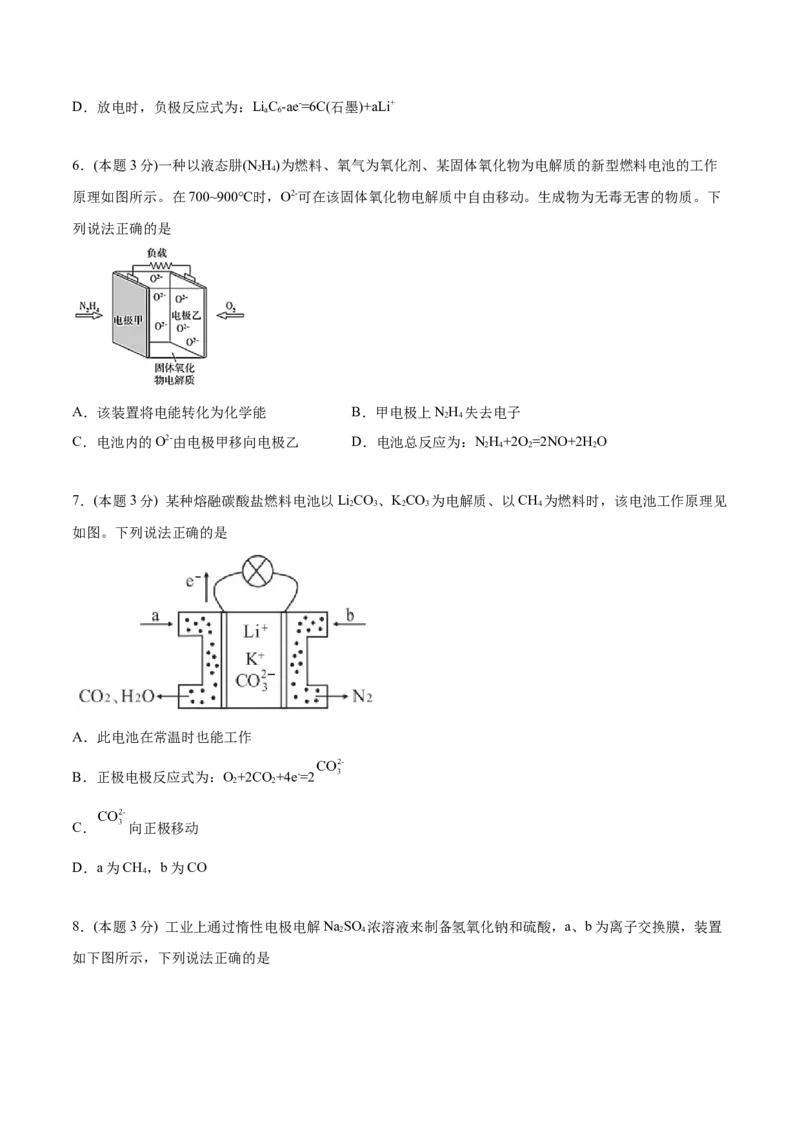
5.(本题3分)三元电池是电动汽车的新能源,其正极材料可表示为LiNiCo MnO。充电时电池总反应为
x y z 2
LiNiCo MnO+6C(石墨)=Li Ni Co MnO+LiC ,其电池工作原理如图所示,两极之间有一个允许特定的
x y z 2 1-a x y z 2 a 6
离子X通过的隔膜。下列说法正确的是
A.允许离子X通过的隔膜属于阴离子交换膜
B.放电时,电流由A经负载回到B
C.充电时,B为阴极,发生还原反应
杨sir化学,侵权必究D.放电时,负极反应式为:LiC -ae-=6C(石墨)+aLi+
a 6
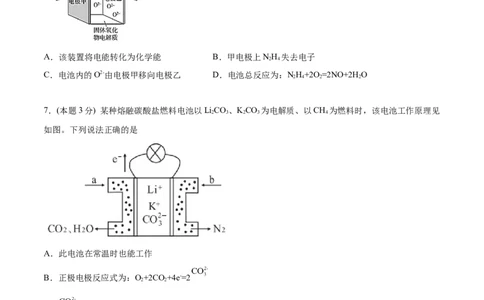
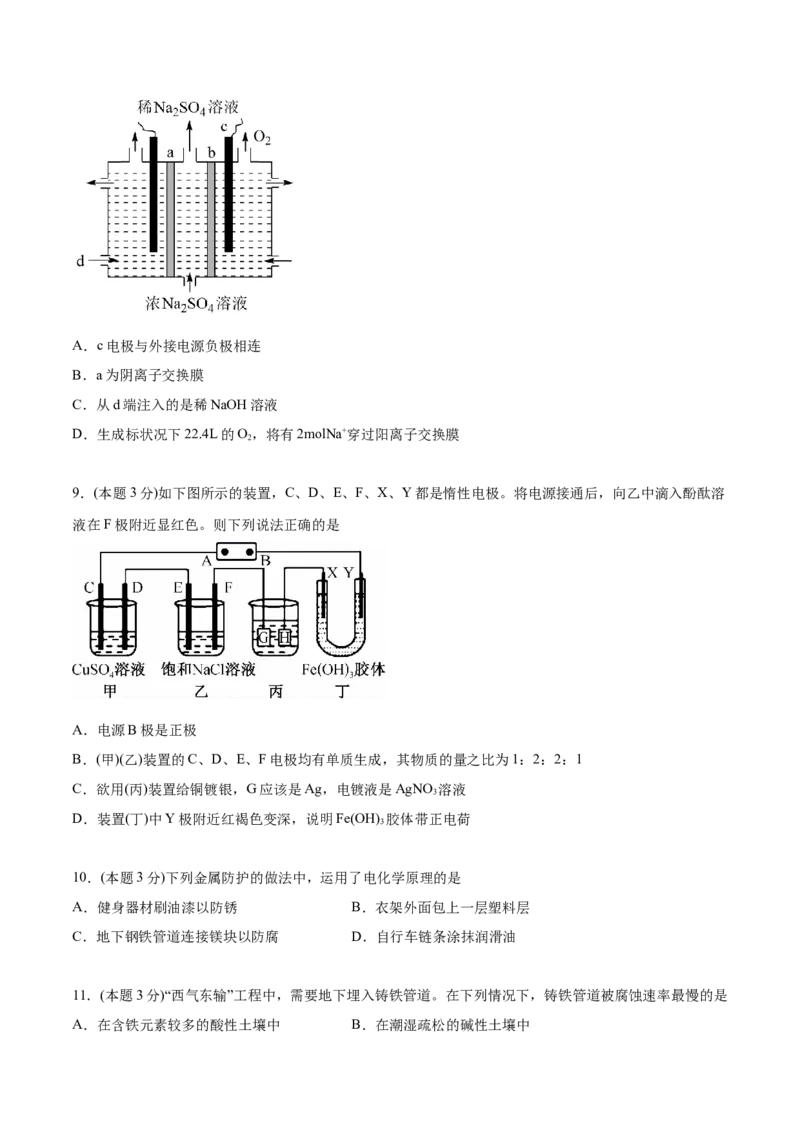
6.(本题3分)一种以液态肼(N H)为燃料、氧气为氧化剂、某固体氧化物为电解质的新型燃料电池的工作
2 4
原理如图所示。在700~900℃时,O2-可在该固体氧化物电解质中自由移动。生成物为无毒无害的物质。下
列说法正确的是
A.该装置将电能转化为化学能 B.甲电极上NH 失去电子
2 4
C.电池内的O2-由电极甲移向电极乙 D.电池总反应为:NH+2O =2NO+2HO
2 4 2 2
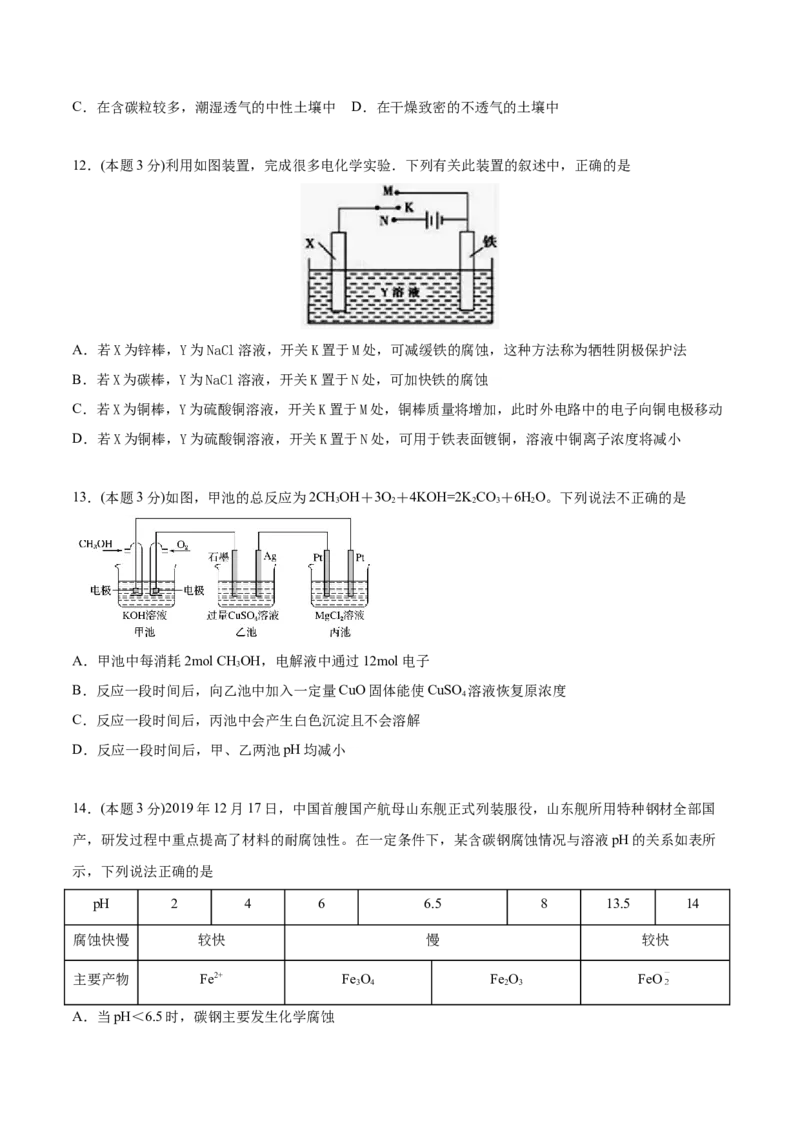
7.(本题3分) 某种熔融碳酸盐燃料电池以LiCO、KCO 为电解质、以CH 为燃料时,该电池工作原理见
2 3 2 3 4
如图。下列说法正确的是
A.此电池在常温时也能工作
B.正极电极反应式为:O+2CO +4e-=2
2 2
C. 向正极移动
D.a为CH,b为CO
4 杨sir化学,侵权必究
8.(本题3分) 工业上通过惰性电极电解NaSO 浓溶液来制备氢氧化钠和硫酸,a、b为离子交换膜,装置
2 4
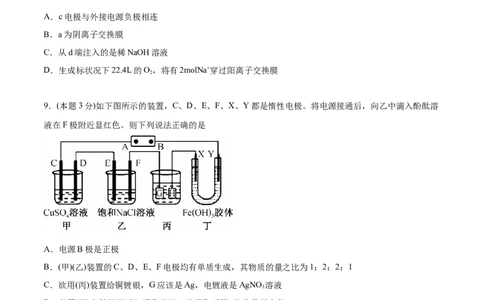
如下图所示,下列说法正确的是A.c电极与外接电源负极相连
B.a为阴离子交换膜
杨sir化学,侵权必究
C.从d端注入的是稀NaOH溶液
D.生成标状况下22.4L的O,将有2molNa+穿过阳离子交换膜
2
9.(本题3分)如下图所示的装置,C、D、E、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞溶
液在F极附近显红色。则下列说法正确的是
A.电源B极是正极
B.(甲)(乙)装置的C、D、E、F电极均有单质生成,其物质的量之比为1:2:2:1
C.欲用(丙)装置给铜镀银,G应该是Ag,电镀液是AgNO 溶液
3
D.装置(丁)中Y极附近红褐色变深,说明Fe(OH) 胶体带正电荷
3 杨sir化学,侵权必究
10.(本题3分)下列金属防护的做法中,运用了电化学原理的是
A.健身器材刷油漆以防锈 B.衣架外面包上一层塑料层
C.地下钢铁管道连接镁块以防腐 D.自行车链条涂抹润滑油
11.(本题3分)“西气东输”工程中,需要地下埋入铸铁管道。在下列情况下,铸铁管道被腐蚀速率最慢的是
A.在含铁元素较多的酸性土壤中 B.在潮湿疏松的碱性土壤中C.在含碳粒较多,潮湿透气的中性土壤中 D.在干燥致密的不透气的土壤中
12.(本题3分)利用如图装置,完成很多电化学实验.下列有关此装置的叙述中,正确的是
A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阴极保护法
B.若X为碳棒,Y为NaCl溶液,开关K置于N处,可加快铁的腐蚀
杨sir化学,侵权必究
C.若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动
D.若X为铜棒,Y为硫酸铜溶液,开关K置于N处,可用于铁表面镀铜,溶液中铜离子浓度将减小
13.(本题3分)如图,甲池的总反应为2CHOH+3O+4KOH=2K CO+6HO。下列说法不正确的是
3 2 2 3 2
A.甲池中每消耗2mol CHOH,电解液中通过12mol电子
3
B.反应一段时间后,向乙池中加入一定量CuO固体能使CuSO 溶液恢复原浓度
4
C.反应一段时间后,丙池中会产生白色沉淀且不会溶解
D.反应一段时间后,甲、乙两池pH均减小
杨sir化学,侵权必究
14.(本题3分)2019年12月17日,中国首艘国产航母山东舰正式列装服役,山东舰所用特种钢材全部国
产,研发过程中重点提高了材料的耐腐蚀性。在一定条件下,某含碳钢腐蚀情况与溶液pH的关系如表所
示,下列说法正确的是
pH 2 4 6 6.5 8 13.5 14
腐蚀快慢 较快 慢 较快
主要产物 Fe2+ Fe O Fe O FeO
3 4 2 3
A.当pH<6.5时,碳钢主要发生化学腐蚀B.当pH<4和pH>13.5时,碳钢主要发生析氢腐蚀
C.pH越大,碳钢的腐蚀速率越慢
D.pH=14时,负极反应为4OH-+Fe-3e-= +2H O
2 杨sir化学,侵权必究
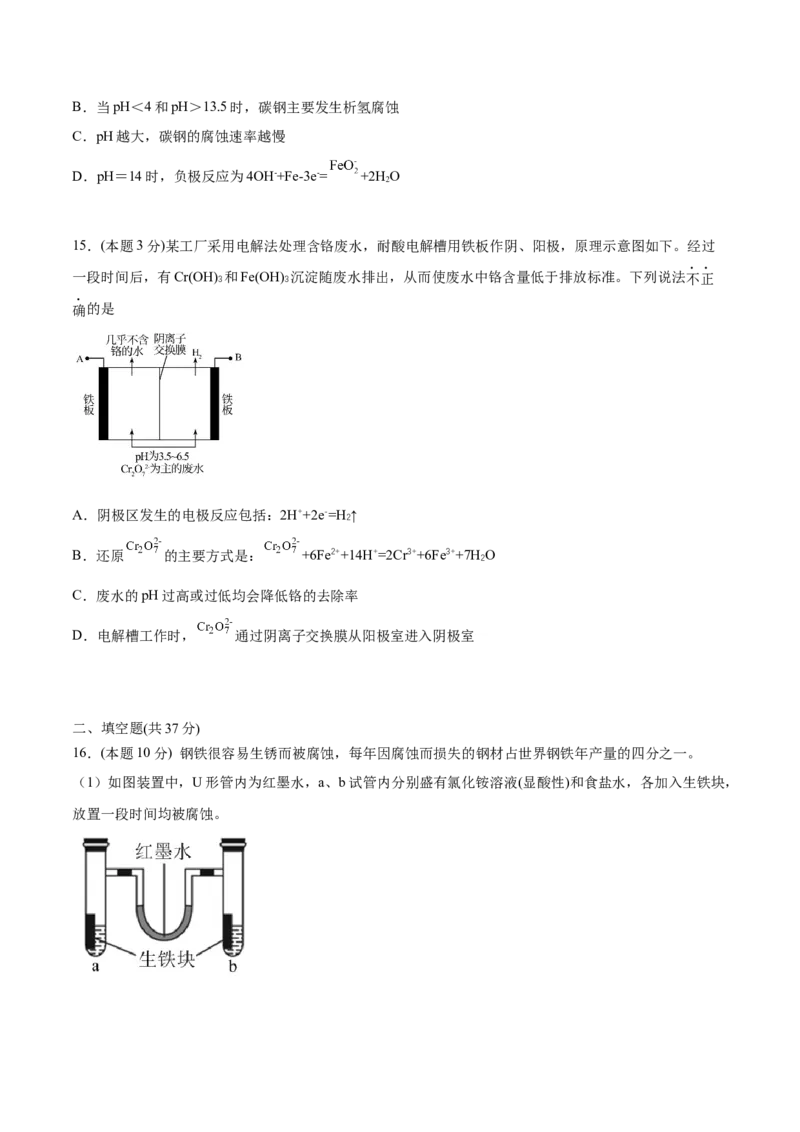
15.(本题3分)某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,原理示意图如下。经过
一段时间后,有Cr(OH)
3
和Fe(OH)
3
沉淀随废水排出,从而使废水中铬含量低于排放标准。下列说法不正
确的是
A.阴极区发生的电极反应包括:2H++2e-=H ↑
2
B.还原 的主要方式是: +6Fe2++14H+=2Cr3++6Fe3++7H O
2
C.废水的pH过高或过低均会降低铬的去除率
D.电解槽工作时, 通过阴离子交换膜从阳极室进入阴极室
杨sir化学,侵权必究
二、填空题(共37分)
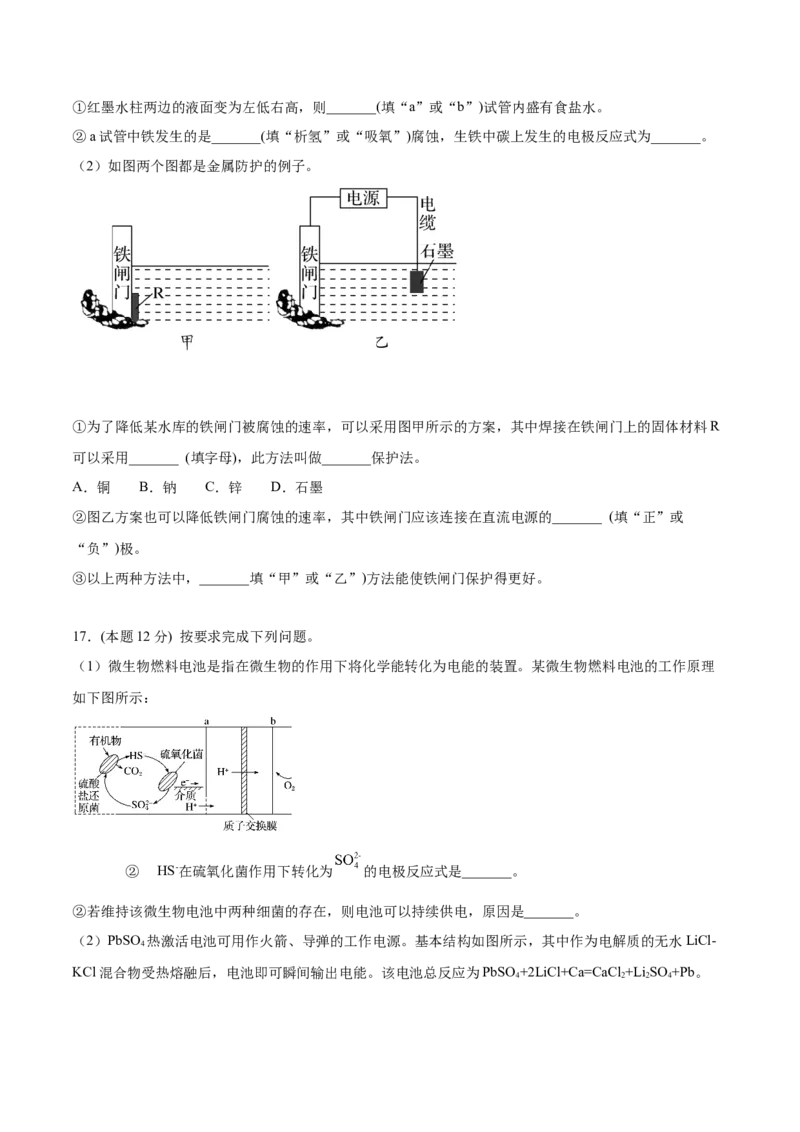
16.(本题10分) 钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。
(1)如图装置中,U形管内为红墨水,a、b试管内分别盛有氯化铵溶液(显酸性)和食盐水,各加入生铁块,
放置一段时间均被腐蚀。①红墨水柱两边的液面变为左低右高,则_______(填“a”或“b”)试管内盛有食盐水。
②a试管中铁发生的是_______(填“析氢”或“吸氧”)腐蚀,生铁中碳上发生的电极反应式为_______。
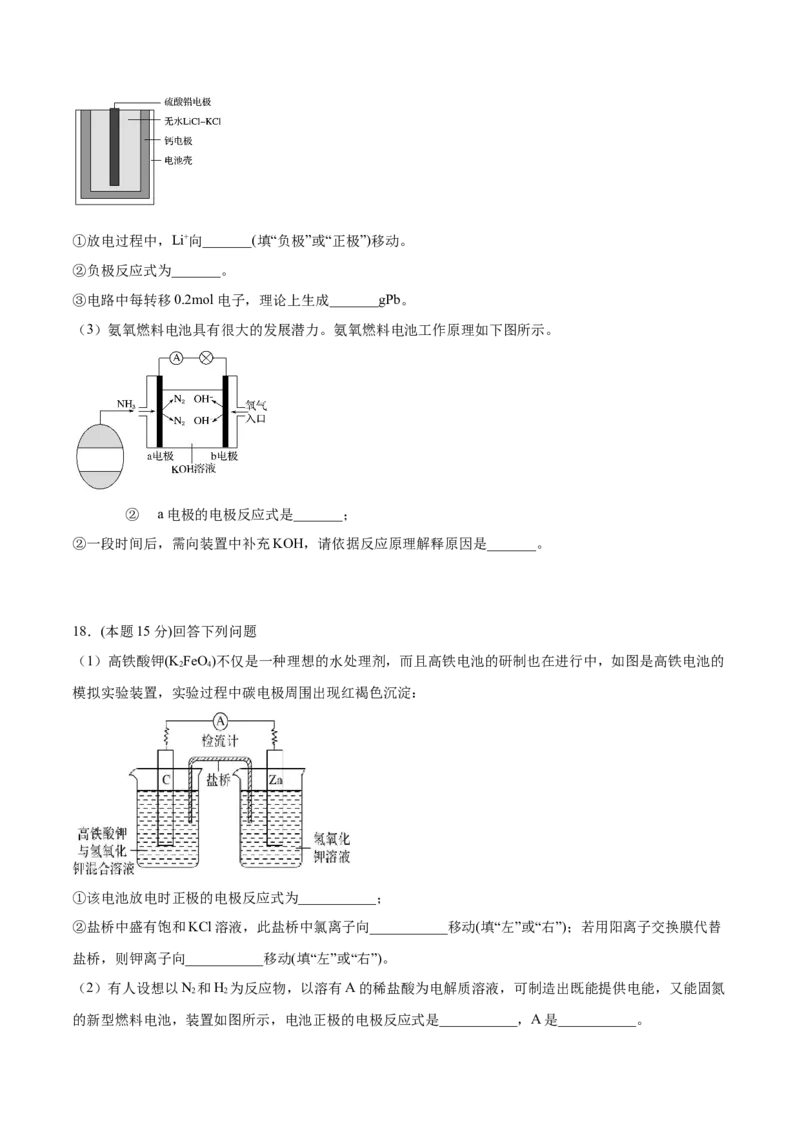
(2)如图两个图都是金属防护的例子。
杨sir化学,侵权必究
①为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R
可以采用_______ (填字母),此方法叫做_______保护法。
A.铜 B.钠 C.锌 D.石墨
②图乙方案也可以降低铁闸门腐蚀的速率,其中铁闸门应该连接在直流电源的_______ (填“正”或
“负”)极。
③以上两种方法中,_______填“甲”或“乙”)方法能使铁闸门保护得更好。
17.(本题12分) 按要求完成下列问题。
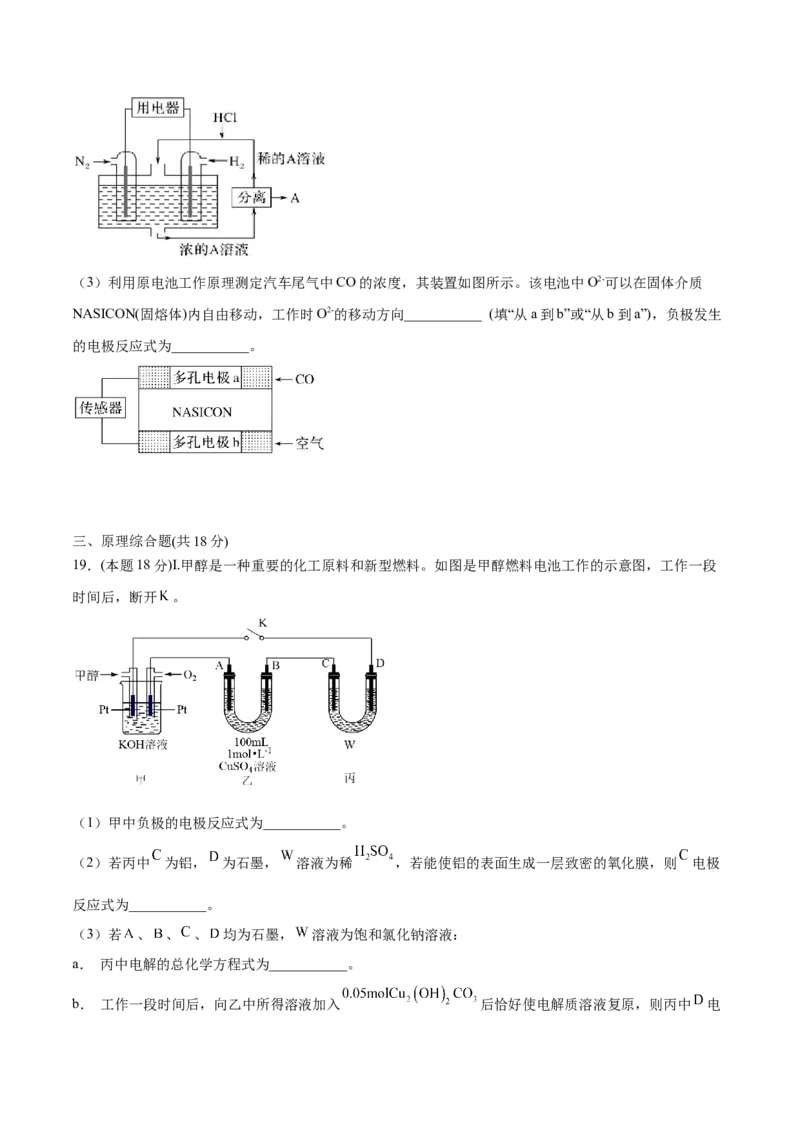
(1)微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理
如下图所示:
② HS-在硫氧化菌作用下转化为 的电极反应式是_______。
②若维持该微生物电池中两种细菌的存在,则电池可以持续供电,原因是_______。
杨sir化学,侵权必究
(2)PbSO 热激活电池可用作火箭、导弹的工作电源。基本结构如图所示,其中作为电解质的无水LiCl-
4
KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为PbSO +2LiCl+Ca=CaCl +Li SO +Pb。
4 2 2 4①放电过程中,Li+向_______(填“负极”或“正极”)移动。
②负极反应式为_______。
③电路中每转移0.2mol电子,理论上生成_______gPb。
(3)氨氧燃料电池具有很大的发展潜力。氨氧燃料电池工作原理如下图所示。
② a电极的电极反应式是_______;
②一段时间后,需向装置中补充KOH,请依据反应原理解释原因是_______。
杨sir化学,侵权必究
18.(本题15分)回答下列问题
(1)高铁酸钾(K FeO)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中,如图是高铁电池的
2 4
模拟实验装置,实验过程中碳电极周围出现红褐色沉淀:
①该电池放电时正极的电极反应式为___________;
②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向___________移动(填“左”或“右”);若用阳离子交换膜代替
盐桥,则钾离子向___________移动(填“左”或“右”)。
杨sir化学,侵权必究
(2)有人设想以N 和H 为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮
2 2
的新型燃料电池,装置如图所示,电池正极的电极反应式是___________,A是___________。(3)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中O2-可以在固体介质
NASICON(固熔体)内自由移动,工作时O2-的移动方向___________ (填“从a到b”或“从b到a”),负极发生
的电极反应式为___________。
三、原理综合题(共18分)
19.(本题18分)Ⅰ.甲醇是一种重要的化工原料和新型燃料。如图是甲醇燃料电池工作的示意图,工作一段
时间后,断开 。
(1)甲中负极的电极反应式为___________。
(2)若丙中 为铝, 为石墨, 溶液为稀 ,若能使铝的表面生成一层致密的氧化膜,则 电极
反应式为___________。
(3)若 、 、 、 均为石墨, 溶液为饱和氯化钠溶液:
杨sir化学,侵权必究
a. 丙中电解的总化学方程式为___________。
b. 工作一段时间后,向乙中所得溶液加入 后恰好使电解质溶液复原,则丙中 电极上生成的气体标况下的体积为___________。
c. 丙中为使两极产物不发生反应,可以在两极之间放置___________(“阴”或“阳”)离子交换膜。
(4)若把乙装置改为精炼铜装置(粗铜含 、 、 、 、 等杂质),下列说法正确的是
___________。
A.电解过程中,阳极减少的质量与阴极增加的质量相等
B. 为粗铜,发生氧化反应
C. 溶液的浓度保持不变
D.杂质都将以单质的形式沉淀到池底
(5)用 盐酸和 溶液反应测定中和热,实验中测得起始平均温度
为 ,反应后最高温度为 ,反应后溶液的比热容为 ,盐酸和 溶液的密度都
近似认为是 ,则中和热 ___________。
Ⅱ.甲烷是一种重要的化工原料和清洁能源,研究其相关反应并合理利用具有重要意义。请回答下列问题:
(6)已知:
a. 工业上甲烷可用于制造合成气,常温常压下其反应为
;
b. 、 的燃烧热依次为 、 。常温常压下, 甲烷完全燃烧生成
液态水放出的热量为___________ 。
杨sir化学,侵权必究
(7)甲烷属于易燃易爆气体,可用电化学原理测定空气中甲烷的含量防止爆炸事故的发生,其原理如图
所示,则负极的电极反应式为___________;若测得标准状况下空气中甲烷的含量为 ,当甲烷完全
被氧化时消耗的 为___________ 。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育