文档内容
第 20 讲 盐类水解的影响因素及应用
知识导航
小杨老师 15521324728 侵权必究
课前引入
NaCO 与NaHCO 同为强碱弱酸盐,其水溶液的碱性是否相同?为什么?
2 3 3 杨sir化学,侵权必究
知识精讲
小杨老师 15521324728 侵权必究
一、水解平衡常数
1. 定义:盐类水解反应的平衡常数(或水解常数),用K 表示。
h
2. 表达式
c(HA)·c(OH-)
对于水解方程式:A- + H
2
O ⇌ HA + OH- ,其平衡常数可表示为:K
h
=
c(A-)
3. 意义:K 表示水解反应趋势的大小,K 数值越大,水解趋势越大。
h h 杨sir化学,侵权必究
4. 影响因素:对于确定的离子,其水解常数只受温度影响。温度越高,水解常数越大。
5. 与电离常数的关系K = K (K 为弱酸的电离平衡常数)或K = K (K 为弱碱的电离平衡常数)
h w a h w b
K K
a b
二、影响盐类水解的因素
1.内因——盐本身的性质
弱酸阴离子、弱碱阳离子对应的酸、碱越弱,就越易发生水解。
如水解程度(碱性):NaCO _____ NaSO ,NaCO_____
2 3 2 3 2 3
NaHCO
3杨sir化学,侵权必究
及时小练
相同温度下,等物质的量浓度的NaX、NaY、NaZ三种正盐溶液,测得溶液的pH分别是7、9、10。
则相对应的酸HX、HY、HZ的酸性强弱顺序为:_________________。
2.外因
因素 水解平衡 水解程度 水解产生离子的浓度
温度 升高
增大
浓度
减小(即稀释)
酸性盐加酸
外加酸碱
酸性盐加碱
酸性盐加酸性盐 相互抑制(如NH Cl中加FeCl )
4 3
外加其他盐
酸性盐加碱性盐 相互促进[如Al (SO ) 中加NaHCO ]
2 4 3 3
三、盐类水解的应用
杨sir化学,侵权必究
应用 举例
判断溶液的酸碱性 FeCl 溶液显酸性,原因是Fe3++3H O Fe(OH) +3H+
3 2 3
判断酸性强弱 NaX、NaY、NaZ三种盐pH分别为7、9、10,则酸性HX>HY>HZ
弱碱阳离子与弱酸阴离子发生完全双水解,则两种离子无法大量共存
判断离子能否共存 ①Al3+与HCO、CO、AlO、SiO、HS-、S2-、ClO-
②Fe3+与HCO、CO、AlO、SiO、ClO-③NH与SiO、AlO
保存、配制某些盐 配制FeCl 溶液时,常加入少量盐酸来抑制FeCl 的水解;
3 3
溶液 盛放NaCO、NaSiO、CHCOONa、NaS等溶液不能用玻璃塞,应用橡胶塞
2 3 2 3 3 2
制取Fe(OH) 胶体:Fe3++3H O Fe(OH) (胶体)+3H+
3 2 3
制取胶体、净水
明矾作净水剂原理:Al3++3H O Al(OH) (胶体)+3H+
2 3
制备化合物 用TiCl 制备TiO:TiCl + (x+2)H O==== TiO·xHO↓+ 4HCl
4 2 4 2 2 2
热的纯碱溶液去污能力强:CO+HO HCO+OH-,升高温度,水解平衡右
去油污 2
移,c(OH-)增大
泡沫灭火器原理 成分为NaHCO 与Al (SO ),发生反应为Al3++3HCO- ===Al(OH) ↓+3CO ↑
3 2 4 3 3 3 2
化肥的使用 铵态氮肥与草木灰不得混用
除锈剂 NH Cl与ZnCl 溶液可作焊接时的除锈剂
4 2
四、判断盐溶液蒸干时所得的产物
1. 水解生成难挥发性酸的强碱盐,蒸干后一般得原物质。
如CuSO (aq)蒸干得CuSO ;NaCO(aq)蒸干得NaCO(s)。
4 4 2 3 2 3
2. 水解生成易挥发性酸的强碱盐,一般蒸干后得对应的氢氧化物,灼烧后得对应的氧化物。
如AlCl (aq)蒸干得Al(OH) ,灼烧得Al O。
3 3 2 3 杨sir化学,侵权必究
3. 若该盐受热易分解,蒸干灼烧后一般得到其分解产物。
如 Ca(HCO ) → CaCO (CaO);NaHCO → NaCO ;KMnO → KMnO 和 MnO ;NH Cl → NH 和
3 2 3 3 2 3 4 2 4 2 4 3
HCl。
4. 还原性盐在蒸干时,易被空气中的O 氧化,得到其氧化产物。
2
如NaSO (aq)蒸干得NaSO (s)。
2 3 2 4
对点训练
小杨老师 15521324728 侵权必究
题型一:水解平衡的移动
杨sir化学,侵权必究
【变1-2】对于0.1 mol/L Na CO 溶液,下列说法正确的是
2 3
A.加入NaOH固体,溶液pH减小
B.升高温度,溶液中c(OH-)增大
C.稀释溶液,溶液中c(H+)减少
D.c(Na+)+c(H+) =c( )+c( )+c(OH-)
杨sir化学,侵权必究
【变1-5】能证明NaSO 溶液中存在SO +HO HSO +OH-水解平衡事实的是( )
2 3 2
A.滴入酚酞溶液变红,再加入HSO 溶液后红色⇌褪去
2 4B.滴入酚酞溶液变红,再加入氯水后红色褪去
C.滴入酚酞溶液变红,再加入BaCl 溶液后产生沉淀且红色褪去
2 杨sir化学,侵权必究
D.滴入酚酞溶液变红,再加入NaHSO 溶液后红色褪去
4
【变1-7】下图所示三个烧瓶中分别装入含酚酞的0.01 mol·L-1 CHCOONa溶液,并分别放置在盛有水的
3
烧杯中,然后向烧杯①中加入生石灰,向烧杯③中加入NH NO 晶体,烧杯②中不加任何物质。
4 3
(1)含酚酞的0.01 mol·L-1 CHCOONa溶液显浅红色的原因为__________________(用离子方程式和必要文
3
字解释)。
(2)实验过程中发现烧瓶①中溶液红色变深,烧瓶③中溶液红色变浅,则下列叙述正确的是________(填字
母序号)。
A.水解反应为放热反应 B.水解反应为吸热反应
C.NH NO 溶于水时放出热量 D.NH NO 溶于水时吸收热量
4 3 4 3
(3)向0.01 mol·L-1 CHCOONa溶液中分别加入NaOH固体、NaCO 固体、FeSO 固体,使CHCOO-水解
3 2 3 4 3
平衡移动的方向分别为__________、____________、____________(填“左”、“右”或“不移动”)。
题型二:盐类水解的应用
杨sir化学,侵权必究
【变2-1】实验室配制和保存FeSO 溶液,应采取的正确措施是
4
①把蒸馏水煮沸,以赶走水中溶解的O;②溶解时加入少量稀硫酸;③加入少量铁粉;④加入少量稀盐酸
2
A.①②③ B.①② C.②③ D.②③④
【变2-2】下列说法中不正确的有
①氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂;
②测定新制氯水的 时,先用玻璃棒蘸取液体滴在 试纸上,再与标准比色卡对照;
③用米汤直接检验食用盐中是否含有碘元素;
④ 在5.6~7.0之间的降水通常称为酸雨;
⑤加入 溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有 存在;
⑥ 通入紫色石蕊试液,溶液先变红后褪色;
⑦配制一定物质的量浓度的氢氧化钠溶液,用烧杯称量后加蒸馏水溶解,未冷却到室温便转移到容量瓶中,
导致结果偏高;⑧分解高锰酸钾制氧气后,残留在试管内壁上的黑色物质可用稀盐酸洗涤;
杨sir化学,侵权必究
⑨蒸干 溶液可得纯净的无水氯化铝;
A.5个 B.6个 C.7个 D.8个
题型三:盐溶液蒸干后的产物判断
杨sir化学,侵权必究
【例3】 (1)K CO 的水溶液蒸干得到的固体物质是________,原因是_________。
2 3
(2)KAl(SO ) 溶液蒸干得到的固体物质是__________,原因是_____________。
4 2
(3)FeCl 溶液蒸干灼烧得到的固体物质是__________,原因是__________。
2
(4)亚硫酸钠溶液蒸干灼烧得到的固体物质是_______,原因是____________。
(5)将0.5 mol·L-1的NaClO溶液加热蒸干灼烧最后所得的固体是________,原因是_________。
(6)将KMnO 溶液加热蒸干、灼烧最后所得的固体是________,原因是____________。
4
题型四:根据K值判断酸碱性
杨sir化学,侵权必究
【例4】根据表中信息,判断 的下列各物质的溶液 最大的是
酸 电离常数(常温下)
,
,
A. B.
C. D.
题型五:水溶液中的图像题
杨sir化学,侵权必究
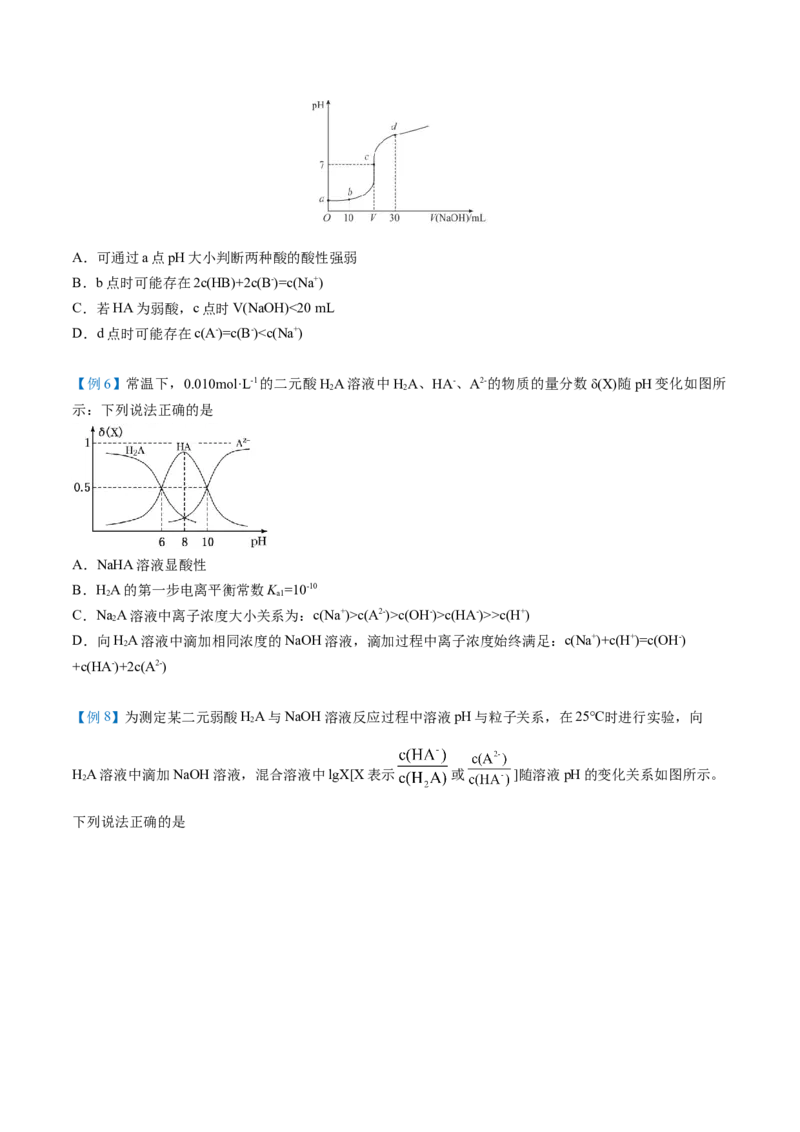
【例5】常温下,用0.01 mol/L的氢氧化钠溶液分别滴定20 mL 0.01 mol/L的两种酸HA、HB,滴定曲线变
化趋势都与如图相似(忽略溶液体积变化),下列说法错误的是( )A.可通过a点pH大小判断两种酸的酸性强弱
B.b点时可能存在2c(HB)+2c(B-)=c(Na+)
C.若HA为弱酸,c点时V(NaOH)<20 mL
D.d点时可能存在c(A-)=c(B-)c(A2-)>c(OH-)>c(HA-)>>c(H+)
2
D.向HA溶液中滴加相同浓度的NaOH溶液,滴加过程中离子浓度始终满足:c(Na+)+c(H+)=c(OH-)
2
+c(HA-)+2c(A2-)
【例8】为测定某二元弱酸HA与NaOH溶液反应过程中溶液pH与粒子关系,在25℃时进行实验,向
2
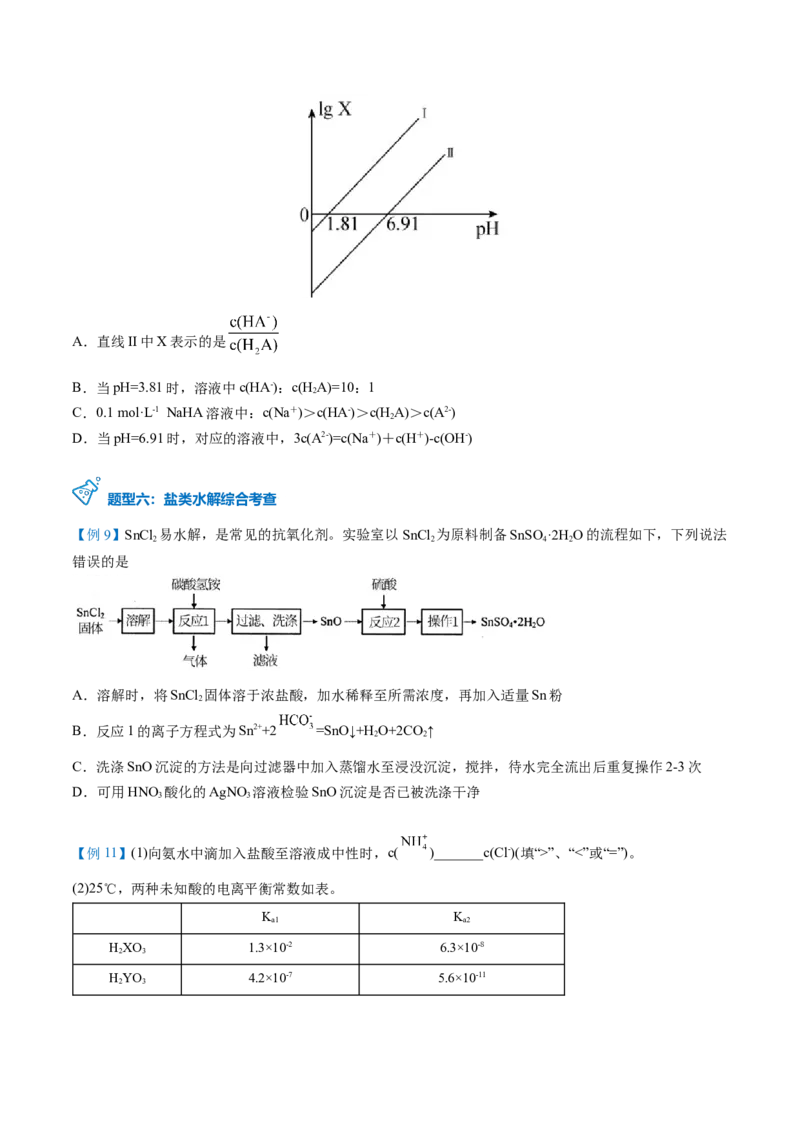
HA溶液中滴加NaOH溶液,混合溶液中lgX[X表示 或 ]随溶液pH的变化关系如图所示。
2
下列说法正确的是A.直线II中X表示的是
B.当pH=3.81时,溶液中c(HA-):c(HA)=10:1
2
C.0.1 mol·L-1 NaHA溶液中:c(Na+)>c(HA-)>c(HA)>c(A2-)
2
D.当pH=6.91时,对应的溶液中,3c(A2-)=c(Na+)+c(H+)-c(OH-)
题型六:盐类水解综合考查
杨sir化学,侵权必究
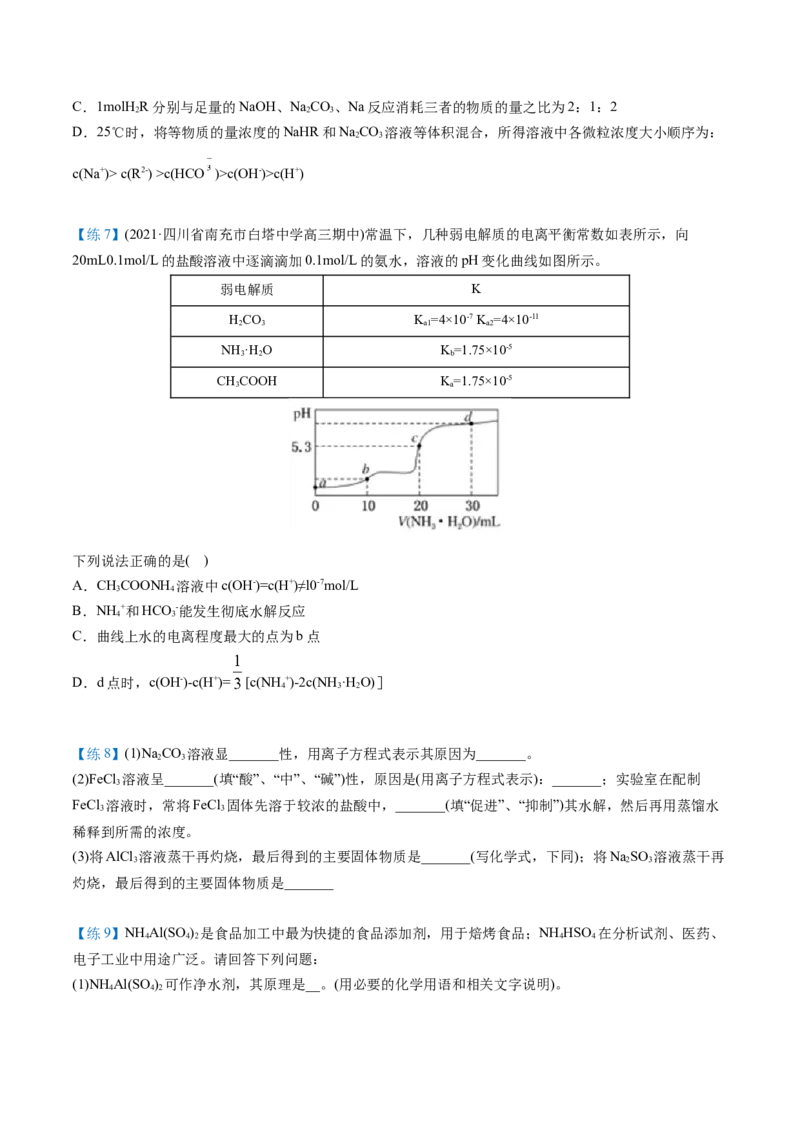
【例9】SnCl 易水解,是常见的抗氧化剂。实验室以SnCl 为原料制备SnSO ·2H O的流程如下,下列说法
2 2 4 2
错误的是
A.溶解时,将SnCl 固体溶于浓盐酸,加水稀释至所需浓度,再加入适量Sn粉
2
B.反应1的离子方程式为Sn2++2 =SnO↓+HO+2CO↑
2 2
C.洗涤SnO沉淀的方法是向过滤器中加入蒸馏水至浸没沉淀,搅拌,待水完全流出后重复操作2-3次
D.可用HNO 酸化的AgNO 溶液检验SnO沉淀是否已被洗涤干净
3 3
【例11】(1)向氨水中滴加入盐酸至溶液成中性时,c( )_______c(Cl-)(填“>”、“<”或“=”)。
(2)25℃,两种未知酸的电离平衡常数如表。
K K
a1 a2
HXO 1.3×10-2 6.3×10-8
2 3
HYO 4.2×10-7 5.6×10-11
2 3①HXO 的电离平衡常数表达式K=_______。
②HXO 溶液和NaHYO 溶液反应的主要离子方程式为_______。
2 3 3
③根据HXO 的电离常数数据,判断NaHXO 溶液显_______(选填“酸性”或“碱性”),原因是_______。
2 3 3
(3)已知:重晶石(BaSO)高温煅烧可发生一系列反应,其中部分反应如下:
4
BaSO(s)+4C(s)=BaS(s)+4CO(g) ∆H=+571.2kJ·mol–1
4
BaS(s)=Ba(s)+S(s) ∆H=+460kJ·mol–1
2C(s)+O(g)=2CO(g) ∆H=-221kJ·mol–1
2
则Ba(s)+S(s)+2O (g)=BaSO (s) ∆H=_______。
2 4
(4)在一密闭容器中一定量A、B的混合气体发生反应:aA(g)+bB(g) cC(s)+dD(g),平衡时测得A的
浓度为0.60mol/L,保持温度不变,将容器的容积扩大到原来的3倍,再达平衡时,测得A的浓度降为
0.20mol/L。下列有关判断正确的是_______。
A.平衡向正反应方向移动 B.A的转化率增大
C.D的体积分数增大 D.a+bHClO
B.pH:HClO>HCN
C.与NaOH恰好完全反应时,消耗NaOH的物质的量:HClO>HCN
D.酸根离子浓度:c(CN-)c(HR-)>c(H R)>c(R2-)
2
B.在NaR溶液中通入足量CO 生成的盐是NaHR和NaHCO
2 2 3杨sir化学,侵权必究C.1molH R分别与足量的NaOH、NaCO、Na反应消耗三者的物质的量之比为2:1:2
2 2 3
D.25℃时,将等物质的量浓度的NaHR和NaCO 溶液等体积混合,所得溶液中各微粒浓度大小顺序为:
2 3
c(Na+)> c(R2-) >c(HCO )>c(OH-)>c(H+)
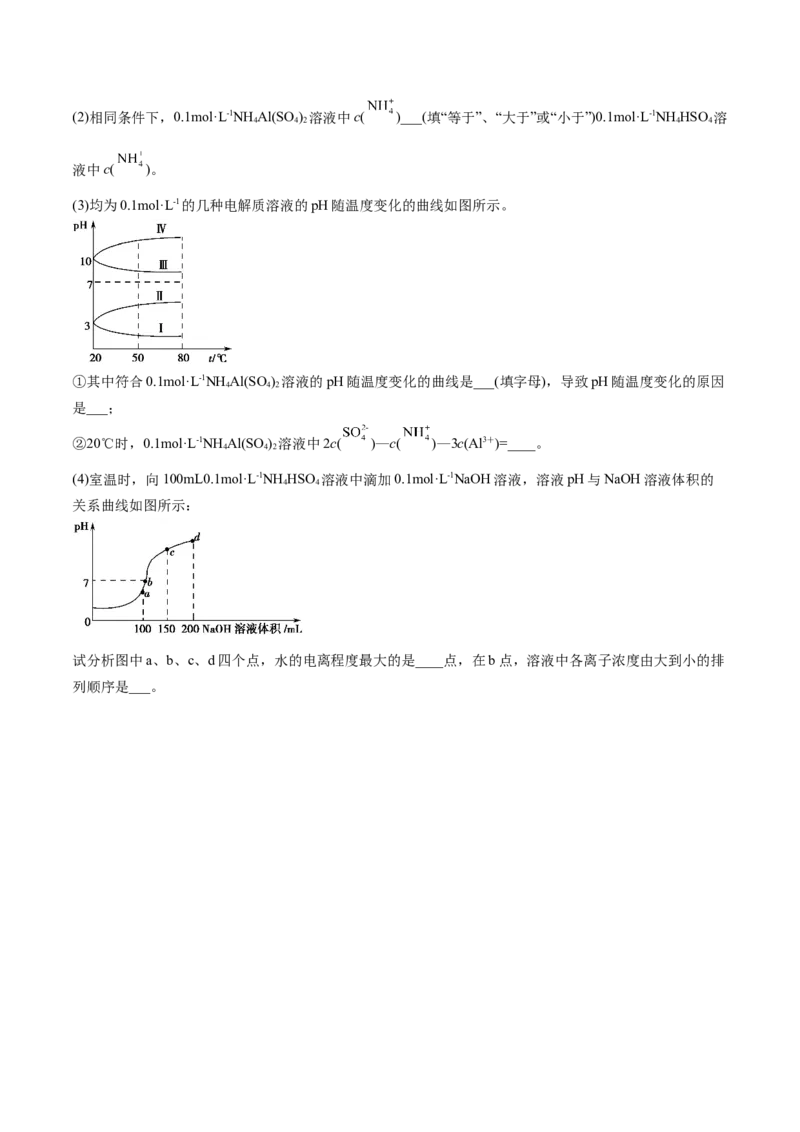
【练7】(2021·四川省南充市白塔中学高三期中)常温下,几种弱电解质的电离平衡常数如表所示,向
20mL0.1mol/L的盐酸溶液中逐滴滴加0.1mol/L的氨水,溶液的pH变化曲线如图所示。
弱电解质 K
HCO K =4×10-7 K =4×10-11
2 3 a1 a2
NH·HO K=1.75×10-5
3 2 b
CHCOOH K=1.75×10-5
3 a
下列说法正确的是( )
A.CHCOONH 溶液中c(OH-)=c(H+)≠l0-7mol/L
3 4
B.NH +和HCO -能发生彻底水解反应
4 3
C.曲线上水的电离程度最大的点为b点
D.d点时,c(OH-)-c(H+)= [c(NH +)-2c(NH ·H O)]
4 3 2 杨sir化学,侵权必究
【练8】(1)Na CO 溶液显_______性,用离子方程式表示其原因为_______。
2 3
(2)FeCl 溶液呈_______(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):_______;实验室在配制
3
FeCl 溶液时,常将FeCl 固体先溶于较浓的盐酸中,_______(填“促进”、“抑制”)其水解,然后再用蒸馏水
3 3
稀释到所需的浓度。
(3)将AlCl 溶液蒸干再灼烧,最后得到的主要固体物质是_______(写化学式,下同);将NaSO 溶液蒸干再
3 2 3
灼烧,最后得到的主要固体物质是_______
【练9】NH Al(SO ) 是食品加工中最为快捷的食品添加剂,用于焙烤食品;NH HSO 在分析试剂、医药、
4 4 2 4 4
电子工业中用途广泛。请回答下列问题:
(1)NH Al(SO ) 可作净水剂,其原理是__。(用必要的化学用语和相关文字说明)。
4 4 2(2)相同条件下,0.1mol·L-1NH Al(SO ) 溶液中c( )___(填“等于”、“大于”或“小于”)0.1mol·L-1NH HSO 溶
4 4 2 4 4
液中c( )。
(3)均为0.1mol·L-1的几种电解质溶液的pH随温度变化的曲线如图所示。
杨sir化学,侵权必究
①其中符合0.1mol·L-1NH Al(SO ) 溶液的pH随温度变化的曲线是___(填字母),导致pH随温度变化的原因
4 4 2
是___;
②20℃时,0.1mol·L-1NH Al(SO ) 溶液中2c( )—c( )—3c(Al3+)=____。
4 4 2
(4)室温时,向100mL0.1mol·L-1NH HSO 溶液中滴加0.1mol·L-1NaOH溶液,溶液pH与NaOH溶液体积的
4 4
关系曲线如图所示:
试分析图中a、b、c、d四个点,水的电离程度最大的是____点,在b点,溶液中各离子浓度由大到小的排
列顺序是___。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育