文档内容
第 21 讲 乙酸
知识导航
知识精讲
一、乙酸的物理性质
颜色 气味 状态 熔点 沸点 溶解性
无色 强烈刺激性气味 液体 16.6℃ 117.9℃ 易溶于水和乙醇
乙酸又称醋酸,当温度低于16.6℃时,乙酸就凝结为类似于冰一样的晶体,所以纯净的乙酸又称冰醋酸。
二、乙酸的结构
官能团
分子式 结构式 结构简式
三、乙酸的化学性质
1.弱酸性
(1)电离方程式:CHCOOH CHCOO- + H+
3 3
(2)酸的通性:①使紫色石蕊溶液变红;②与活泼金属(如 Zn)、金属氧化物(如 CuO)、碱(如
NaOH)、
某些盐(如CaCO )反应。
3
(3)酸性强弱:HCl>CHCOOH>HCO
3 2 3
(4)应用:除水垢 CaCO + 2CHCOOH === Ca(CHCOO) + CO↑+ H O
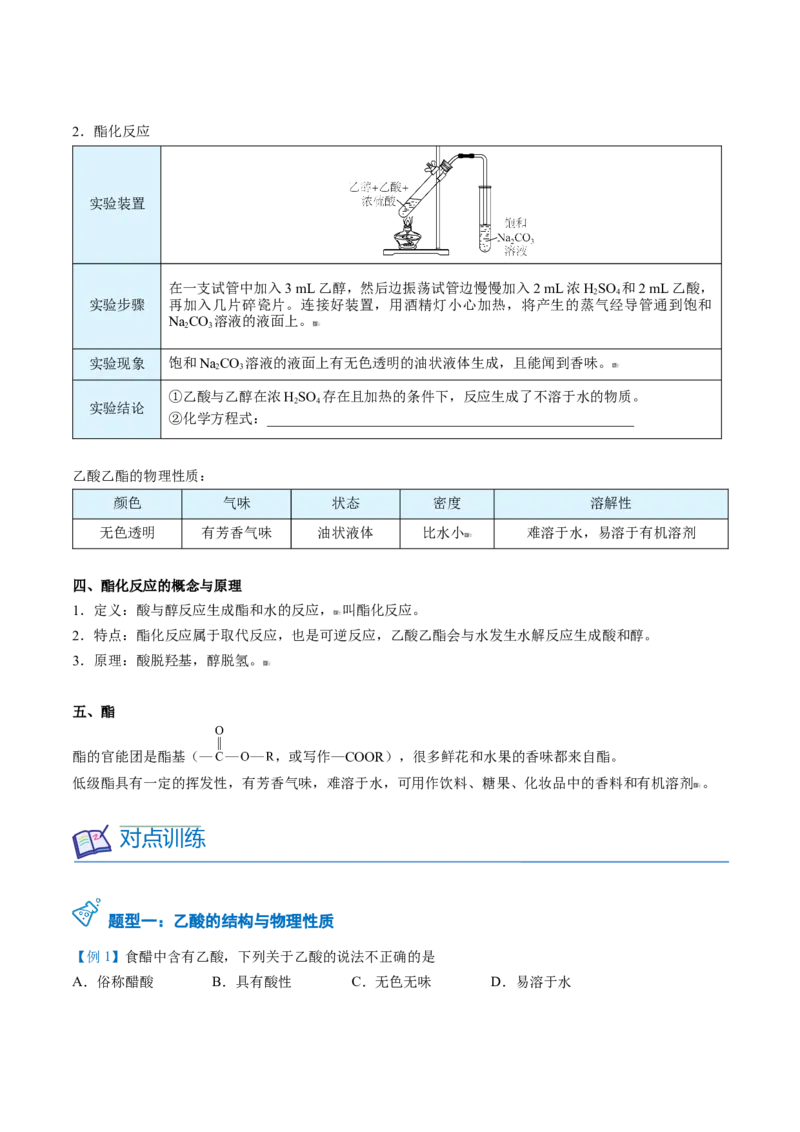
3 3 3 2 2 22.酯化反应
实验装置
在一支试管中加入3 mL乙醇,然后边振荡试管边慢慢加入2 mL浓HSO 和2 mL乙酸,
2 4
实验步骤 再加入几片碎瓷片。连接好装置,用酒精灯小心加热,将产生的蒸气经导管通到饱和
NaCO 溶液的液面上。
2 3
实验现象 饱和NaCO 溶液的液面上有无色透明的油状液体生成,且能闻到香味。
2 3
①乙酸与乙醇在浓HSO 存在且加热的条件下,反应生成了不溶于水的物质。
2 4
实验结论
②化学方程式:____________________________________________________
乙酸乙酯的物理性质:
颜色 气味 状态 密度 溶解性
无色透明 有芳香气味 油状液体 比水小 难溶于水,易溶于有机溶剂
四、酯化反应的概念与原理
1.定义:酸与醇反应生成酯和水的反应, 叫酯化反应。
2.特点:酯化反应属于取代反应,也是可逆反应,乙酸乙酯会与水发生水解反应生成酸和醇。
3.原理:酸脱羟基,醇脱氢。
五、酯
酯的官能团是酯基( ,或写作—COOR),很多鲜花和水果的香味都来自酯。
低级酯具有一定的挥发性,有芳香气味,难溶于水,可用作饮料、糖果、化妆品中的香料和有机溶剂 。
对点训练
题型一:乙酸的结构与物理性质
【例1】食醋中含有乙酸,下列关于乙酸的说法不正确的是
A.俗称醋酸 B.具有酸性 C.无色无味 D.易溶于水题型二:乙酸的酸性
【例3】普通的食醋中一般含3%~5%(质量分数)的乙酸,无水乙酸常被称为冰醋酸。回答下列问题:
(1)乙酸可用于除水垢,写出乙酸与碳酸钙反应的化学方程式:____________________,该反应说明乙酸的
酸性比碳酸的__________(填“强”或“弱”)。
(2)乙酸能与活泼金属反应,写出乙酸与镁反应的离子方程式:_________________________。
(3)乙酸可燃烧,写出乙酸燃烧的化学方程式:_________________________。
题型三:乙酸的结构与化学性质
【变5】下列关于乙酸的叙述正确的是
A.乙酸酸性较弱,不能使紫色石蕊变红
B.乙酸分子中既有极性键,又有非极性键
C.乙酸在常温下能与NaOH、NaCO、乙醇等发生化学反应
2 3
D.等体积等浓度的盐酸和乙酸中加入足量的锌粒,乙酸产生的氢气质量大
【例6】除去括号内杂质所用试剂或方法正确的是
A.乙酸乙酯(乙酸):饱和碳酸钠溶液
B.乙烯( ):酸性 溶液洗气
C.乙烷(乙烯): (催化剂)催化加氢
D.乙醇(水):分液
题型四:酯化反应
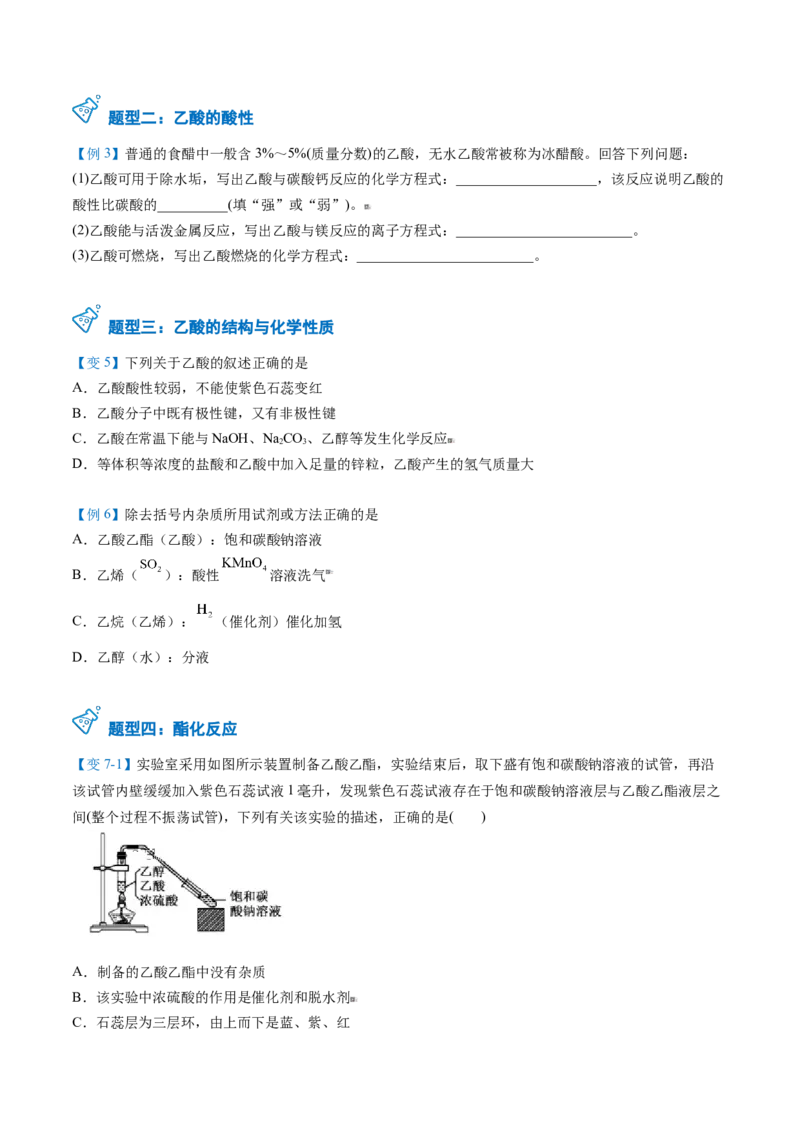
【变7-1】实验室采用如图所示装置制备乙酸乙酯,实验结束后,取下盛有饱和碳酸钠溶液的试管,再沿
该试管内壁缓缓加入紫色石蕊试液1毫升,发现紫色石蕊试液存在于饱和碳酸钠溶液层与乙酸乙酯液层之
间(整个过程不振荡试管),下列有关该实验的描述,正确的是( )
A.制备的乙酸乙酯中没有杂质
B.该实验中浓硫酸的作用是催化剂和脱水剂
C.石蕊层为三层环,由上而下是蓝、紫、红D.饱和碳酸钠溶液主要作用是降低乙酸乙酯的溶解度及吸收乙醇、中和乙酸
【例8】将1 mol乙醇(其中的氧用18O标记)在浓硫酸存在时与足量乙酸充分反应。下列叙述错误的是
A.生成的乙酸乙酯中含有18O B.生成的水分子中含有18O
C.可能生成88 g乙酸乙酯 D.不可能生成90 g乙酸乙酯
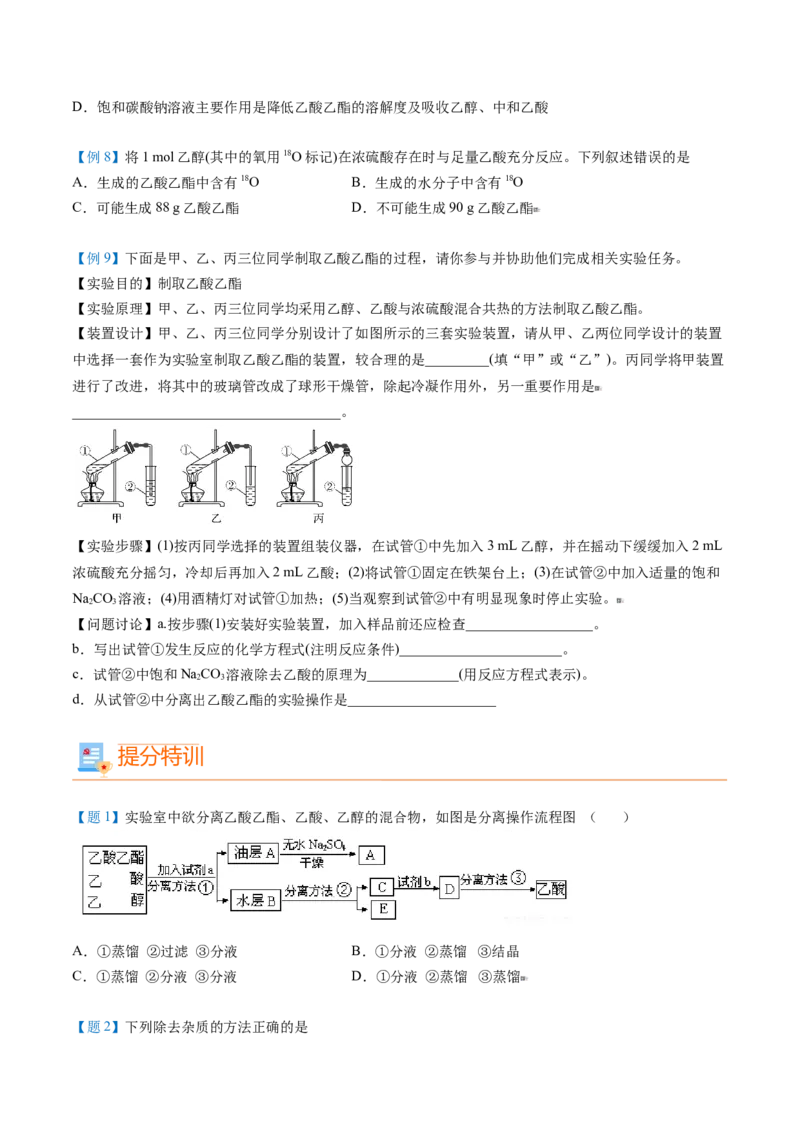
【例9】下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务。
【实验目的】制取乙酸乙酯
【实验原理】甲、乙、丙三位同学均采用乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯。
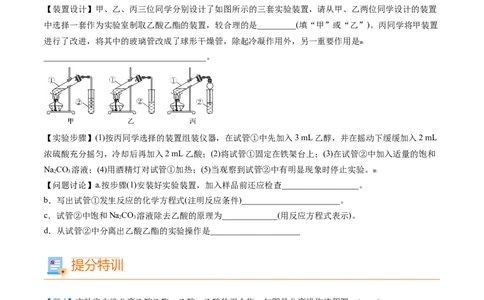
【装置设计】甲、乙、丙三位同学分别设计了如图所示的三套实验装置,请从甲、乙两位同学设计的装置
中选择一套作为实验室制取乙酸乙酯的装置,较合理的是_________(填“甲”或“乙”)。丙同学将甲装置
进行了改进,将其中的玻璃管改成了球形干燥管,除起冷凝作用外,另一重要作用是
______________________________________。
【实验步骤】(1)按丙同学选择的装置组装仪器,在试管①中先加入3 mL乙醇,并在摇动下缓缓加入2 mL
浓硫酸充分摇匀,冷却后再加入2 mL乙酸;(2)将试管①固定在铁架台上;(3)在试管②中加入适量的饱和
NaCO 溶液;(4)用酒精灯对试管①加热;(5)当观察到试管②中有明显现象时停止实验。
2 3
【问题讨论】a.按步骤(1)安装好实验装置,加入样品前还应检查__________________。
b.写出试管①发生反应的化学方程式(注明反应条件)_______________________。
c.试管②中饱和NaCO 溶液除去乙酸的原理为_____________(用反应方程式表示)。
2 3
d.从试管②中分离出乙酸乙酯的实验操作是_____________________
提分特训
【题1】实验室中欲分离乙酸乙酯、乙酸、乙醇的混合物,如图是分离操作流程图 ( )
A.①蒸馏 ②过滤 ③分液 B.①分液 ②蒸馏 ③结晶
C.①蒸馏 ②分液 ③分液 D.①分液 ②蒸馏 ③蒸馏
【题2】下列除去杂质的方法正确的是①除去乙烷中少量的乙烯:光照条件下通入Cl,气液分离 ②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠
2
溶液洗涤,分液、干燥、蒸馏 ③除去CO 中少量的SO :气体通过盛有饱和碳酸钠溶液的洗气瓶 ④除去
2 2
乙醇中少量的乙酸:加足量生石灰,蒸馏
A.①② B.②④ C.③④ D.②③
【题3】酯类物质广泛存在于香蕉、梨等水果中。某实验小组从梨中分离出一种酯,该酯在稀硫酸作用下
加热得到乙酸和另一种分子式为 的物质。下列说法错误的是
A.乙酸分子中含有羧基
B. 可与金属钠发生反应
C.实验小组分离出的酯可表示为
D.稀硫酸是该反应的催化剂
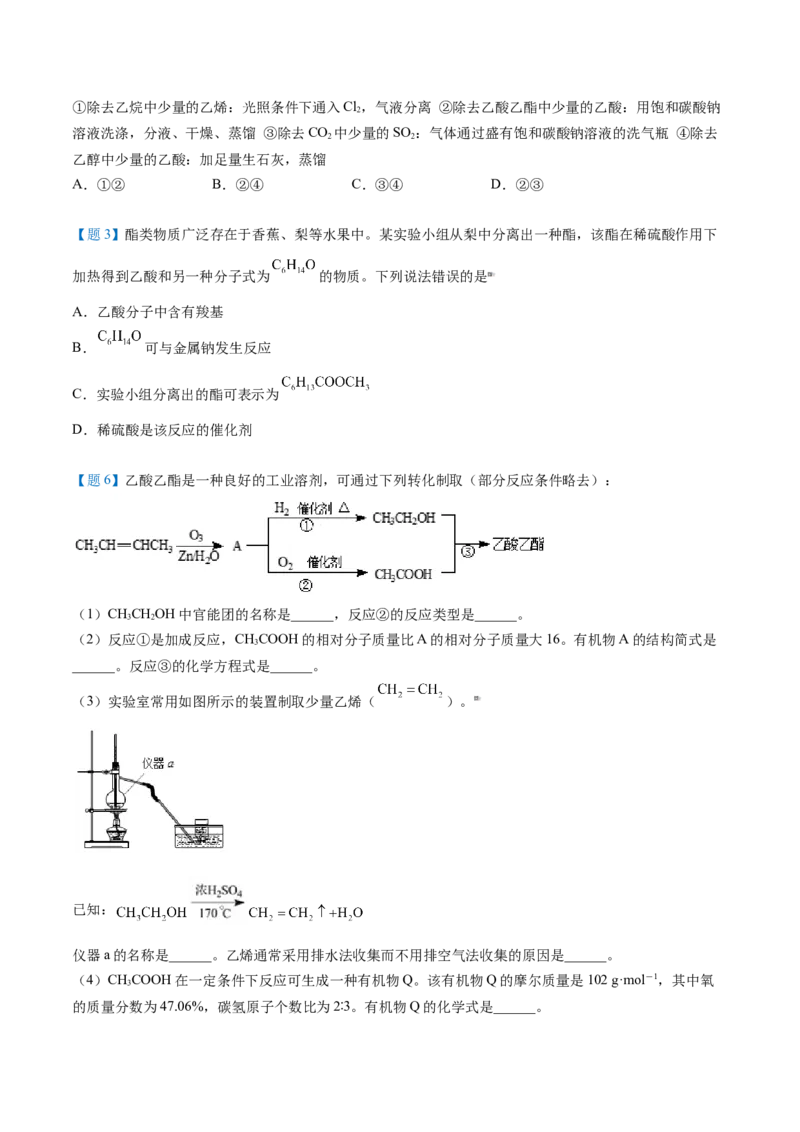
【题6】乙酸乙酯是一种良好的工业溶剂,可通过下列转化制取(部分反应条件略去):
(1)CHCHOH中官能团的名称是______,反应②的反应类型是______。
3 2
(2)反应①是加成反应,CHCOOH的相对分子质量比A的相对分子质量大16。有机物A的结构简式是
3
______。反应③的化学方程式是______。
(3)实验室常用如图所示的装置制取少量乙烯( )。
已知:
仪器a的名称是______。乙烯通常采用排水法收集而不用排空气法收集的原因是______。
(4)CHCOOH在一定条件下反应可生成一种有机物Q。该有机物Q的摩尔质量是102 g·mol-1,其中氧
3
的质量分数为47.06%,碳氢原子个数比为2∶3。有机物Q的化学式是______。提分作业
【练1】下列关于乙酸性质的叙述中,错误的是
A.乙酸的酸性比碳酸强,所以它可以与碳酸盐反应,产生CO 气体
2
B.乙酸能与醇类物质发生酯化反应
C.乙酸分子中含有碳氧双键,所以它能使溴水褪色
D.乙酸在温度低于16.6 ℃时,就凝结成冰状晶体
【练2】除去乙酸乙酯中残留的乙酸,有效的处理方法是
A.用结晶法进行分离
B.用过量氯化钠溶液洗涤后分离
C.用过量氢氧化钠溶液洗涤后分离
D.用过量饱和碳酸钠溶液洗涤后分离
【练3】乙酸是生活中常见的一种有机物,下列关于乙酸的说法中正确的是
A.乙酸的官能团为-OH B.乙酸的酸性比碳酸弱
C.乙酸能够与金属钠反应产生氢气 D.乙酸能使紫色的石蕊溶液变蓝
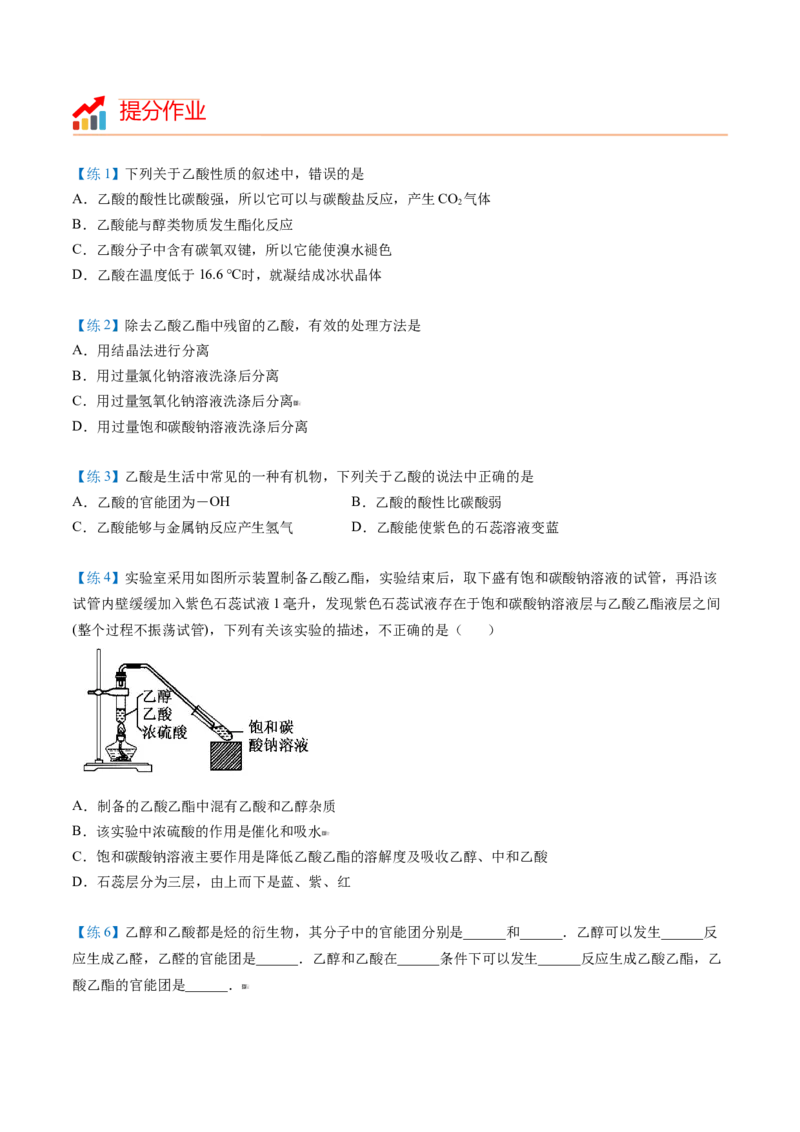
【练4】实验室采用如图所示装置制备乙酸乙酯,实验结束后,取下盛有饱和碳酸钠溶液的试管,再沿该
试管内壁缓缓加入紫色石蕊试液1毫升,发现紫色石蕊试液存在于饱和碳酸钠溶液层与乙酸乙酯液层之间
(整个过程不振荡试管),下列有关该实验的描述,不正确的是( )
A.制备的乙酸乙酯中混有乙酸和乙醇杂质
B.该实验中浓硫酸的作用是催化和吸水
C.饱和碳酸钠溶液主要作用是降低乙酸乙酯的溶解度及吸收乙醇、中和乙酸
D.石蕊层分为三层,由上而下是蓝、紫、红
【练6】乙醇和乙酸都是烃的衍生物,其分子中的官能团分别是______和______.乙醇可以发生______反
应生成乙醛,乙醛的官能团是______.乙醇和乙酸在______条件下可以发生______反应生成乙酸乙酯,乙
酸乙酯的官能团是______.【练8】在中学实验室可用下图所示装置制取少量乙酸乙酯.回答下列问题:
(1)试管a中需加入浓硫酸、冰醋酸各2mL以及乙醇3mL.正确的加入顺序是____________.
(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是____________.
(3)实验中加热试管的目的是:
① ________________________ ;
② _______________ .
(4)试管b中加有饱和NaCO 溶液,其作用是 _________ .
2 3
(5)反应结束后,振荡试管b静置,观察到的现象是 _____________ .倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育