文档内容
第 21 讲 铁的重要化合物
知识导航
知识精讲
一、铁的氧化物
1. 物理性质
化学式 FeO Fe O Fe O
2 3 3 4
俗名 铁红 磁性氧化铁
矿石 赤铁矿 磁铁矿
颜色状态 ____色粉末 ____色粉末 ____色晶体
化合价 +2 +3 +2,+3
溶解性 不溶于水
用途 红色油漆和涂料 炼铁原料
2. 化学性质
①稳定性
FeO不稳定,在空气中受热:__________________________________。
Fe O 和FeO 很稳定。
2 3 3 4
②与非氧化性酸(如稀盐酸、稀硫酸)反应
FeO和Fe O 属于碱性氧化物,与非氧化性酸反应生成亚铁盐和铁盐
2 3
与稀盐酸反应(化学方程式) 与稀盐酸反应(离子方程式)
FeOFe O
2 3
Fe O
3 4
注意
FeO、Fe O 属于碱性氧化物,Fe O 不属于碱性氧化物
2 3 3 4
二、铁的氢氧化物
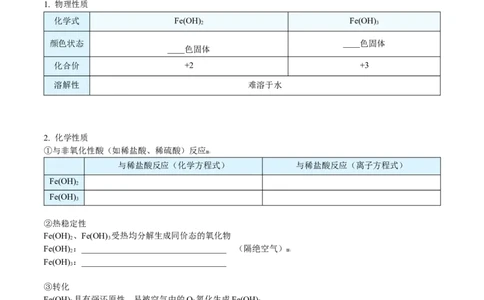
1. 物理性质
化学式 Fe(OH) Fe(OH)
2 3
颜色状态 ____色固体
____色固体
化合价 +2 +3
溶解性 难溶于水
2. 化学性质
①与非氧化性酸(如稀盐酸、稀硫酸)反应
与稀盐酸反应(化学方程式) 与稀盐酸反应(离子方程式)
Fe(OH)
2
Fe(OH)
3
②热稳定性
Fe(OH) 、Fe(OH) 受热均分解生成同价态的氧化物
2 3
Fe(OH) :__________________________________ (隔绝空气)
2
Fe(OH) :__________________________________
3
③转化
Fe(OH) 具有强还原性,易被空气中的O 氧化生成Fe(OH)
2 2 3
现象:_____色絮状沉淀迅速变成_____色,最后变成_____色
方程式:__________________________________
三、Fe(OH) 的制备
2
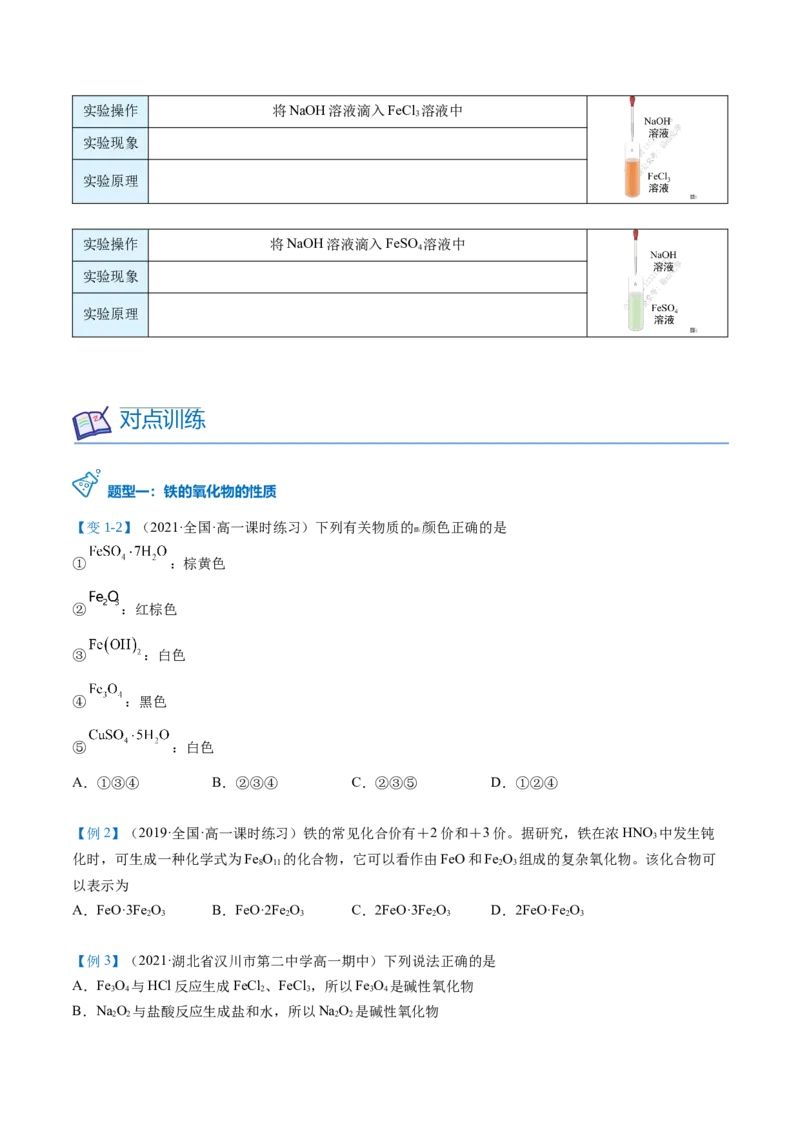
实验探究实验操作 将NaOH溶液滴入FeCl 溶液中
3
实验现象
实验原理
实验操作 将NaOH溶液滴入FeSO 溶液中
4
实验现象
实验原理
对点训练
题型一:铁的氧化物的性质
【变1-2】(2021·全国·高一课时练习)下列有关物质的 颜色正确的是
① :棕黄色
② :红棕色
③ :白色
④ :黑色
⑤ :白色
A.①③④ B.②③④ C.②③⑤ D.①②④
【例2】(2019·全国·高一课时练习)铁的常见化合价有+2价和+3价。据研究,铁在浓HNO 中发生钝
3
化时,可生成一种化学式为Fe O 的化合物,它可以看作由FeO和Fe O 组成的复杂氧化物。该化合物可
8 11 2 3
以表示为
A.FeO·3Fe O B.FeO·2Fe O C.2FeO·3Fe O D.2FeO·Fe O
2 3 2 3 2 3 2 3
【例3】(2021·湖北省汉川市第二中学高一期中)下列说法正确的是
A.Fe O 与HCl反应生成FeCl 、FeCl ,所以Fe O 是碱性氧化物
3 4 2 3 3 4
B.NaO 与盐酸反应生成盐和水,所以NaO 是碱性氧化物
2 2 2 2C.FeO、Fe O 与硫酸反应只生成盐和水,所以都是碱性氧化物
2 3
D.NaHSO 在水中能电离出 氢离子溶液显酸性,所以NaHSO 是酸
4 4
题型二:氢氧化亚铁的制备
【变4】(2021·全国·高一专题练习)铁是人类较早使用的 金属之一。运用所学知识,回答下列问题。
(1)Fe(OH) 很不稳定,露置在空气中容易被氧化,Fe(OH) 被氧化的化学方程为:_______;观察到的现象
2 2
为:_______;为了获得白色的Fe(OH) 沉淀,可以用不含Fe3+的FeSO 溶液与用不含O 的蒸馏水配制的
2 4 2
NaOH溶液反应制备。
(2)用硫酸亚铁晶体配制上述FeSO 溶液时你觉得还需加入_______。
4
(3)除去蒸馏水中溶解的O 常采用_______的方法。
2
(4)生成白色Fe(OH) 沉淀的操作是用长滴管吸取不含O 的NaOH溶液,插入FeSO 溶液液面下,再挤出
2 2 4
NaOH溶液,这样操作的理由是_______。
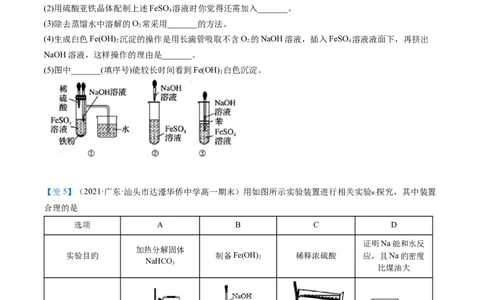
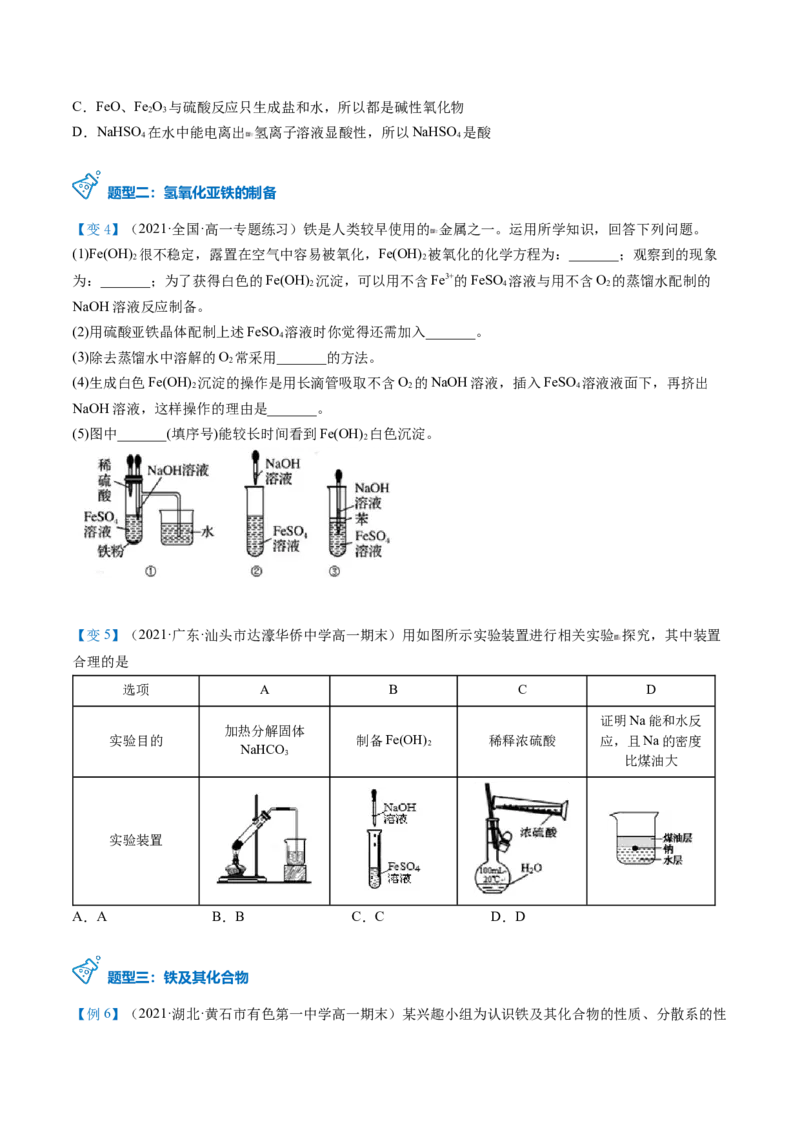
(5)图中_______(填序号)能较长时间看到Fe(OH) 白色沉淀。
2
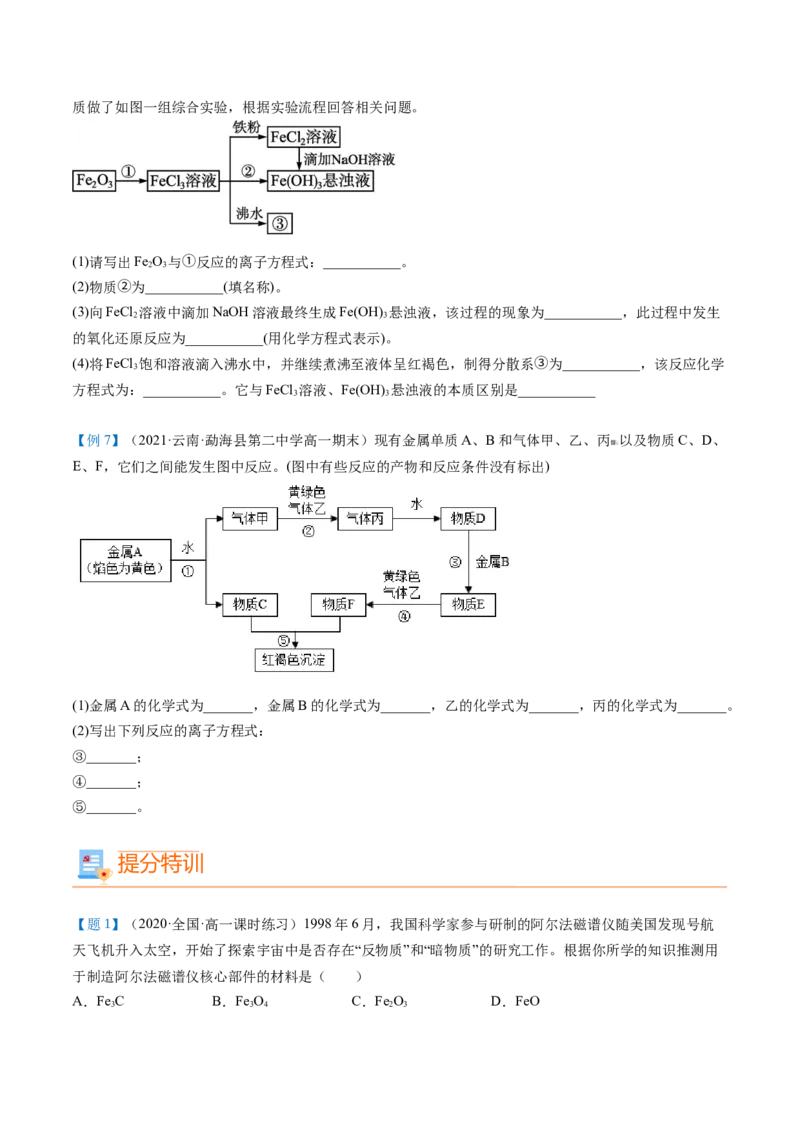
【变5】(2021·广东·汕头市达濠华侨中学高一期末)用如图所示实验装置进行相关实验 探究,其中装置
合理的是
选项 A B C D
证明Na能和水反
加热分解固体
实验目的 制备Fe(OH) 稀释浓硫酸 应,且Na的密度
NaHCO 2
3
比煤油大
实验装置
A.A B.B C.C D.D
题型三:铁及其化合物
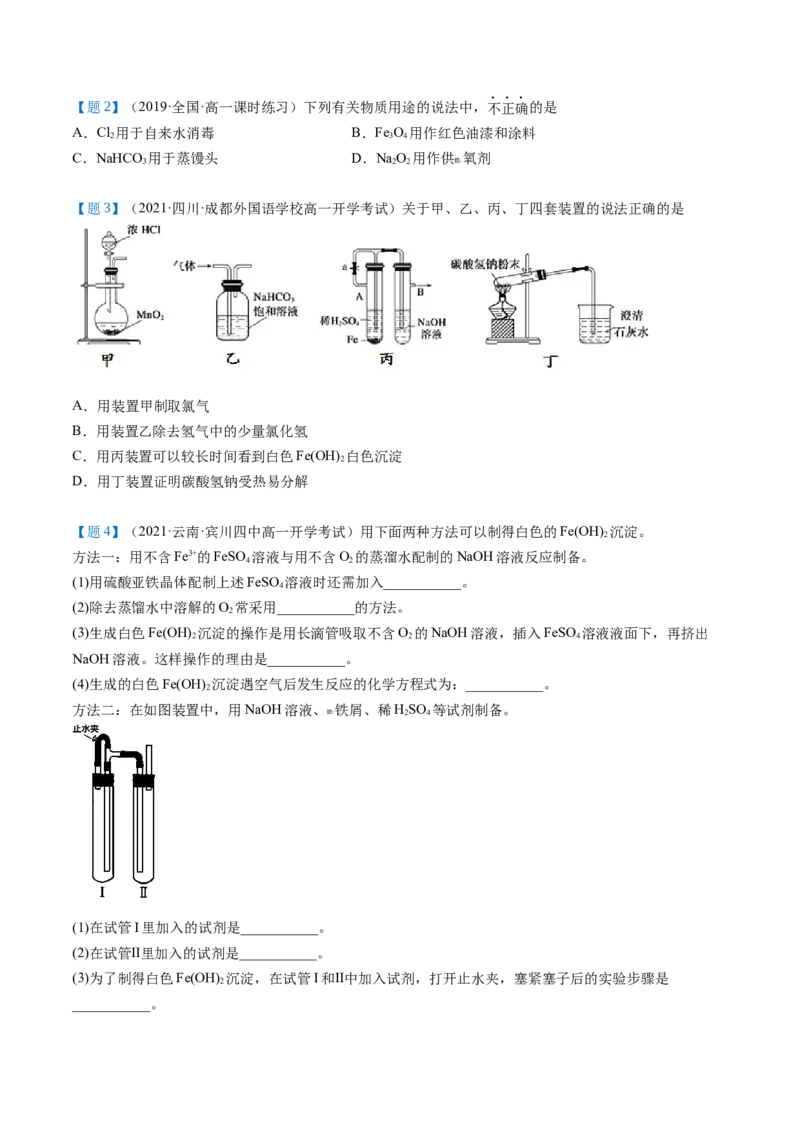
【例6】(2021·湖北·黄石市有色第一中学高一期末)某兴趣小组为认识铁及其化合物的性质、分散系的性质做了如图一组综合实验,根据实验流程回答相关问题。
(1)请写出Fe O 与①反应的离子方程式:___________。
2 3
(2)物质②为___________(填名称)。
(3)向FeCl 溶液中滴加NaOH溶液最终生成Fe(OH) 悬浊液,该过程的现象为___________,此过程中发生
2 3
的氧化还原反应为___________(用化学方程式表示)。
(4)将FeCl 饱和溶液滴入沸水中,并继续煮沸至液体呈红褐色,制得分散系③为___________,该反应化学
3
方程式为:___________。它与FeCl 溶液、Fe(OH) 悬浊液的本质区别是___________
3 3
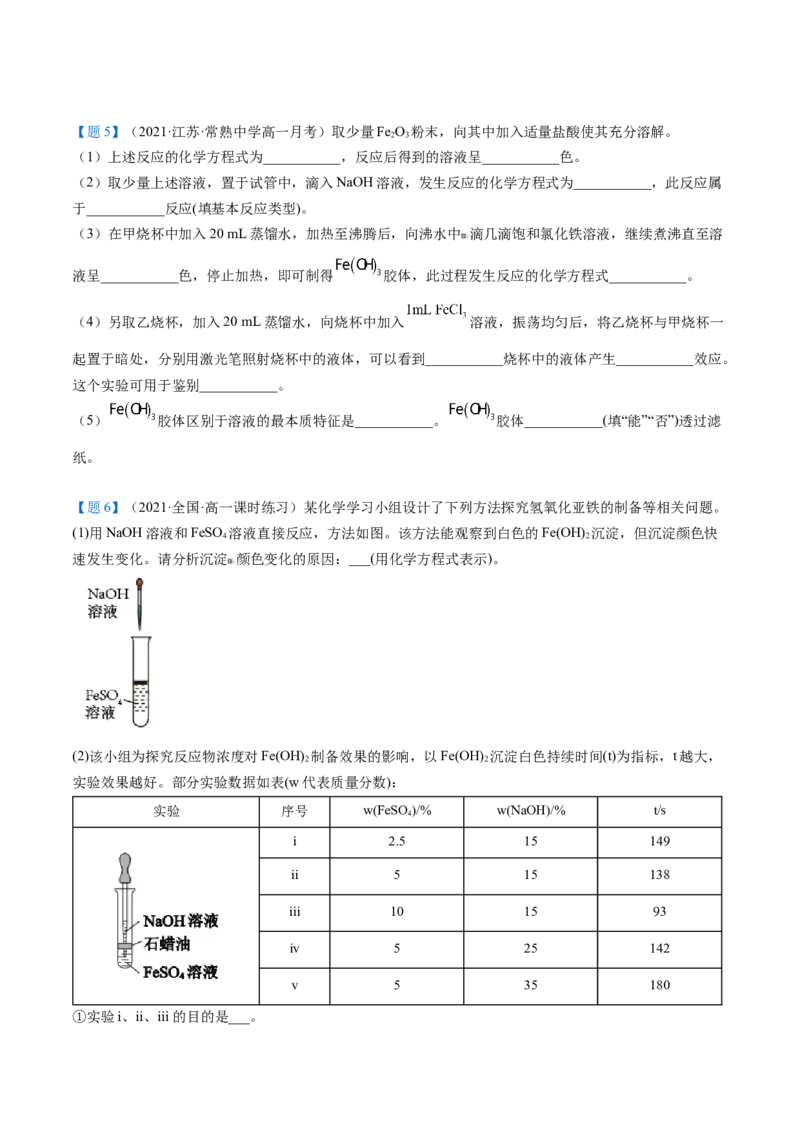
【例7】(2021·云南·勐海县第二中学高一期末)现有金属单质A、B和气体甲、乙、丙 以及物质C、D、
E、F,它们之间能发生图中反应。(图中有些反应的产物和反应条件没有标出)
(1)金属A的化学式为_______,金属B的化学式为_______,乙的化学式为_______,丙的化学式为_______。
(2)写出下列反应的离子方程式:
③_______;
④_______;
⑤_______。
提分特训
【题1】(2020·全国·高一课时练习)1998年6月,我国科学家参与研制的阿尔法磁谱仪随美国发现号航
天飞机升入太空,开始了探索宇宙中是否存在“反物质”和“暗物质”的研究工作。根据你所学的知识推测用
于制造阿尔法磁谱仪核心部件的材料是( )
A.Fe C B.Fe O C.Fe O D.FeO
3 3 4 2 3【题2】(2019·全国·高一课时练习)下列有关物质用途的说法中,不正确的是
A.Cl 用于自来水消毒 B.Fe O 用作红色油漆和涂料
2 3 4
C.NaHCO 用于蒸馒头 D.NaO 用作供 氧剂
3 2 2
【题3】(2021·四川·成都外国语学校高一开学考试)关于甲、乙、丙、丁四套装置的说法正确的是
A.用装置甲制取氯气
B.用装置乙除去氢气中的少量氯化氢
C.用丙装置可以较长时间看到白色Fe(OH) 白色沉淀
2
D.用丁装置证明碳酸氢钠受热易分解
【题4】(2021·云南·宾川四中高一开学考试)用下面两种方法可以制得白色的Fe(OH) 沉淀。
2
方法一:用不含Fe3+的FeSO 溶液与用不含O 的蒸溜水配制的NaOH溶液反应制备。
4 2
(1)用硫酸亚铁晶体配制上述FeSO 溶液时还需加入___________。
4
(2)除去蒸馏水中溶解的O 常采用___________的方法。
2
(3)生成白色Fe(OH) 沉淀的操作是用长滴管吸取不含O 的NaOH溶液,插入FeSO 溶液液面下,再挤出
2 2 4
NaOH溶液。这样操作的理由是___________。
(4)生成的白色Fe(OH) 沉淀遇空气后发生反应的化学方程式为:___________。
2
方法二:在如图装置中,用NaOH溶液、 铁屑、稀HSO 等试剂制备。
2 4
(1)在试管I里加入的试剂是___________。
(2)在试管Ⅱ里加入的试剂是___________。
(3)为了制得白色Fe(OH) 沉淀,在试管I和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是
2
___________。【题5】(2021·江苏·常熟中学高一月考)取少量Fe O 粉末,向其中加入适量盐酸使其充分溶解。
2 3
(1)上述反应的化学方程式为___________,反应后得到的溶液呈___________色。
(2)取少量上述溶液,置于试管中,滴入NaOH溶液,发生反应的化学方程式为___________,此反应属
于___________反应(填基本反应类型)。
(3)在甲烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中 滴几滴饱和氯化铁溶液,继续煮沸直至溶
液呈___________色,停止加热,即可制得 胶体,此过程发生反应的化学方程式___________。
(4)另取乙烧杯,加入20 mL蒸馏水,向烧杯中加入 溶液,振荡均匀后,将乙烧杯与甲烧杯一
起置于暗处,分别用激光笔照射烧杯中的液体,可以看到___________烧杯中的液体产生___________效应。
这个实验可用于鉴别___________。
(5) 胶体区别于溶液的最本质特征是___________。 胶体___________(填“能”“否”)透过滤
纸。
【题6】(2021·全国·高一课时练习)某化学学习小组设计了下列方法探究氢氧化亚铁的制备等相关问题。
(1)用NaOH溶液和FeSO 溶液直接反应,方法如图。该方法能观察到白色的Fe(OH) 沉淀,但沉淀颜色快
4 2
速发生变化。请分析沉淀 颜色变化的原因:___(用化学方程式表示)。
(2)该小组为探究反应物浓度对Fe(OH) 制备效果的影响,以Fe(OH) 沉淀白色持续时间(t)为指标,t越大,
2 2
实验效果越好。部分实验数据如表(w代表质量分数):
实验 序号 w(FeSO)/% w(NaOH)/% t/s
4
i 2.5 15 149
ii 5 15 138
iii 10 15 93
iv 5 25 142
v 5 35 180
①实验i、ii、iii的目的是___。②该小组同学通过实验推断:其他条件不变时,所用NaOH溶液的浓度越大,实验效果越好。推断的证据
是___。
③由绿矾晶体(FeSO •7H O)固体配制250mL0.10mol•L-1FeSO 溶液,需要用到的仪器有药匙、玻璃棒、烧
4 2 4
杯、托盘天平、250mL容量瓶、___。以下操作会导致所配溶液浓度偏低的是___。
A.容量瓶中原有 少量蒸馏水
B.洗涤烧杯和玻璃棒的溶液未转入容量瓶中
C.定容时俯视刻度线
D.定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线
(3)若向FeSO 溶液中加入足量NaO,观察到的现象是___。
4 2 2
提分作业
【练1】(2019·全国·高一课时练习)指南针是我国的四大发明之一,制造指南针的磁性物质是( )
A.FeO B.Fe O C.Fe O D.Fe
2 3 3 4
【练2】(2021·全国·高一课时练习)关于氧化铁、氧化亚铁、四氧化三铁三种氧化物的下列说法中不正确
的是( )
A.铁元素化合价不完全相同
B.氧元素的化合价完全相同
C.氧化亚铁俗称铁红,为红棕色固体
D.铁在氧气中燃烧的产物为黑色固体
【练3】(2020·全国·高一课时练习)下列说法正确的是
A.赤铁矿的主要成分是Fe O
3 4
B.Fe O 为碱性氧化物, 可与水反应生成Fe(OH)
2 3 3
C.铁锈的主要成分是Fe O
2 3
D.Fe O 中铁元素有+2价和+3价,Fe O 是混合物
3 4 3 4
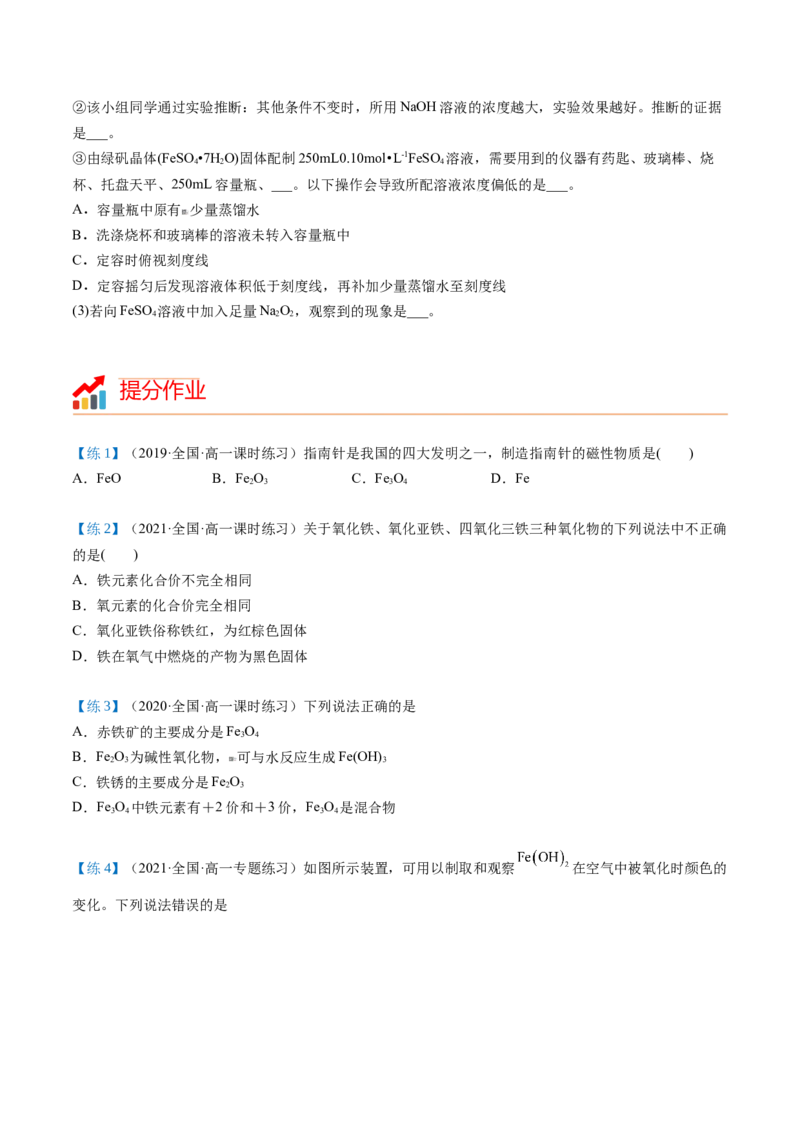
【练4】(2021·全国·高一专题练习)如图所示装置,可用以制取和观察 在空气中被氧化时颜色的
变化。下列说法错误的是A.实验前,应事先煮沸溶液除去溶解氧
B.装置Ⅰ可制取 溶液并排尽装置内空气
C.关闭止水夹可观察到装置Ⅱ中溶液进入装置Ⅰ中
D.取下装置Ⅱ的橡皮塞可观察沉淀颜色变化
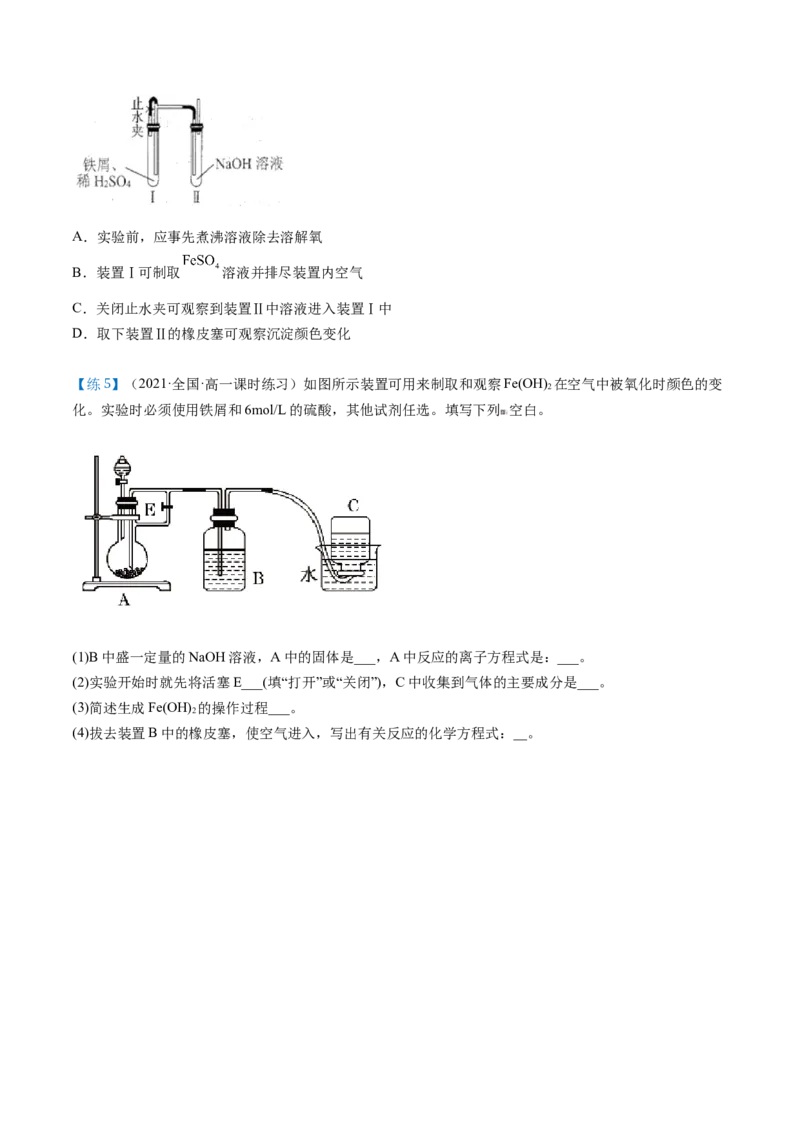
【练5】(2021·全国·高一课时练习)如图所示装置可用来制取和观察Fe(OH) 在空气中被氧化时颜色的变
2
化。实验时必须使用铁屑和6mol/L的硫酸,其他试剂任选。填写下列 空白。
(1)B中盛一定量的NaOH溶液,A中的固体是___,A中反应的离子方程式是:___。
(2)实验开始时就先将活塞E___(填“打开”或“关闭”),C中收集到气体的主要成分是___。
(3)简述生成Fe(OH) 的操作过程___。
2
(4)拔去装置B中的橡皮塞,使空气进入,写出有关反应的化学方程式:__。关注更新免费领取,淘宝唯一每月更新店铺:知二教育