文档内容
第 3 课时 硝酸 酸雨及防治
学业要求 核心素养对接
1.能列举、描述、辨识硝酸的重要物理性
质、化学性质及实验现象。
1.通过浓、稀硝酸性质的不同培养学生
变化观念。
2.能从氧化还原反应的角度分析浓、稀
硝酸的强氧化性。
2.通过研究氮的化合物、硫的化合物的
污染,提高学生的科学态度与社会责
3.硫的化合物、氮的化合物引起的酸雨
任。
及防治。
[知 识 梳 理]
知识点一 硝酸
此为硝酸的安全周知卡,硝酸的危险性类别为什么是“腐蚀”,浓、稀硝酸分别有
什么样的性质?请学习下列知识点找到答案:
1.物理性质
纯硝酸为无色、有刺激性气味的液体,沸点低,易挥发,在空气中呈“白雾”状,
质量分数95%以上的浓硝酸称为“发烟硝酸”。
2.化学性质
(1)酸性:属于强酸,具有酸的通性,如 CaCO 与 HNO 反应 CaCO +
3 3 3
2HNO ( 稀 ) == =Ca(NO ) + CO ↑ + H O。
3 3 2 2 2(2)不稳定性:见光或受热易分解,化学方程式为 4HNO ===== 4NO ↑ + O ↑ +
3 2 2
2H O。
2
市售浓HNO 呈黄色,因硝酸分解产生的NO 溶在硝酸里,故浓HNO 应保存在
3 2 3
棕色试剂瓶,置于冷暗处,不能用橡胶塞。
(3)强氧化性:
①与金属反应:
硝酸具有强氧化性,能与除金、铂、钛以外的大多数金属反应。
a.Cu与浓HNO 反应的化学方程式为 Cu + 4HNO ( 浓 ) == =Cu(NO ) + 2NO ↑ +
3 3 3 2 2
2H O。
2
Cu 与稀 HNO 反应的化学方程式为 3Cu + 8HNO ( 稀 ) == =3Cu(NO ) + 2NO ↑ +
3 3 3 2
4H O。注意:[实验5-8]的实验现象
2
既表现 HNO 的氧化性,又表现酸性,HNO →NO 、NO,氧化性,
3 3 2
HNO →Cu(NO ) ,酸性
3 3 2
b.与Fe、Al反应:常温时浓硝酸可使铁、铝表面形成致密的氧化膜而钝化,所以
可以用铁容器或铝容器盛放浓硝酸。
②与非金属反应:
碳与浓硝酸反应的化学方程式为 C + 4HNO ( 浓 ) ===== CO ↑ + 4NO ↑ + 2H O。
3 2 2 2
只表现氧化性
3.工业制法
硝酸是重要的化工原料,用于制化肥、农药、炸药、染料等。工业上制硝酸的原理
是将氨经过一系列反应得到硝酸,如下图所示:
4.用途
硝酸是一种重要的化工原料,可用于制造炸药、染料、塑料、硝酸盐等。
知识点二 酸雨及其防治这是酸雨危害的漫画,酸雨为什么有这么大的危害,酸雨的成分是什么?酸雨如
何防治?通过掌握以下知识解决这个问题:
正常雨水pH=5.6,是因为溶解了CO
2
微判断
(1)金属与硝酸反应无H 放出是因为硝酸中N元素的化合价处于最高价态,其得
2
电子能力强于H+( )
(2)碳、铜分别与浓硝酸反应,浓硝酸均只表现强氧化性( )
(3)浓硝酸能用铁制容器或铝制器存放是因为铝、铁与浓硝酸不反应( )
(4)向浓硝酸中滴加石蕊溶液,现象为先变红后褪色( )
答案 (1)√ (2)× (3)× (4)√
微训练
1.已知3Cu+8HNO (稀)===3Cu(NO ) +2NO↑+4H O,则下列说法不正确的是
3 3 2 2
( )
A.Cu做还原剂,HNO 做氧化剂
3
B.HNO 在该反应中只有部分表现出了氧化性
3
C.每生成22.4 L(标准状况)NO有3 mol电子转移
D.如果有8 mol HNO 被还原,则生成了2 mol NO
3
解析 根据反应
知,A正确;HNO 在该反应中既表现酸性又表现氧化性,B正确;根据双线桥分
3
析,该反应每生成2 mol NO转移6 mol电子,C正确;HNO 被还原生成NO,若有
3
8 mol HNO 被还原,则生成8 mol NO,D错误。
3
答案 D
2.回答下列问题。
(1)有时在实验室看到的硝酸显黄色,原因是_______________________________
实验室保存硝酸的方法是_______________________________________。
(2)铜与足量浓HNO 反应时,表现酸性的硝酸与做氧化剂的HNO 物质的量之比
3 3为________。
(3)铜粉放入稀硫酸溶液中,加热后无明显变化,但加入某盐一段时间后,发现铜
粉质量减少,则该盐不可能是________(填序号)。
A.FeCl B.NaCl
3
C.KNO D.Cu(NO )
3 3 2
(4)一定量的浓硝酸与足量的铜充分反应,生成气体的成分有________,写出反应
的离子方程式:_________________________________________。
向反应后的溶液中加入稀硫酸,如果反应,写出反应的离子方程式:
________________________________________________________
_________________________________________________________。
(5) 从某金属 粉末 (含有 Au、Cu 、Ag) 中分 离出 Au,加 入的试剂是
________________________________________________________________,
写出Ag参与反应的化学方程式:_______________________________
__________________________________________________________。
(6)往两支分别装有浅绿色的Fe(NO ) 和FeSO 溶液的试管中分别逐滴加入稀盐
3 2 4
酸时,溶液的颜色变化应该为
Fe(NO ) 溶液____________________________________________________;
3 2
FeSO 溶液________________________________________________________。
4
答案 (1)久置硝酸显黄色是由于硝酸见光或受热发生了分解,生成的NO 溶于
2
浓硝酸所致 保存在棕色试剂瓶中,并置于阴凉处 (2)1∶1 (3)B
(4)NO 、NO Cu+4H++2NO===2NO ↑+2H O+Cu2+、3Cu+8H++
2 2 2
2NO===3Cu2++2NO↑+4H O 3Cu+8H++2NO===3Cu2++2NO↑+4H O
2 2
(5)稀硝酸 3Ag+4HNO ===3AgNO +NO↑+2H O
3 3 2
(6)浅绿色变棕黄色 不变色
微思考
1.市售浓HNO 为什么呈黄色,如何去除这个黄色?
3
提示 ①4HNO =====4NO ↑+O ↑+2H O,NO 溶于HNO 显黄色。
3 2 2 2 2 3
②可通入氧气,使NO 转化为HNO 。
2 3
2.浓HNO 反应时,还原产物的价态与什么有关?
3
提示 HNO 的浓度不同,产物不同,浓时为NO ,稀时为NO,如HNO 与较活泼
3 2 3金属反应,HNO 浓度很稀也可生成NH、N 、N O等。
3 2 2
学习任务1 硝酸的强氧化性
资料:
资料一、当硝酸与金属反应时,硝酸被还原的程度取决于酸的浓度和还原剂的强
弱。对于同一还原剂来说,酸越稀,被还原的程度愈大。
资料二、在金属活动性顺序中,位于氢后的金属铜、汞、银等,跟浓硝酸反应时,主
要得到二氧化氮;跟稀硝酸反应时,主要得到一氧化氮。所以说,当硝酸与铜、汞、
银等金属反应时,浓硝酸比稀硝酸的氧化性强。
资料三、当活泼金属锌、镁等跟硝酸反应时,硝酸浓度不同,还原产物不同;前期
有气体(NO )产生,而后期则有铵盐生成。
2
铁与稀硝酸的反应与上述情况类似。上图显示了铁与不同浓度HNO 反应时的还
3
原产物,从上图中可以看出,当其他条件一致时,如温度、还原剂一致时,在浓硝
酸(密度为1.35)中,主要产物是NO ,随着HNO 浓度逐渐下降,产物NO 逐渐减
2 3 2
少,而一氧化氮的相对含量逐渐增多。当密度是1.30时,主要产物是NO,其次是
NO 及少量N O;当密度是1.15时,NO与NH 的相对含量几乎相当;HNO 的密
2 2 3 3
度为1.05时,NH 成为主要的产物。
3
资料四、Fe、Co、Ni、Al等金属遇到浓硝酸会产生钝化现象。是因为在常温下,浓
硝酸跟这些金属接触,能够使金属表面生成一薄层致密的氧化物保护膜阻止内部
金属继续跟硝酸反应。
结合上述四则资料回答下列问题:
1.浓、稀硝酸分别与铜反应时,其还原产物相同吗?
提示 浓HNO 、稀HNO 产物不同,前者生成NO ,后者生成NO。
3 3 2
2.硝酸的氧化性与浓度有关吗?越浓氧化性越强,还是越稀氧化性越强?
提示 与浓度有关,浓硝酸的氧化性比稀硝酸强。
3.实验:在分别盛有少量浓、稀硝酸的试管里,分别滴入几滴紫色石蕊溶液并加
热。
请预测实验现象,并给出解释。
提示 前者溶液先变成红色,过一会红色消失。后者溶液变成红色,但不消失。
这是由于浓硝酸具有强氧化性,而使红色褪去。浓硝酸比稀硝酸氧化性强。
硝酸的强氧化性
HNO 中的+5价氮元素具有很强的得电子能力。
3
硝酸的浓度越大,反应温度越高,其氧化性越强
(1)硝酸与金属的反应
①除 Au、Pt 等少数金属外,硝酸几乎可以氧化所有的金属,如 3Ag+
4HNO (稀)===3AgNO +NO↑+2H O;
3 3 2
②活泼金属与硝酸反应不生成H ,硝酸的浓度不同,还原产物不同;
2
③常温下浓硝酸能使Fe、Al钝化。
(2)硝酸与非金属的反应
①反应规律:非金属单质+浓硝酸→最高价氧化物或其含氧酸+NO ↑+H O;
2 2
②实例:C+4HNO (浓)=====CO ↑+4NO ↑+2H O。
3 2 2 2
(3)硝酸与还原性化合物的反应
硝酸的强氧化性还表现在可以氧化具有还原性的化合物或离子,如HI、HBr、
SO 、Fe2+、FeO、Br-、I-、S2-、SO等均能被HNO 氧化。
2 3
【例题1】 下列关于硝酸的说法中正确的是( )
A.稀硝酸能与Fe发生反应,浓硝酸不能
B.浓硝酸和稀硝酸都是强氧化剂
C.稀硝酸是弱酸,浓硝酸是强酸
D.稀硝酸与Cu反应生成NO,而浓硝酸与Cu反应生成NO ,稀硝酸得电子更多
2故稀硝酸的氧化性大于浓硝酸
解析 A项,加热条件下,浓硝酸也能与Fe发生反应;B项,浓、稀硝酸均具有强
氧化性;C项,硝酸属于强酸,与浓度大小无关;D项,硝酸的氧化性强弱与其浓
度大小有关,浓硝酸的氧化性大于稀硝酸的氧化性,这与 HNO 和Cu反应中
3
HNO 得电子数目多少无关。
3
答案 B
变式训练1 下列反应中硝酸既表现出酸性又表现出氧化性的是(双选)( )
A.FeO与稀硝酸反应生成Fe(NO ) 和NO
3 3
B.与铜反应放出NO气体,生成Cu(NO )
3 2
C.与Na CO 反应放出CO 气体,生成NaNO
2 3 2 3
D.与S单质混合共热时生成H SO 和NO
2 4 2
解析 FeO与稀硝酸反应生成Fe(NO ) ,HNO 部分做氧化剂;B项,Cu与稀硝酸
3 3 3
反应时,部分起酸的作用生成 Cu(NO ) ,部分做氧化剂被还原为 NO;C项,
3 2
2HNO +Na CO ===CO ↑+H O+2NaNO ,HNO 只表现强酸性;D项,HNO 将
3 2 3 2 2 3 3 3
S氧化为H SO ,自身被还原为NO ,在该反应中HNO 只表现强氧化性。
2 4 2 3
答案 B
学习任务2 酸雨的形成与防治
情景:
如图是德国的一座大理石雕像在六十年间的变化,结合所学知识回答下列问题:
(1)造成上述现象的原因________________________________________________。
(2) 写 出 上 述 变 化 中 的 化 学 ( 或 离 子 ) 方 程 式 :
_________________________________
________________________________________________________________
_______________________________________________________________。
(3)为防治酸雨,降低煤燃烧时向大气排放的SO ,工业上将生石灰和含硫煤混合
2
后使用。请写出燃烧时,有关“固硫”(不使硫化合物进入大气)反应的化学方程式:_______________________________________________________
_____________________________________________________________。
答案 (1)酸雨对雕像的腐蚀
(2)SO +H OH SO ,2H SO +O ===2H SO ,
2 2 2 3 2 3 2 2 4
3NO +H O===2HNO +NO,2H++CaCO ===Ca2++H O+CO
2 2 3 3 2 2
(3)CaO+SO =====CaSO ,2CaSO +O ===2CaSO
2 3 3 2 4
1.常见的环境污染
环境污染 形成原因 主要危害
温室效应 大气中CO 含量不断增加 全球变暖,冰雪融化
2
酸雨 SO 和氮氧化物的排放 土壤酸化,腐蚀建筑物
2
光化学烟雾 氮氧化物和碳氢化合物的排放 危害人体健康和植物生长
地球上的生物受太阳紫外线的
臭氧空洞 氮氧化物和氟氯代烃的排放
伤害加剧
使藻类过度繁殖,水质恶化,发
含磷洗衣粉的大量使用及其废
赤潮和水华 生在海水中为赤潮,淡水中为
水的任意排放
水华
聚乙烯塑料的大量使用,任意
白色污染 破坏土壤结构和生态环境
丢弃
2.SO 和氮的氧化物的吸收、转化
2
(1)NaOH溶液吸收
SO +2NaOH===Na SO +H O
2 2 3 2
NO +NO+2NaOH===2NaNO +H O
2 2 2
2NO +2NaOH===NaNO +NaNO +H O
2 2 3 2
(2)氨气吸收
2NH +H O+SO ===(NH ) SO
3 2 2 4 2 3
8NH +6NO =====7N +12H O
3 2 2 2
4NH +6NO=====5N +6H O
3 2 2
(3)汽车尾气转换器
2CO+2NO=====2CO +N
2 2
(4)石灰吸收
CaO+SO =====CaSO 、2CaSO +O ===2CaSO
2 3 3 2 4特别提醒:(1)氮的氧化物是造成酸雨和臭氧层空洞的共同污染物。
(2)NO在破坏臭氧层的过程中可发生如下反应:
NO+O ―→NO +O ①
3 2 2
NO +O―→NO+O ②
2 2
总反应方程式为2O ===3O ,从整个反应来看NO作催化剂。
3 2
(3)NO使人中毒的原理与CO相似,被人吸入后与血红蛋白结合生成一氧化氮血
红蛋白,从而使血红蛋白失去运输O 的能力。
2
【例题2】 下图所示是酸雨的形成示意图。根据图示回答下列问题。
(1)下列气体容易形成酸雨的是________。
A.CO B.SO
2 2
C.N D.NO
2 2
(2)下列措施中,可减少酸雨产生的途径的是________(填字母)。
①少用煤作燃料 ②把工厂烟囱造高 ③燃煤脱硫
④在已酸化的土壤中加生石灰 ⑤开发新能源
A.①②③ B.②③④⑤
C.①③⑤ D.①③④⑤
答案 (1)BD (2)C
变式训练2 酸雨是对呈酸性(pH小于5.6)降水的统称。下列说法错误的是( )
A.空气中的SO 溶于水,最终形成酸雨
2
B.汽车排放的尾气、硝酸厂和化肥厂的废气都含有氮氧化物
C.工业废水任意排放是造成酸雨的主要原因
D.为了减少酸雨的形成,必须减少SO 的排放量,对燃料脱硫处理
2
解析 工业废水任意排放引起江河湖泊污染,而酸雨是由于SO 和NO 溶于水引
2 2起的。
答案 C
学习任务3 (核心素养)硝酸与金属反应的计算
一、知识要点
硝酸与金属反应的计算:
(1)电子守恒法:硝酸与金属反应属于氧化还原反应,氮原子得到的电子总数等于
金属原子失去的电子总数。
(2)原子守恒法:硝酸与金属反应时,反应前硝酸中的NO一部分仍以NO的形式
存在,一部分转化为还原产物,这两部分中N的物质的量之和与反应消耗的硝酸
中N的物质的量相等。
(3)利用离子方程式计算
硝酸与硫酸混合液跟金属的反应,当金属足量时,不能用硝酸与金属反应的化学
方程式计算,应用离子方程式计算,因为生成的硝酸盐中的NO与硫酸电离出的
H+仍
能继续与金属反应。如金属铜与混酸的反应方程式为:3Cu+8H++2NO===3Cu2
++2NO↑+4H O。
2
二、核心素养
硝酸与金属反应的计算⇒培养学生的模型认知意识,提升学生的微观辨析
素养
【素养解题】
[典例示范] 物质的量之比为2∶5的锌与稀硝酸反应,若硝酸被还原的产物为
N O,反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物
2
质的量之比是( )
A.1∶4 B.1∶5
C.2∶3 D.2∶5
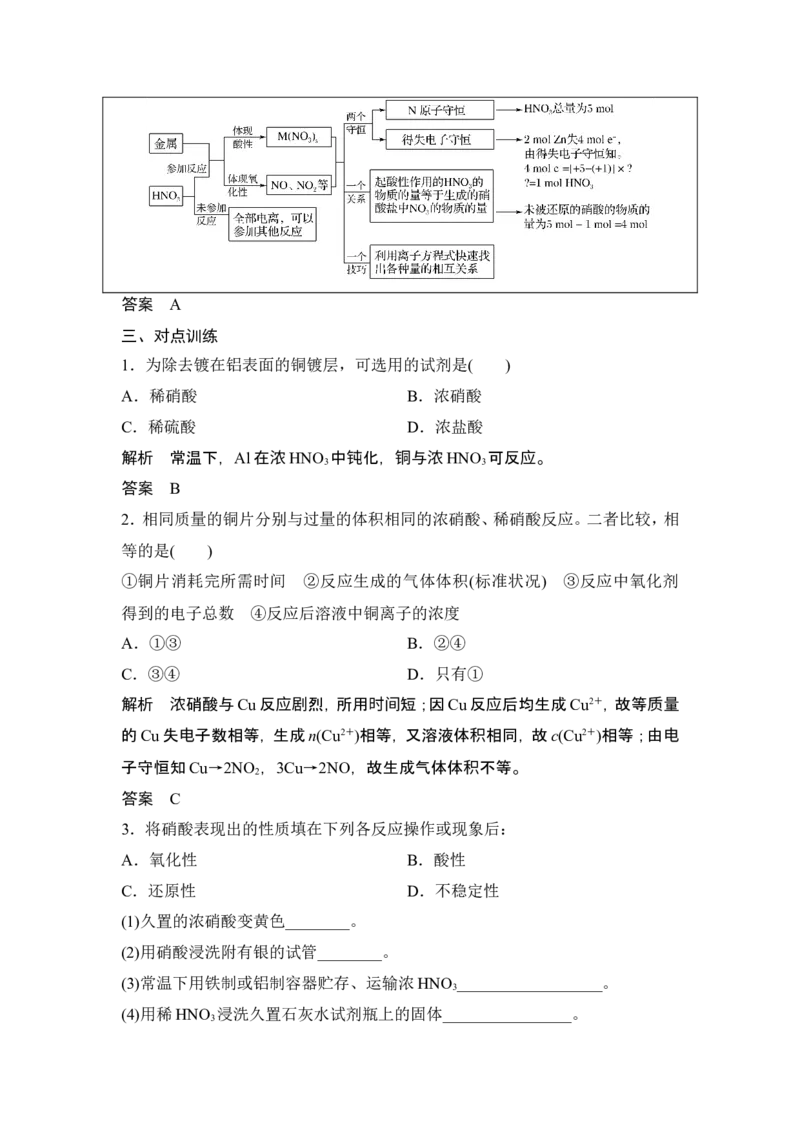
[硝酸与金属反应计算思维模型]答案 A
三、对点训练
1.为除去镀在铝表面的铜镀层,可选用的试剂是( )
A.稀硝酸 B.浓硝酸
C.稀硫酸 D.浓盐酸
解析 常温下,Al在浓HNO 中钝化,铜与浓HNO 可反应。
3 3
答案 B
2.相同质量的铜片分别与过量的体积相同的浓硝酸、稀硝酸反应。二者比较,相
等的是( )
①铜片消耗完所需时间 ②反应生成的气体体积(标准状况) ③反应中氧化剂
得到的电子总数 ④反应后溶液中铜离子的浓度
A.①③ B.②④
C.③④ D.只有①
解析 浓硝酸与Cu反应剧烈,所用时间短;因Cu反应后均生成Cu2+,故等质量
的Cu失电子数相等,生成n(Cu2+)相等,又溶液体积相同,故c(Cu2+)相等;由电
子守恒知Cu→2NO ,3Cu→2NO,故生成气体体积不等。
2
答案 C
3.将硝酸表现出的性质填在下列各反应操作或现象后:
A.氧化性 B.酸性
C.还原性 D.不稳定性
(1)久置的浓硝酸变黄色________。
(2)用硝酸浸洗附有银的试管________。
(3)常温下用铁制或铝制容器贮存、运输浓HNO __________________。
3
(4)用稀HNO 浸洗久置石灰水试剂瓶上的固体________________。
3(5)用Cu和稀HNO 制NO气体________。
3
(6)浓HNO 中滴入石蕊溶液并微热,石蕊溶液先变红后褪色________。
3
解析 浓HNO 见光或受热易分解生成NO ,NO 又溶于硝酸中而使其显黄色。
3 2 2
浓硝酸具有强氧化性,常温下使Fe、Al金属钝化,与金属Cu、Ag等都能发生反应。
硝酸具有酸性,与碱、盐、碱性氧化物等反应。在浓HNO 中滴入石蕊溶液,石蕊
3
溶液先变红,表现出酸性,后褪色,又表现出强氧化性。
答案 (1)D (2)AB (3)A (4)B (5)AB (6)AB
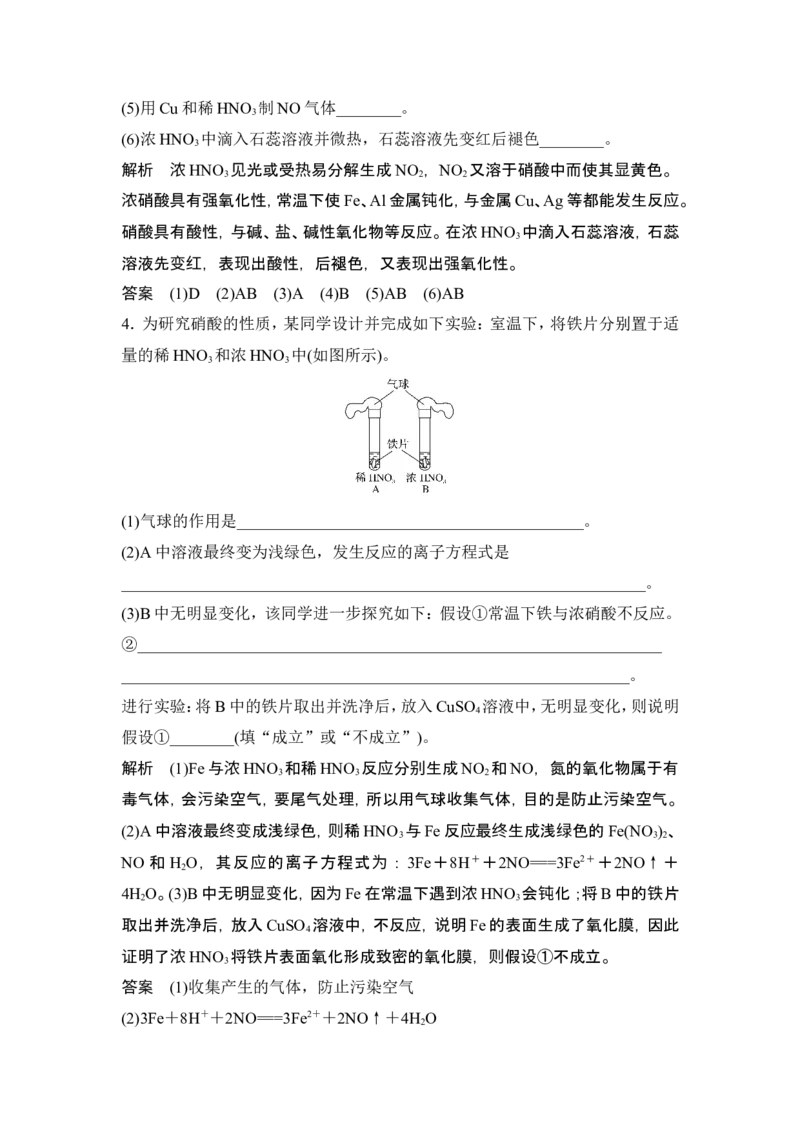
4.为研究硝酸的性质,某同学设计并完成如下实验:室温下,将铁片分别置于适
量的稀HNO 和浓HNO 中(如图所示)。
3 3
(1)气球的作用是___________________________________________。
(2)A中溶液最终变为浅绿色,发生反应的离子方程式是
_________________________________________________________________。
(3)B中无明显变化,该同学进一步探究如下:假设①常温下铁与浓硝酸不反应。
②_________________________________________________________________
_______________________________________________________________。
进行实验:将B中的铁片取出并洗净后,放入CuSO 溶液中,无明显变化,则说明
4
假设①________(填“成立”或“不成立”)。
解析 (1)Fe与浓HNO 和稀HNO 反应分别生成NO 和NO,氮的氧化物属于有
3 3 2
毒气体,会污染空气,要尾气处理,所以用气球收集气体,目的是防止污染空气。
(2)A中溶液最终变成浅绿色,则稀HNO 与Fe反应最终生成浅绿色的Fe(NO ) 、
3 3 2
NO 和 H O,其反应的离子方程式为:3Fe+8H++2NO===3Fe2++2NO↑+
2
4H O。(3)B中无明显变化,因为Fe在常温下遇到浓HNO 会钝化;将B中的铁片
2 3
取出并洗净后,放入CuSO 溶液中,不反应,说明Fe的表面生成了氧化膜,因此
4
证明了浓HNO 将铁片表面氧化形成致密的氧化膜,则假设①不成立。
3
答案 (1)收集产生的气体,防止污染空气
(2)3Fe+8H++2NO===3Fe2++2NO↑+4H O
2(3)浓硝酸将铁片表面氧化形成致密的氧化膜,阻止反应进一步进行 不成立
[学 考 练]
1.与下列物质的反应中,硝酸既表现氧化性,又表现酸性的是( )
A.FeO B.Na CO
2 3
C.CuO D.木炭
解析 A符合要求,FeO与浓HNO 反应生成NO 和Fe(NO ) ,HNO 表现出强氧
3 2 3 3 3
化性,同时又表现出酸性;B、C不符合要求,硝酸与弱酸盐及碱性氧化物反应表
现出酸性;D不符合要求, 硝酸只表现出强氧化性。
答案 A
2.将铜粉置于稀H SO 中,加热后无明显现象,但加入一种盐后,铜粉质量减少,
2 4
而且溶液变蓝,则此盐可能是( )
A.NaCl B.Na SO
2 4
C.NaNO D.Na CO
3 2 3
解析 NO在酸性条件下能将Cu氧化。
答案 C
3.下列叙述正确的是(双选)( )
A.FeO与稀硝酸反应属于复分解反应
B.常温下Fe与浓硝酸不反应
C.铜片与浓硝酸发生离子反应:Cu+2NO+4H+===Cu2++2NO ↑+2H O
2 2
D.向Fe(NO ) 稀溶液中加入盐酸发生反应:3Fe2++4H++NO===3Fe3++NO↑
3 2
+2H O
2
解析 A不正确,FeO与稀硝酸反应,表现硝酸的氧化性和酸性,因此该反应属于
氧化还原反应;B不正确,浓硝酸使Fe钝化属于氧化还原反应;C正确,D正确,
在酸性条件下Fe2+被NO氧化。
答案 CD
4.下列关于浓硝酸和浓硫酸的叙述中正确的是( )
A.常温下不可用铝制容器贮存
B.露置在空气中,容器内酸液的质量都减轻C.常温下都能与铜较快反应
D.露置在空气中,容器内酸液的浓度都降低
解析 常温下,二者均能使铝钝化,A项错误;露置在空气中,浓硫酸吸水质量增
加,B项错误;浓硫酸在常温下与铜没有明显的反应,C项错误;在空气中,浓硝
酸挥发、浓硫酸吸水,二者浓度都降低,D项正确。
答案 D
5.将锌、铁、铜粉末按一定比例混合投入一定量的硝酸中,微热,充分反应后过滤
除去滤渣,滤液中金属阳离子情况不可能是( )
A.只含Cu2+、Fe2+、Zn2+
B.只含Zn2+
C.只含Fe2+、Zn2+
D.只含Cu2+、Fe3+、Zn2+
解析 微热,充分反应后过滤,除去滤渣,说明金属有剩余,溶液中一定不含有
Fe3+。
答案 D
6.下列有关实验操作、现象和解释或结论都正确的是(双选)( )
选项 实验操作 现象 解释或结论
过量的Fe粉中加入稀HNO , 溶液呈
A 3 稀HNO 将Fe氧化为Fe3+
充分反应后,滴入KSCN溶液 红色 3
常温下,Fe、Al放入浓HNO 无明显 Fe、Al与浓HNO 或浓H SO
B 3 3 2 4
或浓H SO 中 现象 发生钝化
2 4
Al箔表面被HNO 氧化,形成
C Al箔插入稀HNO 中 无现象 3
3 致密的氧化膜
试纸先
用玻璃棒蘸取浓HNO 点到红
D 3 变红后 浓HNO 具有酸性和氧化性
色石蕊试纸上 3
褪色
解析 稀硝酸与铁粉反应,铁首先被氧化成Fe3+,过量铁粉将Fe3+还原,最终得
到Fe2+,滴入KSCN溶液不显红色,A项错误;常温下,Fe、Al在浓HNO 或浓
3
H SO 中发生钝化,生成致密的氧化物保护膜阻止了反应进行,B项正确;Al箔能
2 4
与稀HNO 反应放出气体,C项错误。
3
答案 BD
7.碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有
足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是(双选)( )A.洗气瓶中产生的沉淀中有碳酸钡
B.在Z导管出来的气体中有二氧化碳
C.洗气瓶中产生的沉淀是硫酸钡
D.在Z导管口没有红棕色气体出现
解析 碳与浓硫酸共热产生的X气体为CO 和SO 的混合气体,铜与浓硝酸反应
2 2
产生的Y气体是NO ,SO +H O+NO ===H SO +NO,故洗气瓶中产生的是硫
2 2 2 2 2 4
酸钡沉淀,Z处逸出的气体中有CO 和NO,NO遇到空气中的氧气生成了红棕色
2
的NO ,二氧化碳不与氯化钡反应,所以没有BaCO 生成。
2 3
答案 BC
8.用以下三种途径来制取相同质量的硝酸铜:①铜跟浓硝酸反应,②铜跟稀硝酸
反应,③铜跟氧气反应生成氧化铜,氧化铜再跟硝酸反应。以下叙述正确的是(
)
A.三种途径所消耗的铜的物质的量不相等
B.三种途径所消耗的硝酸的物质的量相等
C.所消耗铜的物质的量:途径③>途径①>途径②
D.所消耗硝酸的物质的量:途径①>途径②>途径③
解析 三种途径发生的反应历程如下:
途径①Cu――→Cu(NO ) +NO
3 2 2
途径②Cu――→Cu(NO ) +NO
3 2
途径③Cu――→CuO――→Cu(NO )
3 2
由此可见,途径①、②消耗HNO 量多且产生有毒气体。
3
答案 D
9.将0.1 mol铜与40 mL 10 mol/L HNO 充分反应后,溶液中含a mol H+。由此可
3
知( )
A.生成的气体在标准状况下的体积为4.48 L
B.生成的气体在标准状况下的体积为1.49 L
C.被还原的硝酸的物质的量为(0.2-a)molD.反应后溶液中所含NO的物质的量为0.2 mol
解析 根据题意知剩余HNO 为a mol,Cu(NO ) 的量为0.1 mol,被还原的HNO
3 3 2 3
为0.04×10 mol-a mol-0.1×2 mol=(0.2-a)mol,生成的NO 为(0.2-a) mol。
x
答案 C
10.关于硝酸的说法中正确的是( )
A.硝酸电离出的H+,能被Zn还原成H
2
B.常温下,向浓HNO 中投入Fe片,会产生大量的红棕色气体
3
C.向装有Fe(NO ) 溶液的试管中加入稀H SO ,可在管口观察到红棕色气体
3 2 2 4
D.过量的Fe粉中加入稀HNO ,充分反应后,滴入KSCN溶液,溶液呈红色
3
解析 A不正确,硝酸具有强氧化性,与Zn反应生成氮氧化物等,不能生成H ;
2
B不正确,Fe被浓硝酸钝化,阻止进一步反应;C正确,稀H SO 电离出H+,NO
2 4
在酸性条件下具有强氧化性,被 Fe2+还原为 NO,试管口遇O 生成红棕色的
2
NO ;D不正确,过量的Fe粉中加入稀HNO ,生成Fe2+,与KSCN溶液不反应。
2 3
答案 C
11.将红热的固体单质甲放入显黄色的浓乙溶液中,剧烈反应,产生混合气体A,
A在常温下不与空气作用,发生如下图所示的变化。
气体A――→
则:
(1)写出下列物质的化学式:
丙________,B________,C________,D________。
(2)写出甲跟乙反应的化学方程式:___________________________________
_____________________________________________________________。
(3)单质丙与溶液乙反应生成气体B的离子方程式___________________
_______________________________________________________。
解析 红热的固体单质甲放入黄色的浓乙溶液中产生混合气体A,A不与空气反
应,证明甲为碳,乙为 HNO ,混合气体 A 中含有 CO 和 NO ,3NO +
3 2 2 2
H O===2HNO +NO,CO +Ca(OH) ===CaCO ↓+H O,故 B 为 NO,C 为
2 3 2 2 3 2
CaCO 。单质丙与乙溶液(即稀HNO )反应生成气体B(NO)和蓝色溶液D,知丙为
3 3
铜,D为Cu(NO ) 。
3 2
答案 (1)Cu NO CaCO Cu(NO )
3 3 2(2)C+4HNO (浓)=====CO ↑+4NO ↑+2H O
3 2 2 2
(3)3Cu+8H++2NO===2NO↑+3Cu2++4H O
2
12.如图所示甲是某学生验证铜和浓硝酸反应的装置,乙、丙是另外两位同学对
甲装置改进后的装置:
(1)甲、乙、丙三个装置中都发生的反应的化学方程式:
_______________________________________________________________。
(2)和甲装置相比,乙装置的优点是
①_____________________________________________________________;
②______________________________________________________________。
(3)为了进一步验证NO 和水的反应,某学生设计了丙装置。实验时先关闭止水夹
2
________,再打开止水夹________,才能使NO 气体充满②试管;当气体充满②
2
试管后,将铜丝提起与溶液脱离。欲使烧杯中的水进入②试管,应该
_____________________________________________________________
________________________________________________________________。
解析 铜和浓硝酸反应的化学方程式是 Cu+4HNO (浓)===Cu(NO ) +2NO ↑
3 3 2 2
+2H O。根据题目给定的装置图可知乙装置有尾气处理装置,同时可以通过移动
2
铜丝来控制反应的发生与停止。实验丙中,实验时先关闭止水夹c,再打开止水夹
a、b,才能使NO 气体充满②试管;当气体充满②试管后,将铜丝提起与溶液脱离
2
停止反应。欲使烧杯中的水进入②试管应该先关闭b,再关闭a,然后打开c,用手
捂住试管②。
答案 (1)Cu+4HNO (浓)===Cu(NO ) +2NO ↑+2H O
3 3 2 2 2
(2)①可以控制反应的发生与停止 ②吸收NO 气体,防止污染环境
2
(3)c ab 先关闭b,再关闭a,然后打开c,用手捂住试管②
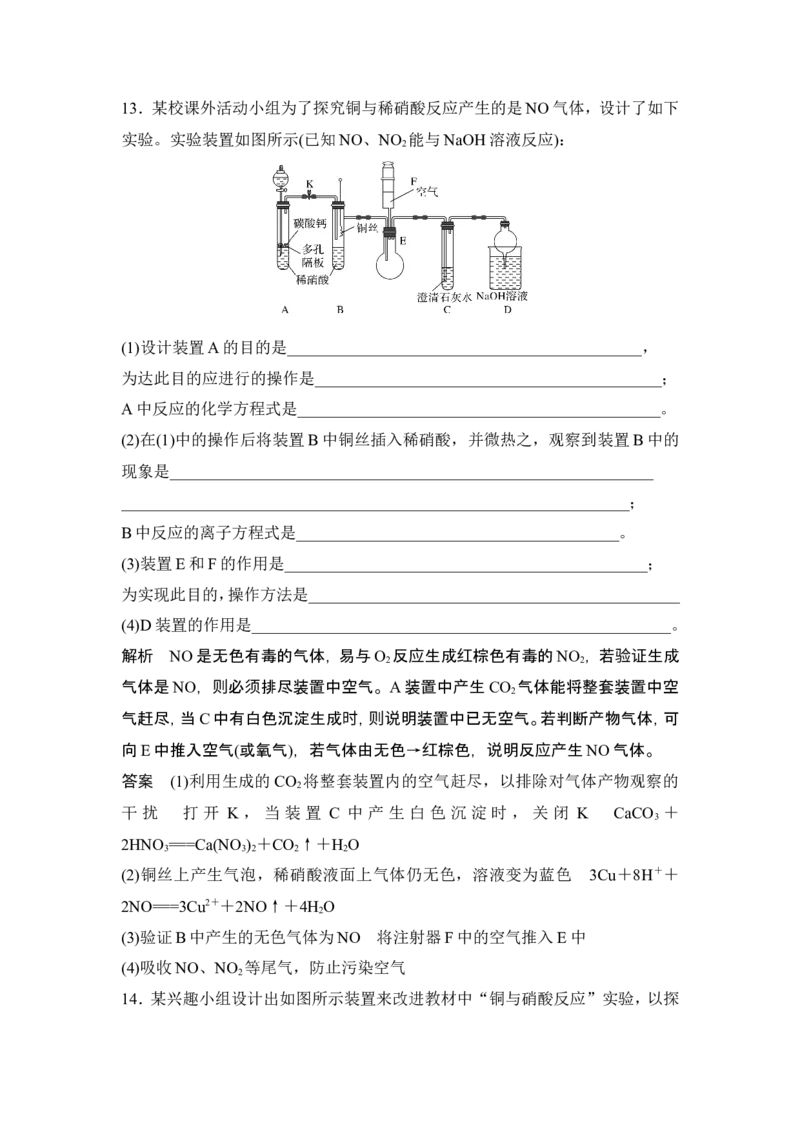
[能 力 练]13.某校课外活动小组为了探究铜与稀硝酸反应产生的是NO气体,设计了如下
实验。实验装置如图所示(已知NO、NO 能与NaOH溶液反应):
2
(1)设计装置A的目的是____________________________________________,
为达此目的应进行的操作是___________________________________________;
A中反应的化学方程式是_____________________________________________。
(2)在(1)中的操作后将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的
现象是____________________________________________________________
_______________________________________________________________;
B中反应的离子方程式是________________________________________。
(3)装置E和F的作用是_____________________________________________;
为实现此目的,操作方法是______________________________________________
(4)D装置的作用是____________________________________________________。
解析 NO是无色有毒的气体,易与O 反应生成红棕色有毒的NO ,若验证生成
2 2
气体是NO,则必须排尽装置中空气。A装置中产生CO 气体能将整套装置中空
2
气赶尽,当C中有白色沉淀生成时,则说明装置中已无空气。若判断产物气体,可
向E中推入空气(或氧气),若气体由无色→红棕色,说明反应产生NO气体。
答案 (1)利用生成的CO 将整套装置内的空气赶尽,以排除对气体产物观察的
2
干 扰 打 开 K , 当 装 置 C 中 产 生 白 色 沉 淀 时 , 关 闭 K CaCO +
3
2HNO ===Ca(NO ) +CO ↑+H O
3 3 2 2 2
(2)铜丝上产生气泡,稀硝酸液面上气体仍无色,溶液变为蓝色 3Cu+8H++
2NO===3Cu2++2NO↑+4H O
2
(3)验证B中产生的无色气体为NO 将注射器F中的空气推入E中
(4)吸收NO、NO 等尾气,防止污染空气
2
14.某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,
加热c,其目的是____________________________________________。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL
浓硝酸,c中反应的化学方程式是________________________________________
再由a向c中加2 mL蒸馏水,c中的实验现象是__________________________
_____________________________________________________________。
(3)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是________,
理由是________________________________________________________。
方案 反应物
甲 Cu、浓HNO
3
乙 Cu、稀HNO
3
丙 Cu、O 、稀HNO
2 3
(4)该小组同学向d中加入KBr溶液,c中加入固体KMnO ,由a向c中加入浓盐
4
酸。观察到的实验现象是_____________________________________________;
该小组同学实验目的是______________________________________________,
但此实验的不足之处是_________________________________________。
解析 (1)形成封闭系统的气体在热胀冷缩作用下压强发生变化,可用于检查装
置封闭是否完好。(2)铜与浓硝酸反应较剧烈,生成NO 气体呈红棕色,铜与稀硝
2
酸反应相对平稳,放出无色气体NO,即混合气体颜色变浅。(3)铜直接与浓、稀
HNO 反应都有对环境有危害的污染物NO 产生,而Cu先与O 化合生成CuO后
3 x 2
再与HNO 发生复分解反应,生成Cu(NO ) 时不产生对环境有危害的物质,且消
3 3 2
耗HNO 量较少。(4)KMnO 在常温下与浓盐酸反应生成氯气,氯气置换KBr溶液
3 4
中的溴使溶液显橙色,同时反应现象证明有氧化还原反应发生,证明给定物质氧
化性(或还原性)强弱;氯气有毒,实验装置中还应该有尾气处理部分。答案 (1)检查装置气密性 (2)Cu+4HNO (浓)===Cu(NO ) +2NO ↑+2H O
3 3 2 2 2
反应变缓,气体颜色变浅
(3)丙 耗酸量最少,无污染
(4)c中有黄绿色气体产生,d中溶液变为橙色 证明氧化性KMnO >Cl >Br 没
4 2 2
有处理尾气