文档内容
九年级化学下册期中测试卷
时间:90分钟 满分:120分
相对原子质量:Al-27,H-1,Cl-35.5,O-16
一.单项选择题(每小题3分,共45分)
1. 下列各组物质相互混合不能形成溶液的是( )
A.蔗糖和水 B.粉笔灰和水 C.碘和酒精 D.植物油和汽油
2. 下列有关溶液性质的说法中错误的是( )
A.溶液一定是无色、透明的混合物
B.溶液加水稀释前后溶质的质量不变
C.食盐水能导电是因为食盐水中含有较多自由移动的离子
D.海水是盐溶液,所以冬天海水不易结冰
3. 下列加速溶解的措施中,能改变固体溶解度的是( )
A.把固体研细 B.加热 C.搅拌 D.振荡
4. 下列物质质量增加的变化属于物理变化是( )
A.铜片在空气中加热 B.敞放的固体烧碱 C.露天堆放的生石灰 D.干燥木材吸
水
5.地球上71%的面积覆盖着水,水是生命之源,也是重要的溶剂,下列说法正确的是( )
A. 将1gCaO投入到99g水中,溶质的质量分数1%
B. 常温下KNO 、Ca(OH) 的饱和溶液降温后仍是饱和溶液
3 2
C. 将NaCl、蔗糖溶于水后,溶质均以分子形式存在
D. 溶质在溶解的过程中,有的放出热量,有的吸收热量
6. 已知氢氧化锂(LiOH)可溶于水,其化学性质与氢氧化钠相似。下列对氢氧化锂的化学性
质的说法中错误的是( )
A.能与二氧化碳反应 B.能使无色酚酞溶液变红
C.能与稀硫酸反应 D.能使紫色石蕊溶液变红
7.现配制溶质质量分数为5%的NaCl溶液,下列说法正确的是( )
A.将氯化钠固体直接放在天平的托盘上称量 B.配制溶液的烧杯留有水
C.为加快固体溶解,用温度计搅拌 D.将配好的溶液倒入细口瓶中,塞紧瓶塞
并贴上标签
8. 某同学为了区别氢氧化钠溶液和澄清石灰水,设计了如图Z-1所示的四组实验方案,其
中能达到目的的是( )
盐酸 酚酞 石蕊 二氧化碳
A B C D
图Z-1
9.下列有关洗涤的说法中错误的是( )
A.用汽油溶解衣物上的油渍 B.用洗洁精乳化餐具上的油污
C.用食醋洗去热水瓶中的水垢 D.用热的纯碱溶液洗去菜刀上的铁锈
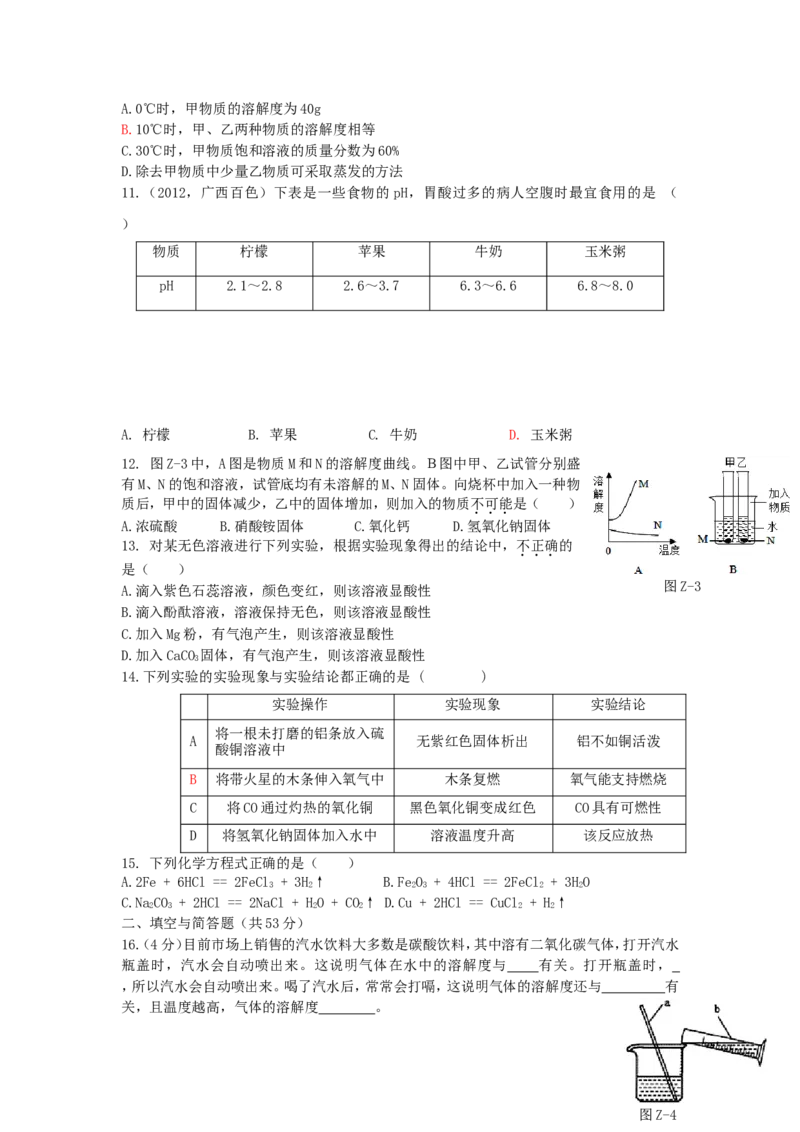
10.图Z-2是甲、乙两种固体物质的溶解度曲线。下列有关叙述正确的是( )
图Z-2A.0℃时,甲物质的溶解度为40g
B.10℃时,甲、乙两种物质的溶解度相等
C.30℃时,甲物质饱和溶液的质量分数为60%
D.除去甲物质中少量乙物质可采取蒸发的方法
11.(2012,广西百色)下表是一些食物的 pH,胃酸过多的病人空腹时最宜食用的是 (
)
物质 柠檬 苹果 牛奶 玉米粥
pH 2.1~2.8 2.6~3.7 6.3~6.6 6.8~8.0
A. 柠檬 B. 苹果 C. 牛奶 D. 玉米粥
12. 图Z-3中,A图是物质M和N的溶解度曲线。B图中甲、乙试管分别盛
有M、N的饱和溶液,试管底均有未溶解的M、N固体。向烧杯中加入一种物
质后,甲中的固体减少,乙中的固体增加,则加入的物质不可能是( )
A.浓硫酸 B.硝酸铵固体 C.氧化钙 D.氢氧化钠固体
13. 对某无色溶液进行下列实验,根据实验现象得出的结论中,不正确的
是( )
图Z-3
A.滴入紫色石蕊溶液,颜色变红,则该溶液显酸性
B.滴入酚酞溶液,溶液保持无色,则该溶液显酸性
C.加入Mg粉,有气泡产生,则该溶液显酸性
D.加入CaCO 固体,有气泡产生,则该溶液显酸性
3
14.下列实验的实验现象与实验结论都正确的是 ( )
实验操作 实验现象 实验结论
将一根未打磨的铝条放入硫
A 无紫红色固体析出 铝不如铜活泼
酸铜溶液中
B 将带火星的木条伸入氧气中 木条复燃 氧气能支持燃烧
C 将CO通过灼热的氧化铜 黑色氧化铜变成红色 CO具有可燃性
D 将氢氧化钠固体加入水中 溶液温度升高 该反应放热
15. 下列化学方程式正确的是( )
A.2Fe + 6HCl == 2FeCl + 3H↑ B.FeO + 4HCl == 2FeCl + 3HO
3 2 2 3 2 2
C.NaCO + 2HCl == 2NaCl + HO + CO↑ D.Cu + 2HCl == CuCl + H↑
2 3 2 2 2 2
二、填空与简答题(共53分)
16.(4分)目前市场上销售的汽水饮料大多数是碳酸饮料,其中溶有二氧化碳气体,打开汽水
瓶盖时,汽水会自动喷出来。这说明气体在水中的溶解度与 有关。打开瓶盖时,
,所以汽水会自动喷出来。喝了汽水后,常常会打嗝,这说明气体的溶解度还与 有
关,且温度越高,气体的溶解度 。
图Z-417.(5分)图Z-4是稀释浓硫酸实验的示意图。
(1)写出图中a、b两种仪器的名称:_________、_______;
(2)b容器所盛的试剂是________(填“水”或“浓硫酸”)。
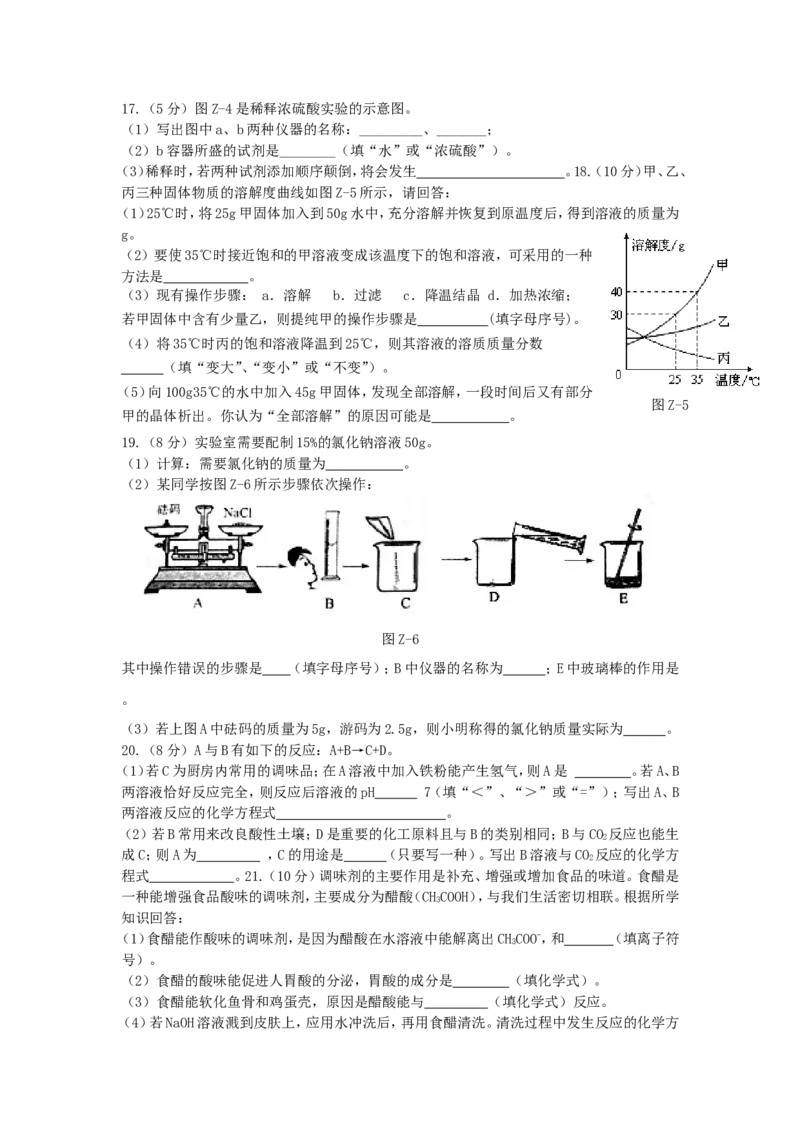
(3)稀释时,若两种试剂添加顺序颠倒,将会发生 。18.(10分)甲、乙、
丙三种固体物质的溶解度曲线如图Z-5所示,请回答:
(1)25℃时,将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为
g。
(2)要使35℃时接近饱和的甲溶液变成该温度下的饱和溶液,可采用的一种
方法是 。
(3)现有操作步骤: a.溶解 b.过滤 c.降温结晶 d.加热浓缩;
若甲固体中含有少量乙,则提纯甲的操作步骤是 (填字母序号)。
(4)将35℃时丙的饱和溶液降温到25℃,则其溶液的溶质质量分数
(填“变大”、“变小”或“不变”)。
(5)向100g35℃的水中加入45g甲固体,发现全部溶解,一段时间后又有部分
图Z-5
甲的晶体析出。你认为“全部溶解”的原因可能是 。
19.(8分)实验室需要配制15%的氯化钠溶液50g。
(1)计算:需要氯化钠的质量为 。
(2)某同学按图Z-6所示步骤依次操作:
图Z-6
其中操作错误的步骤是 (填字母序号);B中仪器的名称为 ;E中玻璃棒的作用是
。
(3)若上图A中砝码的质量为5g,游码为2.5g,则小明称得的氯化钠质量实际为 。
20.(8分)A与B有如下的反应:A+B→C+D。
(1)若C为厨房内常用的调味品;在A溶液中加入铁粉能产生氢气,则A是 。若A、B
两溶液恰好反应完全,则反应后溶液的pH 7(填“<”、“>”或“=”);写出A、B
两溶液反应的化学方程式 。
(2)若B常用来改良酸性土壤;D是重要的化工原料且与B的类别相同;B与CO 反应也能生
2
成C;则A为 ,C的用途是 (只要写一种)。写出B溶液与CO 反应的化学方
2
程式 。21.(10分)调味剂的主要作用是补充、增强或增加食品的味道。食醋是
一种能增强食品酸味的调味剂,主要成分为醋酸(CHCOOH),与我们生活密切相联。根据所学
3
知识回答:
(1)食醋能作酸味的调味剂,是因为醋酸在水溶液中能解离出CHCOO-,和 (填离子符
3
号)。
(2)食醋的酸味能促进人胃酸的分泌,胃酸的成分是 (填化学式)。
(3)食醋能软化鱼骨和鸡蛋壳,原因是醋酸能与 (填化学式)反应。
(4)若NaOH溶液溅到皮肤上,应用水冲洗后,再用食醋清洗。清洗过程中发生反应的化学方程式为 。
(5)生活中常用酒来制取食醋,原理是酒中的CHCHOH在酶的作用下与空气中O 反应得到醋
3 2 2
酸和另一种液体。已知在用酒制取食醋过程中,质量增加了16kg,则所得食醋中醋酸的质量
为 kg。
22.(8分)雨、雪在形成和降落过程中吸收、溶解了空气中SO 及氮氧化物等物质,
2
形成了pH小于5.6的降水称为酸雨,请回答下列有关酸雨的问题:
(l)要测定某地采集到的雨水是否为酸雨,下列提供的试剂(试纸)中宜取用
。
A.蓝色石蕊试纸 B.紫色石蕊溶液 C.无色酚酞试剂 D.pH试纸
(2)已知 CO 的饱和溶液常温下pH不小于 5.6。通常空气中CO 的含量大于 SO
2 2 2
的含量,但人们反而将空气中的 SO 认定为形成酸雨的主要原因之一。有同学想
2
图Z-7
通过如图 Z-7 的实验寻找证据,你认为下一步的实验步骤是测定
,只要出现 的实验结果,就可认定SO 溶于水有形成酸雨的可能。
2
(3)已知SO 与 CO 有许多化学性质是相似的,亚硫酸钙(CaSO)是白色难溶于水但可溶于酸
2 2 3
的固体。某同学向一酸雨样品中滴加 CaCl,溶液未观察到有浑浊现象,继续滴入NaOH溶液
2
后即有白色沉淀产生。在以上实验过程中,下列不可能发生的化学反应是 。
A SO+CaCl+HO== CaSO↓十2HCl B.SO+2NaOH==NaSO+HO
2 2 2 3 2 2 3 2
C. NaSO+CaCl= CaSO↓+2NaCI D.HSO +2NaOH= NaSO+2HO
2 3 2 3 2 3 2 3 2
三、实验探究题(共12分)
23.某化学兴趣小组在做完制取二氧化碳的实验后(用石灰石和稀盐酸制取),对反应后反应
器内的剩余溶液的溶质成分产生了兴趣,他们继续进行了以下实验探究。
【分析推断】根据制取二氧化碳的反应原理,可以确定剩余溶液中一定含有氯化钙。但其中是
否含有氯化氢需要通过实验来证明。若剩余溶液显酸性(含有H+),说明含有氯化氢。
【查阅资料】碳酸钙不溶于水,氢氧化钙微溶于水,氯化钙溶液呈中性。
【实验过程】将剩余的溶液倒入烧杯中,微热后冷却到室温。
实验操作 实验现象 实验结论
取烧杯中溶液少许于试管 现象:溶液变为红色
甲同学 中,向其中滴加______
溶液显酸性
(含有H+);溶
质中有氯化
取烧杯中溶液少许于试管 现象:______________。
氢。
乙同学 中,向其中加入少量锌粒 反 应 的 化 学 方 程 式 是 :
________________。
取烧杯中溶液少许于试管 现象:___________________________。
丙同学 中,向其中加入少量石灰石
【拓展提高】若要从剩余溶液中得到尽可能多的纯净的氯化钙固体,同学们认为可以向剩余
溶液中加入稍过量的____________(填化学式),经____________、蒸发等操作后即可完成。
四、计算题(共10分)
24.(2012.宿迁市)正常情况下人的胃液pH为0.8〜1.5 , 相应含HCl的溶质质量分数为0.
2%〜0.4%,胃液中HCl过多与过少都不利于人体健康。某人出现反胃、吐酸水的症状,经检查
其胃液中HCl的质量分数为1.495%(胃液密度约为1g/cm3)。
(1)正常情况下,人的胃液显 性。
(2)若人的胃液总量为100mL,正常人胃液中HCl的质量范围为 g。
(3)服用碱性药品可以治疗胃液中HCl含量过多,你认为该患者 (填"能"或"不能")服用氢氧化钠来治疗胃液中HCl过多,理由是 。
(4)医生给患者开的药品为胃舒平【有效成分是Al(OH)】,每片胃舒平含Al(OH) 的质量为
3 3
0.39g 。请根据化学方程式计箅该患者至少服用多少片的胃舒平,胃液才能恢复正常?(请
写出计算过程)
答案与点拨
一、单项选择题:
1.B
2.A
3.B 点拨:固体的溶解度受温度的影响,其他措施只能改变固体的溶解速率,但不能改变固
体的溶解度。
4.D
5.D 点拨:氧化钙溶于水与水反应生成氢氧化钙,氢氧化钙做溶质;溶质的质量不是1g;故
溶质的质量分数不是1%;故A错;氢氧化钙随温度的升高而减小降温会变成不饱和溶液;故
B错;氯化钠属于盐在溶液中电离出钠离子和氯离子;故C错;、物质在溶解的过程中,有的放
出热量,有的吸收热量,D正确。
6.D
7.D
8.D
9.D 点拨:碳酸钠不能与三氧化二铁反应,除去铁锈应用酸性物质,如食醋或稀盐酸等。
10.B 点拨:从0℃向上作垂线,甲的溶解度为20g,故A错;曲线中交点表示该温度时两种
物质的溶解度相等,所以10℃时,甲、乙两种物质的溶解度相等,故B正确; 30℃时,甲物质
饱和溶液的质量分数为 ×100%=37.5%,故C错;如果溶解度受温度影响较大的物
质从溶液中结晶析出的方法是冷却热饱和溶液,如果溶解度受温度影响不大的物质从溶液
中结晶析出的方法是蒸发溶剂,由于甲物质溶解度随温度变化比较大,所以用降温结晶,故D
错。
11.D
12.B 点拨:根据题意不难得知,向烧杯中加入一种物质后,甲中的固体减少,即溶液中溶质
增多;而乙中的固体增加,即溶液中溶质减少,根据两物质的溶解度曲线可知,应该是温度升
高时所引起的这系列的变化,因此加入的物质应该是溶于水放热的,而浓硫酸、氧化钙、氢氧
化钠溶于水都会放热,故选B。
13.B
14.B 点拨:未打磨的铝条表面有氧化铝,因为氧化铝与硫酸铜溶液不反应,因此无变化,不
能证明铝不如铜活泼,故A选项错误;将带火星的木条伸入氧气中,木条复燃,说明氧气能支
持燃烧,即氧气具有助燃性,故选项B正确;将CO通过灼热的氧化铜,黑色氧化铜变成红色,
说明CO具有还原性,不是可燃性,故选项C错误;将氢氧化钠固体加入水中,溶液温度升高,
说明氢氧化钠溶于水放热,但是没有发生化学变化,故选项D错误。
15.C
二、填空与简答题:
16.压强 压强减小,气体的溶解度减小 温度 越小17. (1)玻璃棒 量筒 (2)浓硫酸 (3)酸液飞溅
18. (1)65 (2)加入甲物质(溶质)或恒温蒸发溶剂(水) (3)adcb (4)不变
(5)甲固体溶于水时放热
19.(1)7.5g (2)AB 量筒 搅拌,加速固体溶解 (3)2.5g
20.(1)稀盐酸 = HCl+NaOH═NaCl+HO
2
(2)NaCO 建筑材料(合理即可)
2 3
CO+Ca(OH)=CaCO↓+HO
2 2 3 2
21.(1)H+ (2)HCl (3)CaCO
3
(4)CHCOOH+NaOH=CHCOONa+HO (5)30
3 3 2
22. (1)D (2)HSO 溶液的酸碱性 pH值小于5.6 (3)A
2 3
点拨:测溶液的酸碱性可用酸碱指示剂,但是测溶液的酸碱度必须用pH试纸;题目中已经告
诉我们CO 的饱和溶液常温下pH不小于5.6,即排除CO 溶于水形成酸雨的可能,那么只要证
2 2
明SO 溶于水生成的溶液是成酸性的即可;CO 不能和CaCl 反应生成盐酸,所以这个反应也
2 2 2
不能进行,一般来说,强酸可以制取弱酸,反之则不行。
三、实验探究题:
23. 紫色石蕊试液 锌粒逐渐溶解,有气泡产生Zn+2HCl=ZnCl+H ↑ 石灰石逐渐溶解,
2 2
有气泡产生 CaCO 过滤
3
四、计算题:
24. (1)酸 (2)0.2~0.4 (3)不能 氢氧化钠有很强的腐蚀性
(4)解:该患者胃酸中至少多出HCl的质量为:100ml×1g/cm3×1.495%-0.4g =1.095g
设要使该患者恢复正常,至少需要消耗Al(OH) 的质量为x。
3
3HCl + Al(OH) = AlCl + 3HO
3 3 2
109.5 78
1.095g x
X=0.78g
至少服用胃舒平的片数为:0.78÷0.39g∕片=2片
答:至少服用2片胃舒平。