文档内容
优秀领先 飞翔梦
想
2016年浙江省杭州市中考化学试卷
一、选择题(共7小题,每小题3分,满分21分)
1.下列选项正确的是( )
A.
检验甲烷燃烧有CO 生成
2
B.
读液体体积
C.
将带有残留夜的滴管倒持
D.
吹灭酒精灯
2.中国科学院某研究小组设计了一种高性能锂空气电池,其反应原理可表示为:2Li+O
2
Li O ,已知锂元素在化合物中显+1价,下列说法错误的是( )
2 2
A.反应物锂是金属单质
B.该反应中MnO 是催化剂
2
www.youyi100.com
第 1 页 共 14 页优秀领先 飞翔梦
想
C.Li O 中氧元素的化合价显﹣2价
2 2
D.该反应是化合反应
原图片版是科学试题,所以题号不一致
4.下列有关钠在氯气中燃烧的实验,分析合理的是( )
A.钠在氯气中燃烧时,钠原子得到电子
B.反应物钠由分子构成,生成物氯化钠由离子构成
C.钠能在氯气中燃烧,说明燃烧不一定需要氧气参与
D.钠在氯气中燃烧生成的氯化钠与家庭中食用的氯化钠化学性质不同
5.一杯70℃的硝酸钾饱和溶液,冷却后有晶体析出(晶体不含结晶水),若不考虑溶剂的蒸
发,则剩余溶液与原溶液相比( )
A.由饱和溶液变为不饱和溶液B.溶质质量不变
C.溶液质量不变 D.溶质的质量分数减小
6.小金制作了一个如图甲所示的简易酸碱灭火器,并进行了如图乙所示的灭火操作,结束后
对瓶中残留液进行了如下实验:①取少量残留液于试管中,滴加2滴紫色石蕊试液,变红色;
②另取少量残留液于试管中滴加适量氯化钡溶液,有白色沉淀,则残留液中有大量的( )
www.youyi100.com
第 2 页 共 14 页优秀领先 飞翔梦
想
A.硫酸钠 B.碳酸钠 C.盐酸 D.氯化钠
7.向一定质量的甲中连续加入乙至过量,此过程中溶液的总质量与加入乙的质量之间关系,
符合如图曲线表示的是( )
甲 乙
A 稀硫酸 氢氧化钠溶液
B 稀盐酸 碳酸钙粉末
C 稀盐酸 锌粒
[来源:学科网ZXXK]
D 硝酸银溶液 铜粉
[来源:学科网]
A.A B.BC.CD.D
8.如表是生活中常见4种饮料及主要成分,下列关于这些饮料的组成、性质和用途表述错误
的是( )
名称 主要成分
雪碧 碳水化合物、水
苏打水(弱碱性) 碳酸氢钠、水
盐汽水 氯化钠、水
柠檬汁 水、碳水化合物、蛋白质、纤维、维生素 等
A.雪碧是一种混合物
B.4种饮料中,苏打水的PH值最小
C.从事高温作业的人员,适宜补充盐汽水
D.喝适量柠檬汁有助于补充人体的维生素
二、解答题(共4小题,满分20分)
9.如图为核聚变的示意图,其中①②③表示三种原子,“●”、“○”、“.”表示原子中的
不同微粒,③是 元素的原子,①②③中属于同种元素的原子是
(选填序号).
www.youyi100.com
第 3 页 共 14 页优秀领先 飞翔梦
想
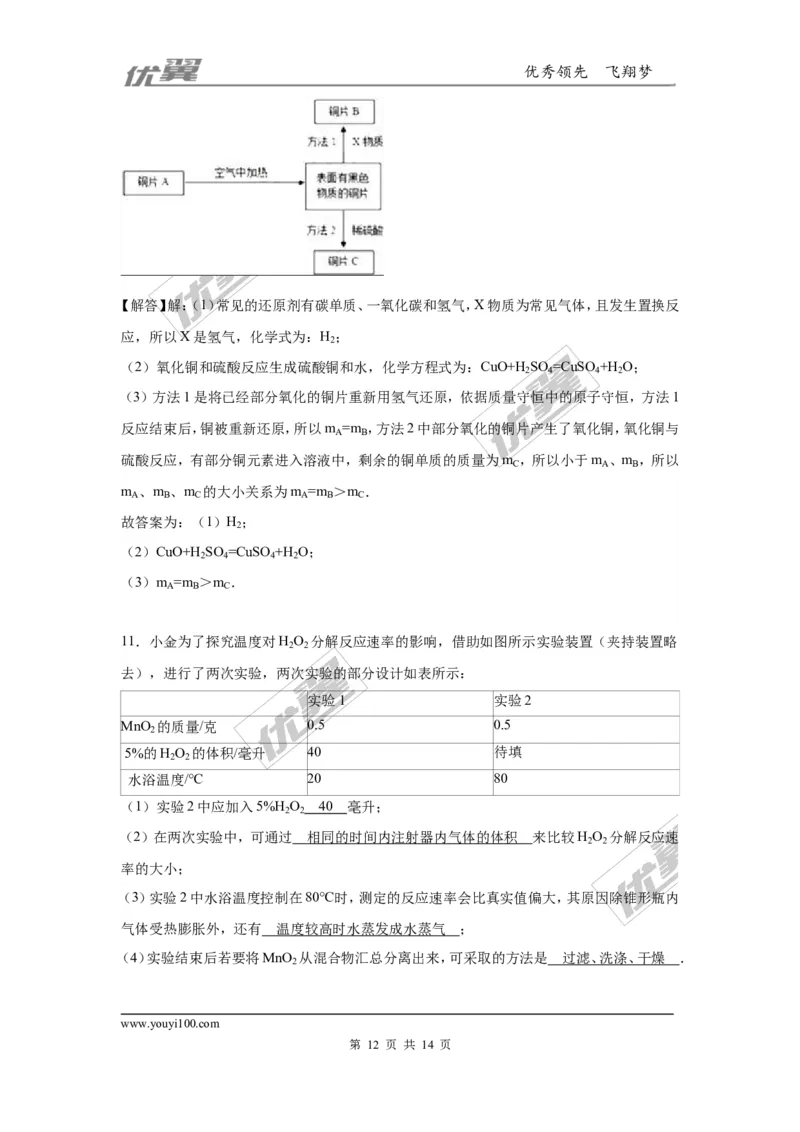
10.若方法1中的X物质为常见气体,且发生置换反应,则X是 (填化学式);
(2)写出方法2的化学方程式 ;
(2)铜片A、铜片B、铜片C的质量分别为m 、m 、m ,其中方法1和方法2均完全反应,则
A B C
m 、m 、m 的大小关系为 .
A B C
11.小金为了探究温度对H O 分解反应速率的影响,借助如图所示实验装置(夹持装置略
2 2
去),进行了两次实验,两次实验的部分设计如表所示:
实验1 实验2
MnO 的质量/克 0.5 0.5
2
5%的H O 的体积/毫升 40 待填
2 2
水浴温度/℃ 20 80
(1)实验2中应加入5%H O 毫升;
2 2
(2)在两次实验中,可通过 来比较H O 分解反应速率的大小;
2 2
(3)实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因除锥形瓶内
气体受热膨胀外,还有 ;
(4)实验结束后若要将MnO 从混合物汇总分离出来,可采取的方法是 .
2
www.youyi100.com
第 4 页 共 14 页优秀领先 飞翔梦
想
12.焦亚硫酸钠(Na S O )是一种常用的食品抗氧化剂,小金模仿化工生产,用如图装置来制
2 2 5
取Na S O .
2 2 5
已知:A中发生的反应为:H SO (浓)+Na SO ═Na SO +SO ↑+H O
2 4 2 3 2 4 2 2
B中发生的反应为:Na SO +SO ═Na S O
2 3 2 2 2 5
(1)图中盛放浓硫酸的仪器名称是 ;
(2)写出C中发生反应的化学方程式 ;
(3)在实验过程中,滴加浓硫酸不宜过快,理由是 .
(4)该实验开始滴加浓硫酸时,应先除尽装置内的空气,若忘记这一操作,新制取的Na S O
2 2 5
产品中会混有Na SO 杂质,这与O 的 有关(填化学性质)
2 4 2
www.youyi100.com
第 5 页 共 14 页优秀领先 飞翔梦
想
2016 年浙江省杭州市中考化学试卷
参考答案与试题解析
一、选择题(共7小题,每小题3分,满分21分)
1.下列选项正确的是( )
A.
检验甲烷燃烧有CO 生成 B.
2
读液体体积
C.
将带有残留夜的滴管倒持 D.
吹灭酒精灯
【解答】解:A、检验甲烷燃烧有CO 生成,在火焰上方罩一个内壁涂有澄清石灰水的烧杯,澄
2
清石灰水变浑浊,证明有二氧化碳生成,故正确;
B、量筒读数时,视线要与凹液面最低处保持水平,故错误;
C、将带有残留液的滴管倒持,会使残留液倒流,腐蚀胶头.故错误;
D、熄灭酒精灯不能吹灭,要用灯帽盖灭,故错误;
故选A.
www.youyi100.com
第 6 页 共 14 页优秀领先 飞翔梦
想
2.中国科学院某研究小组设计了一种高性能锂空气电池,其反应原理可表示为:2Li+O
2
Li O ,已知锂元素在化合物中显+1价,下列说法错误的是( )
2 2
A.反应物锂是金属单质
B.该反应中MnO 是催化剂
2
C.Li O 中氧元素的化合价显﹣2价
2 2
D.该反应是化合反应
【解答】解:A、锂是由金属元素锂组成的纯净物,属于金属单质,故A正确;
B、由化学反应方程式可知,该反应中MnO 是催化剂,故B正确;
2
C、Li O 是化合物,在化合物中正负化合价代数和为零,锂元素在钙化合物中显+1价,故氧
2 2
元素的化合价为﹣1价,故C错误;
D、该反应由两种物质生成了一种物质,属于化合反应,故D正确.
故选C.
www.youyi100.com
第 7 页 共 14 页优秀领先 飞翔梦
想
4.下列有关钠在氯气中燃烧的实验,分析合理的是( )
A.钠在氯气中燃烧时,钠原子得到电子
B.反应物钠由分子构成,生成物氯化钠由离子构成
C.钠能在氯气中燃烧,说明燃烧不一定需要氧气参与
D.钠在氯气中燃烧生成的氯化钠与家庭中食用的氯化钠化学性质不同
【解答】解:A、钠原子的最外层电子数是1,在化学反应中容易失去电子,故A错误;
B、钠是金属,金属是由原子直接构成的氯化钠是由钠离子、氯离子构成的,故B错误;
C、钠能在氯气中燃烧,说明燃烧不一定需要氧气参与,故C正确;
D、钠在氯气中燃烧生成的氯化钠与家庭中食用的氯化钠化学性质相同,故D错误.
故选:C.
www.youyi100.com
第 8 页 共 14 页优秀领先 飞翔梦
想
5.一杯70℃的硝酸钾饱和溶液,冷却后有晶体析出(晶体不含结晶水),若不考虑溶剂的蒸
发,则剩余溶液与原溶液相比( )
A.由饱和溶液变为不饱和溶液B.溶质质量不变
C.溶液质量不变 D.溶质的质量分数减小
【解答】解:A、一杯70℃的硝酸钾饱和溶液,冷却后有晶体析出,剩余溶液不能继续溶解硝酸
钾,仍为饱和溶液,故选项说法错误.
B、一杯70℃的硝酸钾饱和溶液,冷却后有晶体析出,溶质的质量减少,故选项说法错误.
C、一杯70℃的硝酸钾饱和溶液,冷却后有晶体析出,溶质的质量减少,溶剂的质量不变,则
溶液质量减少,故选项说法错误.
D、一杯70℃的硝酸钾饱和溶液,冷却后有晶体析出,溶质的质量减少,溶剂的质量不变,则
溶质的质量分数减小,故选项说法正确.
故选:D.
6.小金制作了一个如图甲所示的简易酸碱灭火器,并进行了如图乙所示的灭火操作,结束后
对瓶中残留液进行了如下实验:①取少量残留液于试管中,滴加2滴紫色石蕊试液,变红色;
②另取少量残留液于试管中滴加适量氯化钡溶液,有白色沉淀,则残留液中有大量的( )
A.硫酸钠 B.碳酸钠 C.盐酸 D.氯化钠
【解答】解:简易酸碱灭火器中碳酸钠溶液与一种常见的酸反应;结束后对瓶中残留液进行了
如下实验:①取少量残留液于试管中,滴加2滴紫色石蕊试液,变红色,石蕊溶液遇酸性溶液
变红色,遇碱性溶液变蓝色,则说明残留液显酸性.
②另取少量残留液于试管中滴加适量氯化钡溶液,有白色沉淀存在,说明此沉淀是氯化银或
硫酸钡沉淀,由于反应物是一种酸,酸与碳酸钠溶液反应生成盐、水和二氧化碳,同时酸有剩
余,则原酸溶液为硫酸,硫酸与碳酸钠溶液反应生成硫酸钠、水和二氧化碳,则残留液中有大
量的硫酸钠、硫酸.
故选:A.
www.youyi100.com
第 9 页 共 14 页优秀领先 飞翔梦
想
7.向一定质量的甲中连续加入乙至过量,此过程中溶液的总质量与加入乙的质量之间关系,
符合如图曲线表示的是( )
甲 乙
A 稀硫酸 氢氧化钠溶液
B 稀盐酸 碳酸钙粉末
C 稀盐酸 锌粒
D 硝酸银溶液 铜粉
A.A B.BC.CD.D
【解答】解:A、硫酸溶液中加入NaOH溶液发生中和反应,溶液总质量应该是随着NaOH的
加入而不断上升的,图象上不会有水平的那个阶段;不符合题意;
B、开始时,溶液总质量就是盐酸的质量,随着加入大理石,溶液质量是不断增加的,当大理
石和盐酸全部反应完时,溶液质量就不变了,因为盐酸已反应完,再加入大理石就不反应,且
大理石是固体,它的质量不属于溶液的质量,所以最后总溶液的质量的不变;不符合题意;
C、锌置换氢气,显然质量增加,当盐酸反应完后,锌是固体,所以开始溶液质量增加,至反应
完全后溶液总质量不再增加;不符合题意;
D、铜粉置换银,因为铜的相对原子质量是64,银的相对原子质量是108.所以开始反应时,溶
液总质量是降低的,至反应完全后溶液总质量不变;正确.
故选D.
8.如表是生活中常见4种饮料及主要成分,下列关于这些饮料的组成、性质和用途表述错误
的是( )
名称 主要成分
雪碧 碳水化合物、水
苏打水(弱碱性) 碳酸氢钠、水
盐汽水 氯化钠、水
柠檬汁 水、碳水化合物、蛋白质、纤维、维生素 等
A.雪碧是一种混合物
B.4种饮料中,苏打水的PH值最小
www.youyi100.com
第 10 页 共 14 页优秀领先 飞翔梦
想
C.从事高温作业的人员,适宜补充盐汽水
D.喝适量柠檬汁有助于补充人体的维生素
【解答】解:A.雪碧中含有水、碳水化合物等多种物质,属于混合物,故正确;
B.苏打水成弱碱性,其pH>7,是最大,故错误;
C.高温工作人员由于大量出汗,体内无机盐流失,可补充盐汽水调节人体内无机盐的平衡,
故正确;
D.柠檬汁含有维生素,喝适量的柠檬水可补充维生素,故正确.
故选B.
二、解答题(共4小题,满分20分)
9.如图为核聚变的示意图,其中①②③表示三种原子,“●”、“○”、“.”表示原子中的
不同微粒,③是 氦 元素的原子,①②③中属于同种元素的原子是 ①② (选填序号).
【解答】解:在原子中,电子在原子核的外部,所以小圈表示的是电子,在原子中,质子数=电
子数,所以白球表示质子,黑圈表示中子;再根据元素的种类是由质子数决定的可知,③这种
元素的原子核内有2个质子,所以是氦元素的原子;质子数决定元素的种类,由微观结构示
意图可知,①和②这两种粒子核内的质子数均为1,故属于同种元素.
故答案为:氦;①②.
10.若方法1中的X物质为常见气体,且发生置换反应,则X是 H (填化学式);
2
(2)写出方法2的化学方程式 CuO+H SO =CuSO +H O ;
2 4 4 2
(2)铜片A、铜片B、铜片C的质量分别为m 、m 、m ,其中方法1和方法2均完全反应,则
A B C
m 、m 、m 的大小关系为 m =m > m .
A B C A B C
www.youyi100.com
第 11 页 共 14 页优秀领先 飞翔梦
想
【解答】解:(1)常见的还原剂有碳单质、一氧化碳和氢气,X物质为常见气体,且发生置换反
应,所以X是氢气,化学式为:H ;
2
(2)氧化铜和硫酸反应生成硫酸铜和水,化学方程式为:CuO+H SO =CuSO +H O;
2 4 4 2
(3)方法1是将已经部分氧化的铜片重新用氢气还原,依据质量守恒中的原子守恒,方法1
反应结束后,铜被重新还原,所以m =m ,方法2中部分氧化的铜片产生了氧化铜,氧化铜与
A B
硫酸反应,有部分铜元素进入溶液中,剩余的铜单质的质量为m ,所以小于m 、m ,所以
C A B
m 、m 、m 的大小关系为m =m >m .
A B C A B C
故答案为:(1)H ;
2
(2)CuO+H SO =CuSO +H O;
2 4 4 2
(3)m =m >m .
A B C
11.小金为了探究温度对H O 分解反应速率的影响,借助如图所示实验装置(夹持装置略
2 2
去),进行了两次实验,两次实验的部分设计如表所示:
实验1 实验2
MnO 的质量/克 0.5 0.5
2
5%的H O 的体积/毫升 40 待填
2 2
水浴温度/℃ 20 80
(1)实验2中应加入5%H O 4 0 毫升;
2 2
(2)在两次实验中,可通过 相同的时间内注射器内气体的体积 来比较H O 分解反应速
2 2
率的大小;
(3)实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因除锥形瓶内
气体受热膨胀外,还有 温度较高时水蒸发成水蒸气 ;
(4)实验结束后若要将MnO 从混合物汇总分离出来,可采取的方法是 过滤、洗涤、干燥 .
2
www.youyi100.com
第 12 页 共 14 页优秀领先 飞翔梦
想
【解答】解:(1)利用对比试验探究温度对H O 分解反应速率的影响时,变量应是温度,其余
2 2
的量应相同,所以,实验2中应加入5%H O 40毫升;
2 2
(2)在两次实验中,可通过相同的时间内注射器内气体的体积 来比较H O 分解反应速率的
2 2
大小;
(3)实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因除锥形瓶内
气体受热膨胀外,还有温度较高时水蒸发成水蒸气;
(4)实验结束后若要将MnO 从混合物汇总分离出来,由于MnO 不溶于水,可采取的方法是
2 2
过滤、洗涤、干燥.
故答为:(1)40;(2)相同的时间内注射器内气体的体积小;(3)温度较高时水蒸发成水蒸气;
(4)过滤、洗涤、干燥.
12.焦亚硫酸钠(Na S O )是一种常用的食品抗氧化剂,小金模仿化工生产,用如图装置来制
2 2 5
取Na S O .
2 2 5
已知:A中发生的反应为:H SO (浓)+Na SO ═Na SO +SO ↑+H O
2 4 2 3 2 4 2 2
B中发生的反应为:Na SO +SO ═Na S O
2 3 2 2 2 5
(1)图中盛放浓硫酸的仪器名称是 分液漏斗 ;
(2)写出C中发生反应的化学方程式 SO +2NaOH═Na SO +H O ;
2 2 3 2
(3)在实验过程中,滴加浓硫酸不宜过快,理由是 防止生成二氧化硫气体过快,来不及与 B
中的亚硫酸钠进一步反应生成 N a S O .
2 2 5
(4)该实验开始滴加浓硫酸时,应先除尽装置内的空气,若忘记这一操作,新制取的Na S O
2 2 5
产品中会混有Na SO 杂质,这与O 的 氧化性 有关(填化学性质)
2 4 2
www.youyi100.com
第 13 页 共 14 页优秀领先 飞翔梦
想
【解答】解:(1)图中盛放浓硫酸的仪器的名称为分液漏斗;故填分液漏斗;
(2)反应过程中产生有害气体二氧化硫,需要进行尾气处理,二氧化硫与二氧化碳性质相似,
与氢氧化钠反应生成相应的盐和水;反应的化学方程式为:SO +2NaOH═Na SO +H O;故填:
2 2 3 2
SO +2NaOH═Na SO +H O
2 2 3 2
(3)若滴加浓硫酸过快,则生成二氧化硫气体较快,可能导致二氧化硫气体来不及与B中的
亚硫酸钠进一步反应生成Na S O ;故填:防止生成二氧化硫气体过快,来不及与B中的亚硫
2 2 5
酸钠进一步反应生成Na S O ;
2 2 5
(4)该实验开始滴加浓硫酸时,应先除尽装置内的空气,是为了防止Na S O 被氧化成
2 2 5
Na SO ,这里反映了氧气的氧化性;故填:氧化性.
2 4
www.youyi100.com
第 14 页 共 14 页