文档内容
第四章 生物大分子
第一节 糖类
学习导航 1.从糖类的官能团微观探析糖类的结构特点,了解糖类的分类,理解糖类的化学性质,掌握
糖类的特殊性。
2.了解糖类在人体供能、储能等方面的作用,也要了解糖类的摄入和代谢与人体健康之间的
关系,科学合理地搭配饮食。
教学过程 一、糖类的组成和分类
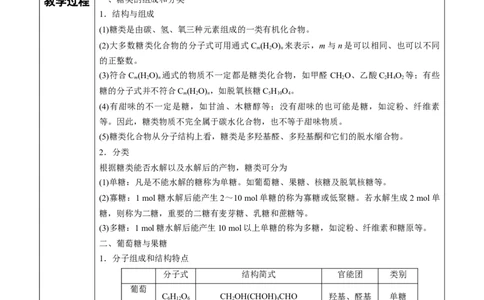
1.结构与组成
(1)糖类是由碳、氢、氧三种元素组成的一类有机化合物。
(2)大多数糖类化合物的分子式可用通式C (H O) 来表示,m与n是可以相同、也可以不同
m 2 n
的正整数。
(3)符合C (H O) 通式的物质不一定都是糖类化合物,如甲醛 CHO、乙酸C HO 等;有些
m 2 n 2 2 4 2
糖的分子式并不符合C (H O) ,如脱氧核糖C H O。
m 2 n 5 10 4
(4)有甜味的不一定是糖,如甘油、木糖醇等;没有甜味的也可能是糖,如淀粉、纤维素
等。因此,糖类物质不完全属于碳水化合物,也不等于甜味物质。
(5)糖类化合物从分子结构上看,糖类是多羟基醛、多羟基酮和它们的脱水缩合物。
2.分类
根据糖类能否水解以及水解后的产物,糖类可分为
(1)单糖:凡是不能水解的糖称为单糖。如葡萄糖、果糖、核糖及脱氧核糖等。
(2)寡糖:1 mol糖水解后能产生2~10 mol单糖的称为寡糖或低聚糖。若水解生成2 mol单
糖,则称为二糖,重要的二糖有麦芽糖、乳糖和蔗糖等。
(3)多糖:1 mol糖水解后能产生10 mol以上单糖的称为多糖,如淀粉、纤维素和糖原等。
二、葡萄糖与果糖
1.分子组成和结构特点
分子式 结构简式 官能团 类别
葡萄
C H O CHOH(CHOH) CHO 羟基、醛基 单糖
6 12 6 2 4
糖
羟基、酮羰
果糖 C H O 单糖
6 12 6
基
从组成和结构上看,葡萄糖和果糖互为同分异构体。
2.葡萄糖分子结构的探究
步骤 探究实验 推理 结论
1.80 g葡萄糖完全燃烧,得
① 0.01 mol葡萄糖中, 最简式为
2.64 g CO 和1.08 g H O
2 2n(C)=0.06 mol
n(H)=0.12 mol CHO
2
n(O)=0.06 mol
经质谱法测出葡萄糖的相 分子式为
② M[(CH O) ] =180,得n=6
r 2 n
对分子质量为180 C H O
6 12 6
n(葡萄糖)=0.01 mol,1 mol羟
一定条件下,1.80 g葡萄糖 基与乙酸发生酯化反应,生成 1 mol葡萄糖
③ 与乙酸完全酯化,生成相 酯的质量比原物质的质量增加 中有5 mol
应的酯3.90 g 42 g(即C HO),现增加2.10 羟基
2 2
g,即含有羟基0.05 mol
分子中含有
④ 葡萄糖可以发生银镜反应 —
醛基
葡萄糖可以被还原为直链 葡萄糖分子
⑤ —
己六醇 为直链结构
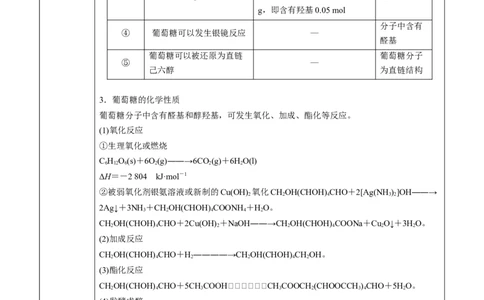
3.葡萄糖的化学性质
葡萄糖分子中含有醛基和醇羟基,可发生氧化、加成、酯化等反应。
(1)氧化反应
①生理氧化或燃烧
C H O(s)+6O(g)――→6CO(g)+6HO(l)
6 12 6 2 2 2
ΔH=-2 804 kJ·mol-1
②被弱氧化剂银氨溶液或新制的Cu(OH) 氧化CHOH(CHOH) CHO+2[Ag(NH)]OH――→
2 2 4 3 2
2Ag↓+3NH +CHOH(CHOH) COONH+HO。
3 2 4 4 2
CHOH(CHOH) CHO+2Cu(OH) +NaOH――→CHOH(CHOH) COONa+Cu O↓+3HO。
2 4 2 2 4 2 2
(2)加成反应
CHOH(CHOH) CHO+H――――→CHOH(CHOH) CHOH。
2 4 2 2 4 2
(3)酯化反应
CHOH(CHOH) CHO+5CHCOOHCHCOOCH (CHOOCCH )CHO+5HO。
2 4 3 3 2 3 4 2
(4)发酵成醇
――→2C HOH+2CO↑。
C6H12O6 2 5 2
三、二糖
1.蔗糖、麦芽糖的结构和化学性质的实验探究
实验步骤 实验现象 实验结论
蔗糖分子中无醛基,是非
试管内无明显现象 还原性糖;麦芽糖分子中
含有醛基,是还原性糖试管内产生砖红色
沉淀
加入银氨溶液的试
蔗糖的水解产物分子中含
管中都产生银镜;
有醛基,具有还原性;
加入新制的
麦芽糖的水解产物分子中
Cu(OH) 的试管中
2
① 含有醛基,具有还原性
都出现砖红色沉淀
②把蔗糖溶液换为麦芽糖溶
液,重复实验操作
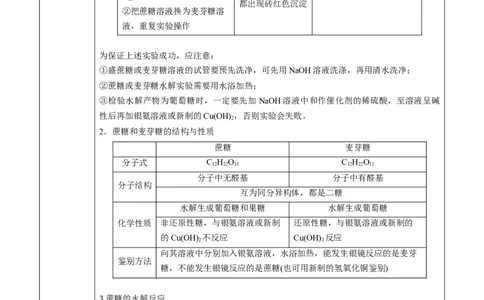
为保证上述实验成功,应注意:
①盛蔗糖或麦芽糖溶液的试管要预先洗净,可先用NaOH溶液洗涤,再用清水洗净;
②蔗糖或麦芽糖水解实验需要用水浴加热;
③检验水解产物为葡萄糖时,一定要先加NaOH溶液中和作催化剂的稀硫酸,至溶液呈碱
性后再加银氨溶液或新制的Cu(OH) ,否则实验会失败。
2
2.蔗糖和麦芽糖的结构与性质
蔗糖 麦芽糖
分子式 C H O C H O
12 22 11 12 22 11
分子中无醛基 分子中有醛基
分子结构
互为同分异构体,都是二糖
水解生成葡萄糖和果糖 水解生成葡萄糖
化学性质 非还原性糖,与银氨溶液或新制 还原性糖,与银氨溶液或新制的
的Cu(OH) 不反应 Cu(OH) 反应
2 2
向其溶液中分别加入银氨溶液,水浴加热,能发生银镜反应的是麦芽
鉴别方法
糖,不能发生银镜反应的是蔗糖(也可用新制的氢氧化铜鉴别)
3.蔗糖的水解反应
(1)蔗糖水解反应实验需用稀硫酸(1∶5)作催化剂,水浴加热。水解反应的化学方程式为
+HO――――→ + 。
C12H22O11 2 C6H12O6 C6H12O6
(2)水解产物中葡萄糖的检验:欲要检验水解产物中的葡萄糖,必须先加入 NaOH溶液中和
多余的硫酸,再加入银氨溶液或新制的Cu(OH) 进行检验。
2
四、淀粉和纤维素
1.糖类还原性的检验
糖类的还原性是指糖类能发生银镜反应或与新制的Cu(OH) 反应,若糖不能发生银镜反应或
2
不与新制的Cu(OH) 反应,则该糖不具有还原性,为非还原性糖。
22.淀粉水解程度的判断
(1)实验原理
判断淀粉水解的程度时,要注意检验产物中是否生成葡萄糖,同时还要确认淀粉是否水解
完全。用银氨溶液或新制的Cu(OH) 和碘水来检验淀粉是否发生了水解及水解是否完全。
2
(2)实验步骤
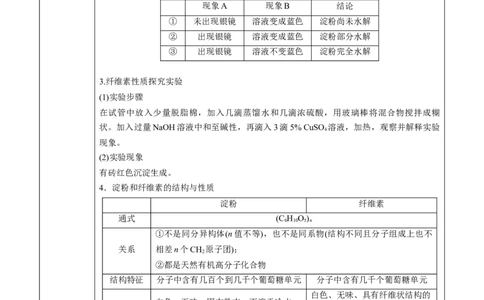
(3)实验现象和结论
现象A 现象B 结论
① 未出现银镜 溶液变成蓝色 淀粉尚未水解
② 出现银镜 溶液变成蓝色 淀粉部分水解
③ 出现银镜 溶液不变蓝色 淀粉完全水解
3.纤维素性质探究实验
(1)实验步骤
在试管中放入少量脱脂棉,加入几滴蒸馏水和几滴浓硫酸,用玻璃棒将混合物搅拌成糊
状。加入过量NaOH溶液中和至碱性,再滴入3滴5% CuSO 溶液,加热,观察并解释实验
4
现象。
(2)实验现象
有砖红色沉淀生成。
4.淀粉和纤维素的结构与性质
淀粉 纤维素
通式 (C H O)
6 10 5 n
①不是同分异构体(n值不等),也不是同系物(结构不同且分子组成上也不
关系 相差n个CH 原子团);
2
②都是天然有机高分子化合物
结构特征 分子中含有几百个到几千个葡萄糖单元 分子中含有几千个葡萄糖单元
白色、无味、具有纤维状结构的
白色、无味、固态粉末,不溶于冷水,
物理性质 固体,不溶于水,也不溶于一般
在热水中发生糊化作用
的有机溶剂
①无还原性 ①无还原性
化学性质 ②能水解生成葡萄糖 ②能水解生成葡萄糖(难)
③遇碘单质变蓝 ③能发生酯化反应
存在 植物光合作用的产物 构成细胞壁的基础物质
纺织、造纸、制纤维素硝酸酯、
用途 制葡萄糖和酒精,人体的能源之一
纤维素乙酸酯等课时训练
1.化学与生活密切相关。下列说法错误的是
A.非处方药的包装上印有“OTC”标示
B.减少使用氟氯代烷作制冷剂,能保护臭氧层
C.在酒化酶的作用下葡萄糖水解为乙醇和二氧化碳
D.维生素 C具有还原性,在人体内起抗氧化作用
2.化学学习的价值之一是以化学的视角去看待生产、生活中的问题。下列说法错误的是
A.煤的气化和液化均属于物理变化
B.工业上冶炼金属的过程涉及氧化还原反应
C.植物油转化为脂肪的过程发生了加成反应
D.医疗中血糖的检测过程利用了醛基的性质
3.下列关于有机物的叙述正确的是
A.C H 有三种同分异构体
4 10
B.乙醇不能发生取代反应
C.乙烯和甲烷可用溴的四氯化碳溶液鉴别
D.糖类、油脂、蛋白质均属于高分子化合物
4.下列说法正确的是
A.化合物2-苯基丙烯( )易溶于水及甲苯
B.纤维素的水解产物为葡萄糖,葡萄糖在酒化酶作用下再进一步水解可得酒精
C.硫酸作催化剂, 水解所得乙醇分子中有
D.粗苯甲酸经过加热溶解、趁热过滤、蒸发结晶,可获得纯苯甲酸
5.下列实验的失败原因可能是因为缺少必要的实验步骤造成的有几项
①将乙醇和乙酸混合,再加入稀硫酸共热制乙酸乙酯
②实验室用无水乙醇和浓硫酸共热到140℃制乙烯
③验证某RX是碘代烷,把RX与烧碱水溶液混合加热后,将溶液冷却后再加入硝酸银溶液出现褐色沉淀
④做醛的还原性实验时,当加入新制的氢氧化铜悬浊液后,未出现红色沉淀
⑤检验淀粉已经水解,将淀粉与少量稀硫酸加热一段时间后,加入银氨溶液后未析出银镜
A.2 B.3 C.4 D.5
6.下列有关实验说法不正确的是
A.检验牙膏中是否含有甘油可选用新制的氢氧化铜悬浊液,若含有甘油,则溶液呈绛蓝色
B.探究温度对反应速率的影响时,应先将硫代硫酸钠溶液、硫酸溶液混合,然后将混合液在水浴中加热
C.分离乙醇和溴乙烷的混合物可用萃取法,分离氨基酸混合液可采用控制pH法
D.往含硫酸的淀粉水解液中加入银氨溶液,水浴加热后无银镜,不能说明淀粉未水解
7.下列实验操作合理的是A.制氯气时,可以用饱和NaHCO 溶液和浓硫酸净化气体
3
B.检验溶液中是否含有Fe3+:取少量待检验溶液,向其中加入少量新制氯水,再滴加KSCN溶液,观察
实验现象
C.除去乙烷中的乙烯,可以选择在Ni催化、加热条件下通入H
2
D.鉴定蔗糖水解产物中有无葡萄糖:在水解液中加入碱液中和酸后,再加入新制的Cu(OH) 悬浊液,加
2
热并观察实验现象
8.下列关于蔗糖的说法中,不正确的是
A.在蔗糖中加入浓硫酸,可观察到颜色变黑,并有泡沫生成
B.纯净的蔗糖配成的溶液中加入银氨溶液,微热,不发生银镜反应
C.在蔗糖与稀硫酸共热后的溶液中,滴加银氨溶液,再水浴加热,看不到有银镜
D.蔗糖是最重要的二糖,它的式量是葡萄糖的二倍
9.为了检验淀粉水解的产物,设计如图实验方案:
请回答下列问题:
(1)淀粉水解的化学方程式为___。
(2)试剂1为稀硫酸(1:5),作用是___;水浴加热的优点是___。
(3)试剂2为___,发生的离子反应方程式为___。
(4)为检验淀粉是否已完全水解,取少量水解液于试管中,加入碘水,则证明淀粉未完全水解的现象是
___。
(5)用2%AgNO 溶液和2%氨水溶液配制银氨溶液的操作是___。
3
10.以淀粉为主要原料合成一种有机酸B的合成路线如下图所示。
(1)检验反应①是否进行完毕,可使用的试剂是___________(填序号)。
A.FeCl 溶液 B.碘水
3
C.新制的Cu(OH) 悬浊液 D.NaOH溶液
2
(2)葡萄糖的化学式为___________,反应⑤的反应类型为___________。
(3)反应②和③的化学方程式依次为___________、___________。
(4)X中溶剂为CCl ,则反应④的现象为___________。
4
(5)已知B的相对分子质量为118,其中碳、氢两种元素的质量分数分别为40.68%、5.08%,其余为氧元
素,则B的分子式为___________。
答案解析
1.C
【详解】A.药品包装上“R”代表处方药,“OTC”代表非处方药,A正确;
B.氟氯代烷能催化O 分解成O,从而造成臭氧层空洞,故减少氟氯代烷使用能保护臭氧层,B正确;
3 2
C.葡萄糖属于单糖,不能水解,其转化为乙醇和CO,属于氧化还原反应,C错误;
2
D.维生素C具有还原性,在人体内能起到抗氧化、延缓衰老、抑制黑色素形成等作用,D正确;
故答案选C。
2.A
【详解】
A.煤的气化、液化指将煤转化为气体、液体燃料,属于化学变化,A错误;
B.金属冶炼指将化合物中金属元素还原为金属单质,涉及氧化还原反应,B正确;
C.液态植物油转化为固态或半固态脂肪属于油脂的硬化,实质是植物油烃基部分的不饱和键(如碳碳双
键)与H 的加成反应,C正确;
2
D.血糖指血液中葡萄糖,医疗中利用葡萄糖中醛基与试纸中的葡萄糖氧化酶反应产生的电流测量血糖浓
度,D正确;
故答案选A。
3.C
【详解】
A.C H 有两种同分异构体:CHCHCHCH、(CH)CHCH ,A错误;
4 10 3 2 2 3 3 2 3
B.乙醇能与HBr、CHCOOH等发生取代反应,B错误;
3
C.乙烯中含碳碳双键,能与Br 发生加成反应,使溴的四氯化碳溶液褪色,甲烷不能使溴的四氯化碳溶液
2
褪色,故用溴的四氯化碳溶液可鉴别乙烯和甲烷,C正确;
D.糖类中的单糖和二糖、油脂都不属于高分子化合物,糖类中的多糖、蛋白质属于高分子化合物,D错
误;
答案选C。
4.C
【详解】
A. 烃基是憎水基团,化合物2-苯基丙烯( )难溶于水、易溶于甲苯,A错误;
B. 纤维素的水解的最终产物为葡萄糖,葡萄糖在酒化酶作用下再进一步发酵可得酒精,B错误;
C. 酯化反应是可逆反应,酯化反应时“酸脱羟基醇去氢”,其逆反应是酯的水解,酯在硫酸作催化剂下
发生水解,则 水解所得乙醇分子中有 ,C正确;
D.苯甲酸的溶解度不大,趁热过滤可防止损失,然后冷却结晶、过滤、洗涤、干燥可提纯,故D错误。
答案选C。
5.B
【详解】
①将乙醇和乙酸混合,再加入浓硫酸共热制乙酸乙酯,加错试剂,故不选①;
②实验室用无水乙醇和浓硫酸共热到170℃制乙烯,控制反应条件错误,故不选②;
③验证某RX是碘代烷,把RX与烧碱水溶液混合加热后,发生水解反应,检验卤素离子在酸性条件下,
缺少加硝酸的步骤,故选③;④做醛的还原性实验时,在碱性条件下,缺少加碱的步骤,加入新制的氢氧化铜悬浊液后,未出现红色沉
淀,故选④;
⑤淀粉在酸性溶液中水解,检验葡萄糖应在碱性条件下,缺少加碱的步骤,加入银氨溶液后未析出银镜,
故选⑤;
选B。
6.B
【详解】
A.甘油与氢氧化铜悬浊液反应,溶液为绛蓝色,若含有甘油,则溶液呈绛蓝色,故A正确;
B.应改变温度,保证其它量相同,均在水浴中不能比较温度对速率的影响,故B错误;
C.乙醇和水互溶,溴乙烷难溶于水,分离乙醇和溴乙烷的混合物可用水进行萃取,不同氨基酸的pH不
同,分离氨基酸混合液可采用控制pH法据此分离,故C正确;
D.银镜反应需要在碱性溶液中进行,所以往含硫酸的淀粉水解液中加入银氨溶液,水浴加热后无银镜,
不能说明淀粉未水解,故D正确;
故选B。
7.D
【详解】
A.氯气溶于水生成HCl和HClO,HCl和NaHCO 反应,故不能用饱和NaHCO 溶液净化氯气,A项错
3 3
误;
B.若溶于中含有Fe2+,加入新制氯水,Fe2+被氧化为Fe3+,再滴加KSCN溶液,溶液变红,不能证明溶液
中含有Fe3+,B项错误;
C.在Ni催化、加热条件下通入H,H 与乙烯反应生成乙烷,但H 的用量不易控制,容易引入新杂质,C
2 2 2
项错误;
D.蔗糖水解用稀硫酸作催化剂,水解后液体呈酸性,加入碱液中和酸,时水解液呈碱性后,加入新制的
Cu(OH) 悬浊液并加热,出现砖红色则证明水解产物中含有葡萄糖,D项正确;
2
答案选D。
8.D
【详解】
A.浓硫酸具有脱水性和强氧化性,在蔗糖中加入浓硫酸,蔗糖脱水碳化,可观察到颜色变黑,碳接着被
浓硫酸氧化为二氧化碳,所以有泡沫生成,A正确;
B.蔗糖分子中没有醛基,纯净的蔗糖配成的溶液中加入银氨溶液,微热,不发生银镜反应,B正确;
C.在蔗糖与稀硫酸共热后的溶液中,如果不加入氢氧化钠中和硫酸,直接滴加银氨溶液,再水浴加热,
看不到有银镜,C正确;
D.蔗糖是最重要的二糖,其相对分子质量为342,葡萄糖的相对分子质量是180,D不正确。
9.(C H O)(淀粉)+nH O nC H O(葡萄糖) 做催化剂 受热均匀便于控制温度 NaOH溶
6 10 5 n 2 6 12 6
液 H++OH-=H O 溶液显蓝色 在一支洁净的试管中,加入2%AgNO 溶液,边振荡边滴加2%氨
2 3
水,直至最初产生的沉淀恰好消失,便得到银氨溶液
【详解】
(1) 淀粉的水解生成葡萄糖,化学方程式为(C H O)(淀粉)+nH O nC H O(葡萄糖),故答案为:
6 10 5 n 2 6 12 6
(C H O)(淀粉)+nH O nC H O(葡萄糖);
6 10 5 n 2 6 12 6(2) 稀硫酸在淀粉的水解过程中作催化剂,加快了淀粉的水解速率,水浴加热受热均匀便于控制温度,故
答案为:做催化剂;受热均匀便于控制温度;
(3) 水解液中加入少量NaOH溶液中和硫酸,试剂2为NaOH溶液,反应离子方程式为H++OH-=H O,故答
2
案为:NaOH溶液;H++OH-=H O;
2
(4)如果加入淀粉后显示蓝色,则证明淀粉没有完全水解,故答案为:溶液显蓝色;
(5) 配制银氨溶液要注意加入试剂的顺序,操作是:在一支洁净的试管中,加入2%AgNO 溶液,边振荡边
3
滴加2%氨水,直至最初产生的沉淀恰好消失,便得到银氨溶液。故答案为:在一支洁净的试管中,加入
2%AgNO 溶液,边振荡边滴加2%氨水,直至最初产生的沉淀恰好消失,便得到银氨溶液。
3
10.B C H O 取代反应 2C HOH+O 2CHCHO+2H O C HOH
6 12 6 2 5 2 3 2 2 5
CH=CH ↑+H O 溴的四氯化碳溶液变浅或褪色 C HO
2 2 2 4 6 4
【详解】
(1)检验反应①是否进行完毕,需要检验淀粉是否存在,所以可使用的试剂是碘水,故选B。答案为:B;
(2)葡萄糖由淀粉(C H O) 水解生成,所以葡萄糖的化学式为C H O,反应⑤为BrCHCHBr与NaCN发
6 10 5 n 6 12 6 2 2
生反应生成NCCH CHCN和NaBr,所以反应类型为取代反应。答案为:C H O;取代反应;
2 2 6 12 6
(3)反应②为乙醇催化氧化可制得乙醛,反应③为乙醇在浓硫酸、170℃的条件下发生消去反应生成乙烯和
水,化学方程式依次为2C HOH+O 2CHCHO+2H O、C HOH CH=CH ↑+H O。
2 5 2 3 2 2 5 2 2 2
答案为:2C HOH+O 2CHCHO+2H O;C HOH CH=CH ↑+H O;
2 5 2 3 2 2 5 2 2 2
(4)X中溶剂为CCl ,发生的是CH=CH 与Br 的加成反应,生成物BrCHCHBr呈无色,则反应④的现象
4 2 2 2 2 2
为溴的四氯化碳溶液变浅或褪色。答案为:溴的四氯化碳溶液变浅或褪色;
(5)1mol有机物B中,含碳原子的物质的量为 mol≈4mol,含氢原子的物质的量为
mol≈6mol,含氧原子的物质的量为 mol≈4mol,从而得出B的分子式为
C HO。答案为:C HO。
4 6 4 4 6 4