文档内容
第三章 烃的衍生物
第五节 有机合成
第 1 课时 有机合成的主要任务
学习导航 1.通过碳骨架的构建、官能团的转化,体会有机合成基本任务,掌握有机化合物分子骨架的
构建,官能团引入、转化或消除的方法。
2.体会有机合成在发展经济、提高生活质量方面的贡献及对健康、环境造成的影响,能用
“绿色化学”的理念指导合成路线的选择。
教学过程 一、有机合成
1.有机合成的概念
有机合成指利用相对简单、易得的原料,通过有机化学反应来构建碳骨架和引入官能团,
由此合成出具有特定结构和性质的目标分子的过程方法。
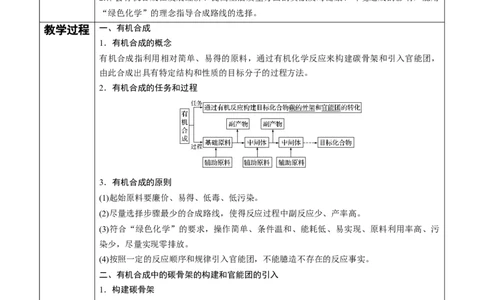
2.有机合成的任务和过程
3.有机合成的原则
(1)起始原料要廉价、易得、低毒、低污染。
(2)尽量选择步骤最少的合成路线,使得反应过程中副反应少、产率高。
(3)符合“绿色化学”的要求,操作简单、条件温和、能耗低、易实现、原料利用率高、污
染少,尽量实现零排放。
(4)按照一定的反应顺序和规律引入官能团,不能臆造不存在的反应事实。
二、有机合成中的碳骨架的构建和官能团的引入
1.构建碳骨架
(1)增长碳链
①卤代烃与NaCN的反应
CHCHCl+NaCN―→CHCHCN(丙腈)+NaCl;
3 2 3 2
CHCHCN―――→CHCHCOOH。
3 2 3 2
②醛、酮与氢氰酸的加成反应
CHCHO+HCN―→ ;
3―――→ 。
③卤代烃与炔钠的反应
2CHC≡CH+2Na――→2CHC≡CNa+H;
3 3 2
CHC≡CNa+CHCHCl―→CHC≡CCH CH+NaCl。
3 3 2 3 2 3
④羟醛缩合反应
CHCHO+ ――→ 。
3
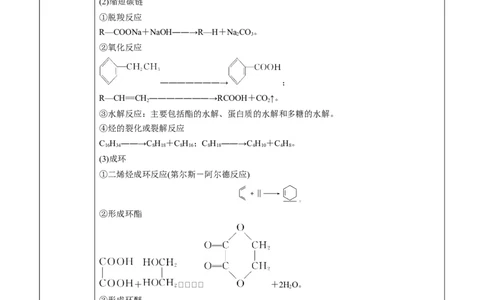
(2)缩短碳链
①脱羧反应
R—COONa+NaOH――→R—H+NaCO。
2 3
②氧化反应
―――――――→ ;
R—CH==CH ―――――――→RCOOH+CO↑。
2 2
③水解反应:主要包括酯的水解、蛋白质的水解和多糖的水解。
④烃的裂化或裂解反应
C H ――→C H +C H ;C H ――→C H +C H。
16 34 8 18 8 16 8 18 4 10 4 8
(3)成环
①二烯烃成环反应(第尔斯-阿尔德反应)
②形成环酯
+ +2HO。
2
③形成环醚
(4)开环
①环酯水解开环
②环烯烃氧化开环2.常见官能团引入或转化的方法
(1)碳碳双键
①醇的消去反应
CHCHOH―――→CH==CH ↑+HO。
3 2 2 2 2
②卤代烃的消去反应
CH—CH—Br+NaOH――→CH==CH↑+NaBr+HO。
3 2 2 2 2
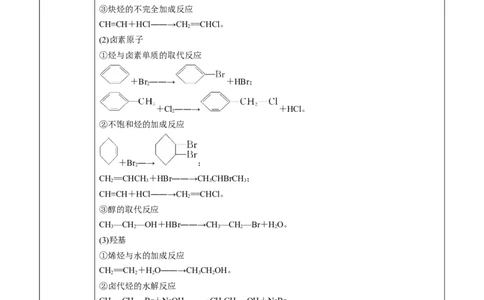
③炔烃的不完全加成反应
CH≡CH+HCl――→CH==CHCl。
2
(2)卤素原子
①烃与卤素单质的取代反应
+Br ――→ +HBr;
2
+Cl――→ +HCl。
2
②不饱和烃的加成反应
+Br ―→ ;
2
CH==CHCH +HBr――→CHCHBrCH ;
2 3 3 3
CH≡CH+HCl――→CH==CHCl。
2
③醇的取代反应
CH—CH—OH+HBr――→CH—CH—Br+HO。
3 2 3 2 2
(3)羟基
①烯烃与水的加成反应
CH==CH +HO――→CHCHOH。
2 2 2 3 2
②卤代烃的水解反应
CH—CH—Br+NaOH――→CHCH—OH+NaBr。
3 2 3 2
③醛或酮的还原反应
CHCHO+H――→CHCHOH;
3 2 3 2
+H――→ 。
2
④酯的水解反应
CHCOOCH CH+HOCHCOOH+CHCHOH;
3 2 3 2 3 3 2
CHCOOCH CH+NaOH――→CHCOONa+CHCHOH。
3 2 3 3 3 2(4)官能团的转化
熟悉烃及其衍生物之间的相互转化是有机合成的基础。
课时训练
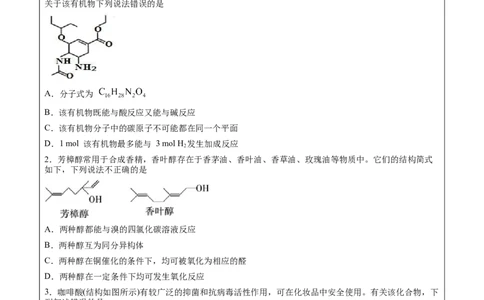
1.磷酸奥司他韦是临床常用的抗病毒药物,常用于甲型和乙型流感治疗。其中间体结构简式如图所示,
关于该有机物下列说法错误的是
A.分子式为
B.该有机物既能与酸反应又能与碱反应
C.该有机物分子中的碳原子不可能都在同一个平面
D.1 mol 该有机物最多能与 3 mol H 发生加成反应
2
2.芳樟醇常用于合成香精,香叶醇存在于香茅油、香叶油、香草油、玫瑰油等物质中。它们的结构简式
如下,下列说法不正确的是
A.两种醇都能与溴的四氯化碳溶液反应
B.两种醇互为同分异构体
C.两种醇在铜催化的条件下,均可被氧化为相应的醛
D.两种醇在一定条件下均可发生氧化反应
3.咖啡酸(结构如图所示)有较广泛的抑菌和抗病毒活性作用,可在化妆品中安全使用。有关该化合物,下
列叙述错误的是
A.分子式为C HO
9 8 4
B.能与NaOH、NaHCO 反应
3
C.能够发生酯化反应
D.所有原子不可能共平面
4.每逢春节,一种“本宝宝福禄双全”的有机物就会刷爆朋友圈,其结构简式如图。有关该物质的说法不正确的是
A.该有机物的分子式:C HOClF
8 4 2
B.一定条件下,1mol该物质最多消耗5molH
2
C.该分子最多有12个原子共面
D.具有相同官能团且2个醛基在邻位的同分异构体还有5种
5.某有机物的结构简式如图所示,下列说法中不正确的是
A.1 mol 该有机物和过量的金属钠反应最多可以生成1.5 mo1 H
2
B.1 mol 该有机物分别与Na、NaOH、 NaHCO 反应,依次消耗这三种物质量之比为3:2:2
3
C.可以用酸性KMnO 溶液检验其中的碳碳双键
4
D.在一定条件下,该有机物能发生取代加成酯化和加聚反应
6.1mol某烃在氧气中充分燃烧,需要消耗氧气179.2L(标准状况下)。它在光照的条件下与氯气反应能生
成3种不同的一氯取代物。该烃的结构简式是( )
A. B.CHCHCHCHCH
3 2 2 2 3
C. D.
7.冠醚分子中有空穴,能够与金属离子形成稳定的络合物,该物质在有机工业中发挥着重要的作用。二
环己烷并-18-冠-6(III)的制备原理如图,下列相关说法错误的是
A.I、II、Ⅲ三种有机物中都是含有醚键
B.有机物II在NaOH溶液中水解可得到有机物I
C.上述制备有机物Ⅲ的反应属于取代反应
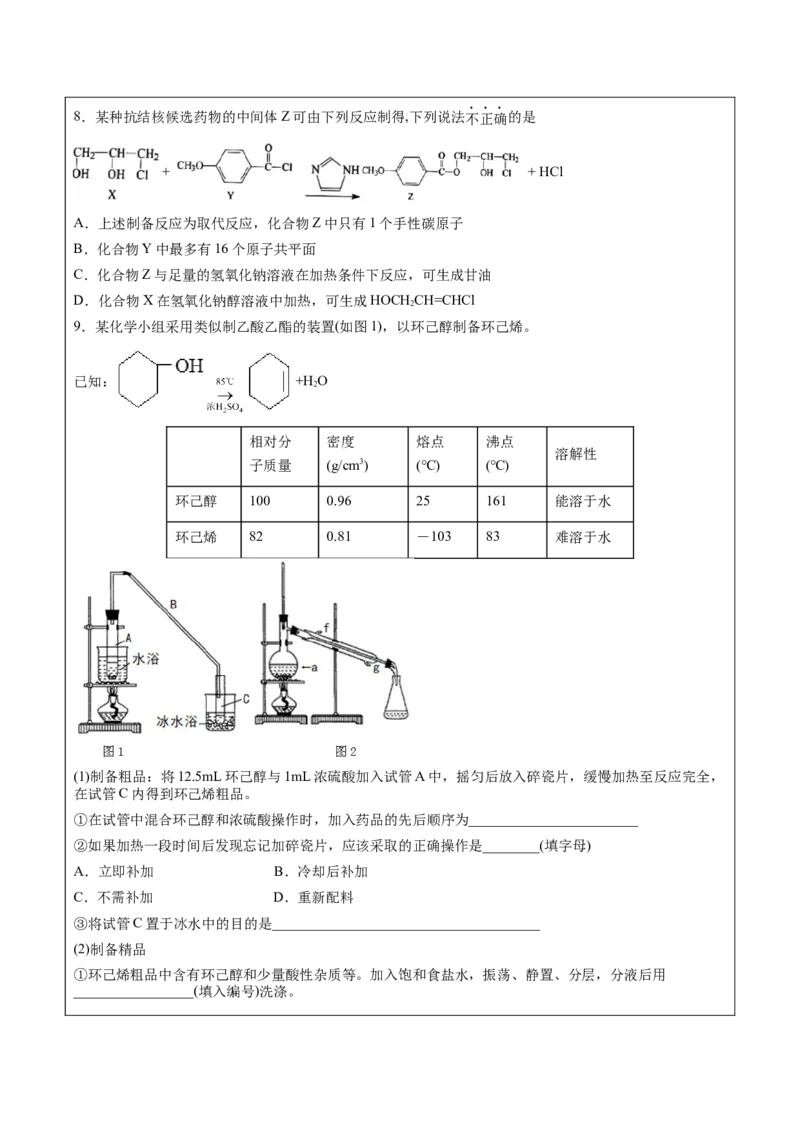
D.有机物Ⅲ的一溴取代物有4种8.某种抗结核候选药物的中间体Z可由下列反应制得,下列说法不正确的是
+ + HCl
A.上述制备反应为取代反应,化合物Z中只有1个手性碳原子
B.化合物Y中最多有16个原子共平面
C.化合物Z与足量的氢氧化钠溶液在加热条件下反应,可生成甘油
D.化合物X在氢氧化钠醇溶液中加热,可生成HOCH CH=CHCl
2
9.某化学小组采用类似制乙酸乙酯的装置(如图1),以环己醇制备环己烯。
已知: +H O
2
相对分 密度 熔点 沸点
溶解性
子质量 (g/cm3) (℃) (℃)
环己醇 100 0.96 25 161 能溶于水
环己烯 82 0.81 -103 83 难溶于水
(1)制备粗品:将12.5mL环己醇与1mL浓硫酸加入试管A中,摇匀后放入碎瓷片,缓慢加热至反应完全,
在试管C内得到环己烯粗品。
①在试管中混合环己醇和浓硫酸操作时,加入药品的先后顺序为________________________
②如果加热一段时间后发现忘记加碎瓷片,应该采取的正确操作是________(填字母)
A.立即补加 B.冷却后补加
C.不需补加 D.重新配料
③将试管C置于冰水中的目的是______________________________________
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,分液后用
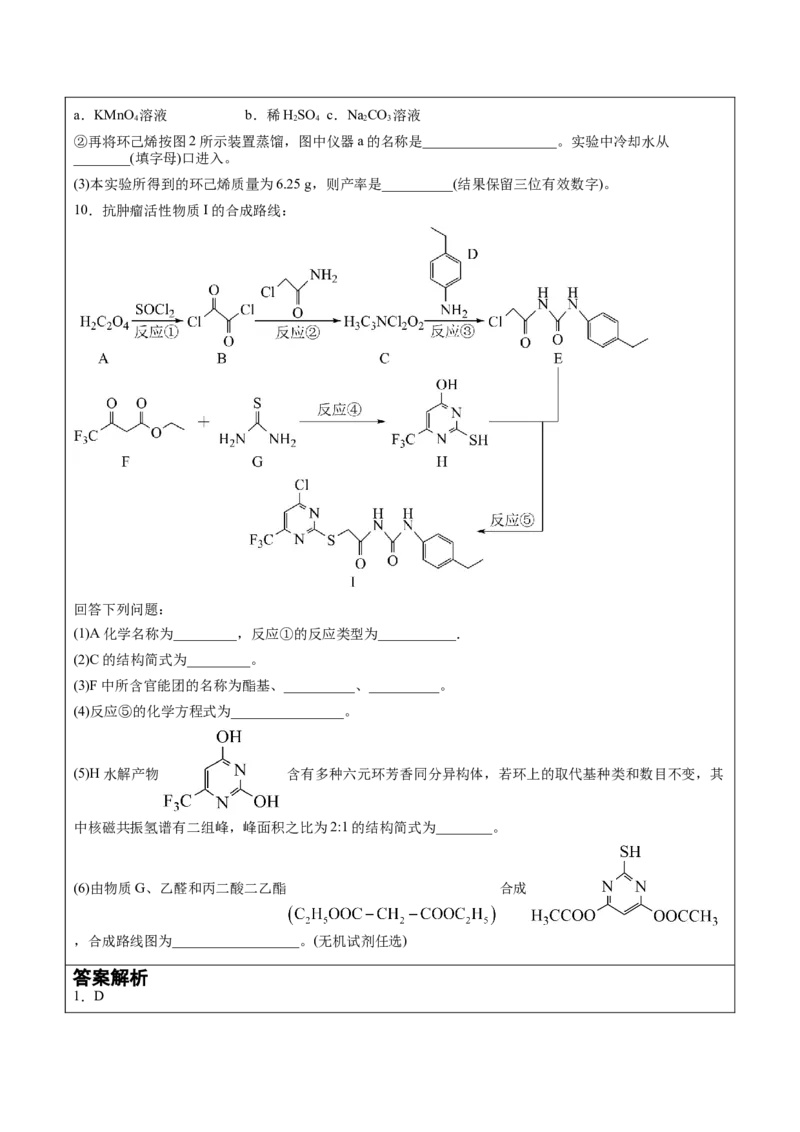
_________________(填入编号)洗涤。a.KMnO 溶液 b.稀HSO c.NaCO 溶液
4 2 4 2 3
②再将环己烯按图2所示装置蒸馏,图中仪器a的名称是___________________。实验中冷却水从
________(填字母)口进入。
(3)本实验所得到的环己烯质量为6.25 g,则产率是__________(结果保留三位有效数字)。
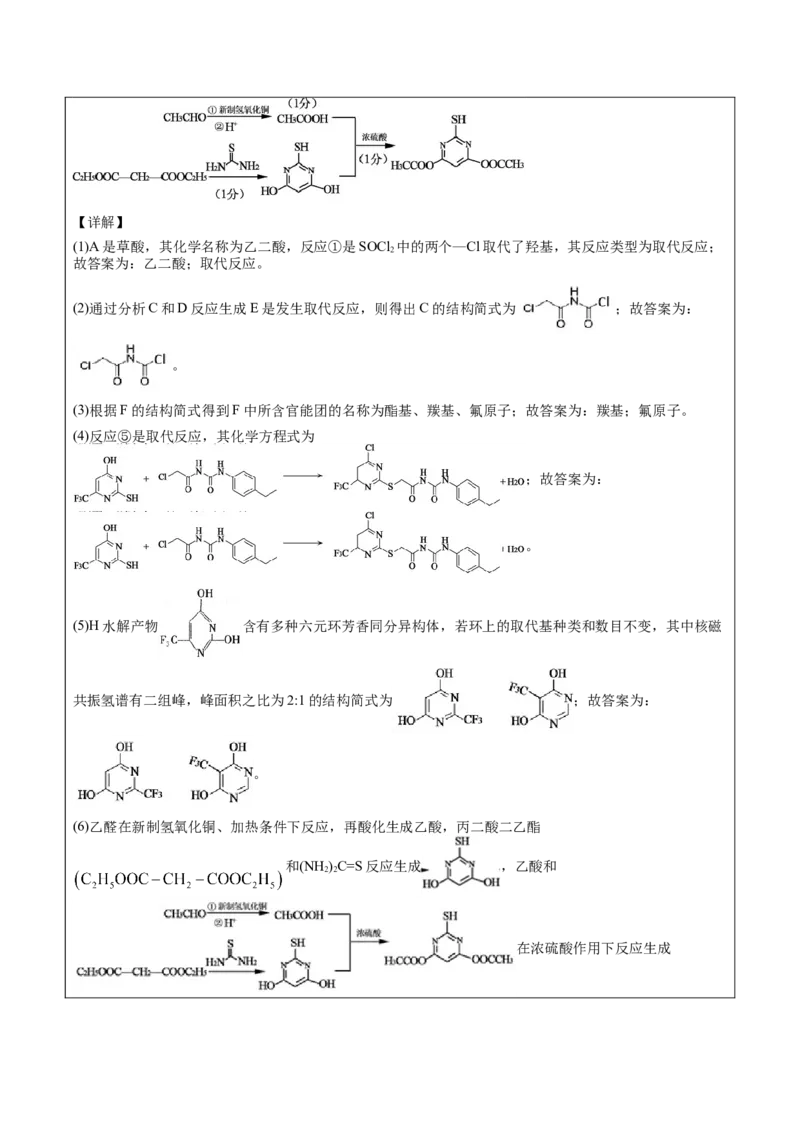
10.抗肿瘤活性物质I的合成路线:
回答下列问题:
(1)A化学名称为_________,反应①的反应类型为___________.
(2)C的结构简式为_________。
(3)F中所含官能团的名称为酯基、__________、__________。
(4)反应⑤的化学方程式为________________。
(5)H水解产物 含有多种六元环芳香同分异构体,若环上的取代基种类和数目不变,其
中核磁共振氢谱有二组峰,峰面积之比为2:1的结构简式为________。
(6)由物质G、乙醛和丙二酸二乙酯 合成
,合成路线图为__________________。(无机试剂任选)
答案解析
1.D【详解】
A.由结构简式可知,有机物为分子式为C H NO,故A正确;
16 28 2 4
B.含有酯基,可在酸性或碱性条件下水解,故B正确;
C.该结构中含有烷基结构,所以该有机物分子中的碳原子不可能都在同一个平面,故C正确;
D.能与氢气反应的为碳碳双键,则1 mol该有机物最多能与1 mol H 发生加成反应,故D错误;
2
故选D。
2.C
【详解】
A.芳樟醇、香叶醇分子中均含碳碳双键,均能与溴的四氯化碳溶液中的溴发生加成反应,A正确;
B.芳樟醇、香叶醇的分子式均为C H O,结构不同,互为同分异构体,B正确;
10 18
C.芳樟醇分子中与-OH相连的C上没有H,不能被催化氧化,C错误;
D.两种醇在一定条件下均可发生氧化反应,如燃烧、碳碳双键被强氧化剂氧化,D正确;
答案选C。
3.D
【详解】
A.根据结构简式可知,1个咖啡酸分子中含9个碳原子,不饱和度为6,所以分子式为C HO,A正确;
9 8 4
B.分子中含羧基,可与NaOH、NaHCO 发生反应,B正确;
3
C.分子中含(酚)羟基和羧基,能够发生酯化反应,C正确;
D.因为苯环的12个原子共平面,乙烯的6个原子共平面,单键可旋转,组成羧基的原子也可能共平面,
即咖啡酸分子中所有原子可能共平面,D错误;
故选D。
4.C
【详解】
A.根据有机物的结构简式可知该有机物的分子式为C HOClF,A正确;
8 4 2
B.苯环、醛基均能和氢气发生加成反应,1mol苯环消耗3mol氢气,1mol醛基消耗1mol氢气,则1mol
该物质最多消耗5mol H,B正确;
2
C.根据苯、甲醛平面模型可知,该分子最多有16个原子共面,C错误;
D.如图 ,满足条件的还有5种,分别为F在1号C上有3种,F在2号上有2种,共5种,
D正确;
答案选C。
5.C
【详解】
A.-COOH、-OH均与Na反应生成氢气,则1mol该有机物和过量的金属钠反应最多可以生成1.5 molH ,
2
故A正确;
B.-COOH、-OH均与Na反应,只有-COOH与NaOH、NaHCO 反应,该有机物消耗Na、NaOH、
3
NaHCO 的物质的量之比为3:2:2,故B正确;
3
C.-OH、碳碳双键均能被高锰酸钾氧化,则用酸性KMnO 溶液不能检验其中的碳碳双键,故C错误;
4D.含有羧基、羟基,可发生取代、酯化反应,含有碳碳双键,可发生加成、加聚反应,故D正确。
故选:C。
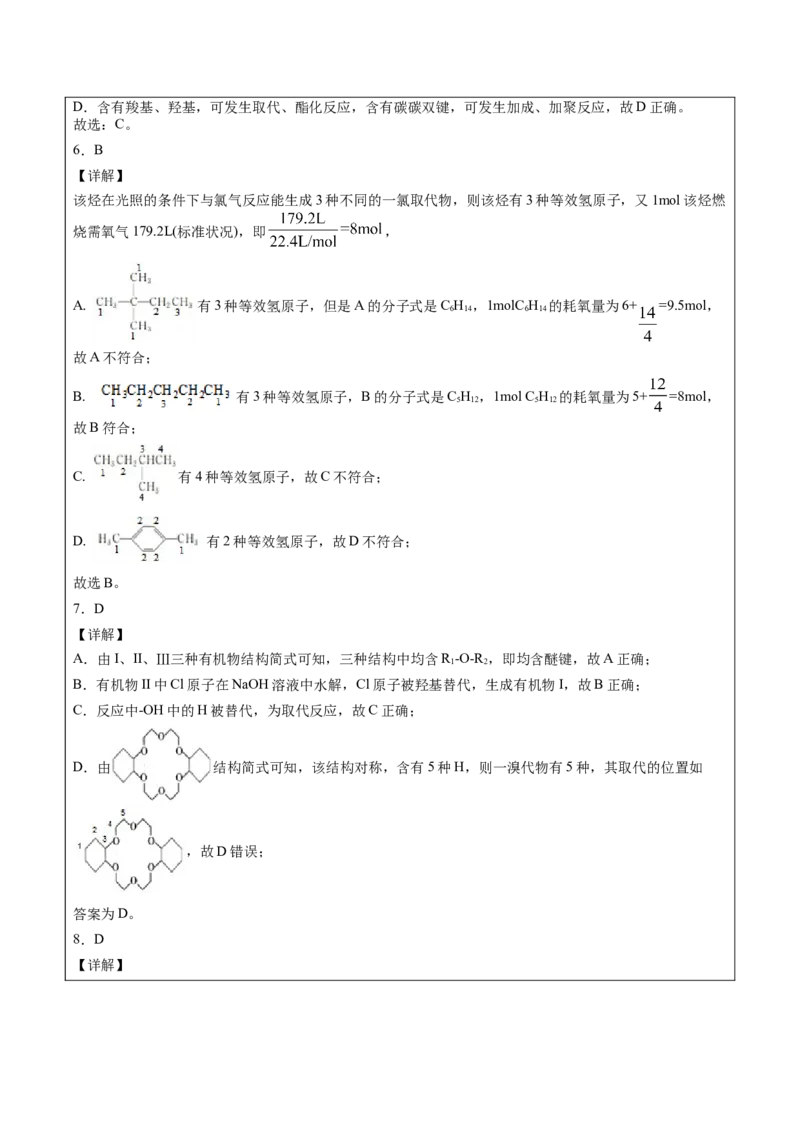
6.B
【详解】
该烃在光照的条件下与氯气反应能生成3种不同的一氯取代物,则该烃有3种等效氢原子,又1mol该烃燃
烧需氧气179.2L(标准状况),即 ,
A. 有3种等效氢原子,但是A的分子式是C H ,1molC H 的耗氧量为6+ =9.5mol,
6 14 6 14
故A不符合;
B. 有3种等效氢原子,B的分子式是C H ,1mol C H 的耗氧量为5+ =8mol,
5 12 5 12
故B符合;
C. 有4种等效氢原子,故C不符合;
D. 有2种等效氢原子,故D不符合;
故选B。
7.D
【详解】
A.由I、II、Ⅲ三种有机物结构简式可知,三种结构中均含R -O-R ,即均含醚键,故A正确;
1 2
B.有机物II中Cl原子在NaOH溶液中水解,Cl原子被羟基替代,生成有机物I,故B正确;
C.反应中-OH中的H被替代,为取代反应,故C正确;
D.由 结构简式可知,该结构对称,含有5种H,则一溴代物有5种,其取代的位置如
,故D错误;
答案为D。
8.D
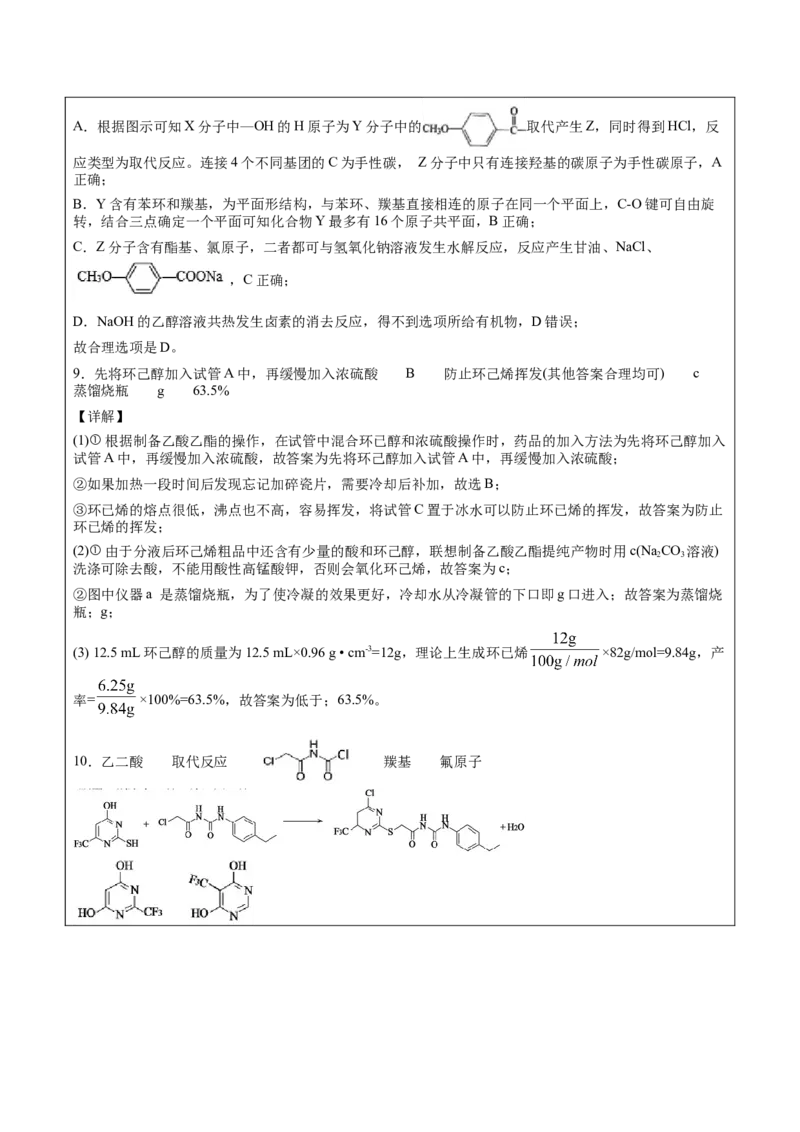
【详解】A.根据图示可知X分子中—OH的H原子为Y分子中的 取代产生Z,同时得到HCl,反
应类型为取代反应。连接4个不同基团的C为手性碳, Z分子中只有连接羟基的碳原子为手性碳原子,A
正确;
B.Y含有苯环和羰基,为平面形结构,与苯环、羰基直接相连的原子在同一个平面上,C-O键可自由旋
转,结合三点确定一个平面可知化合物Y最多有16个原子共平面,B正确;
C.Z分子含有酯基、氯原子,二者都可与氢氧化钠溶液发生水解反应,反应产生甘油、NaCl、
,C正确;
D.NaOH的乙醇溶液共热发生卤素的消去反应,得不到选项所给有机物,D错误;
故合理选项是D。
9.先将环己醇加入试管A中,再缓慢加入浓硫酸 B 防止环己烯挥发(其他答案合理均可) c
蒸馏烧瓶 g 63.5%
【详解】
(1)①根据制备乙酸乙酯的操作,在试管中混合环已醇和浓硫酸操作时,药品的加入方法为先将环己醇加入
试管A中,再缓慢加入浓硫酸,故答案为先将环己醇加入试管A中,再缓慢加入浓硫酸;
②如果加热一段时间后发现忘记加碎瓷片,需要冷却后补加,故选B;
③环已烯的熔点很低,沸点也不高,容易挥发,将试管C置于冰水可以防止环已烯的挥发,故答案为防止
环已烯的挥发;
(2)①由于分液后环己烯粗品中还含有少量的酸和环己醇,联想制备乙酸乙酯提纯产物时用c(Na CO 溶液)
2 3
洗涤可除去酸,不能用酸性高锰酸钾,否则会氧化环己烯,故答案为c;
②图中仪器a 是蒸馏烧瓶,为了使冷凝的效果更好,冷却水从冷凝管的下口即g口进入;故答案为蒸馏烧
瓶;g;
(3) 12.5 mL环己醇的质量为12.5 mL×0.96 g • cm-3=12g,理论上生成环已烯 ×82g/mol=9.84g,产
率= ×100%=63.5%,故答案为低于;63.5%。
10.乙二酸 取代反应 羰基 氟原子【详解】
(1)A是草酸,其化学名称为乙二酸,反应①是SOCl 中的两个—Cl取代了羟基,其反应类型为取代反应;
2
故答案为:乙二酸;取代反应。
(2)通过分析C和D反应生成E是发生取代反应,则得出C的结构简式为 ;故答案为:
。
(3)根据F的结构简式得到F中所含官能团的名称为酯基、羰基、氟原子;故答案为:羰基;氟原子。
(4)反应⑤是取代反应,其化学方程式为
;故答案为:
。
(5)H水解产物 含有多种六元环芳香同分异构体,若环上的取代基种类和数目不变,其中核磁
共振氢谱有二组峰,峰面积之比为2:1的结构简式为 ;故答案为:
。
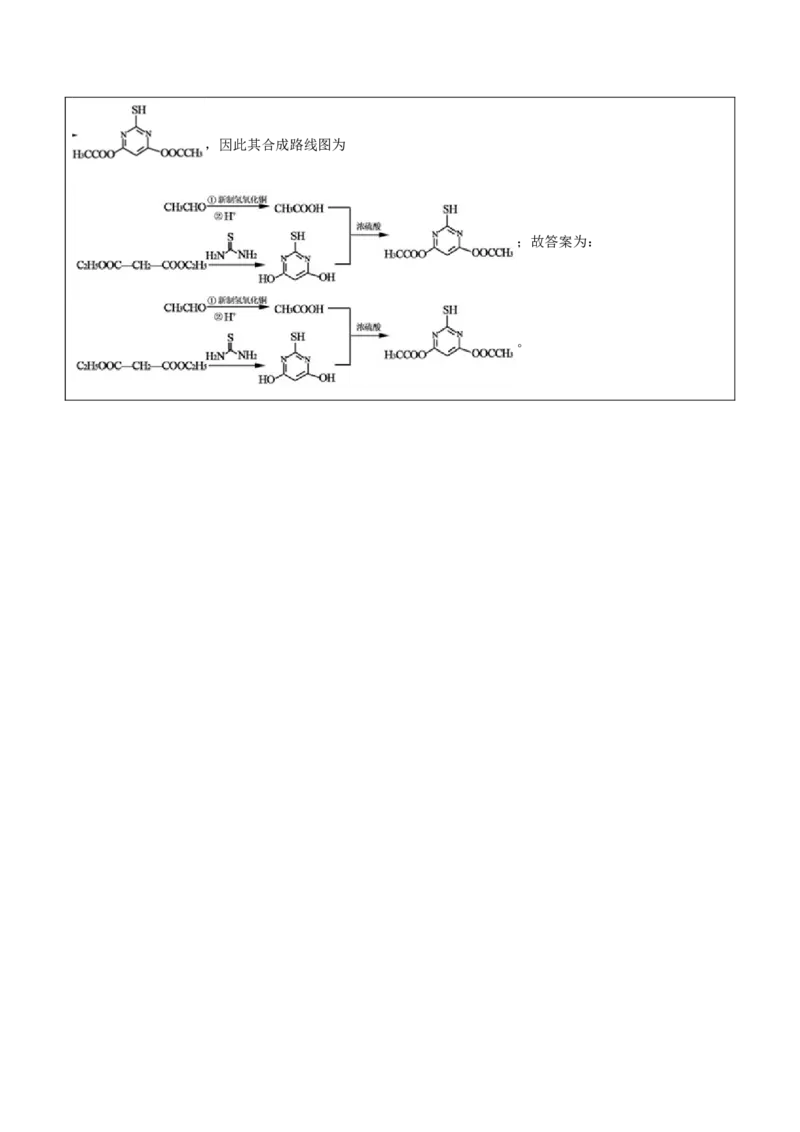
(6)乙醛在新制氢氧化铜、加热条件下反应,再酸化生成乙酸,丙二酸二乙酯
和(NH )C=S反应生成 ,乙酸和
2 2
在浓硫酸作用下反应生成,因此其合成路线图为
;故答案为:
。