文档内容
第三节 乙醇与乙酸
第 1 课时 乙醇
学业要求 核心素养对接
1.了解烃的衍生物和官能团的概念。
2.掌握乙醇的分子结构、主要性质。
通过对乙醇结构和性质的学习,培养学
3.了解乙醇的主要用途及与人类日常生
生宏观辨识与微观探析的能力。
活与健康的关系。
4.初步学会分析官能团与性质关系的方
法。
[知 识 梳 理]
知识点一 烃的衍生物
如图烃的衍生物的知识框图,那么什么是烃的衍生物呢?请完成下列知识点:
1.烃的衍生物
烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物称为烃的
衍生物。如:乙醇可看成是乙烷分子的一个氢原子被羟基取代后的衍生物。
2.官能团
决定有机化合物化学特性的原子或原子团。如—Cl(氯原子)、—OH(羟基)、
(碳碳双键)等。
知识点二 乙醇日常生活中,人们喝的形形色色的酒,主要成分都是乙醇,俗名酒精,那么乙醇究
竟有什么样的性质呢?请完成下列知识点:
1.物理性质
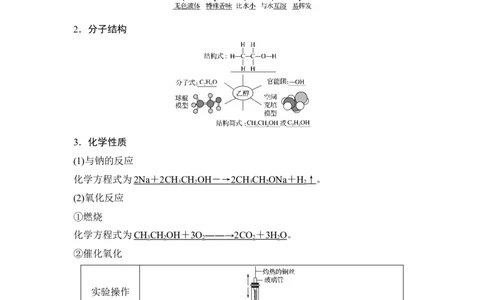
2.分子结构
3.化学性质
(1)与钠的反应
化学方程式为 2Na + 2CH CH OH ― → 2CH CH ONa + H ↑。
3 2 3 2 2
(2)氧化反应
①燃烧
化学方程式为CH CH OH + 3O ――→ 2CO + 3H O。
3 2 2 2 2
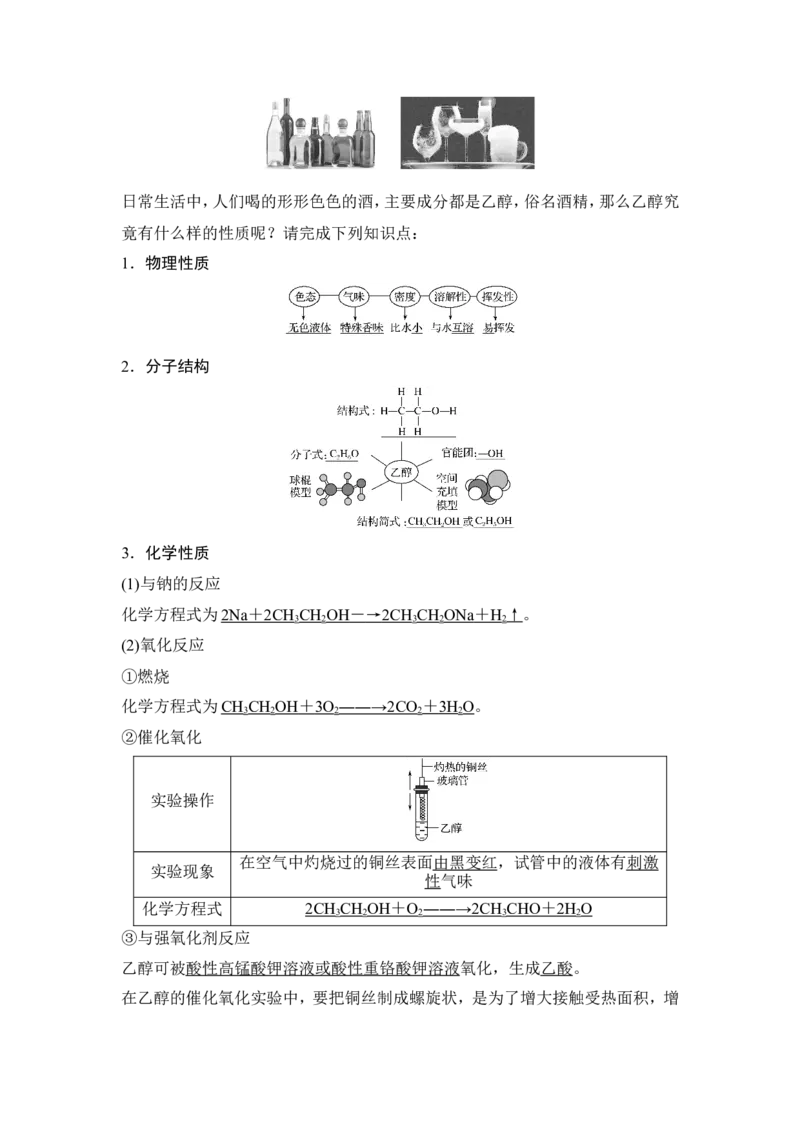
②催化氧化
实验操作
在空气中灼烧过的铜丝表面由黑变红,试管中的液体有刺激
实验现象
性气味
化学方程式 2CH CH OH + O ――→ 2CH CHO + 2H O
3 2 2 3 2
③与强氧化剂反应
乙醇可被酸性高锰酸钾溶液或酸性重铬酸钾溶液氧化,生成乙酸。
在乙醇的催化氧化实验中,要把铜丝制成螺旋状,是为了增大接触受热面积,增强实验效果。
4.用途
(1)用作酒精灯、火锅、内燃机等的燃料。
(2)用作化工原料。
(3)医疗上常用体积分数为75%的乙醇溶液作消毒剂。
微判断
(1)能用分液的方法分离酒精和水的混合物( )
(2)可用无水硫酸铜检验工业酒精中是否有水( )
(3)乙醇中的羟基不如水中的羟基活泼( )
(4)乙醇分子中含有六个氢原子,故1 mol乙醇与足量的钠反应可以生成3 mol的
氢气( )
答案 (1)× (2)√ (3)√ (4)×
微训练
1.把质量为m g的铜丝灼烧变黑,立即放入下列物质中,能使铜丝变红,而且质
量仍为m g的是( )
A.稀硫酸 B.烧碱溶液
C.乙醇 D.蒸馏水
答案 C
2.下列物质中不能用来区分乙醇和苯的是( )
A.金属钠 B.溴水
C.碳酸钠溶液 D.四氯化碳
解析 乙醇和金属钠反应缓慢,苯和金属钠不反应,可以区分,A不符合题意;乙
醇溶于溴水,且不分层,苯可以把溴水中的溴萃取出来,出现分层,可以区分,B
不符合题意;乙醇和碳酸钠互溶,不分层,苯不溶于碳酸钠,出现分层,可以区分,
C不符合题意;乙醇和苯均与四氯化碳互溶,不分层,无法区分二者,D符合题意
答案 D
3.下列物质属于烃的衍生物的是___________________________________。⑤CH CHO ⑥CH CH CH OH ⑦CH COOH
3 3 2 2 3
解析 烃分子的氢原子被其他原子或原子团所代替的一系列物质称为烃的衍生
物。即烃的衍生物除了含有C、H元素之外,还含有其他元素。
答案 ②④⑤⑥⑦
微思考
1.交警检查司机是否酒后驾车的仪器中含有橙色的酸性K Cr O 溶液,利用的是
2 2 7
什么原理?
提示 酸性K Cr O 溶液遇到乙醇时,能把乙醇氧化,同时自身被还原为Cr3+,溶
2 2 7
液由橙色变成绿色,由此可以判断司机是否饮酒。
2.比较乙醇与金属钠的反应和水与金属钠的反应,哪个更剧烈?这说明什么?
提示 钠与水反应更剧烈,说明水分子中的羟基氢比乙醇分子中的羟基氢活泼。
3.如何证明乙醇分子中含有一个羟基?二甲醚( )是乙醇的
同分异构体,判断二甲醚是否与钠反应?为什么?
提示 根据1 mol CH CH OH与足量的Na反应产生0.5 mol H ,证明一个乙醇分
3 2 2
子中含有一个羟基;二甲醚中无羟基,氢原子全部以C—H键结合,不与金属钠反
应。
学习任务1 乙醇的结构与化学性质
资料:
资料一 关于中国酒的起源,晋代文人江统的《酒诰》中有段介绍: “酒之所兴
肇自上皇;或云仪狄,一曰杜康。有饭不尽,委之空桑,积郁成味,久蓄气芳,本出
于此,不由奇方”。
资料二 明代医学家李时珍在《本草纲目》中写道: “烧酒非古法也,自元时始
创。其法用浓酒和糟入甑,蒸令汽上,用器承取滴露,凡酸坏之酒,皆可蒸烧。近时
惟以糯米或粳米或黍或秫或大麦蒸熟,和曲酿瓮中七日以甑蒸取。其清如水,味
极浓烈,盖酒露也。辛、甘、大热、有大毒。过饮败胃伤胆,丧心损寿,甚则黑肠腐
胃而死。与姜、蒜同食,令人生痔。盐、冷水、绿豆粉解其毒”。清代檀萃的《滇海虞衡志》中说:“盖烧酒名酒露,元初传入中国。”
由此可知酒在我国历史悠久,那么作为它的主要成分乙醇有什么样的性质呢?请
完成下列讨论:
1.乙醇催化氧化反应实验中铜丝是否参与反应?铜丝的作用是什么?
提示 铜丝参与化学反应,铜丝先被氧气氧化成氧化铜,后又被乙醇还原为铜,
反应前后的质量和化学性质没有变化,起催化剂的作用。
2.结合乙醇催化氧化反应的实质判断相同碳原子数且结构相似的醛与醇相比较,
它们的相对分子质量有何关系?
提示 醇催化氧化时,分子中去掉两个氢原子,故醛比生成它的醇的相对分子质
量小2。
3.已知反应:CH CH OH+HBr――→CH CH Br+H O,则该反应的类型是什么?
3 2 3 2 2
断裂的化学键有哪些?
提示 该反应相当于HBr中的溴原子代替乙醇分子中的—OH,属于取代反应,
断裂的化学键有C—O键和H—Br键。
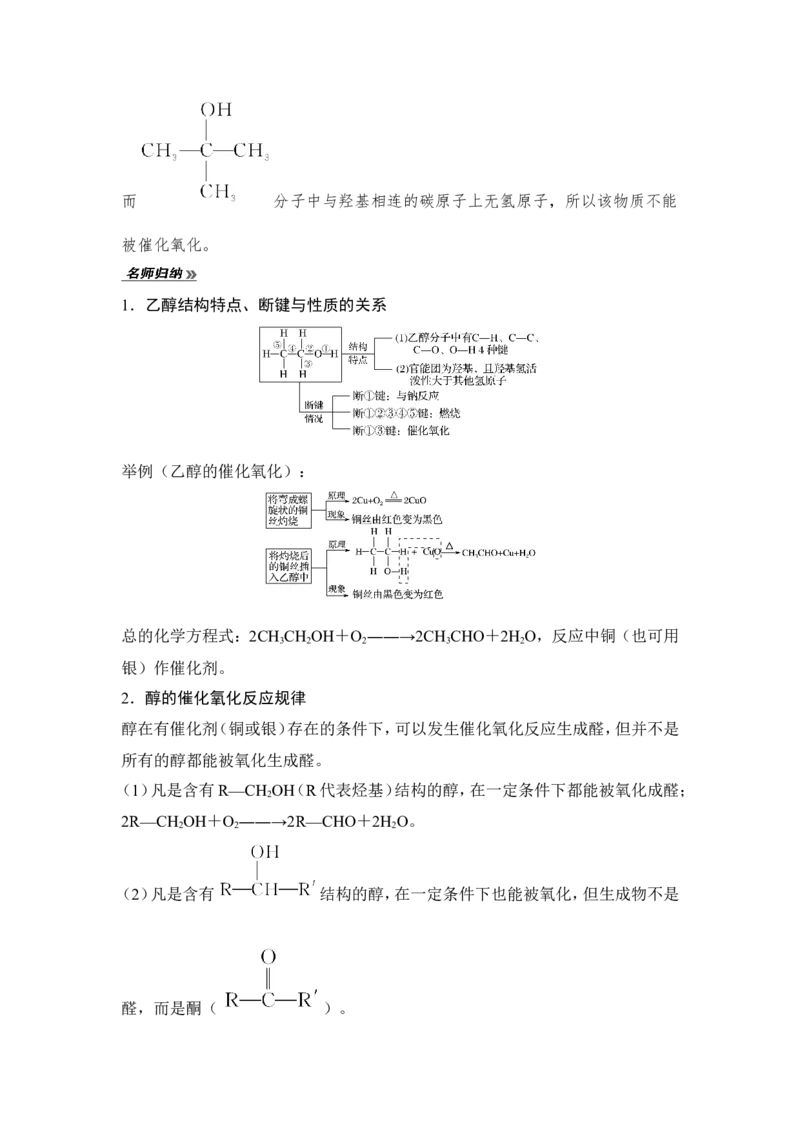
4.根据乙醇催化氧化的实质,推测 的催化氧化产物是什么,
能被催化氧化吗?
提示 因为乙醇催化氧化的实质是: ――→
,故 的催化氧化产物为 ,而 分子中与羟基相连的碳原子上无氢原子,所以该物质不能
被催化氧化。
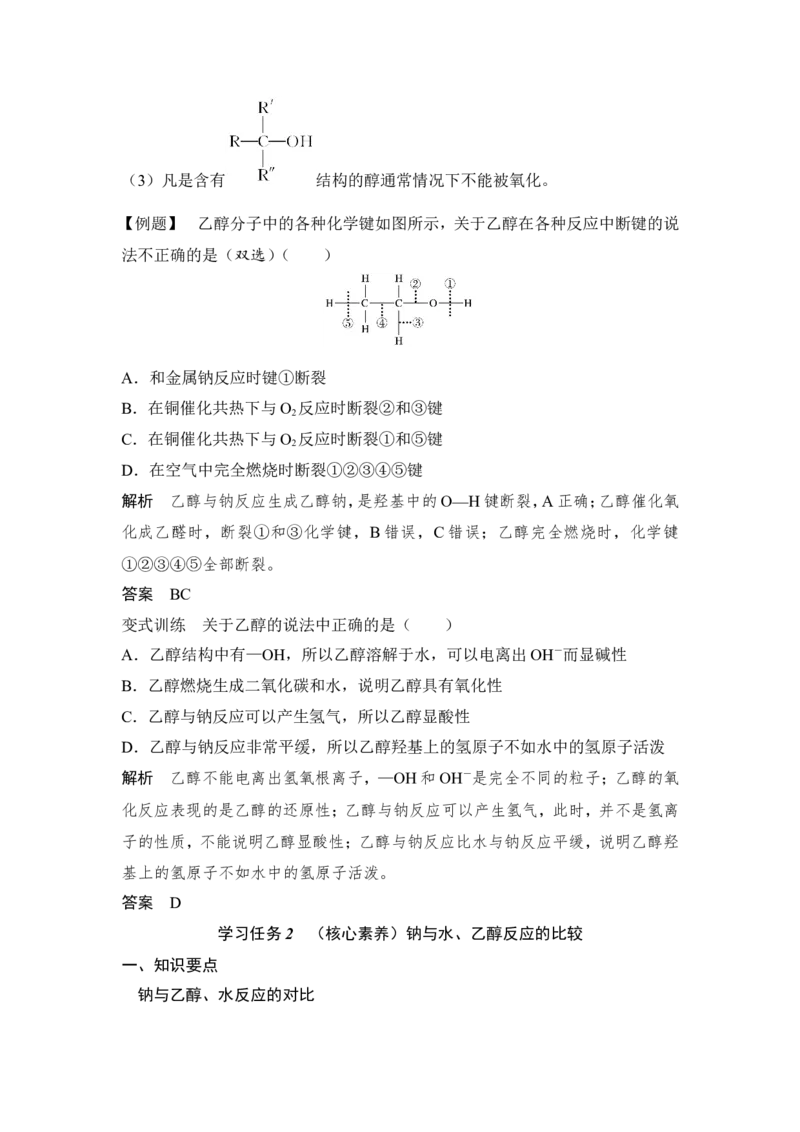
1.乙醇结构特点、断键与性质的关系
举例(乙醇的催化氧化):
总的化学方程式:2CH CH OH+O ――→2CH CHO+2H O,反应中铜(也可用
3 2 2 3 2
银)作催化剂。
2.醇的催化氧化反应规律
醇在有催化剂(铜或银)存在的条件下,可以发生催化氧化反应生成醛,但并不是
所有的醇都能被氧化生成醛。
(1)凡是含有R—CH OH(R代表烃基)结构的醇,在一定条件下都能被氧化成醛;
2
2R—CH OH+O ――→2R—CHO+2H O。
2 2 2
(2)凡是含有 结构的醇,在一定条件下也能被氧化,但生成物不是
醛,而是酮( )。(3)凡是含有 结构的醇通常情况下不能被氧化。
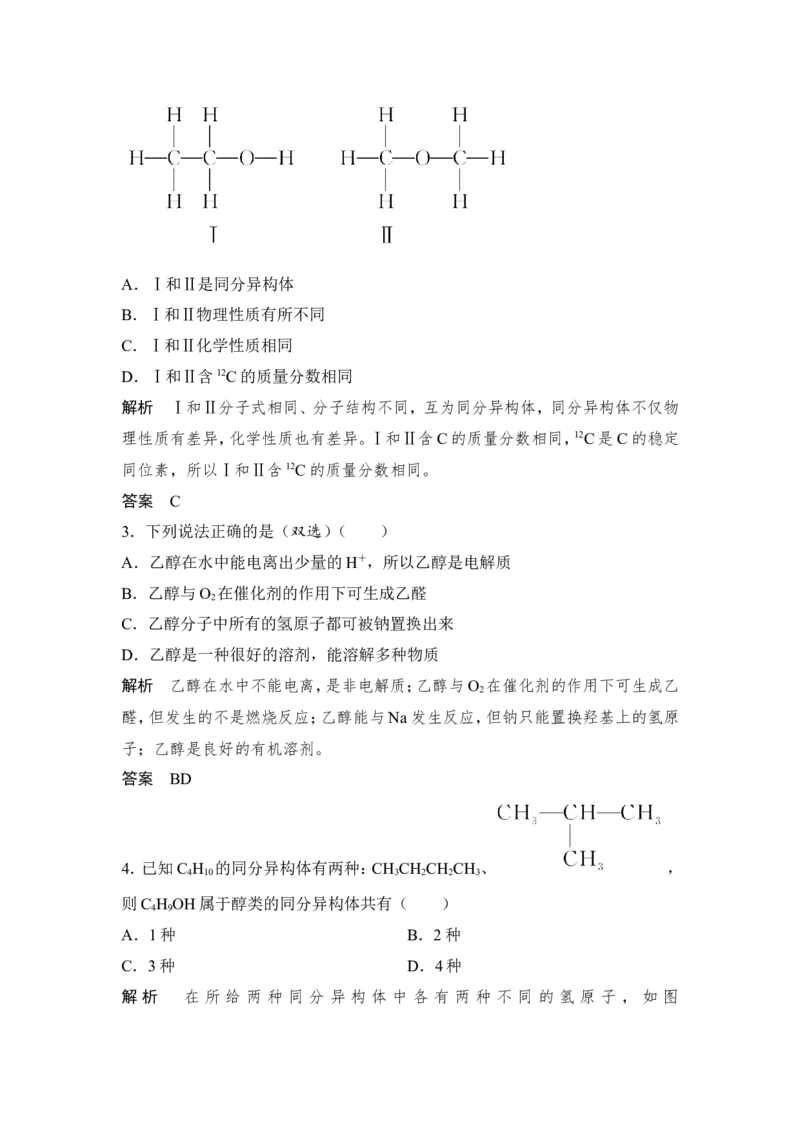
【例题】 乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断键的说
法不正确的是(双选)( )
A.和金属钠反应时键①断裂
B.在铜催化共热下与O 反应时断裂②和③键
2
C.在铜催化共热下与O 反应时断裂①和⑤键
2
D.在空气中完全燃烧时断裂①②③④⑤键
解析 乙醇与钠反应生成乙醇钠,是羟基中的O—H键断裂,A正确;乙醇催化氧
化成乙醛时,断裂①和③化学键,B错误,C错误;乙醇完全燃烧时,化学键
①②③④⑤全部断裂。
答案 BC
变式训练 关于乙醇的说法中正确的是( )
A.乙醇结构中有—OH,所以乙醇溶解于水,可以电离出OH-而显碱性
B.乙醇燃烧生成二氧化碳和水,说明乙醇具有氧化性
C.乙醇与钠反应可以产生氢气,所以乙醇显酸性
D.乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼
解析 乙醇不能电离出氢氧根离子,—OH和OH-是完全不同的粒子;乙醇的氧
化反应表现的是乙醇的还原性;乙醇与钠反应可以产生氢气,此时,并不是氢离
子的性质,不能说明乙醇显酸性;乙醇与钠反应比水与钠反应平缓,说明乙醇羟
基上的氢原子不如水中的氢原子活泼。
答案 D
学习任务2 (核心素养)钠与水、乙醇反应的比较
一、知识要点
钠与乙醇、水反应的对比水与钠反应 乙醇与钠反应
钠粒浮于水面,熔成闪亮的小球,并快 钠粒开始沉于试管底部,
钠的变化
速地四处游动,很快消失 未熔化,最终慢慢消失
声的现象 有“嘶嘶”声响 无声响
气体检验 点燃,发出淡蓝色的火焰 点燃,发出淡蓝色的火焰
钠的密度比乙醇的大。钠
钠的密度小于水,熔点低。钠与水剧烈
与乙醇缓慢反应生成氢
实验结论 反应,生成氢气。水分子中羟基上的氢
气。乙醇中羟基上的氢原
原子比较活泼
子相对不活泼
2Na+
反应的化
2Na+2H O===2NaOH+H ↑ 2CH CH OH―→2CH CH
2 2 3 2 3 2
学方程式
ONa+H ↑
2
二、核心素养
通过比较钠与水、乙醇的反应⇒培养学生科学探究与创新意识
【素养解题】
[典例示范] 向装有乙醇的烧杯中投入一小块金属钠,下列对该实验现象的描述
中正确的是( )
A.钠块沉在乙醇液面的下面 B.钠块熔化成小球
C.钠块在乙醇的液面上游动 D.钠块剧烈反应放出气体
[解题思路]
读题干 Na与乙醇反应
①ρ >ρ
Na 乙醇
知识支持
②Na与乙醇的反应缓慢
A:因ρ >ρ ,故在液面下面,正确,则C不正确。因Na与乙
析选项 Na 乙醇
醇反应缓慢,故B、D不正确。
得答案 A
三、对点训练
1.下列物质,都能与Na反应放出H ,其产生H 的速率排列顺序正确的是( )
2 2
①C H OH ②H CO 溶液 ③H O
2 5 2 3 2
A.①>②>③ B.②>①>③
C.③>①>② D.②>③>①
解析 Na与H O反应比与C H OH反应剧烈,故反应速率:③>①,可排除A、B
2 2 5
两项。H CO 溶液中不仅含有H O,而且含有H CO ,H CO 电离出H+使溶液呈
2 3 2 2 3 2 3
酸性,Na 与 H CO 反应比与 H O 反应剧烈得多,故可知反应速率排序为
2 3 2②>③>①。
答案 D
2.下列说法正确的是( )
①检测乙醇中是否含有水可加入少量的无水硫酸铜,如变蓝则含水 ②除去乙醇
中微量水可加入金属钠,使其完全反应 ③获得无水乙醇的方法是直接加热蒸馏
④获得无水乙醇的方法通常采用先用生石灰吸水,然后再加热蒸馏
A.①③ B.②④
C.①④ D.③④
解析 用无水CuSO 可检验是否有水存在,因为无水CuSO 遇水变蓝,故①正确;
4 4
乙醇和水均与金属钠反应生成气体,故②错误;含水的酒精直接加热蒸馏,水也
会挥发,酒精不纯,③错误;④正确。
答案 C
3.结合乙烯和乙醇的结构与性质,推测丙烯醇(CH ===CH—CH OH)不能发生
2 2
的化学反应有( )
A.加成反应
B.氧化反应
C.与Na反应
D.与Na CO 溶液反应放出CO
2 3 2
解析 丙烯醇分子中含碳碳双键,应具有烯烃的性质,能发生加成反应和氧化反
应;含有醇羟基,具有醇的性质,与钠反应,但不具有酸性,不能与Na CO 溶液反
2 3
应放出CO 。
2
答案 D
4.按照下图装置持续通入X气体或蒸气,可以看到a处有红色物质生成,b处变
蓝,c处得到液体,则X气体或蒸气可能是(假设每个反应均完全)( )
A.CH CH OH B.CO或H
3 2 2
C.NH D.H
3 2
解析 选项中气体均可还原CuO,但本题的关键点是所得产物冷凝后得到液体,该液体不可能是水(干燥管中盛有足量CuSO ),所以一定是乙醛,X气体为乙醇。
4
答案 A
5.乙烯的产量通常用来衡量一个国家的石油化工水平。以乙烯为主要原料合成
重要的有机化合物的路线如图所示。请回答下列问题。
(1)物质A的结构简式 。A物质所含官能团的名称是 。
(2)反应②的反应类型是 。
(3)以乙烯为原料可合成有机高分子化合物D(聚乙烯),反应的化学方程式是
_____________________________________________________________。
解析 乙烯和水发生加成反应CH ===CH +H O――→CH CH OH生成A,则A
2 2 2 3 2
是乙醇,乙醇和氧气在铜或银的催化作用下生成 B(乙醛):2CH CH OH+
3 2
O ――→2CH CHO+2H O,乙烯分子含有碳碳双键,发生加聚反应,反应为
2 3 2
nCH ===CH ―→CH -CH ,生成聚乙烯,D为聚乙烯。据此可得下列结论:
2 2 2 2
(1)由上述分析可知,A的结构简式为CH CH OH。其官能团的名称是羟基。
3 2
(2)乙烯和水发生加成反应:CH ===CH +H O――→CH CH OH。
2 2 2 3 2
(3)乙烯分子含有碳碳双键,发生加聚反应,反应为
nCH ===CH ――→CH -CH
2 2 2 2
答案 (1)CH CH OH 羟基 (2)加成反应
3 2
(3)nCH ===CH ――→CH -CH
2 2 2 2
[学 考 练]
1.下列化学用语正确的是( )
A.乙醇的官能团:—OH
B.乙醇的分子式:CH CH OH
3 2
C.乙烯的结构简式:CH CH
2 2
D.乙烯无官能团
答案 A
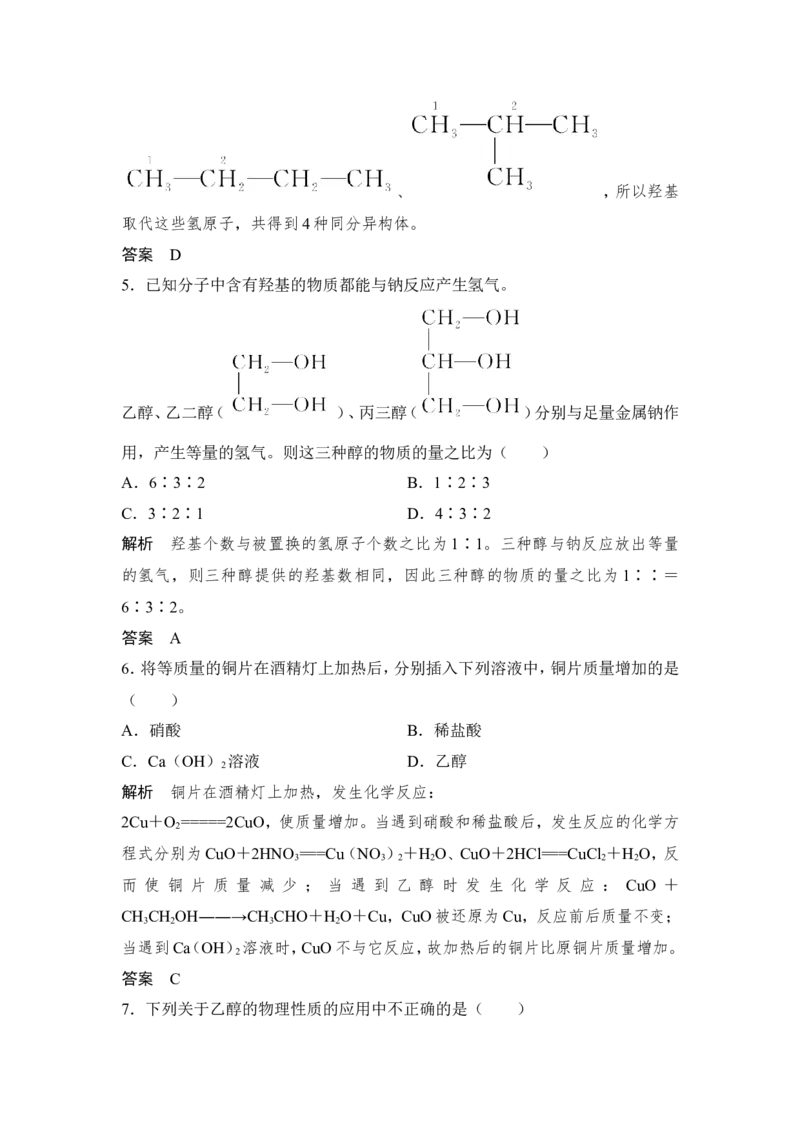
2.有机物Ⅰ和Ⅱ的结构式如下,下列说法中不正确的是( )A.Ⅰ和Ⅱ是同分异构体
B.Ⅰ和Ⅱ物理性质有所不同
C.Ⅰ和Ⅱ化学性质相同
D.Ⅰ和Ⅱ含12C的质量分数相同
解析 Ⅰ和Ⅱ分子式相同、分子结构不同,互为同分异构体,同分异构体不仅物
理性质有差异,化学性质也有差异。Ⅰ和Ⅱ含C的质量分数相同,12C是C的稳定
同位素,所以Ⅰ和Ⅱ含12C的质量分数相同。
答案 C
3.下列说法正确的是(双选)( )
A.乙醇在水中能电离出少量的H+,所以乙醇是电解质
B.乙醇与O 在催化剂的作用下可生成乙醛
2
C.乙醇分子中所有的氢原子都可被钠置换出来
D.乙醇是一种很好的溶剂,能溶解多种物质
解析 乙醇在水中不能电离,是非电解质;乙醇与O 在催化剂的作用下可生成乙
2
醛,但发生的不是燃烧反应;乙醇能与Na发生反应,但钠只能置换羟基上的氢原
子;乙醇是良好的有机溶剂。
答案 BD
4.已知C H 的同分异构体有两种:CH CH CH CH 、 ,
4 10 3 2 2 3
则C H OH属于醇类的同分异构体共有( )
4 9
A.1种 B.2种
C.3种 D.4种
解 析 在 所 给 两 种 同 分 异 构 体 中 各 有 两 种 不 同 的 氢 原 子 , 如 图、 ,所以羟基
取代这些氢原子,共得到4种同分异构体。
答案 D
5.已知分子中含有羟基的物质都能与钠反应产生氢气。
乙醇、乙二醇( )、丙三醇( )分别与足量金属钠作
用,产生等量的氢气。则这三种醇的物质的量之比为( )
A.6∶3∶2 B.1∶2∶3
C.3∶2∶1 D.4∶3∶2
解析 羟基个数与被置换的氢原子个数之比为1∶1。三种醇与钠反应放出等量
的氢气,则三种醇提供的羟基数相同,因此三种醇的物质的量之比为1∶∶=
6∶3∶2。
答案 A
6.将等质量的铜片在酒精灯上加热后,分别插入下列溶液中,铜片质量增加的是
( )
A.硝酸 B.稀盐酸
C.Ca(OH) 溶液 D.乙醇
2
解析 铜片在酒精灯上加热,发生化学反应:
2Cu+O =====2CuO,使质量增加。当遇到硝酸和稀盐酸后,发生反应的化学方
2
程式分别为CuO+2HNO ===Cu(NO )+H O、CuO+2HCl===CuCl +H O,反
3 3 2 2 2 2
而 使 铜 片 质 量 减 少 ; 当 遇 到 乙 醇 时 发 生 化 学 反 应 : CuO +
CH CH OH――→CH CHO+H O+Cu,CuO被还原为Cu,反应前后质量不变;
3 2 3 2
当遇到Ca(OH)溶液时,CuO不与它反应,故加热后的铜片比原铜片质量增加。
2
答案 C
7.下列关于乙醇的物理性质的应用中不正确的是( )A.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中药的有效成分
C.由于乙醇能够以任意比与水互溶,所以酒厂可以勾兑各种浓度的酒
D.从化学学科角度看,俗语“酒香不怕巷子深”中包含乙醇容易挥发的性质
解析 由于乙醇与H O互溶不分层,故不能用分液法除去乙醇中的水。
2
答案 A
8.为减少汽车尾气对大气造成的污染,市场上推出了使用乙醇汽油(在汽油中加
入适量乙醇)的汽车。下列叙述错误的是( )
A.乙醇汽油是一种化合物
B.汽车使用乙醇汽油可以减少有害气体的排放
C.乙醇充分燃烧生成CO 和H O
2 2
D.用粮食发酵可制得乙醇
解析 乙醇汽油属于混合物,因此A错误。
答案 A
9.下列有机物中,不属于烃的衍生物的是( )
A. B.CH CH NO
3 2 2
C.CH ===CHBr D.CH —CH
2 2 2
解析 可看作甲苯分子中的一个氢原子被 Cl取代;
CH CH NO 可看作CH CH 分子中的一个氢原子被硝基取代;CH ===CHBr可看
3 2 2 3 3 2
作CH ===CH 分子中的一个氢原子被Br所取代的产物;只有CH —CH 不属
2 2 2 2
于烃的衍生物。
答案 D
10.下列物质中不能使酸性高锰酸钾溶液褪色,也不能使溴水因发生反应褪色的
是(双选)( )
A.甲烷 B.乙烯
C.乙醇 D.苯
解析 甲烷既不能使酸性高锰酸钾溶液褪色,也不能使溴水褪色;苯不能使酸性高锰酸钾溶液褪色,不能使溴水因发生反应褪色;乙烯使二者都能褪色;乙醇可
被酸性高锰酸钾溶液氧化而使之褪色,但不与溴水反应,不能使之褪色。
答案 AD
11.如图是A分子的球棍模型和B分子的空间充填模型,回答下列问题:
(1)A和B的关系是___________________________________________________
(2)写出 A 分子在催化剂存在条件下加热和氧气反应的化学方程式:
_____________________________________________________。
(3)写出B分子和金属钠反应的化学方程式:_____________________________
__________________________________________________________。
(4)B在加热条件下能够和HBr发生反应生成溴乙烷,该反应类型是 。
解析 根据成键原则,可以判断 A和B的结构简式分别是 CH OH(甲醇)和
3
CH CH OH,它们结构相似,互称为同系物;它们都含—OH,甲醇和乙醇性质相似,
3 2
能被氧化成相应的醛,能够与金属钠反应;根据B在加热条件下能与HBr发生反
应生成溴乙烷的特点可知该反应为取代反应。
答案 (1)同系物
(2)2CH OH+O ――→2HCHO+2H O
3 2 2
(3)2CH CH OH+2Na―→2CH CH ONa+H ↑
3 2 3 2 2
(4)取代反应
12.乙醇能与紫红色的酸性KMnO 溶液或橙色的酸性K Cr O 溶液反应,现象为
4 2 2 7
__________________________________________________________________
__________________________________________________________________,
乙醇最终被 为 。交通警察判断某驾驶员酒后驾车的依据是驾驶
员呼出的气体使检测仪中的溶液由 色变为 色。
答案 酸性KMnO 溶液褪色;酸性K Cr O 溶液由橙色变为绿色 氧化 乙酸
4 2 2 7
橙 绿
[能 力 练]
13.乙醇在能源、生产及日常生活等许多方面都有十分广泛的应用。请计算:
(1)将足量乙醇与9.2 g金属钠充分反应,则标准状况下生成气体的体积是L。
(2)若一定量的乙醇和O 在密闭容器中燃烧后的产物为CO 、CO和H O(g)。产
2 2 2
物依次经过浓硫酸和碱石灰使其被充分吸收,浓硫酸增重 10.8 g,碱石灰增重
13.2 g。则氧气的物质的量是 mol,燃烧产物的平均摩尔质量是
g·mol-1。
解析 (1)由题意:
2Na ~ H ↑
2
46 g 22.4 L
9.2 g V(H )
2
V(H )==4.48 L。
2
(2)根据氢原子守恒,可得:
C H OH ~ 3H O
2 5 2
1 mol 54 g
n(C H OH) 10.8 g
2 5
n(C H OH)==0.2 mol。
2 5
碱石灰增重的质量即为生成CO 的质量,故n(CO )==0.3 mol。
2 2
根据化学反应过程中碳原子守恒可得:n(CO)=2×0.2 mol-0.3 mol=0.1 mol。
根据氧原子守恒:
n(O )==0.55 mol。产物的总物质的量n=(0.6+0.3+0.1)mol=1 mol;产物的
2
总质量m=(10.8+13.2+2.8)g=26.8 g;产物平均摩尔质量M=26.8 g·mol-1。
答案 (1)4.48 (2)0.55 26.8
14.乙醇是生活中常见的有机物,能进行如下图所示的多种反应,A、C都是有机
物。
写出下列反应的化学方程式:
①__________________________________________________________________;
②_________________________________________________________________;
③______________________________________________________________。答案 ①2CH CH OH+2Na―→2CH CH ONa+H ↑
3 2 3 2 2
②CH CH OH+3O ――→2CO +3H O
3 2 2 2 2
③2CH CH OH+O ――→2CH CHO+2H O
3 2 2 3 2
15.有关催化剂的催化机理等问题可从“乙醇催化氧化实验”得到一些认识,其
实验装置如图所示。其实验操作为预先使棉花团浸透乙醇,并照图安装好装置;
在铜丝的中间部分加热,片刻后开始(间歇性)鼓入空气,即可观察到明显的实验
现象。
请回答下列问题:
(1)被加热的铜丝处发生反应的化学方程式为__________________________
________________________________________________________________。
(2)从A管中可观察到的实验现象是__________________________________
_________________________________________________________________。
从中可认识到在该实验过程中,催化剂参加了化学反应,还可认识到催化剂起催
化作用时需要一定的__________________________________________________。
(3)实验一段时间后,如果撤掉酒精灯,反应还能否继续进行?
_________________________________________________________________,
原受热部分的铜丝有什么现象?____________________________________
__________________________________________________________________,
其原因是_____________________________________________________________。
解析 乙醇在Cu作催化剂时发生氧化反应的机理为2Cu+O =====2CuO(铜丝
2
变黑);CH CH OH+CuO――→CH CHO+Cu+H O(铜丝由黑变红)。
3 2 3 2
答案 (1)2CH CH OH+O ――→2CH CHO+2H O
3 2 2 3 2
(2)受热部分的铜丝随间歇性地鼓入空气而交替出现变黑、变红 温度
(3)能 仍可看到原受热部分的铜丝交替出现变黑、变红的现象
醇的催化氧化反应是放热反应