文档内容
2007 全国初中化学竞赛(广东省初赛)试题
1、本试卷分两部分,第一部分100分,第二部分30分,满分共130分。考试时间l20分钟。
2、答题前,考生必须将自己所在的学校、班级、姓名、座号写在密封线内。
3、可能用到的相对原子质量:H—l Li—7 C—12 N—14 S—16 K—39
Ca—40 I—l27 Zn—65 Fe一56 S一32 Na一23 Mg—24
第一部分(共100分)
一、选择题(本题l4小题,每小题2分,共28分。每小题有一个选项符合题意)
1.下表为家庭中一些常见物质的pH
物质 食醋 牙膏 食盐水 肥皂水 火碱液
pH 3 9 7 10 13
有些人昆虫如蜂、蚂蚁等叮咬人时,会向人体射入一种叫蚁酸(具有酸的性质)的物质,使
皮肤发红、瘙痒,甚至疼痛,要消除这种症状,可在叮咬处涂上下列物质中的( )
A.牙膏或肥皂水 B.食盐水 C.火碱液 D.食醋
2.氢气是一种绿色能源,科学家们最近研制出利用太阳能产生激光,再用激光分解
海水得到氢气的新技术,其中海水分解可以用化学方程式表示为:
激光
2H O ==== 2H ↑+ O ↑,据此下列说法不正确的是( )
2 2 2
TiO
2
A.TiO 在反应中作催化剂 B.水分解不产生污染物
2
C.TiO 在反应中作氧化剂 D.该技术可以将太阳能转化为氢能
2
3.“神舟六号”载人飞船的成功发射与回收,表明我国的载人航天技术已经达到了国际
领先水平。在飞船的火箭推进器中常装有液态肼(用A表示)和过氧化氢(H O ),它们混合
2 2
时的反应方程式为: 2H O +A=N +4H O 则肼(A)的化学式为( )
2 2 2 2
A.N H B.N H C.NH D.N H O
2 2 2 4 2 2 4 2
4.某学生用量筒量取液体,量筒摆放平稳,且学生面对刻度,他首先俯视液面读数为
79mL,倾倒出部分液体后,又仰视读数为70mL,则该生实际倒出的液体的体积为 ( )
A.9mL B.大于9mL C.小于9mL D.无法判断
5.液化石油气作为燃料,已进入千家万户,它是含有下列物质的混合物,常温下,它们的
沸点如 下表所示:
在常温下使用至无气体放出时,钢瓶中常有一些残液,它最有可能是( )
A.乙烷B.己烷 C.乙烷、丙烷、丁烷D.,戊烷、己烷
6.我国兰州的近代物理研究所曾经研究制出首批重氧气(18O ),其价格远远超过黄金。
2
则下列说法正确的是( )
A.重氧气的相对分子质量为32 8.H 18O的相对分子质量为20
2
C.重氧气中氧元素的化合价为-2 C.18O 是一种化合物
2
7.物质A里只有1 X 1022个分子,在这些分子里共含有2X 1022个原子,那么A物质一
定是( )
A.单质 B.纯净物 C.混合物 D.不能断定
8.在天平的两盘分别放入质量相等的烧杯,烧杯中各盛l00 g 9.8%的硫酸溶液,此时天平保持平衡。向两个烧杯中同时放入哪组金属,反应终止时天平仍保持平衡( )
A.锌、铁各7 g B .锌、铁各5 9g C.锌、铁各4 g D.锌、铁各3 g
9.有一包不纯的CaCO 样品,其中只含一种杂质,现取该样品5 g与足量稀盐酸反应生
3
成2.3 g CO , 则所混杂质可能是( )
2
10.室温下,在pH=13的溶液中不可能大量共存的是( )
11.某工厂排出的废水经检验pH<7,并含有较多的Cu2+,它们对人体、牲畜和农作物都有害,
从回收利用和环境保护的角度考虑,切合实际的废水处理方案是加入适量的( )
A.食盐和盐酸 8.硫酸钠和氯化镁 C。石灰石和铁粉 D.石灰石和银
12.现有a、b、c、d四种无色溶液,分别是碳酸钠溶液、硫酸、氯化钡溶液、盐酸中的一种。根
据下表中它们两两间相互反应的实验记录,推断a、b、c、d的顺序正确的是( )
13.在配制l0%NaCl溶液的过程中,导致溶液中NaCl质量分数小于l0%的可能的原因是:
①用量筒量取水时仰视读数②配制溶液时烧杯用少量蒸馏水润洗③在托盘天平的左盘称量
氯化钠时,游码不在零位置就调节天平平衡,后将游码移动得到读数④盛装溶液的试剂瓶用
蒸馏水润洗⑤氯化钠晶体不纯 ( )
A.①②③④⑥ B.只有①⑦④⑤ C.只有①②③ D.只有②⑨④⑤
14.质子和中子都是由u夸克和d夸克组成,U夸克带电量为(2/3)e,d夸克带电量为(-1/3)
e,e为基元电荷。下列论断可能正确的是( )
A.质子由l个U夸克和1个d夸克组成,中子由l个U夸克和2个d夸克组成
B.质子由l个U夸克和2个d夸克组成,中子由2个U夸克和1个d夸克组成
C.质子由2个U夸克和1个d夸克组成,中子由l个U夸克和2个d夸克组成
D.质子由2个U夸克和1个d夸克组成,中子由l个U夸克和1个d夸克组成
二、填空题(本题包括5小题,共24分)
15.(5分)下表县某地市场销售的~种“加碘食盐”包装袋上的部分文字说明:
(1)由食用方法和贮藏指南可推测碘酸钾的化学性质之一是 ;
(2)用单质碘与氯酸钾发生置换反应可制得碘酸钾,该反应的化学方程式为
(3)50瞻该“加碘食盐”中碘酸钾最多约为 mg。
16.(2分)“非典”肆虐时期,过氧乙酸(C H O )是被人们广泛使用的消毒剂,它无色且有
2 4 3
刺激性气味,具有强氧化性,温度稍高即分解放出氧气并生成醋酸(CH COOH),请写出
3过氧乙酸分解的化学方程式 。
17.(6分)如果以碳酸钙、纯碱、水等为原料制取氢氧化钠溶液可以设计如下过程:
加热 水 碳酸钠
碳酸钙 ——→ 氧化钙——→氢氧化钙 ——→ 氢氧化钠
如果以锌、稀硫酸、氧化铜为原料制取单质铜,有两种设计方法,请你按照前面的实
验设计格式,写出你的实验方案。
方案一:Zn ——→
方案二:CuO ——→
你设计的方案一和方案二中,方案 操作简便。原因是
18.(4分)近年来出现的厄尔尼诺现象与大气中的二氧化碳含量的增多有关,请回答以下
问题:
(1)空气中二氧化碳的主要来源是 ;
(2)绿色植物消耗二氧化碳的过程是 作用,写出该反应的文字表达式:
19.(7分,方程式两分,其余每空l分)某学校化学兴趣小组同学在学习了制取氧气这~节内
容后,发现在实验室里用5%H O 溶液加热制O ,用带火星的木条检验,木条很难复燃。同
2 2 2
学们经过认真观察, 猜想其可能原因是 或 。为
了验证此猜想是否正确,兴趣小组的同学经过热烈讨论,制定了实验方案并进行了实验。
(1)第一组同学采取增大H O 溶液浓度的方法,用l0%的H O 溶液加热,结果一段时间后,
2 2 2 2
用带火星的木条检验,木条复燃;
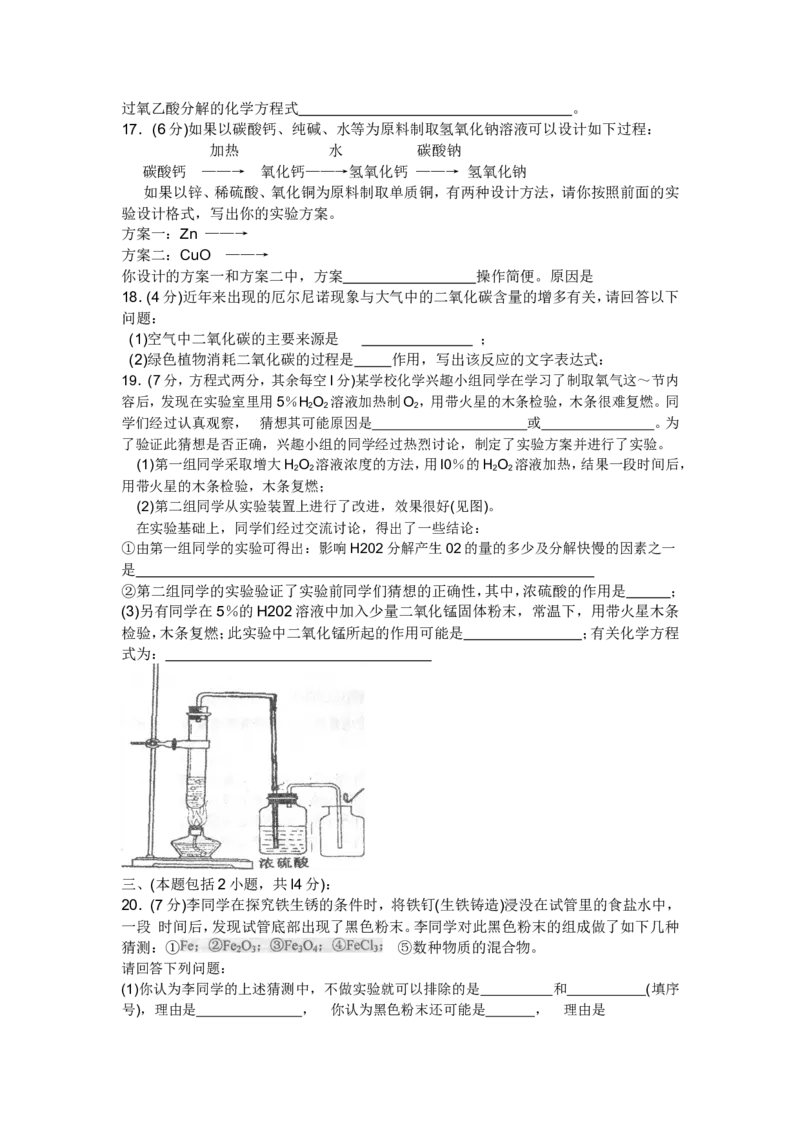
(2)第二组同学从实验装置上进行了改进,效果很好(见图)。
在实验基础上,同学们经过交流讨论,得出了一些结论:
①由第一组同学的实验可得出:影响H202分解产生02的量的多少及分解快慢的因素之一
是
②第二组同学的实验验证了实验前同学们猜想的正确性,其中,浓硫酸的作用是 ;
(3)另有同学在5%的H202溶液中加入少量二氧化锰固体粉末,常温下,用带火星木条
检验,木条复燃;此实验中二氧化锰所起的作用可能是 ;有关化学方程
式为:
三、(本题包括2小题,共l4分):
20.(7分)李同学在探究铁生锈的条件时,将铁钉(生铁铸造)浸没在试管里的食盐水中,
一段 时间后,发现试管底部出现了黑色粉末。李同学对此黑色粉末的组成做了如下几种
猜测:① ⑤数种物质的混合物。
请回答下列问题:
(1)你认为李同学的上述猜测中,不做实验就可以排除的是 和 (填序
号),理由是 , 你认为黑色粉末还可能是 , 理由是(2)设计一个实验方案,用化学方法验证黑色粉末是否为Fe粉:
(3)李同学将黑色粉末干燥后,用磁铁靠近,发现粉末能被磁铁吸引,于是得出结论:黑色粉末
一定是Fe粉,你认为李同学的结论对吗? ,理由是
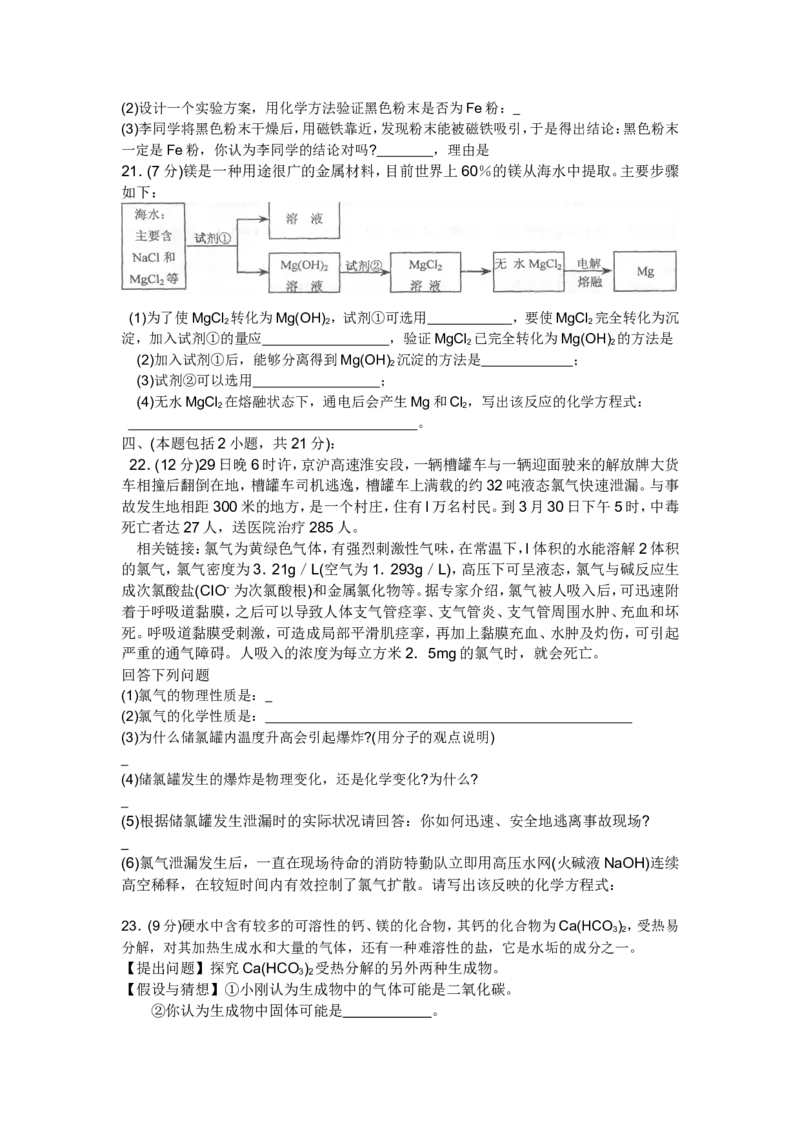
21.(7分)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。主要步骤
如下:
(1)为了使MgCl 转化为Mg(OH) ,试剂①可选用 ,要使MgCl 完全转化为沉
2 2 2
淀,加入试剂①的量应 ,验证MgCl 已完全转化为Mg(OH) 的方法是
2 2
(2)加入试剂①后,能够分离得到Mg(OH) 沉淀的方法是 ;
2
(3)试剂②可以选用 ;
(4)无水MgCl 在熔融状态下,通电后会产生Mg和Cl ,写出该反应的化学方程式:
2 2
。
四、(本题包括2小题,共21分):
22.(12分)29日晚6时许,京沪高速淮安段,一辆槽罐车与一辆迎面驶来的解放牌大货
车相撞后翻倒在地,槽罐车司机逃逸,槽罐车上满载的约32吨液态氯气快速泄漏。与事
故发生地相距300米的地方,是一个村庄,住有l万名村民。到3月30日下午5时,中毒
死亡者达27人,送医院治疗285人。
相关链接:氯气为黄绿色气体,有强烈刺激性气味,在常温下,l体积的水能溶解2体积
的氯气,氯气密度为3.21g/L(空气为1.293g/L),高压下可呈液态,氯气与碱反应生
成次氯酸盐(CIO- 为次氯酸根)和金属氯化物等。据专家介绍,氯气被人吸入后,可迅速附
着于呼吸道黏膜,之后可以导致人体支气管痉挛、支气管炎、支气管周围水肿、充血和坏
死。呼吸道黏膜受刺激,可造成局部平滑肌痉挛,再加上黏膜充血、水肿及灼伤,可引起
严重的通气障碍。人吸入的浓度为每立方米2.5mg的氯气时,就会死亡。
回答下列问题
(1)氯气的物理性质是:
(2)氯气的化学性质是:
(3)为什么储氯罐内温度升高会引起爆炸?(用分子的观点说明)
(4)储氯罐发生的爆炸是物理变化,还是化学变化?为什么?
(5)根据储氯罐发生泄漏时的实际状况请回答:你如何迅速、安全地逃离事故现场?
(6)氯气泄漏发生后,一直在现场待命的消防特勤队立即用高压水网(火碱液NaOH)连续
高空稀释,在较短时间内有效控制了氯气扩散。请写出该反映的化学方程式:
23.(9分)硬水中含有较多的可溶性的钙、镁的化合物,其钙的化合物为Ca(HCO ) ,受热易
3 2
分解,对其加热生成水和大量的气体,还有一种难溶性的盐,它是水垢的成分之一。
【提出问题】探究Ca(HCO ) 受热分解的另外两种生成物。
3 2
【假设与猜想】①小刚认为生成物中的气体可能是二氧化碳。
②你认为生成物中固体可能是 。【设计实验方案】请你设计出简单的实验方案,来验证上述猜想是否正确。
【现象与结论】如果小刚的猜想正确,现象应该是
如果你的猜想正确,现象应该是
由此得出Ca(HCO ) 受热分解的化学方程式为:
3 2
五、计算题(本题2小题,共l3分):
24. (6分)某学校化学兴趣小组的同学为了测定石灰石中碳酸钙的质量分数,称取了4
份石灰石样品(设该石灰石中不含其他碳酸盐),分别加入过量的稀盐酸进行实验,结果
如下:
分析上述实验数据并回答:
(1)哪次实验数据有明显错误?为什么?
(2)计算这种石灰石样品中碳酸钙的质量分数。
25.(7分)宇宙飞船内,宇航员所呼出的气体要通过盛有氢氧化锂的过滤网,以除去所含
的二辐化碳,如下式:
(1)计算l g氢氧化锂所能吸收二氧化碳的质量。(计算结果精确到0.01)
(2)若用氢氧化钾代替氢氧化锂,1 g氢氧化钾能吸收多少克二氧化碳?
(3)利用(1)和(2)所得结果判断用氢氧化锂还是用氢氧化钾来吸收二氧化碳更好?为什么?
第二部分(共 30 分)
一、选择题(本题5小题,每小题3分,共15分。每小题有一个或两个选项符合题意,
若有两
个答案的选错一个不得分,漏选l个扣l分):
1.溶液中存在有五种离子,其中各离子个数比Cl— :
为( )
2、如右图所示,烧瓶内盛有X气体,若挤压滴管的胶头a,使液体Y进入烧瓶中,振荡烧
瓶,并倒放在铁架台上,将导管伸入滴有Z的水中,打开弹簧夹b,可见烧杯中液体如喷
泉一样喷入烧瓶中,并出现颜色的改变,则X、y、z可能是( )3.密闭容器内有M、N、Q、Z四种物质,在一定条件下充分反应,测得反应前后个物质的质量
如下表:
下列说法中正确的是( )
A.物质Q一定是化合物,物质Z可能是单质
B.反应后密闭容器中M的质量为29.7g
C。反应过程中,物质N与物质Z变化的质量比为87:36
D.若物质M与物质Q的相对分子质量之比为l97:158,则反应中M与Q的质量比为l:4。
4.某有机物的相对分子质量为46,4.6 g该物质在氧气中充分燃烧生成8.8 g二氧化碳和
5.4 g水,据此判断,该有机物 ( )
A. 只由碳、氢两种元素组成 8. 一定含有碳、氢、氧三种元素
C. 化学式为CH O D. 分子中C、H、O原子个数比为2:6:i
2 2
5.60℃时,化合物甲的溶解度比乙大。分别取等质量60℃时的甲、乙的饱和溶液,降温至
20℃后,析出甲和乙的质量分别为a g和b g(甲、乙均无结晶水)。以下叙述中正确的是( )
A.60℃时等质量的甲饱和溶液与乙饱和溶液相比,前者所含溶质的质量大
B.20℃时,若甲的溶解度与乙的相等,则a一定小于b
C.20℃时,若甲的溶解度仍比乙的大,则a一定小于b
D.20℃时,若甲的溶解度比乙的小,则a一定大于b
二、(本题包括3小题,共l5分)
6.(4分)物质之间既相互联系,又存在某些规律,这是我们学好化学应该掌握的一种
基本方法。请你仿照下表中的示例,找出O 、CH 、CO 、NH 、C H (乙烯)五种气体之
2 4 2 3 2 4
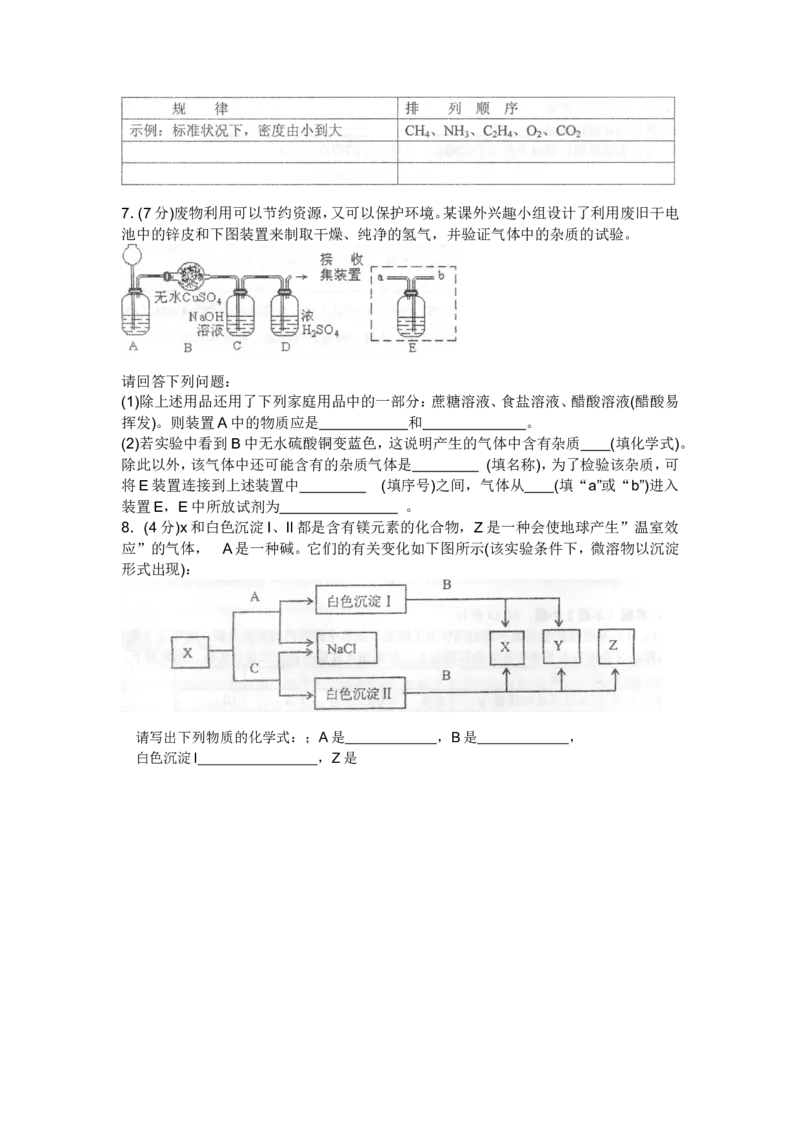
间存在的另外两个规律,并排列出顺序,将答案填在下表中的空格内。7.(7分)废物利用可以节约资源,又可以保护环境。某课外兴趣小组设计了利用废旧干电
池中的锌皮和下图装置来制取干燥、纯净的氢气,并验证气体中的杂质的试验。
请回答下列问题:
(1)除上述用品还用了下列家庭用品中的一部分:蔗糖溶液、食盐溶液、醋酸溶液(醋酸易
挥发)。则装置A中的物质应是 和 。
(2)若实验中看到B中无水硫酸铜变蓝色,这说明产生的气体中含有杂质 (填化学式)。
除此以外,该气体中还可能含有的杂质气体是 (填名称),为了检验该杂质,可
将E装置连接到上述装置中 (填序号)之间,气体从 (填“a”或“b”)进入
装置E,E中所放试剂为 。
8.(4分)x和白色沉淀I、Il都是含有镁元素的化合物,Z是一种会使地球产生”温室效
应”的气体, A是一种碱。它们的有关变化如下图所示(该实验条件下,微溶物以沉淀
形式出现):
请写出下列物质的化学式:;A是 ,B是 ,
白色沉淀l ,Z是2007 初中化学竞赛广东省初赛试题参考答案
第一部分(共 100 分)
一、选择题(本题14小题,每小题2分,共28分):
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 A C B C D B D A C D C B A C
二、填空题(本题包括5小题,共24分):
15.(1)见光受热分解;(1分)(2)I+2KClO =2KIO+Cl;(2分)(3)33.7;(2分)
2 3 3 2
16.2C HO=2CH COOH+O↑;(2分)
2 4 3 3 2
17.Zn H Cu(2分,全部答对才给分)
2
CuO CuSO Cu(2分,全部答对才给分)
4
方案二,(1分)只用试管就可以完成,不需要加热、验纯等操作,(1分)
18.(1)煤、天然气、石油等矿物燃料的燃烧和动植物的呼吸(1分);
(2)光合作用(1分) 水+二氧化碳 葡萄糖+氧气(2分);
19.(7分,方程式每个两分,其余每空1分)HO 溶液的浓度太低,以致于产生的氧气太少
2 2
加热时伴随的水蒸气太多等
① HO 溶液的浓度大小;②干燥(吸水) ③催化作用;2H O 2H O + O
2 2 2 2 2 2
三、(本题包括2小题,共14分):
20.(1)②(1分) ④(1分); Fe O 是红棕色的(1分);FeCl 可溶于水(1分);
2 3 3
碳粉,制造铁钉的铁是铁碳合金(1分);
(2)取少量黑色粉末与稀盐酸反应,观察有无气体放出(1分);
(3)不对,四氧化三铁也能被磁铁吸引(1分);
21.(1)NaOH(1分);过量(1分); 取上层清液,滴入NaOH溶液,无沉淀生成(1分);(2)过
滤(1分); (3)HCl(1分);(4)MgCl Mg+Cl ↑(2分)
2 2
四、(本题包括2小题,共21分):
22.(12分,每小题2分)(1)在常温下,氯气为黄绿色气体,有刺激性气味,能溶于水,密度为
3.21g/L。
(2)氯气与碱反应生成次氯酸盐和金属氯化物。
(3)氯气是由分子构成的,温度升高分子的运动加快,分子之间的距离增大导致压强增大
并超过氯罐的承受极限,故爆炸。
(4)物理变化,因为爆炸后无新物质生成。
(5)用湿布或用尿将衣服尿湿捂住嘴、鼻,迅速逆风跑到新鲜空气的高处。
(6)2NaOH+Cl =NaCl +NaClO+H O
2 2
23.碳酸钙(1分)验证猜想①的方案 将生成的气体通入澄清石灰水(2分)
验证猜想②的方案 往固体中加入稀盐酸,并将生成的气体通入澄清石灰水(2分)
澄清石灰水变浑浊(1分);有气体生成,澄清石灰水变浑浊(1分);Ca(HCO )
3 2
CaCO + HO + CO↑(2分)
3 2 2
五、计算题(本题2小题,共13分):
24.(6分)(1)(2分)第二次实验数据明显有误。因为根据化学方程式中的量比关系,可知当
稀盐酸过量时,二氧化碳的质量应与碳酸钙的质量成正比,即应为:1.76g。
(2)(4分)设2.5g样品中含碳酸钙的质量为x,则:
CaCO + 2HCl == CaCl + CO + HO
3 2 2 2
100 44
X 0.88g
X = 2.0g
故样品中含碳酸钙的质量分数为2.0/2.5× 100%=80%
答:样品中含碳酸钙的质量分数为80%
25.(7分)(1)设1g氢氧化锂能吸收二氧化碳的质量为X
2LiOH + CO = LiCO + HO
2 2 3 2
48 44
1g X
X=0.92g …………(2分)
(2)设1g氢氧化钾能吸收二氧化碳的质量为Y
2KOH + CO = KCO + HO …………(1分)
2 2 3 2
112 44
1g Y
Y=0.39g …………(2分)
(3)用氢氧化锂吸收二氧化碳好。 …………(1分)
因为相同质量的氢氧化锂吸收的二氧化碳更多。…………(1分)
第二部分(共 30 分)
一、(本题5小题,每小题3分,共15分。每小题有一个或两个选项符合题意,若
有两个答案的选错一个不得分,漏选1个扣1分)
题号 1 2 3 4 5
答案 C BD A BD AD
二、(本题包括3小题,共15分)
6.(4分,每空1分)
规 律 排 列 顺 序
相对分子质量,由小到大 CH、NH 、C H、O、CO
4 3 2 4 2 2
每个分子所含原子个数依次增多 O、CO、NH 、CH、C H
2 2 3 4 2 4
7.(7分,每空1分)(1)锌皮 醋酸溶液
(2)HO 醋酸蒸汽 BC b 滴有石蕊试液的水
2
8.(4分,每空1分) NaOH HCl Mg(OH) CO
2 2