文档内容
第 20 讲 盐类水解的影响因素及应用
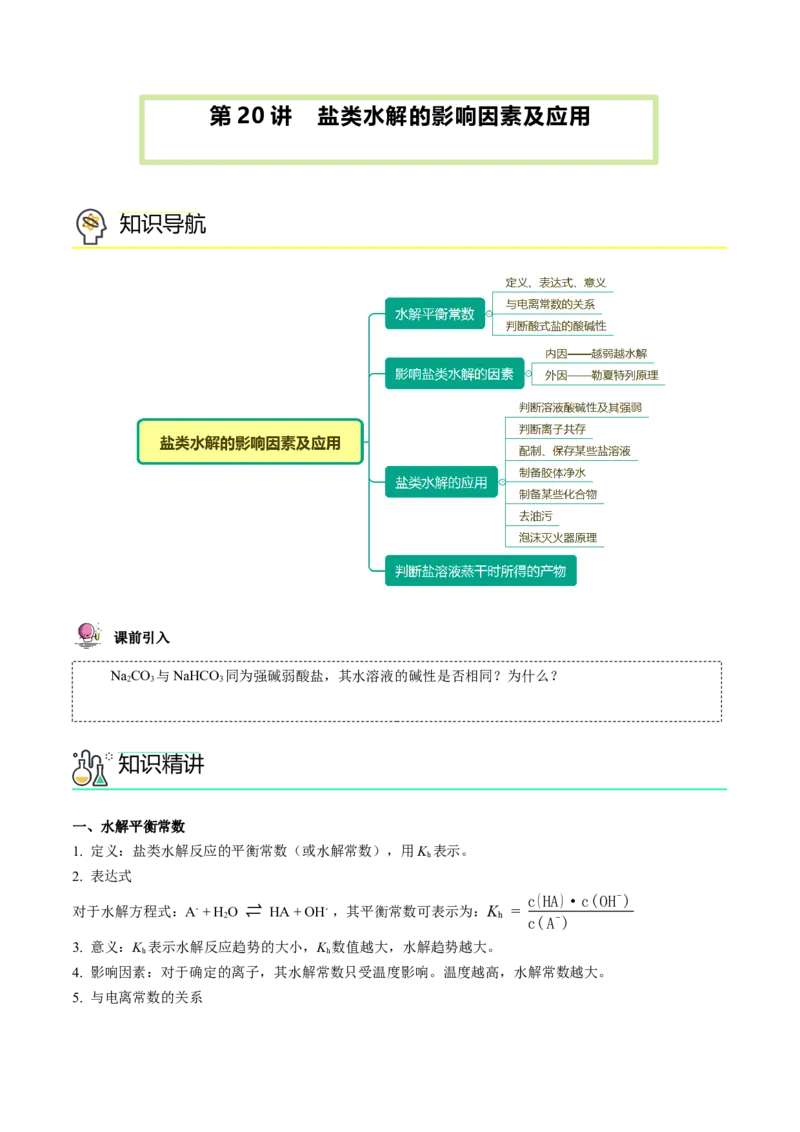
知识导航
小杨老师 15521324728 侵权必究
课前引入
NaCO 与NaHCO 同为强碱弱酸盐,其水溶液的碱性是否相同?为什么?
2 3 3 杨sir化学,侵权必究
知识精讲
小杨老师 15521324728 侵权必究
一、水解平衡常数
1. 定义:盐类水解反应的平衡常数(或水解常数),用K 表示。
h
2. 表达式
c(HA)·c(OH-)
对于水解方程式:A- + H
2
O ⇌ HA + OH- ,其平衡常数可表示为:K
h
=
c(A-)
3. 意义:K 表示水解反应趋势的大小,K 数值越大,水解趋势越大。
h h 杨sir化学,侵权必究
4. 影响因素:对于确定的离子,其水解常数只受温度影响。温度越高,水解常数越大。
5. 与电离常数的关系K K
K = w (K 为弱酸的电离平衡常数)或K = w (K 为弱碱的电离平衡常数)
h K a h K b
a b
二、影响盐类水解的因素
1.内因——盐本身的性质
弱酸阴离子、弱碱阳离子对应的酸、碱越弱,就越易发生水解。
如水解程度(碱性):NaCO _____ NaSO ,NaCO_____NaHCO
2 3 2 3 2 3 3杨sir化学,侵权必究
【答案】> >
及时小练
相同温度下,等物质的量浓度的NaX、NaY、NaZ三种正盐溶液,测得溶液的pH分别是7、9、10。
则相对应的酸HX、HY、HZ的酸性强弱顺序为:_________________。
【答案】HX>HY>HZ
2.外因
因素 水解平衡 水解程度 水解产生离子的浓度
温度 升高 右移 增大 增大
增大 右移 减小 增大
浓度
减小(即稀释) 右移 增大 减小
酸性盐加酸 左移 减小 减小
外加酸碱
酸性盐加碱 右移 增大 增大
酸性盐加酸性盐 相互抑制(如NH Cl中加FeCl )
4 3
外加其他盐
酸性盐加碱性盐 相互促进[如Al (SO ) 中加NaHCO ]
2 4 3 3
三、盐类水解的应用
杨sir化学,侵权必究
应用 举例
判断溶液的酸碱性 FeCl 溶液显酸性,原因是Fe3++3H O Fe(OH) +3H+
3 2 3
判断酸性强弱 NaX、NaY、NaZ三种盐pH分别为7、9、10,则酸性HX>HY>HZ
弱碱阳离子与弱酸阴离子发生完全双水解,则两种离子无法大量共存
①Al3+与HCO、CO、AlO、SiO、HS-、S2-、ClO-
判断离子能否共存
②Fe3+与HCO、CO、AlO、SiO、ClO-
③NH与SiO、AlO
保存、配制某些盐 配制FeCl 溶液时,常加入少量盐酸来抑制FeCl 的水解;
3 3
溶液 盛放NaCO、NaSiO、CHCOONa、NaS等溶液不能用玻璃塞,应用橡胶塞
2 3 2 3 3 2
制取Fe(OH) 胶体:Fe3++3H O Fe(OH) (胶体)+3H+
3 2 3
制取胶体、净水
明矾作净水剂原理:Al3++3H O Al(OH) (胶体)+3H+
2 3
制备化合物 用TiCl 制备TiO:TiCl + (x+2)H O==== TiO·xHO↓+ 4HCl
4 2 4 2 2 2热的纯碱溶液去污能力强:CO+HO HCO+OH-,升高温度,水解平衡右
去油污 2
移,c(OH-)增大
泡沫灭火器原理 成分为NaHCO 与Al (SO ),发生反应为Al3++3HCO- ===Al(OH) ↓+3CO ↑
3 2 4 3 3 3 2
化肥的使用 铵态氮肥与草木灰不得混用
除锈剂 NH Cl与ZnCl 溶液可作焊接时的除锈剂
4 2
四、判断盐溶液蒸干时所得的产物
1. 水解生成难挥发性酸的强碱盐,蒸干后一般得原物质。
如CuSO (aq)蒸干得CuSO ;NaCO(aq)蒸干得NaCO(s)。
4 4 2 3 2 3
2. 水解生成易挥发性酸的强碱盐,一般蒸干后得对应的氢氧化物,灼烧后得对应的氧化物。
如AlCl (aq)蒸干得Al(OH) ,灼烧得Al O。
3 3 2 3 杨sir化学,侵权必究
3. 若该盐受热易分解,蒸干灼烧后一般得到其分解产物。
如 Ca(HCO ) → CaCO (CaO);NaHCO → NaCO ;KMnO → KMnO 和 MnO ;NH Cl → NH 和
3 2 3 3 2 3 4 2 4 2 4 3
HCl。
4. 还原性盐在蒸干时,易被空气中的O 氧化,得到其氧化产物。
2
如NaSO (aq)蒸干得NaSO (s)。
2 3 2 4
对点训练
小杨老师 15521324728 侵权必究
题型一:水解平衡的移动
杨sir化学,侵权必究
【变1-2】对于0.1 mol/L Na CO 溶液,下列说法正确的是
2 3
A.加入NaOH固体,溶液pH减小
B.升高温度,溶液中c(OH-)增大
C.稀释溶液,溶液中c(H+)减少
D.c(Na+)+c(H+) =c( )+c( )+c(OH-)
杨sir化学,侵权必究
【答案】B
【详解】
A. 加入NaOH固体,溶液中氢氧根离子浓度增大,溶液pH增大,A错误;
B. NaCO 溶液水解呈碱性,升高温度,促进盐类水解、促进水电离,溶液中c(OH-)增大,B正确;
2 3
C. 温度不变,水的离子积常数不变,稀释溶液,NaCO 溶液浓度下降,溶液碱性下降,氢氧根离子浓度
2 3
减小,溶液中c(H+)增大,C错误;
D.溶液呈电中性,则 根据电荷守恒得:c(Na+)+c(H+) =c( )+2c( )+c(OH-),D错误;
答案选B。
【变1-5】能证明NaSO 溶液中存在SO +HO HSO +OH-水解平衡事实的是( )
2 3 2
⇌A.滴入酚酞溶液变红,再加入HSO 溶液后红色褪去
2 4
B.滴入酚酞溶液变红,再加入氯水后红色褪去
C.滴入酚酞溶液变红,再加入BaCl 溶液后产生沉淀且红色褪去
2 杨sir化学,侵权必究
D.滴入酚酞溶液变红,再加入NaHSO 溶液后红色褪去
4
【答案】C
【详解】
A.滴入酚酞试液变红,说明亚硫酸钠溶液中氢氧根离子浓度大于氢离子浓度,溶液呈碱性,酚酞在pH大
于8时,呈红色,加入硫酸溶液后,溶液褪色,溶液可能呈酸性越可能呈碱性,若为酸性,不能说明平衡
移动,故A错误;
B.滴入酚酞试液变红,说明溶液中氢氧根离子浓度大于氢离子浓度,氯水具有强氧化性,具有漂白性,
再加入氯水后溶液褪色,不能说明存在水解平衡,故B错误;
C.滴入酚酞试液变红,说明溶液中氢氧根离子浓度大于氢离子浓度,再加入氯化钡溶液后,钡离子和亚
硫酸根离子反应而和亚硫酸氢根离子不反应,钡离子和亚硫酸根离子反应生成亚硫酸钡沉淀,且溶液红色
褪去,所以说明存在水解平衡,故C正确;
D.滴入酚酞试液变红,说明亚硫酸钠溶液中氢氧根离子浓度大于氢离子浓度,溶液呈碱性,酚酞在pH大
于8时,呈红色,加入NaHSO 溶液后,溶液褪色,溶液可能呈酸性越可能呈碱性,若为酸性,不能说明
4
平衡移动,故D错误;
故选C。
【变1-7】下图所示三个烧瓶中分别装入含酚酞的0.01 mol·L-1 CHCOONa溶液,并分别放置在盛有水的
3
烧杯中,然后向烧杯①中加入生石灰,向烧杯③中加入NH NO 晶体,烧杯②中不加任何物质。
4 3
(1)含酚酞的0.01 mol·L-1 CHCOONa溶液显浅红色的原因为__________________(用离子方程式和必要文
3
字解释)。
(2)实验过程中发现烧瓶①中溶液红色变深,烧瓶③中溶液红色变浅,则下列叙述正确的是________(填字
母序号)。
A.水解反应为放热反应 B.水解反应为吸热反应
C.NH NO 溶于水时放出热量 D.NH NO 溶于水时吸收热量
4 3 4 3
(3)向0.01 mol·L-1 CHCOONa溶液中分别加入NaOH固体、NaCO 固体、FeSO 固体,使CHCOO-水解
3 2 3 4 3
平衡移动的方向分别为__________、____________、____________(填“左”、“右”或“不移动”)。
【答案】CHCOO-+HO CHCOOH+OH-,使溶液显碱性 BD 左 左 右
3 2 3
【详解】
(1)CH COONa中CHCOO-水解使溶液显碱性,反应的离子方程式为:CHCOO-+HO CHCOOH+OH
3 3 3 2 3-,酚酞试液遇碱显红色;
(2)生石灰与水剧烈反应放出大量热,根据烧瓶①中溶液红色变深,判断水解平衡向右移动,说明水解反应
是吸热反应,同时烧瓶③中溶液红色变浅,则NH NO 溶于水时吸收热量,故选BD;
4 3
(3)加入NaOH固体,c(OH-)增大,抑制CHCOO-的水解,平衡向左移动; 水解显碱性,与CHCOO
3 3
-的水解相互抑制,平衡向左移动;Fe2+水解显酸性,与CHCOO-的水解相互促进,平衡向右移动。
3
题型二:盐类水解的应用
杨sir化学,侵权必究
【变2-1】实验室配制和保存FeSO 溶液,应采取的正确措施是
4
①把蒸馏水煮沸,以赶走水中溶解的O;②溶解时加入少量稀硫酸;③加入少量铁粉;④加入少量稀盐酸
2
A.①②③ B.①② C.②③ D.②③④
【答案】A
【详解】
①亚铁离子具有极强的还原性,所以把蒸馏水煮沸,以赶走水中溶解的O,故正确;
2
②溶解时加入少量稀HSO ,抑制亚铁离子水解,故正确;
2 4
③为了防止亚铁离子被氧化,加入少量还原铁粉,并充分振荡,故正确;
④加入少量盐酸,引入新杂质氯离子,故错误;
故选A。
【变2-2】下列说法中不正确的有
①氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂;
②测定新制氯水的 时,先用玻璃棒蘸取液体滴在 试纸上,再与标准比色卡对照;
③用米汤直接检验食用盐中是否含有碘元素;
④ 在5.6~7.0之间的降水通常称为酸雨;
⑤加入 溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有 存在;
⑥ 通入紫色石蕊试液,溶液先变红后褪色;
⑦配制一定物质的量浓度的氢氧化钠溶液,用烧杯称量后加蒸馏水溶解,未冷却到室温便转移到容量瓶中,
导致结果偏高;
⑧分解高锰酸钾制氧气后,残留在试管内壁上的黑色物质可用稀盐酸洗涤;
杨sir化学,侵权必究
⑨蒸干 溶液可得纯净的无水氯化铝;
A.5个 B.6个 C.7个 D.8个
【答案】C
【详解】
①氯气与烧碱溶液或石灰乳反应分别生成的NaClO、Ca(ClO) 都是含氯消毒剂,正确;②由于Cl 水中含有
2 2
HClO分子,具有漂白性,故测定新制氯水的 时,不能用pH试纸,应该用pH计,不正确;③加碘盐中加入的是KIO ,故用米汤不能直接检验食用盐中是否含有碘元素,不正确;④酸雨是指pH小于5.6的酸
3
性降雨,不正确;⑤加入 溶液,生成白色沉淀,加稀盐酸沉淀不消失,由于HNO 能将BaSO 氧
3 3
化为BaSO,不可确定有 存在,也可能含有 ,不正确;⑥ 通入紫色石蕊试液,溶液只变红不
4
褪色,不正确;⑦配制一定物质的量浓度的氢氧化钠溶液,用烧杯称量后加蒸馏水溶解,未冷却到室温便
转移到容量瓶中,导致所加溶液体积偏小,故结果偏高,正确;⑧分解高锰酸钾制氧气后,残留在试管内
壁上的黑色物质为MnO 和KMnO ,MnO 与稀盐酸不反应,故不可用稀盐酸洗涤,应该用浓盐酸并加热,
2 2 4 2
不正确;⑨AlCl 水解且生成HCl,故蒸干 溶液HCl挥发,促进水解,直接蒸干AlCl 溶液将得不到
3 3
纯净的无水氯化铝,不正确;综上分析可知,有②③④⑤⑥⑧⑨共7个不正确,故答案为:C。
题型三:盐溶液蒸干后的产物判断
杨sir化学,侵权必究
【例3】 (1)K CO 的水溶液蒸干得到的固体物质是________,原因是_________。
2 3
(2)KAl(SO ) 溶液蒸干得到的固体物质是__________,原因是_____________。
4 2
(3)FeCl 溶液蒸干灼烧得到的固体物质是__________,原因是__________。
2
(4)亚硫酸钠溶液蒸干灼烧得到的固体物质是_______,原因是____________。
(5)将0.5 mol·L-1的NaClO溶液加热蒸干灼烧最后所得的固体是________,原因是_________。
(6)将KMnO 溶液加热蒸干、灼烧最后所得的固体是________,原因是____________。
4
【答案】(1)K CO 尽管加热过程促进水解,但生成的KHCO 和KOH反应后又生成KCO 。
2 3 3 2 3
(2)KAl(SO )·12H O 尽管Al3+水解,但由于HSO 为难挥发性酸,最后仍然为结晶水合物。注意温度过
4 2 2 2 4
高,会脱去结晶水。
(3) Fe O Fe2+水解生成Fe(OH) 和HCl,在加热蒸干过程中HCl挥发,Fe(OH) 逐渐被氧化生成
2 3 2 2
Fe(OH) ,Fe(OH) 灼烧分解生成Fe O。
3 3 2 3
(4) Na SO Na SO 被空气中的O 氧化,发生反应:2NaSO +O=2Na SO 。
2 4 2 3 2 2 3 2 2 4
(5)NaCl NaClO水解的化学方程式为NaClO+HO=NaOH+HClO,2HClO 2HCl+O↑,HCl+
2 2
NaOH=NaCl+HO,故最终得到NaCl。
2
(6)K MnO 、MnO KMnO 加热时发生反应:2KMnO KMnO +MnO +O↑。
2 4 2 4 4 2 4 2 2
【解析】(1)碳酸钾中的碳酸根可以水解,尽管加热过程能促进碳酸钾水解,但生成的碳酸氢钾和氢氧化钾
反应后仍为碳酸钾;(2)明矾中的铝离子可以水解,但是Al3+水解生成氢氧化铝和硫酸,硫酸是高沸点酸,
不能挥发,最后氢氧化铝和硫酸又反应生成Al3+,最后蒸干得到明矾晶体;(3)蒸发FeCl 溶液,Fe2+水解生
2
成Fe(OH) 和HCl,在加热蒸干过程中HCl挥发,得到的是氢氧化亚铁,氢氧化亚铁被氧气氧化为氢氧化
2
铁,灼烧后得到氧化铁;(4)亚硫酸钠在蒸干的过程中不断被空气氧化而变成硫酸钠,所以最后得到的固体
物质是硫酸钠;(5)NaClO溶液加热蒸干,NaClO发生水解生成次氯酸和氢氧化钠,次氯酸受热生成氯化氢
和氧气,根据钠与氯1∶1,则最终生成的氢氧化钠与氯化氢刚好反应生成氯化钠和水,所以最终加热蒸干
最后所得的固体是氯化钠;(6)将KMnO 溶液加热蒸干得到KMnO 固体、灼烧,KMnO 固体分解生成锰酸
4 4 4
钾、二氧化锰和氧气,最后所得的固体为锰酸钾和二氧化锰。题型四:根据K值判断酸碱性
杨sir化学,侵权必究
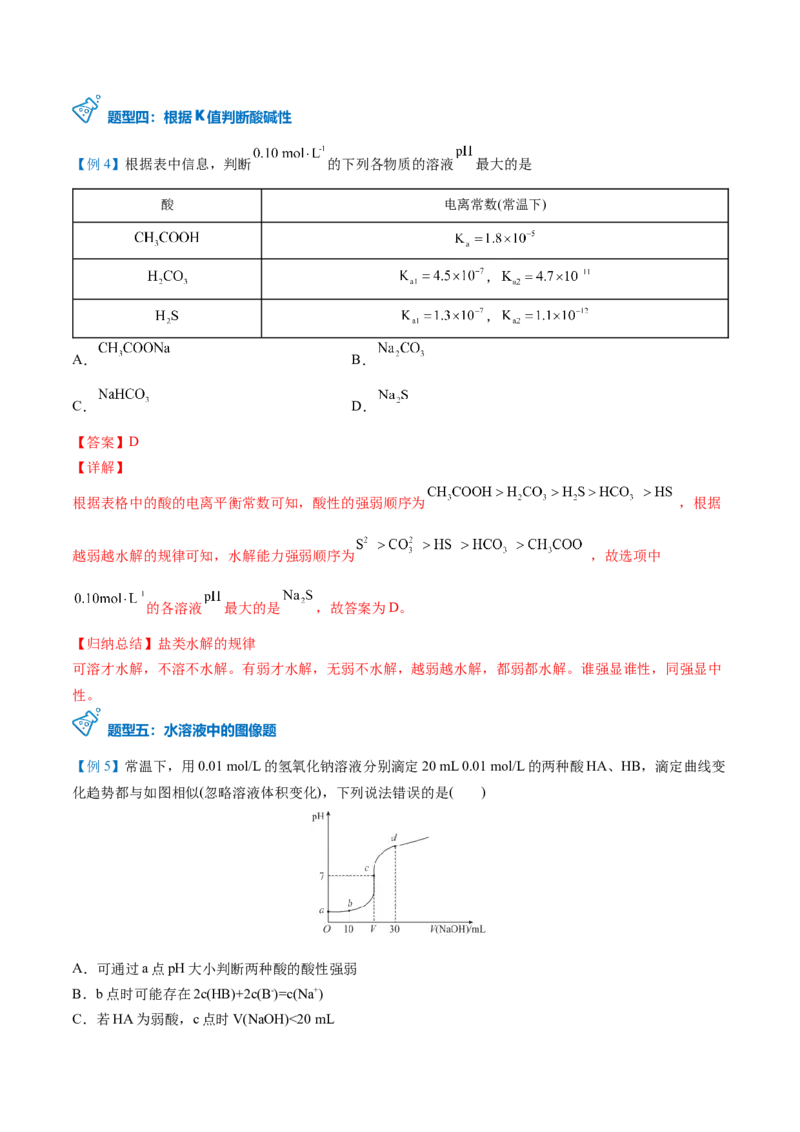
【例4】根据表中信息,判断 的下列各物质的溶液 最大的是
酸 电离常数(常温下)
,
,
A. B.
C. D.
【答案】D
【详解】
根据表格中的酸的电离平衡常数可知,酸性的强弱顺序为 ,根据
越弱越水解的规律可知,水解能力强弱顺序为 ,故选项中
的各溶液 最大的是 ,故答案为D。
【归纳总结】盐类水解的规律
可溶才水解,不溶不水解。有弱才水解,无弱不水解,越弱越水解,都弱都水解。谁强显谁性,同强显中
性。
题型五:水溶液中的图像题
杨sir化学,侵权必究
【例5】常温下,用0.01 mol/L的氢氧化钠溶液分别滴定20 mL 0.01 mol/L的两种酸HA、HB,滴定曲线变
化趋势都与如图相似(忽略溶液体积变化),下列说法错误的是( )
A.可通过a点pH大小判断两种酸的酸性强弱
B.b点时可能存在2c(HB)+2c(B-)=c(Na+)
C.若HA为弱酸,c点时V(NaOH)<20 mLD.d点时可能存在c(A-)=c(B-)c(A2-)>c(OH-)>c(HA-)>>c(H+)
2
D.向HA溶液中滴加相同浓度的NaOH溶液,滴加过程中离子浓度始终满足:c(Na+)+c(H+)=c(OH-)
2
+c(HA-)+2c(A2-)
【答案】CD
【分析】
由图像可知,HA溶液中含有HA、HA-、A2-,则HA为二元弱酸,其电离常数K = ,由图
2 2 2 a1
可知HA、HA-浓度相同时,pH=6,则K =10-6;K = ,由图可知A2-、HA-浓度相同时,
2 a1 a2
pH=10,则K =10-10。
a2
【详解】
A.HA-的电离常数即K =10-10,HA-水解离子方程式为HA-+H O ,HA-的水解常数K= =
a2 2 h
=10-8,则HA-的水解程度大于电离程度,NaHA溶液呈碱性,A项错误;
B.由分析可知K =1×10-6,B项错误;
a1C.A2-的水解程度较小,Na+不水解,因此c(Na+)>c(A2-);A2-水解产生HA-和OH-,水电离还产生OH-,故
c(OH-)>c(HA-);由于水解本质是A2-结合了水电离的H+,因此c(OH-)>c(HA-)>>c(H+),故NaA溶液中离子
2
浓度大小关系为:c(Na+)>c(A2-)>c(OH-)>c(HA-)>>c(H+),C项正确;
D.向HA溶液中滴加相同浓度的NaOH溶液,溶液呈电中性,根据电荷守恒的可得c(Na+)+c(H+)=c(OH-)
2
+c(HA-)+2c(A2-),D项正确;
答案选CD。
【例8】为测定某二元弱酸HA与NaOH溶液反应过程中溶液pH与粒子关系,在25℃时进行实验,向
2
HA溶液中滴加NaOH溶液,混合溶液中lgX[X表示 或 ]随溶液pH的变化关系如图所示。
2
下列说法正确的是
A.直线II中X表示的是
B.当pH=3.81时,溶液中c(HA-):c(HA)=10:1
2
C.0.1 mol·L-1 NaHA溶液中:c(Na+)>c(HA-)>c(HA)>c(A2-)
2
D.当pH=6.91时,对应的溶液中,3c(A2-)=c(Na+)+c(H+)-c(OH-)
【答案】D
【解析】A项,当pH=0时,c(H+)=1mol/L,K = = ,K = =
a1 a2
,由于K <K ,故直线Ⅱ中X表示 ,A错误;B项,当lgX=0时溶液的pH=1.81,带入
a2 a1
K 计算式中可求出K =1×10-1.81,当pH=3.81时,c(H+)=1×10-3.81mol/L,所以有K =1×10-1.81=
a1 a1 a1
=1×10-3.81× ,解得c(HA-):c(H A)=100:1,B错误;C项,与B项同理,可求出
2
K =1×10-6.91>10-7,由此可知HA-的电离能力强于其水解能力,电离生成的c(A2-)比水解生成的c(H A)大,
a2 2C错误;D项,当pH=6.91时,对应的溶液中c(HA-)=c(A2-),又因电荷守恒c(Na+)+c(H+)=c(OH-)+c(HA-)
+2c(A2-),所以3c(A2-)=c(Na+)+c(H+)-c(OH-),D正确;故选D。
题型六:盐类水解综合考查
杨sir化学,侵权必究
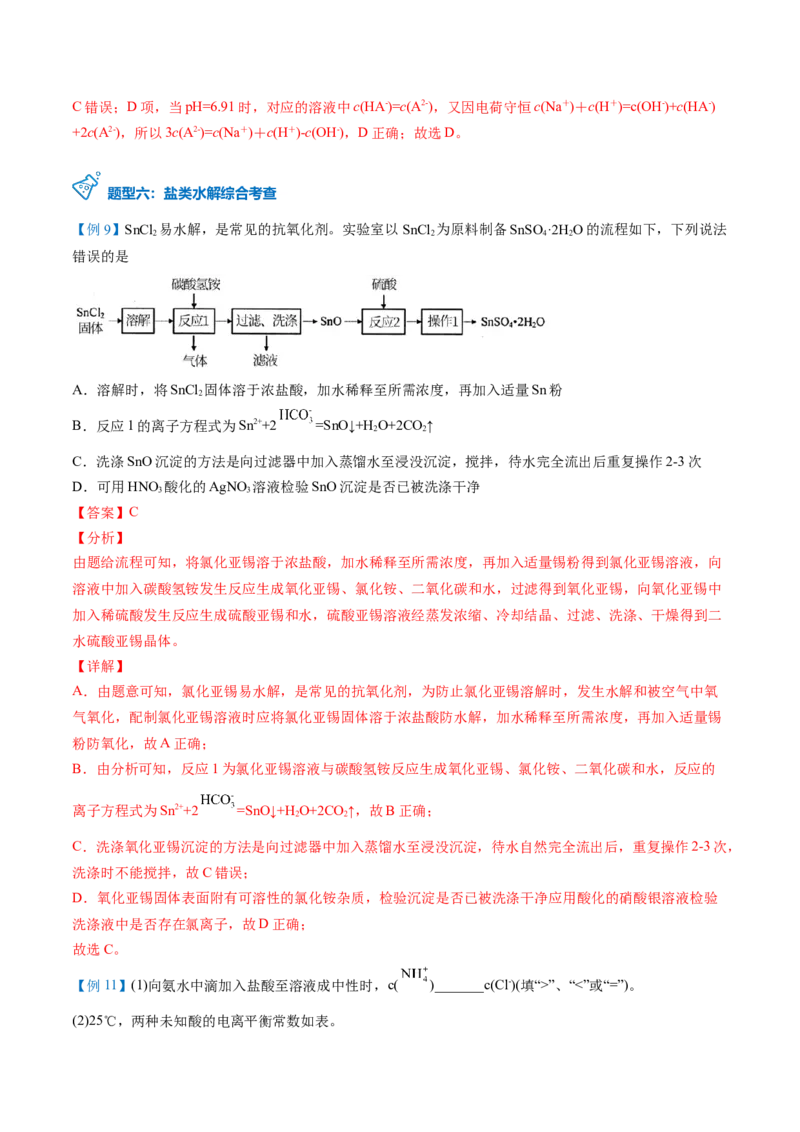
【例9】SnCl 易水解,是常见的抗氧化剂。实验室以SnCl 为原料制备SnSO ·2H O的流程如下,下列说法
2 2 4 2
错误的是
A.溶解时,将SnCl 固体溶于浓盐酸,加水稀释至所需浓度,再加入适量Sn粉
2
B.反应1的离子方程式为Sn2++2 =SnO↓+HO+2CO↑
2 2
C.洗涤SnO沉淀的方法是向过滤器中加入蒸馏水至浸没沉淀,搅拌,待水完全流出后重复操作2-3次
D.可用HNO 酸化的AgNO 溶液检验SnO沉淀是否已被洗涤干净
3 3
【答案】C
【分析】
由题给流程可知,将氯化亚锡溶于浓盐酸,加水稀释至所需浓度,再加入适量锡粉得到氯化亚锡溶液,向
溶液中加入碳酸氢铵发生反应生成氧化亚锡、氯化铵、二氧化碳和水,过滤得到氧化亚锡,向氧化亚锡中
加入稀硫酸发生反应生成硫酸亚锡和水,硫酸亚锡溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥得到二
水硫酸亚锡晶体。
【详解】
A.由题意可知,氯化亚锡易水解,是常见的抗氧化剂,为防止氯化亚锡溶解时,发生水解和被空气中氧
气氧化,配制氯化亚锡溶液时应将氯化亚锡固体溶于浓盐酸防水解,加水稀释至所需浓度,再加入适量锡
粉防氧化,故A正确;
B.由分析可知,反应1为氯化亚锡溶液与碳酸氢铵反应生成氧化亚锡、氯化铵、二氧化碳和水,反应的
离子方程式为Sn2++2 =SnO↓+HO+2CO↑,故B正确;
2 2
C.洗涤氧化亚锡沉淀的方法是向过滤器中加入蒸馏水至浸没沉淀,待水自然完全流出后,重复操作2-3次,
洗涤时不能搅拌,故C错误;
D.氧化亚锡固体表面附有可溶性的氯化铵杂质,检验沉淀是否已被洗涤干净应用酸化的硝酸银溶液检验
洗涤液中是否存在氯离子,故D正确;
故选C。
【例11】(1)向氨水中滴加入盐酸至溶液成中性时,c( )_______c(Cl-)(填“>”、“<”或“=”)。
(2)25℃,两种未知酸的电离平衡常数如表。K K
a1 a2
HXO 1.3×10-2 6.3×10-8
2 3
HYO 4.2×10-7 5.6×10-11
2 3
①HXO 的电离平衡常数表达式K=_______。
②HXO 溶液和NaHYO 溶液反应的主要离子方程式为_______。
2 3 3
③根据HXO 的电离常数数据,判断NaHXO 溶液显_______(选填“酸性”或“碱性”),原因是_______。
2 3 3
(3)已知:重晶石(BaSO)高温煅烧可发生一系列反应,其中部分反应如下:
4
BaSO(s)+4C(s)=BaS(s)+4CO(g) ∆H=+571.2kJ·mol–1
4
BaS(s)=Ba(s)+S(s) ∆H=+460kJ·mol–1
2C(s)+O(g)=2CO(g) ∆H=-221kJ·mol–1
2
则Ba(s)+S(s)+2O (g)=BaSO (s) ∆H=_______。
2 4
(4)在一密闭容器中一定量A、B的混合气体发生反应:aA(g)+bB(g) cC(s)+dD(g),平衡时测得A的
浓度为0.60mol/L,保持温度不变,将容器的容积扩大到原来的3倍,再达平衡时,测得A的浓度降为
0.20mol/L。下列有关判断正确的是_______。
A.平衡向正反应方向移动 B.A的转化率增大
C.D的体积分数增大 D.a+b K (H YO )> K (H XO )> K (H YO ), H XO 溶液和NaHYO 溶液反应的
a1 2 3 a1 2 3 a2 2 3 a2 2 3 2 3 3
主要离子方程式为HXO +HYO =H YO +HXO (或HXO +HYO =H O+YO ↑+HXO );
2 3 2 3 2 3 2 2③根据表中数据可知K (H XO )= 6.3×10-8,NaHXO 既要电离又要水解,水解常数为:
a2 2 3 3
,由计算可知电离大于水解,溶液显酸性,故答案为:酸性;HXO 既要
电离又要水解,HXO +H O=HXO +OH-,设水解常数K ,则 , ,
2 2 3 h2
故NaHXO 溶液显酸性;
3
(3)设①BaSO(s)+4C(s)=BaS(s)+4CO(g) ∆H=+571.2kJ·mol–1
4
②BaS(s)=Ba(s)+S(s) ∆H=+460kJ·mol–1,③2C(s)+O(g)=2CO(g) ∆H=-221kJ·mol–1
2
④Ba(s)+S(s)+2O (g)=BaSO (s)
2 4
根据盖斯定律得 ,
故答案为:-1473.2kJ/mol;
(4)平衡时测得A的浓度为0.60mol/L,将容器的容积扩大到原来的3倍,再达平衡时,测得A的浓度降为
0.20mol/L,说明平衡没有移动,说明该反应aA(g)+bB(g) cC(s)+dD(g)前后气体分子数相等,即
a+b=d,a+bc>d>b BC
【分析】
(1)
铝离子和硫离子在水溶液中会发生双水解生成氢氧化铝沉淀和硫化氢气体,
;
(2)
A. 会和氯化铁、氯化铜都反应,错误;
B.氯化铁水解生成氢氧化铁,加入 可以调节溶液的pH,促进铁离子水解且不引入新杂质,正确;
C. 会和氯化铁、氯化铜都反应,错误;
D.加入 可以调节溶液的pH,促进铁离子水解且不引入新杂质,正确;
故选BD。
(3)
次氯酸根离子水解生成次氯酸,次氯酸受热生成HCl,HCl会与次氯酸钙溶液中水解生成的氢氧化钙得到
氯化钙,故蒸干并灼烧 溶液,得到的产物是CaCl 。
2
(4)
铍和铝元素化学性质相似,则铍离子也容易水解,故从 溶液中得到 固体的操作是在 气流中
加热蒸干 溶液。
(5)
①酸的酸性越强对应酸根离子水解程度越弱,由图表可知,相同浓度的a. 、b. 、c.、d. 酸性由强到弱的顺序是a>c>d>b;
②A.由图表可知,醋酸酸性大于氢氰酸,故反应可以发生,正确;
B.由图表可知,电离程度 > > ,故反应得到碳酸氢钠而不是碳酸钠,错误;
C.电离程度 > > ,故反应得到碳酸氢钠而不是碳酸钠,错误;
D.电离程度 > ,故反应可以发生,正确;
故选BC。
提分作业
小杨老师 15521324728 侵权必究
【练1】关于盐类水解反应的说法正确的是
A.溶液呈中性的盐一定是强酸与强碱生成的盐
B.含有弱酸根离子的盐的水溶液一定呈碱性
C.盐溶液的酸碱性主要决定于形成盐的酸、碱电离程度的相对大小
D.NaS水解的离子方程式为:S2-+2HO HS+2OH-
2 2 2
【答案】C
【详解】
A.溶液呈中性的盐不一定是强酸强碱盐,可能是弱酸弱碱盐,如醋酸铵溶液呈中性,A错误;
B.含有弱酸根离子的盐的水溶液不一定呈碱性,如醋酸铵溶液呈中性,亚硫酸氢钠溶液呈酸性,B错误;
C.盐溶液的酸碱性主要决定于形成盐的酸、碱电离程度的大小,强酸弱碱盐溶液呈酸性,强碱弱酸盐溶
液呈碱性,弱酸弱碱盐水溶液酸碱性决定于形成盐的酸和碱电离程度的大小,C正确;
D.S2-水解离子方程式为S2-+HO HS-+OH-、HS-+HO HS+OH-,D错误;
2 2 2
答案选C。
【练2】在一定条件下,NaCO 溶液存在水解平衡: +H O +OH-,升高温度,c( )
2 3 2
A.增大 B.减小 C.不变 ⇌ D.无法判断
杨sir化学,侵权必究
【答案】B
【详解】
NaCO 溶液存在水解平衡: +H O +OH-,水解过程是吸热反应,升高温度,平衡向正反应方向
2 3 2
⇌
移动,c( )减小,
故选:B。
【练3】相同物质的量浓度NaCN和NaClO相比,NaCN溶液的pH较大,则下列关于同温同体积同浓度的
HCN和HClO溶液的说法中正确的是
A.酸性强弱:HCN>HClOB.pH:HClO>HCN
C.与NaOH恰好完全反应时,消耗NaOH的物质的量:HClO>HCN
D.酸根离子浓度:c(CN-)c(HR-)>c(H R)>c(R2-)
2
B.在NaR溶液中通入足量CO 生成的盐是NaHR和NaHCO
2 2 3杨sir化学,侵权必究
C.1molH R分别与足量的NaOH、NaCO、Na反应消耗三者的物质的量之比为2:1:2
2 2 3
D.25℃时,将等物质的量浓度的NaHR和NaCO 溶液等体积混合,所得溶液中各微粒浓度大小顺序为:
2 3
c(Na+)> c(R2-) >c(HCO )>c(OH-)>c(H+)
【答案】C
【详解】
A. 溶液中 电离常数为 ,水解常数 , 溶液呈酸
性,根据分析,电离大于水解,HR是由于 水解产生的,故c(R2-)>c(H R),A项错误;
2 2
B.根据题中电离常数得到酸性: > ,因此 溶液中通入足量 是不反应的,B项错误;
C. 与足量的 反应消耗2mol ,与 反应消耗1mol ,与 反应消耗
2molNa,因此消耗三者的物质的量之比为2:1:2,C项正确;
D. 溶液中 电离常数为 ,25℃时,NaCO 溶液中 的水解常数
2 3
,则 水解产生的HCO 浓度大于 电离产生的R2-浓度,溶液呈碱
性,因此所得溶液中各离子浓度大小顺序为:c(Na+)>c(HCO )> c(R2-) >c(OH-)>c(H+),D项错误;
答案选C。
【练7】(2021·四川省南充市白塔中学高三期中)常温下,几种弱电解质的电离平衡常数如表所示,向
20mL0.1mol/L的盐酸溶液中逐滴滴加0.1mol/L的氨水,溶液的pH变化曲线如图所示。
弱电解质 K
HCO K =4×10-7 K =4×10-11
2 3 a1 a2
NH·HO K=1.75×10-5
3 2 bCHCOOH K=1.75×10-5
3 a
下列说法正确的是( )
A.CHCOONH 溶液中c(OH-)=c(H+)≠l0-7mol/L
3 4
B.NH +和HCO -能发生彻底水解反应
4 3
C.曲线上水的电离程度最大的点为b点
D.d点时,c(OH-)-c(H+)= [c(NH +)-2c(NH ·H O)]
4 3 2 杨sir化学,侵权必究
【答案】D
【解析】A项,氨水和醋酸的电离常数相同,铵根离子和醋酸根离子都发生水解,促进水的电离,且二者
水解程度相同,所以CHCOONH 溶液中:c(OH-)=c(H+)=10-7mol/L,溶液的pH=7,A错误;B项,NH +和
3 4 4
HCO -可以双水解,但因水解产物溶解度较大,无法脱离溶液,所以反应不彻底, B错误;C项,盐类水
3
解促进水的电离,酸或碱抑制水的电离,加入氨水20mL,恰好生成氯化铵,所以曲线上水的电离程度最
大的点为c点,C错误;D项,d点加入30mL氨水,溶液中存在的氯化铵和氨水比为:2:1,根据电荷守
恒:c(H+)+c(NH +)=c(OH-)+c(Cl-),根据物料守恒:2c[(NH ·H O)+c(NH +)]=3c(Cl-),c(OH-)-c(H+)=c(NH +)-
4 3 2 4 4
c(Cl-),所以c(OH-)-c(H+)= [c(NH +)-2c(NH ·H O)],D正确;故选D。
4 3 2
【练8】(1)Na CO 溶液显_______性,用离子方程式表示其原因为_______。
2 3
(2)FeCl 溶液呈_______(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):_______;实验室在配制
3
FeCl 溶液时,常将FeCl 固体先溶于较浓的盐酸中,_______(填“促进”、“抑制”)其水解,然后再用蒸馏水
3 3
稀释到所需的浓度。
(3)将AlCl 溶液蒸干再灼烧,最后得到的主要固体物质是_______(写化学式,下同);将NaSO 溶液蒸干再
3 2 3
灼烧,最后得到的主要固体物质是_______
【答案】碱 +H O +OH- 酸 Fe3++3H O Fe(OH) +3H+ 抑制 Al O NaSO
2 2 3 2 3 2 4
【分析】 ⇌ ⇌
根据盐在水溶液中发生水解的反应实质进行判断溶液的酸碱性,根据反应的实际离子书写水解方程式,注
意水解方程式是可逆的;利用可逆反应的特点及生成物的性质,判断水解平衡移动的方向,利用平衡移动
判断最终产物。【详解】
(1)Na CO 是强碱弱酸盐,在溶液中 发生水解反应,消耗水电离产生的H+,最终达到平衡时,溶液中
2 3
c(OH-)>c(H+),使溶液显碱性,用离子方程式表示为: +H O +OH-;
2
(2)FeCl 是强酸弱碱盐,在溶液中Fe3+消耗水电离产生的OH-,最终达到平衡时,溶液中c(H+)>c(OH-),溶
3
液呈酸性,用离子方程式表示为:Fe3++3H O Fe(OH) +3H+;
2 3
实验室在配制FeCl 溶液时,常将FeCl 固体先溶于较浓的盐酸中,增大溶液中H+的浓度,使盐的水解平衡
3 3
逆向移动,抑制FeCl 的水解,然后再用蒸馏水稀释到所需的浓度;
3
(3)Fe3+水解产生Fe(OH) 胶体,能够吸附水中悬浮的物质形成沉淀而除去,从而达到净水的目的,其反应
3
原理用离子方程式表示为:Fe3++3HO Fe(OH) (胶体)+3H+;AlCl 溶液在加热时水解生成Al(OH) ,生
2 3 3 3
成的HCl易挥发,蒸干后最终生成Al(OH) ,在灼烧时,Al(OH) 不稳定,分解生成Al O;亚硫酸钠在蒸
3 3 2 3
干的过程中不断被空气氧化而变成硫酸钠,所以最后得到的固体物质是硫酸钠,故答案为:NaSO ,
2 4
NaSO 在蒸干的过程中不断被空气中的O 氧化而变成NaSO 。
2 3 2 2 4
【练9】NH Al(SO ) 是食品加工中最为快捷的食品添加剂,用于焙烤食品;NH HSO 在分析试剂、医药、
4 4 2 4 4
电子工业中用途广泛。请回答下列问题:
(1)NH Al(SO ) 可作净水剂,其原理是__。(用必要的化学用语和相关文字说明)。
4 4 2
(2)相同条件下,0.1mol·L-1NH Al(SO ) 溶液中c( )___(填“等于”、“大于”或“小于”)0.1mol·L-1NH HSO 溶
4 4 2 4 4
液中c( )。
(3)均为0.1mol·L-1的几种电解质溶液的pH随温度变化的曲线如图所示。
杨sir化学,侵权必究
①其中符合0.1mol·L-1NH Al(SO ) 溶液的pH随温度变化的曲线是___(填字母),导致pH随温度变化的原因
4 4 2
是___;
②20℃时,0.1mol·L-1NH Al(SO ) 溶液中2c( )—c( )—3c(Al3+)=____。
4 4 2
(4)室温时,向100mL0.1mol·L-1NH HSO 溶液中滴加0.1mol·L-1NaOH溶液,溶液pH与NaOH溶液体积的
4 4
关系曲线如图所示:试分析图中a、b、c、d四个点,水的电离程度最大的是____点,在b点,溶液中各离子浓度由大到小的排
列顺序是___。
【答案】Al3+在溶液中发生水解反应Al3++3HO Al(OH) +3H+,水解生成的Al(OH) 胶体具有吸附性,
2 3 3
能吸附水中悬浮颗粒产生沉降,从而达到净化水的目的 小于 Ⅰ NH Al(SO ) 溶于水电离出的铵
4 4 2
根离子和铝离子水解使溶液呈酸性,水解反应是吸热反应,升高温度,铵根离子和铝离子的水解程度增大,
氢离子浓度增大,pH减小 10—3 mol·L-1—c(OH-) a c(Na+)>c( )>c( )>c(OH-)=c(H+)
【详解】
(1) NHAl(SO ) 溶于水电离出Al3+,Al3+在溶液中发生水解反应Al3++3HO Al(OH) +3H+,水解生成
4 4 2 2 3
的Al(OH) 胶体具有吸附性,能吸附水中悬浮颗粒产生沉降,从而达到净化水的目的,故答案为:Al3+在
3
溶液中发生水解反应Al3++3HO Al(OH) +3H+,水解生成的Al(OH) 胶体具有吸附性,能吸附水中悬
2 3 3
浮颗粒产生沉降,从而达到净化水的目的;
(2) 相同条件下,氢离子和铝离子均能拟制铵根离子水解,但等浓度的氢离子的抑制程度大于铝离子,则
0.1 mol·L-1NH Al(SO ) 中c( )小于0.1 mol·L-1NH HSO 中c(NH +),故答案为:小于;
4 4 2 4 4 4
(3) ①由于 NH Al(SO ) 溶于水电离出的NH +、Al3+在溶液中水解使溶液显酸性,水解反应是吸热反应,
4 4 2 4
升高温度,平衡向正反应方向移动,溶液中氢离子浓度增大,pH减小,则符合条件的曲线是I,故答案为:
I;NH Al(SO ) 溶于水电离出的铵根离子和铝离子水解使溶液呈酸性,水解反应是吸热反应,升高温度,
4 4 2
铵根离子和铝离子的水解程度增大,氢离子浓度增大,pH减小;
②由图可知,20 ℃时,0.1 mol·L-1NH Al(SO ) 溶液的pH为3,由溶液中的电荷守恒关系2c(SO 2-)+
4 4 2 4
c(OH-) =c(NH +)+c(H+)+3 c(OH-) (Al3+)可得20 ℃时,2c( )—c( )—3c(Al3+)=c(H+)-c(OH-)
4
=10-3 mol·L-1—c(OH-),故答案为:10-3 mol·L-1—c(OH-);
(4) 向100 mL 0.1 mol·L-1 NH HSO 溶液中滴加0.1 mol·L-1 NaOH溶液,发生的反应为H++OH-
4 4
=H O、OH-+NH +=NH·HO,由方程式可知,a点时氢氧化钠溶液恰好中和溶液中氢离子,得到等浓度
2 4 3 2
的硫酸铵和硫酸钠的混合溶液,溶液中的铵根水解促进水的电离;a点之后,铵根离子与氢氧根离子反应
生成抑制水电离的一水合氨,铵根离子浓度越小,促进水的电离程度越小,所以溶液中水的电离程度最大
是a点;由图可知b点时,溶液pH为7,该点为硫酸钠、硫酸铵和一水合氨的混合溶液,则溶液中各离子
浓度由大到小的排列顺序是c(Na+)>c( )>c( )>c(OH-)=c(H+),故答案为:c(Na+)>c( )>c(
)>c(OH-)=c(H+)。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育