文档内容
第六章 化学反应与能量
第一节 化学反应与能量变化
第 1 课时 化学反应与热能
学业要求 核心素养对接
1.知道化学键的断裂与形成是化学反应
中能量变化的主要原因。
通过对化学能与热能的学习培养学生宏
2.知道反应物与生成物总能量的相对高
观辨识与微观探析的能力、变化观念与
低是反应过程中能量变化的决定因素。
平衡思想、证据推理与模型认知的能
力。
3.了解化学能与热能的相互转化。
4.了解能量转化在生产、生活中的应用。
[知 识 梳 理]
知识点一 化学能与热能的相互转化
如图,我们知道有些燃烧反应能够释放出热能,那么其它反应的吸热和放热由什
么决定的?请完成下列知识点:1.吸热反应和放热反应
(1)定义
吸热反应:吸收热量的化学反应;
放热反应:放出热量的化学反应。
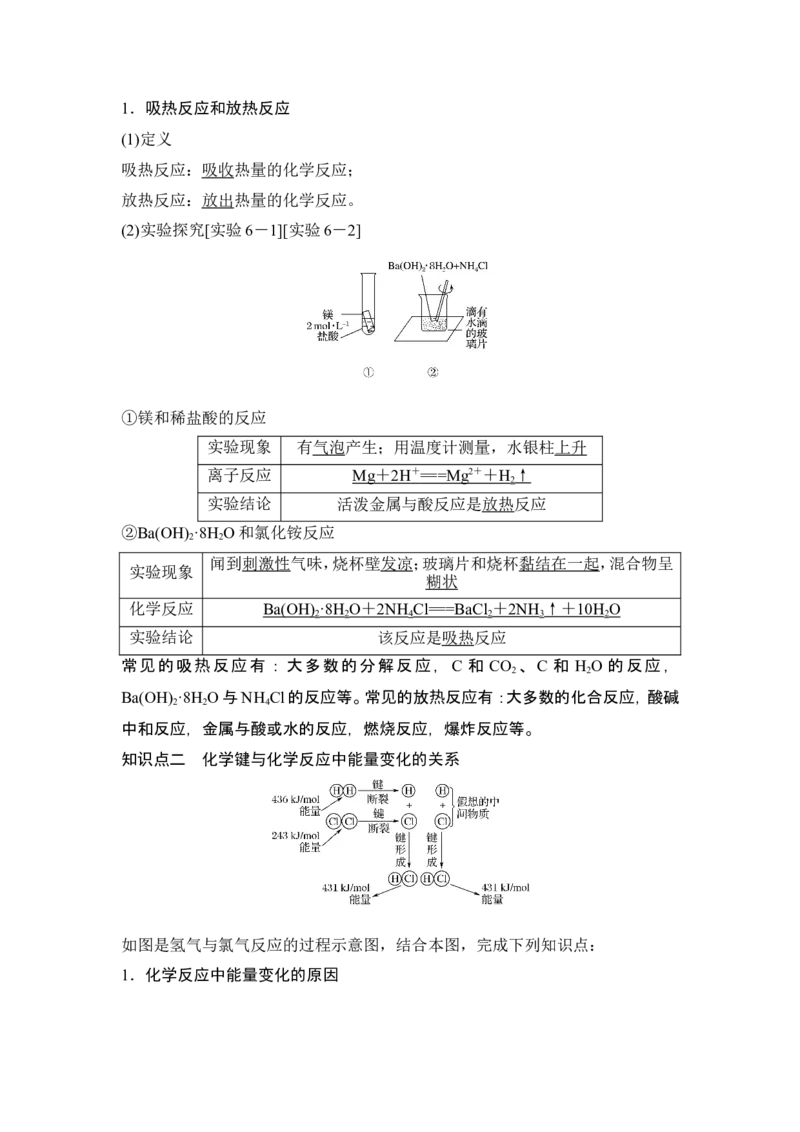
(2)实验探究[实验6-1][实验6-2]
①镁和稀盐酸的反应
实验现象 有气泡产生;用温度计测量,水银柱上升
离子反应 Mg + 2H + == =Mg 2 + + H ↑
2
实验结论 活泼金属与酸反应是放热反应
②Ba(OH) ·8H O和氯化铵反应
2 2
闻到刺激性气味,烧杯壁发凉;玻璃片和烧杯黏结在一起,混合物呈
实验现象
糊状
化学反应 Ba(OH) ·8H O + 2NH Cl == =BaCl + 2NH ↑ + 10H O
2 2 4 2 3 2
实验结论 该反应是吸热反应
常见的吸热反应有:大多数的分解反应,C 和 CO 、C 和 H O 的反应,
2 2
Ba(OH) ·8H O与NH Cl的反应等。常见的放热反应有:大多数的化合反应,酸碱
2 2 4
中和反应,金属与酸或水的反应,燃烧反应,爆炸反应等。
知识点二 化学键与化学反应中能量变化的关系
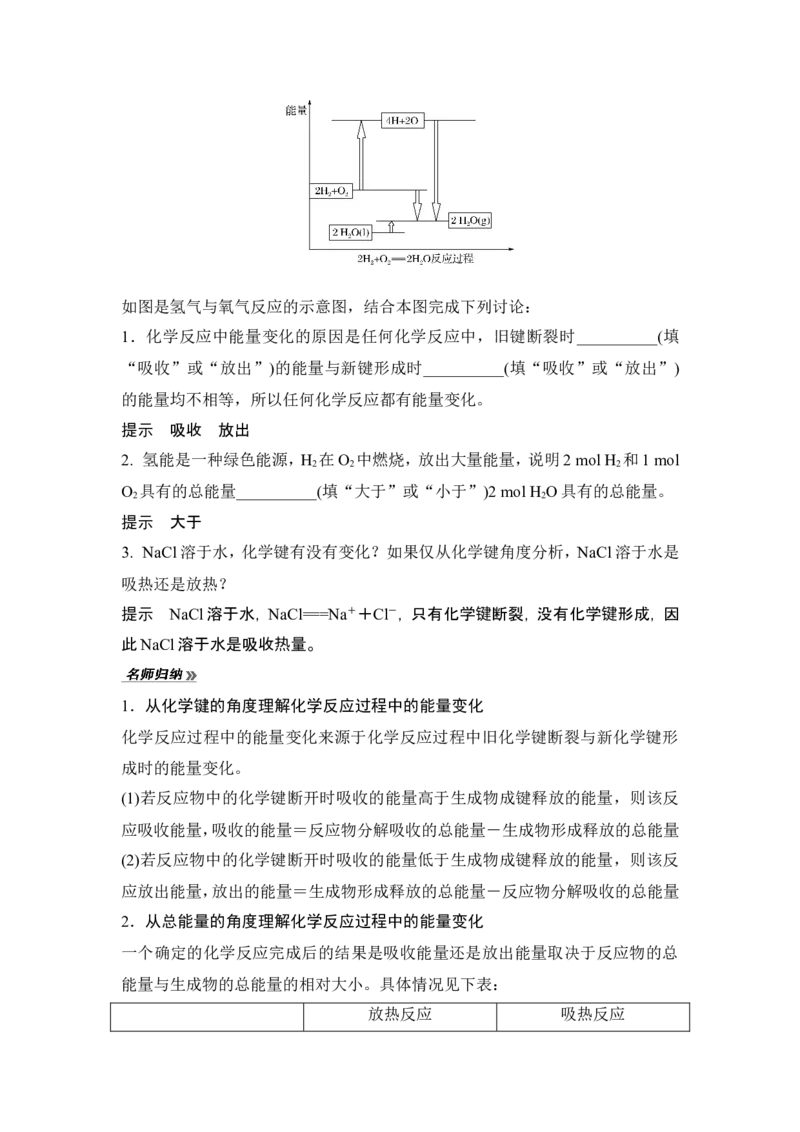
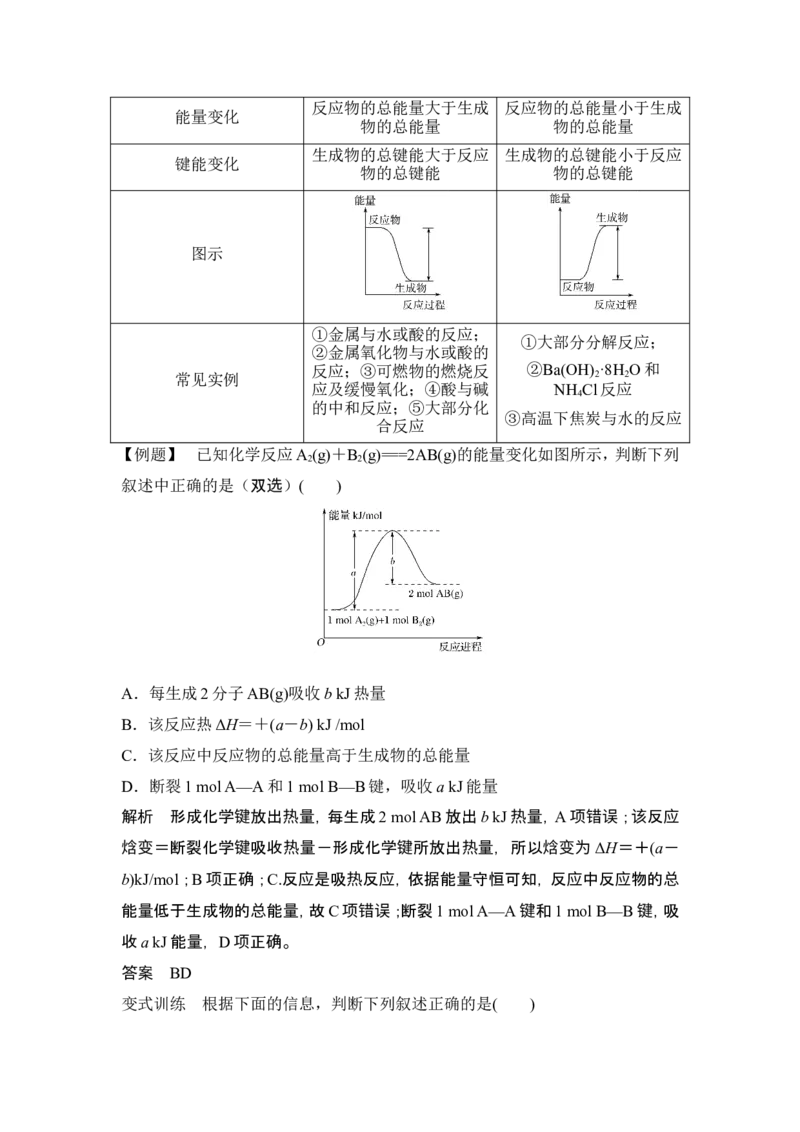
如图是氢气与氯气反应的过程示意图,结合本图,完成下列知识点:
1.化学反应中能量变化的原因可以用键能计算反应类型
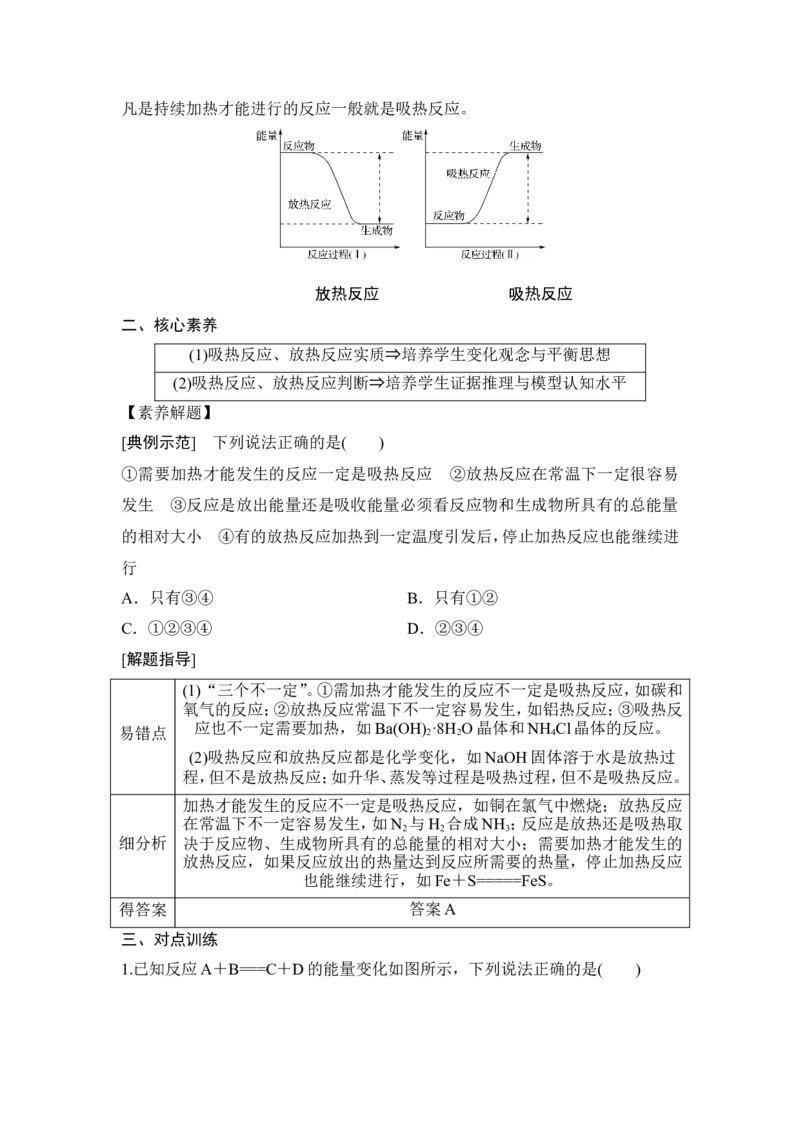
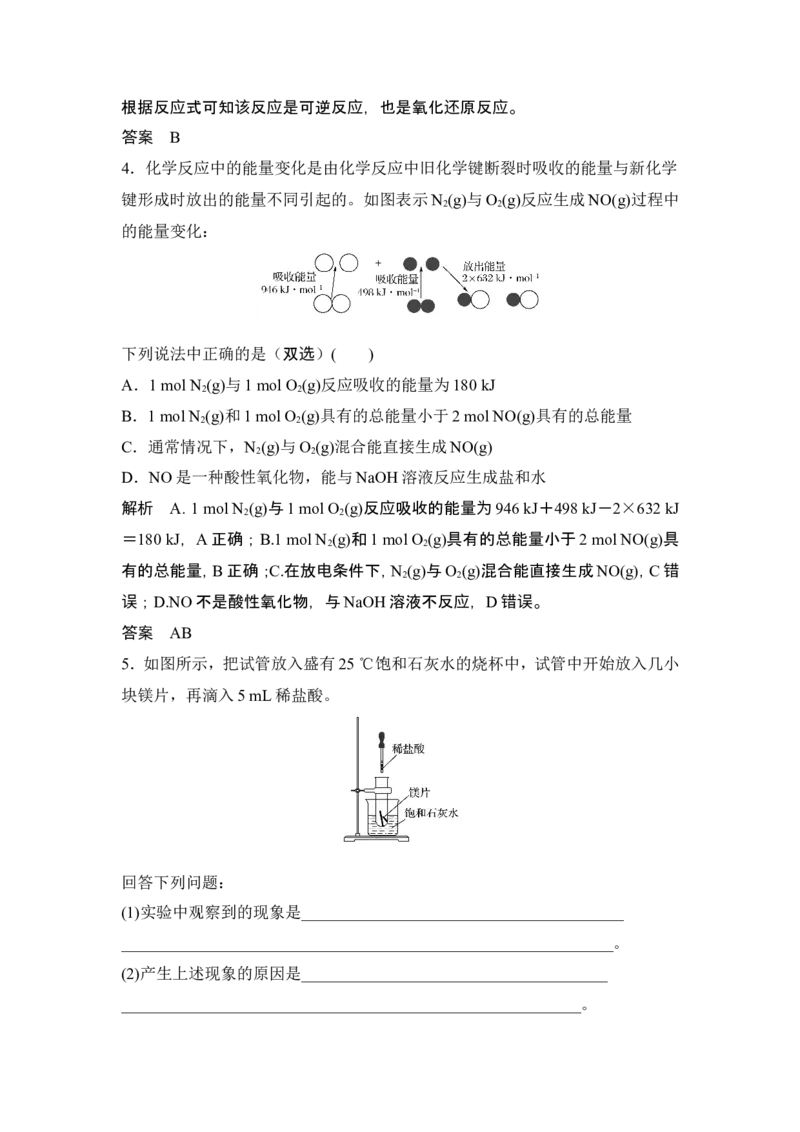
E >E ,反应吸收能量;E E ,则该反应为__________热反应,该反应的过程可看成是“贮存”在
1 2
物质内部的能量转化为________能而被释放出来的过程。
(2)若E 甲>丙
D.氢气和氧气的总能量小于水的能量
解析 根据能量变化可知,1 mol H 与 mol O 断键时吸收685 kJ能量,而生成1
2 2
mol H O放出930 kJ能量,所以H 燃烧生成H O的反应是放热反应,则H O的分
2 2 2 2
解是吸热反应。
答案 C
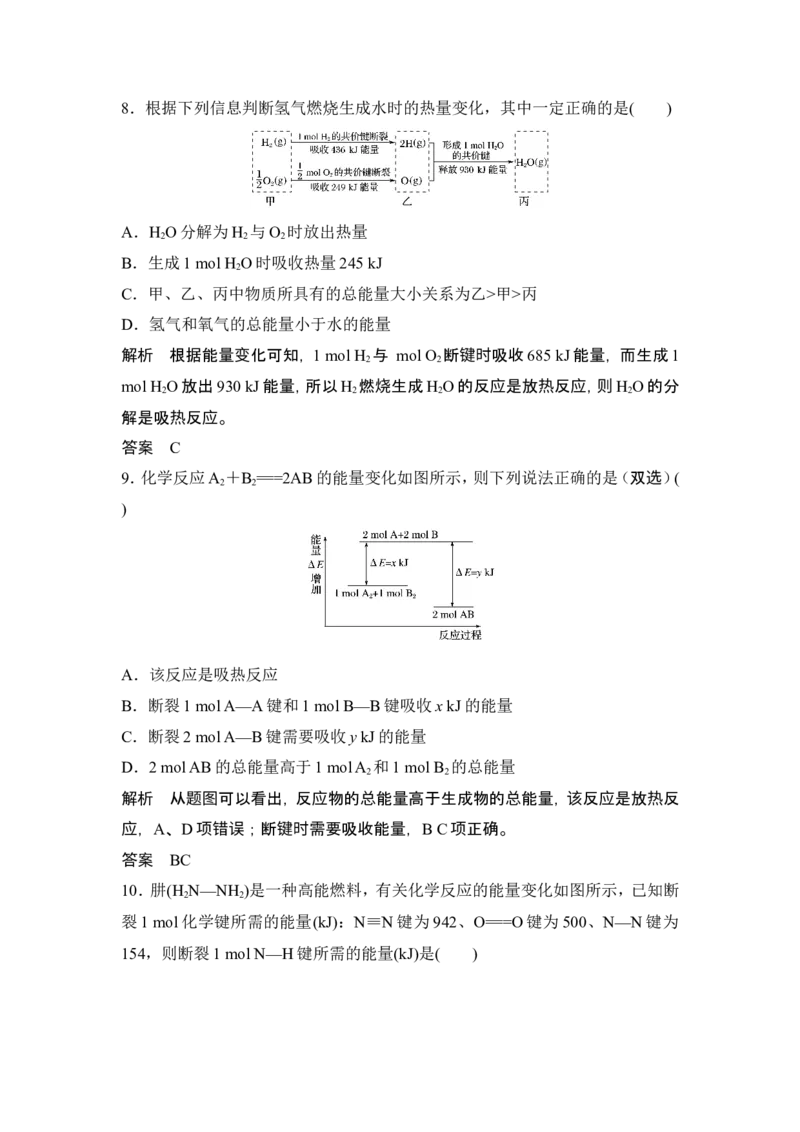
9.化学反应A +B ===2AB的能量变化如图所示,则下列说法正确的是(双选)(
2 2
)
A.该反应是吸热反应
B.断裂1 mol A—A键和1 mol B—B键吸收x kJ的能量
C.断裂2 mol A—B键需要吸收y kJ的能量
D.2 mol AB的总能量高于1 mol A 和1 mol B 的总能量
2 2
解析 从题图可以看出,反应物的总能量高于生成物的总能量,该反应是放热反
应,A、D项错误;断键时需要吸收能量,B C项正确。
答案 BC
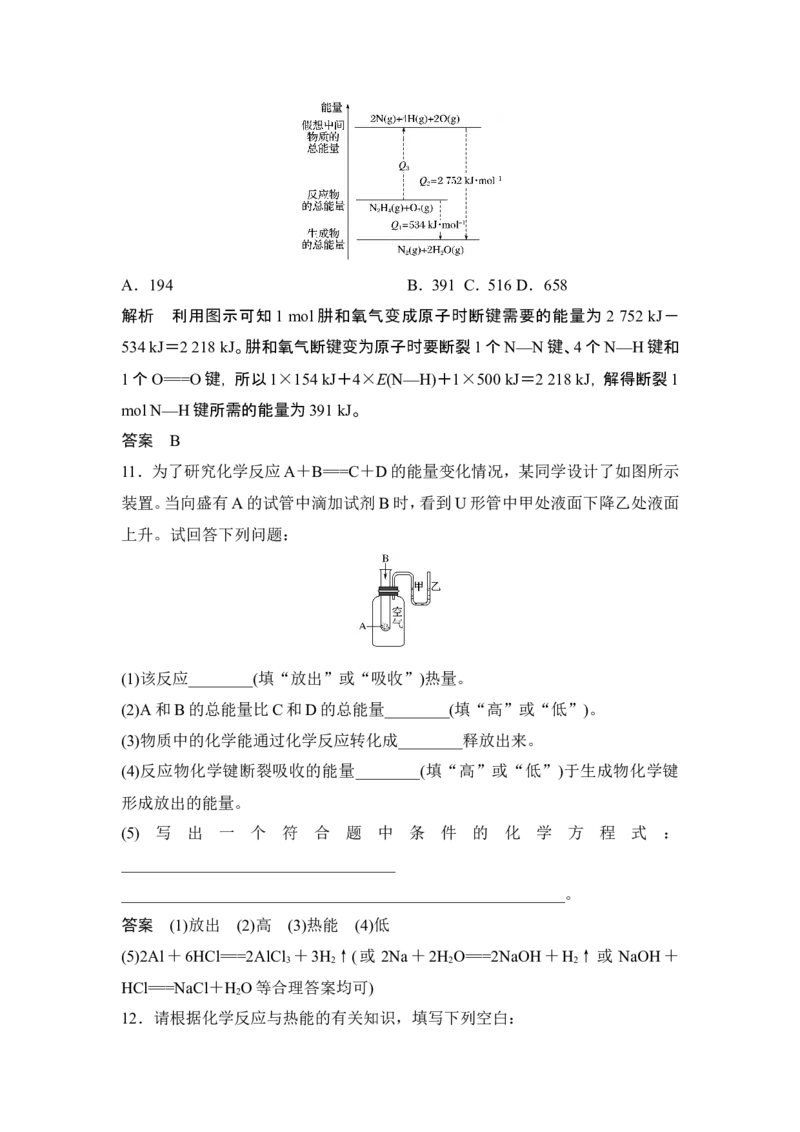
10.肼(H N—NH )是一种高能燃料,有关化学反应的能量变化如图所示,已知断
2 2
裂1 mol化学键所需的能量(kJ):N≡N键为942、O===O键为500、N—N键为
154,则断裂1 mol N—H键所需的能量(kJ)是( )A.194 B.391 C.516 D.658
解析 利用图示可知1 mol肼和氧气变成原子时断键需要的能量为 2 752 kJ-
534 kJ=2 218 kJ。肼和氧气断键变为原子时要断裂1个N—N键、4个N—H键和
1个O===O键,所以1×154 kJ+4×E(N—H)+1×500 kJ=2 218 kJ,解得断裂1
mol N—H键所需的能量为391 kJ。
答案 B
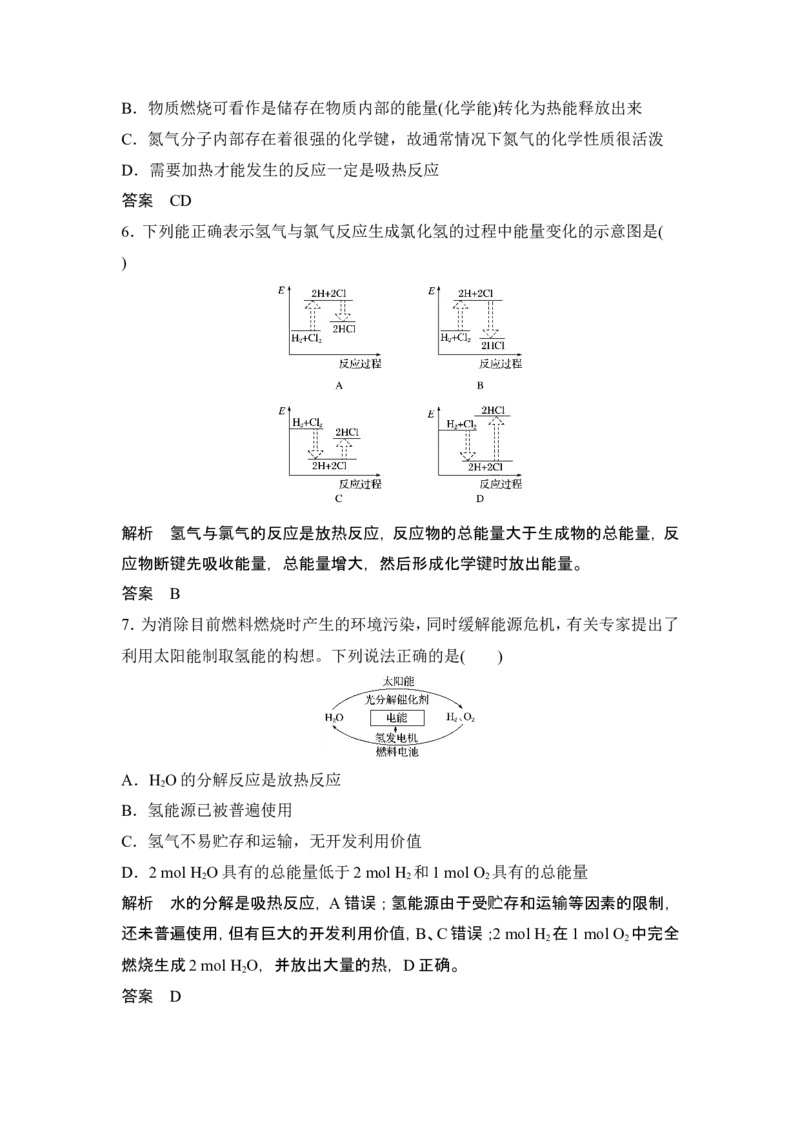
11.为了研究化学反应A+B===C+D的能量变化情况,某同学设计了如图所示
装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面
上升。试回答下列问题:
(1)该反应________(填“放出”或“吸收”)热量。
(2)A和B的总能量比C和D的总能量________(填“高”或“低”)。
(3)物质中的化学能通过化学反应转化成________释放出来。
(4)反应物化学键断裂吸收的能量________(填“高”或“低”)于生成物化学键
形成放出的能量。
(5) 写 出 一 个 符 合 题 中 条 件 的 化 学 方 程 式 :
__________________________________
_______________________________________________________。
答案 (1)放出 (2)高 (3)热能 (4)低
(5)2Al+6HCl===2AlCl +3H ↑(或 2Na+2H O===2NaOH+H ↑或 NaOH+
3 2 2 2
HCl===NaCl+H O等合理答案均可)
2
12.请根据化学反应与热能的有关知识,填写下列空白:(1)在一个小烧杯里,加入20 g Ba(OH) ·8H O粉末,将小烧杯放在事先已滴有4~
2 2
5滴水的玻璃片上。然后加入10 g NH Cl晶体,并用玻璃棒迅速搅拌。
4
① 实 验 中 玻 璃 棒 的 作 用 是
________________________________________________
________________________________________________________________。
②写出有关反应的化学方程式:________________________________________
__________________________________________________________。
③实验中观察到的现象有__________________________________________
_______________________________________________________________和反应
混合物呈糊状。
(2)下列过程中不一定释放能量的是________(填编号)。
①形成化学键 ②燃料燃烧 ③化合反应 ④葡萄糖在体内的氧化反应 ⑤酸
碱中和 ⑥炸药爆炸
(3)等质量的下列物质分别完全燃烧,放出热量较多的是________(填编号)。
①固体硫 ②硫蒸气
(4)已知H 和O 反应放热,且断开1 mol H—H键、1 mol O===O键、1 mol O—H
2 2
键需吸收的能量分别为Q kJ、Q kJ、Q kJ,由此可以推知下列关系正确的是
1 2 3
________(填编号)。
①Q +Q >Q ②Q +Q >2Q
1 2 3 1 2 3
③2Q +Q <4Q ④2Q +Q <2Q
1 2 3 1 2 3
解析 (1)用玻璃棒迅速搅拌,可以知道玻璃棒的作用是搅拌使混合物充分接触
并反应;氯化铵属于铵盐,能和强碱氢氧化钡反应生成氨气、水以及氯化钡,化学
方程式为 Ba(OH) ·8H O+2NH Cl===BaCl +2NH ↑+10H O。氯化铵和
2 2 4 2 3 2
Ba(OH) ·8H O的反应是吸热反应,温度降低能让水结冰,导致烧杯和玻璃片黏在
2 2
一起,同时生成的氨气具有刺激性气味。
(2)一般的化合反应放热,但有的化合反应吸热,如二氧化碳和碳反应生成一氧化
碳。
(3)固态变为气态需要吸收能量,所以硫蒸气的能量大于固体硫,等质量的固体硫
硫蒸气分别完全燃烧,放出热量较多的是硫蒸气。
(4)已知2 mol H 和1 mol O 反应生成2 mol H O,反应断开2 mol H—H键吸收能
2 2 2量2Q kJ、1 mol O===O键吸收能量Q kJ,形成4 mol O—H键放出能量4Q kJ,
1 2 3
总反应放热,则2Q +Q <4Q 。
1 2 3
答案 (1)①搅拌使混合物充分接触并反应
②Ba(OH) ·8H O+2NH Cl===BaCl +2NH ↑+10H O ③玻璃片与烧杯之间结
2 2 4 2 3 2
冰黏在一起,有少许刺激性气味的气体逸出
(2)③ (3)② (4)③
[能 力 练]
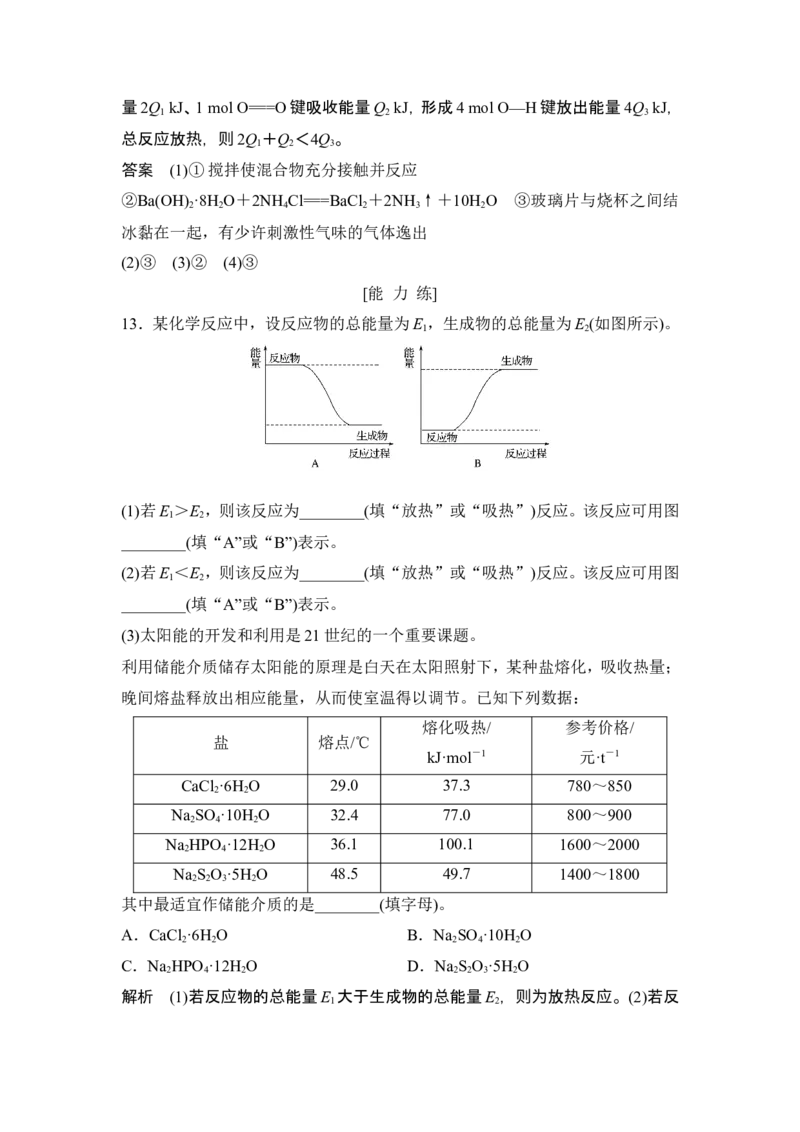
13.某化学反应中,设反应物的总能量为E ,生成物的总能量为E (如图所示)。
1 2
(1)若E >E ,则该反应为________(填“放热”或“吸热”)反应。该反应可用图
1 2
________(填“A”或“B”)表示。
(2)若E <E ,则该反应为________(填“放热”或“吸热”)反应。该反应可用图
1 2
________(填“A”或“B”)表示。
(3)太阳能的开发和利用是21世纪的一个重要课题。
利用储能介质储存太阳能的原理是白天在太阳照射下,某种盐熔化,吸收热量;
晚间熔盐释放出相应能量,从而使室温得以调节。已知下列数据:
熔化吸热/ 参考价格/
盐 熔点/℃
kJ·mol-1 元·t-1
CaCl ·6H O 29.0 37.3 780~850
2 2
Na SO ·10H O 32.4 77.0 800~900
2 4 2
Na HPO ·12H O 36.1 100.1 1600~2000
2 4 2
Na S O ·5H O 48.5 49.7 1400~1800
2 2 3 2
其中最适宜作储能介质的是________(填字母)。
A.CaCl ·6H O B.Na SO ·10H O
2 2 2 4 2
C.Na HPO ·12H O D.Na S O ·5H O
2 4 2 2 2 3 2
解析 (1)若反应物的总能量E 大于生成物的总能量E ,则为放热反应。(2)若反
1 2应物的总能量E 小于生成物的总能量E ,则为吸热反应。(3)选择的物质应该具
1 2
有的特点:白天在太阳照射下,某种盐熔化,熔化时单位质量的物质吸收热量应
该较多,同时价格不能太高,Na SO ·10H O的性价比最高,故选B。
2 4 2
答案 (1)放热 A (2)吸热 B (3)B
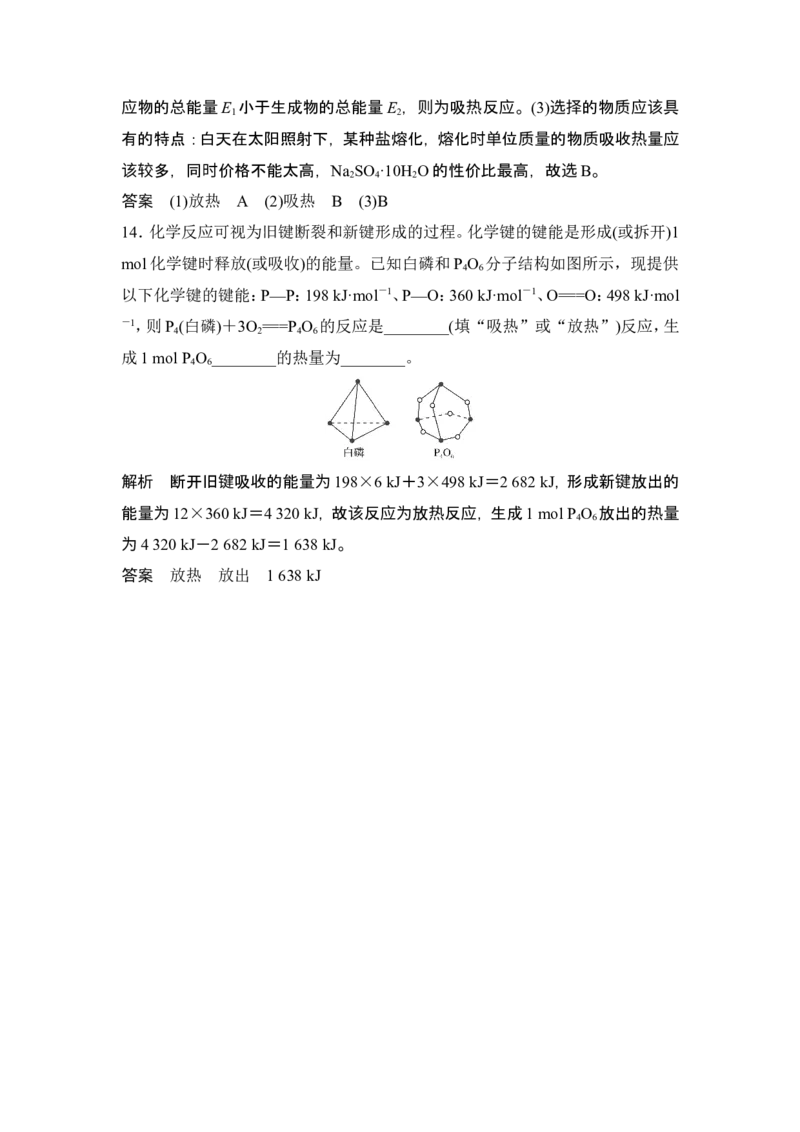
14.化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1
mol化学键时释放(或吸收)的能量。已知白磷和P O 分子结构如图所示,现提供
4 6
以下化学键的键能:P—P:198 kJ·mol-1、P—O:360 kJ·mol-1、O===O:498 kJ·mol
-1,则P (白磷)+3O ===P O 的反应是________(填“吸热”或“放热”)反应,生
4 2 4 6
成1 mol P O ________的热量为________。
4 6
解析 断开旧键吸收的能量为198×6 kJ+3×498 kJ=2 682 kJ,形成新键放出的
能量为12×360 kJ=4 320 kJ,故该反应为放热反应,生成1 mol P O 放出的热量
4 6
为4 320 kJ-2 682 kJ=1 638 kJ。
答案 放热 放出 1 638 kJ