文档内容
第 22 讲 铁盐和亚铁盐
知识导航
知识精讲
一、Fe2+、Fe3+的性质
Fe3+具有较强的氧化性,Fe2+既有氧化性,又有还原性,但以还原性为主。
1. Fe3+的氧化性
①与Fe反应:______________________________。
②与Cu反应:______________________________。(应用:______________)
③与 I- 反应:______________________________。
2. Fe2+的还原性
Fe2+遇Br 、Cl、等均表现还原性
2 2
①与Cl 反应:______________________________。
2
②与HO 反应:______________________________。
2 2
③与MnO -反应:______________________________。
4
二、Fe、Fe2+、Fe3+的转化(铁三角)
1. 转化关系图:2. Fe只有还原性,可以被氧化成+2价或+3价的铁
①Fe能被Fe3+、Cu2+、H+、S等较弱氧化剂氧化为Fe2+
与Fe3+:______________________________________
与Cu2+:______________________________________
与H+:______________________________________
与S:______________________________________
②Fe能被Cl、Br 、HNO、浓HSO 等强氧化剂氧化为Fe3+
2 2 3 2 4
与Cl:______________________________________
2
少量Fe与稀HNO:Fe+4HNO(稀)===Fe(NO)+NO↑+2HO
3 3 3 3 2
3. Fe2+既有氧化性又有还原性,主要表现还原性
①还原性:Fe2+能被Cl、O、HNO、HO、KMnO (H+)等氧化为Fe3+
2 2 3 2 2 4
与Cl:_____________________________________________
2
与O:______________________________________________
2
与HNO:___________________________________________
3
与HO:________ ____________________________________
2 2
与KMnO (H+):______________________________________
4
②氧化性:Fe2+能被Zn、Al、CO、H 等还原为Fe
2
如与Zn:Fe2++Zn===Fe+Zn2+
4. Fe3+具有较强的氧化性
①能被Fe、Cu、S2-(H S)、I-(HI)还原成Fe2+
2
与Fe:______________________________ _______________
与Cu:______________________________________________
与I-(HI):___________________________________________
②能被C、CO、H、Zn等还原成Fe
2
如与Zn反应:2Fe3++3Zn===2Fe+3Zn2+
三、Fe2+、Fe3+的检验
1. 观察法
溶液呈棕黄色,证明含有Fe3+;溶液呈浅绿色,证明含有Fe2+。2. 化学法
盐溶液
Fe2+ Fe3+
添加试剂
NaOH
KSCN
KMnO(H+)
4
淀粉- KI
Cu
思考与交流:如何检验混合溶液中同 时含有Fe2+和Fe3+?
思考与交流:如何检验某溶液 中:①含Fe2+,不含Fe3+;②含Fe3+,不含Fe2+;③既不含Fe3+也不
含Fe2+。
对点训练
题型一:Fe2+、Fe3+的检验
【变1-2】(2021·河北·河间四中高一期中)要 证明某溶液中不含Fe3+而可能含有Fe2+进行如下实验操作时,
最佳顺序为
①加入足量氯水 ②加入足量酸性KMnO 溶液 ③加入少量NH SCN溶液
4 4
A.①③ B.③② C.③① D.①②③
题型二:Fe2+、Fe3+的除杂
【例2】(2021·全国·高一课时练习)要除去F eCl 溶液中少量的FeCl ,可行的方法是
2 3
A.滴入KSCN溶液
B.通入氯气
C.加入适量铜粉并过滤
D.加入适量铁粉并过滤题型三:铁及其化合物
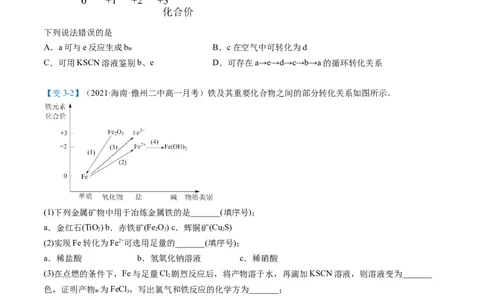
【例3】(2021·全国·高一专题练习)部分含铁物质的分类与相应化合价的关系如图所示。
下列说法错误的是
A.a可与e反应生成b B.c在空气中可转化为d
C.可用KSCN溶液鉴别b、e D.可存在a→e→d→c→b→a的循环转化关系
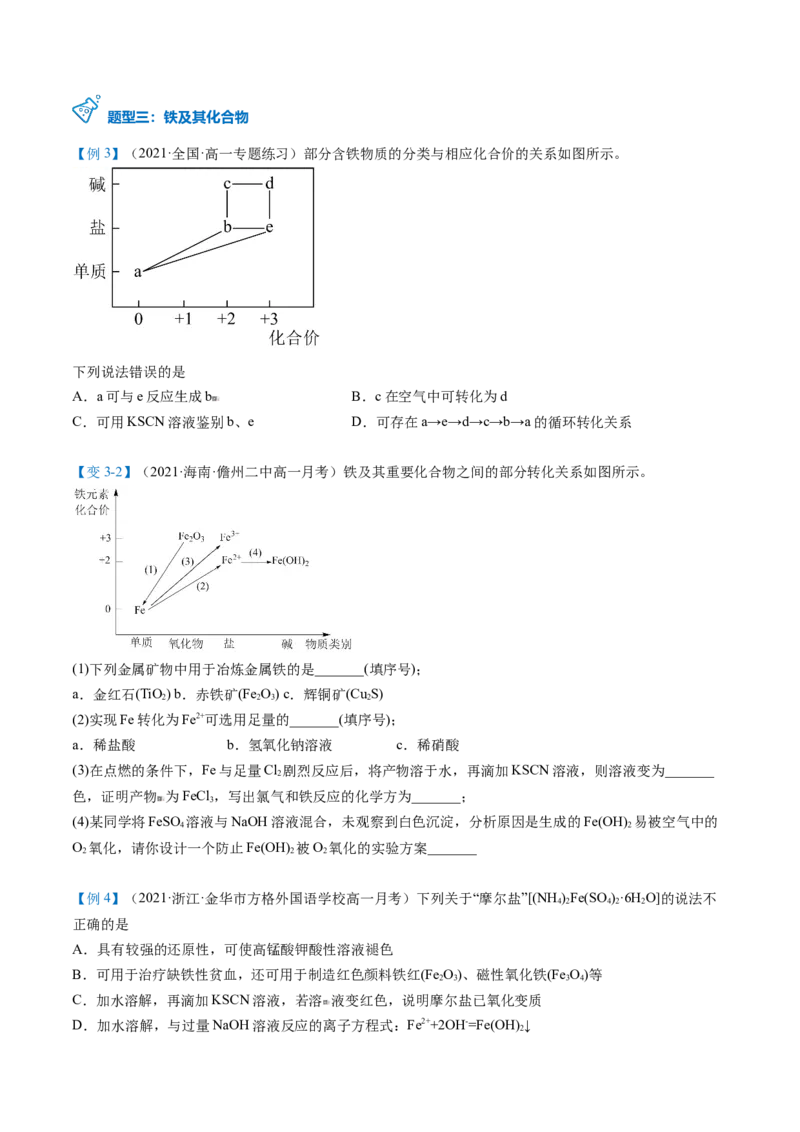
【变3-2】(2021·海南·儋州二中高一月考)铁及其重要化合物之间的部分转化关系如图所示。
(1)下列金属矿物中用于冶炼金属铁的是_______(填序号);
a.金红石(TiO) b.赤铁矿(Fe O) c.辉铜矿(Cu S)
2 2 3 2
(2)实现Fe转化为Fe2+可选用足量的_______(填序号);
a.稀盐酸 b.氢氧化钠溶液 c.稀硝酸
(3)在点燃的条件下,Fe与足量Cl 剧烈反应后,将产物溶于水,再滴加KSCN溶液,则溶液变为_______
2
色,证明产物 为FeCl ,写出氯气和铁反应的化学方为_______;
3
(4)某同学将FeSO 溶液与NaOH溶液混合,未观察到白色沉淀,分析原因是生成的Fe(OH) 易被空气中的
4 2
O 氧化,请你设计一个防止Fe(OH) 被O 氧化的实验方案_______
2 2 2
【例4】(2021·浙江·金华市方格外国语学校高一月考)下列关于“摩尔盐”[(NH )Fe(SO )·6H O]的说法不
4 2 4 2 2
正确的是
A.具有较强的还原性,可使高锰酸钾酸性溶液褪色
B.可用于治疗缺铁性贫血,还可用于制造红色颜料铁红(Fe O)、磁性氧化铁(Fe O)等
2 3 3 4
C.加水溶解,再滴加KSCN溶液,若溶 液变红色,说明摩尔盐已氧化变质
D.加水溶解,与过量NaOH溶液反应的离子方程式:Fe2++2OH-=Fe(OH) ↓
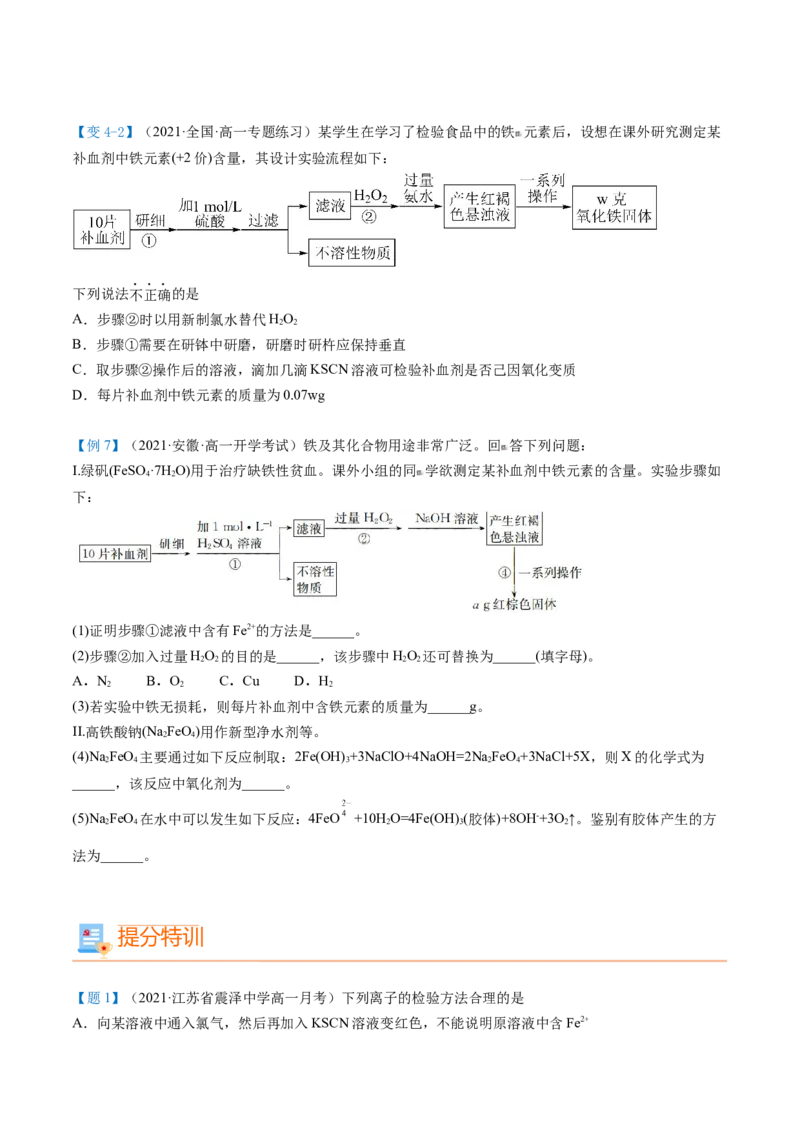
2【变4-2】(2021·全国·高一专题练习)某学生在学习了检验食品中的铁 元素后,设想在课外研究测定某
补血剂中铁元素(+2价)含量,其设计实验流程如下:
下列说法不正确的是
A.步骤②时以用新制氯水替代HO
2 2
B.步骤①需要在研钵中研磨,研磨时研杵应保持垂直
C.取步骤②操作后的溶液,滴加几滴KSCN溶液可检验补血剂是否己因氧化变质
D.每片补血剂中铁元素的质量为0.07wg
【例7】(2021·安徽·高一开学考试)铁及其化合物用途非常广泛。回 答下列问题:
I.绿矾(FeSO ·7H O)用于治疗缺铁性贫血。课外小组的同 学欲测定某补血剂中铁元素的含量。实验步骤如
4 2
下:
(1)证明步骤①滤液中含有Fe2+的方法是______。
(2)步骤②加入过量HO 的目的是______,该步骤中HO 还可替换为______(填字母)。
2 2 2 2
A.N B.O C.Cu D.H
2 2 2
(3)若实验中铁无损耗,则每片补血剂中含铁元素的质量为______g。
II.高铁酸钠(Na FeO)用作新型净水剂等。
2 4
(4)Na FeO 主要通过如下反应制取:2Fe(OH) +3NaClO+4NaOH=2Na FeO+3NaCl+5X,则X的化学式为
2 4 3 2 4
______,该反应中氧化剂为______。
(5)Na FeO 在水中可以发生如下反应:4FeO +10H O=4Fe(OH) (胶体)+8OH-+3O ↑。鉴别有胶体产生的方
2 4 2 3 2
法为______。
提分特训
【题1】(2021·江苏省震泽中学高一月考)下列离子的检验方法合理的是
A.向某溶液中通入氯气,然后再加入KSCN溶液变红色,不能说明原溶液中含Fe2+B.向某溶液中加入NaOH溶液, 最终得到红褐色沉淀,说明溶液中含Fe3+
C.向某溶液中滴加 KSCN溶液呈红色,说明不含Fe2+
D.向某溶液中加入NaOH溶液得白色沉淀,又观察到逐渐变成红褐色,说明只含Fe2+不含Mg2+
【题2】(2021·全国·高一课时练习)将 投入 溶液中,可观察到的现象是
A.生成白色沉淀及气泡 B.生成红褐色沉淀及气泡
C.仅有气泡产生 D.无变化
【题3】(2021·辽宁·高一月考)已知氯气有强氧化性, 能氧化Fe2+、Br-、I-等。又已知还原性I-
>Fe2+>Br-。向含有Fe2+、I-、Br-的溶液中通入一定量氯气后,对所得溶液中离子的成分分析正确的是
A.I-、Fe3+、Cl- B.Fe2+、Cl-、Br-
C.Fe2+、Fe3+、Cl- D.Fe2+、I-、Cl-
【题4】(2020·营口市第二高级中学高一期末)取少量FeCl 溶液,滴入几滴KSCN溶液,不显红色,再
2
滴入几滴氯水,溶液变红,这是因为( )
A.Cl 可将FeCl 还原 B.Cl 可将KSCN氧化
2 2 2
C.Cl 可将FeCl 氧化 D.Cl 可将KSCN还原
2 2 2
【题5】(2021·云南省楚雄天人中学高一月考)由硫铁矿“烧渣”(主要成分:Fe O、Fe O 和FeO)制备绿矾
3 4 2 3
(FeSO ·7H O)的流程如图:已知: FeS(S的化合价为-1)难溶于水。
4 2 2
(1)①中加入的酸为_______,滤渣2的主要成分是_______。
(2)①中生成Fe3+的离子方程式为Fe O+8H+=2Fe3++Fe2++4H O、_______。
3 4 2
(3)检验②中Fe3+已经完全转化成Fe2+的实验方法:取适量溶液2,_______。
(4) 通过③得到绿矾晶体的实验操作:_______、_______、_______、_______、_______。
【题6】(2021·北京·101中学高一期中)某研究小组欲探究 能否与 溶液反应。
(查阅资料)
i. 具有较强的还原性, 具有较强的氧化性。ii. 遇 可生成 , 溶液呈血红色,可用于 的检验。
(提出猜想)
(1)小组同学经过讨论后,认为 溶液可以与 溶液反应,请从化合价的角度加以解释:
___________。
(设计实验)
(2)实验I:在试管中加入 溶液和 溶液,再加入 溶液,发现溶液_____,小组同学认为
和 溶液反应生成了 。
(3)甲同学注意到盛放 溶液的试剂瓶中有空气,因此不同意该结论,他的理由是______。
重新设计实验:
实验II:在试管中加入 溶液,然后加入 溶液,发现溶液无明显变化,再加入 溶液,发现
溶液变红。
(获得结论)
(4)过氧化氢___________(填“能”或者“不能”)氧化 。
(发现异常)
乙同学继续向实验II所得溶液中滴加溶液,发现溶液褪色。
小组同学经过重新查阅资料后,发现可以将 氧化为 。乙同学设计实验III并证实了该资料中的说
法。
(5)补全实验III的方案:在试管中加入 溶液,加入 溶液,再加入___________,产生
___________。
(总结反思)
(6)小组同学经过讨论后,提出了 的检验方法:取待测液于试管中,___________,证明待测液含有
。
(7)从上述实验中可以得出结论,在物 质性质的检验中,应注意___________(至少写出两条)对实验结果
的影响。
提分作业【练1】(2021·四川内江·高一期末)为检验FeCl 溶液中是否含有Fe3+,可选择的试剂是
2
A.稀盐酸 B.AgNO 溶液 C.KSCN溶液 D.HO
3 2 2
【练2】(2021·安徽·池州市江南中学高一期末)证明某溶液只含有Fe2+而不含有Fe3+的实验方法是
A.只需滴加硫氰化钾溶液
B.先滴加硫氰化钾溶液,不显红色,再滴 加氯水后显红色
C.先滴加氯水,再滴加硫氰化钾溶液后显红色
D.滴加氢氧化钠溶液,立即产生红褐色沉淀
【练3】(2020·阜新市第二高级中学高一期末)用FeCl 溶液腐蚀印刷电路板上的铜,所得溶液中加入过
3
量的铁粉,充分反应后,最终溶液中的金属阳离子( )
A.只含Fe2+ B.含Cu2+和Fe2+ C.含Cu2+和Fe3+ D.只含Fe3+
【练4】(2021·山西·太原五中高一月考)下列 各组物质中,能一步实现如图所示①~⑤转化关系的是
选项 X Y Z W
A C CO CO
2
B
C
D
A.A B.B C.C D.D
【练5】(2020·吉林·长春市第二十中学高一月考)铁是一种重要的金属材料,它的单质及化合物在生产生
活中应用广泛。
(1)铁元素有三种常见的氧化物,分别是 FeO、Fe O、Fe O。其中具有磁性的是 _______,可作为红色颜
2 3 3 4
料的是_______。
(2)某补铁口服液中含有 Fe2+,为检验其是否被氧化变质,可取少量该口服液,向其中 滴加 KSCN 溶液,
若溶液变为红色,则说明其已变质。向该口服液中加入维生素 C 可防止其被氧化变质,此过程中利用了
维生素 C 的_______性。
(3)FeCl 可作为铜电路板的腐蚀液,其反应原理为Cu与FeCl 溶液反应生成FeCl 和CuCl ,该反应的化学
3 3 2 2
方程式为_______。向反应后的溶液中加入_______,可回收 Cu,并得到FeCl 溶液。
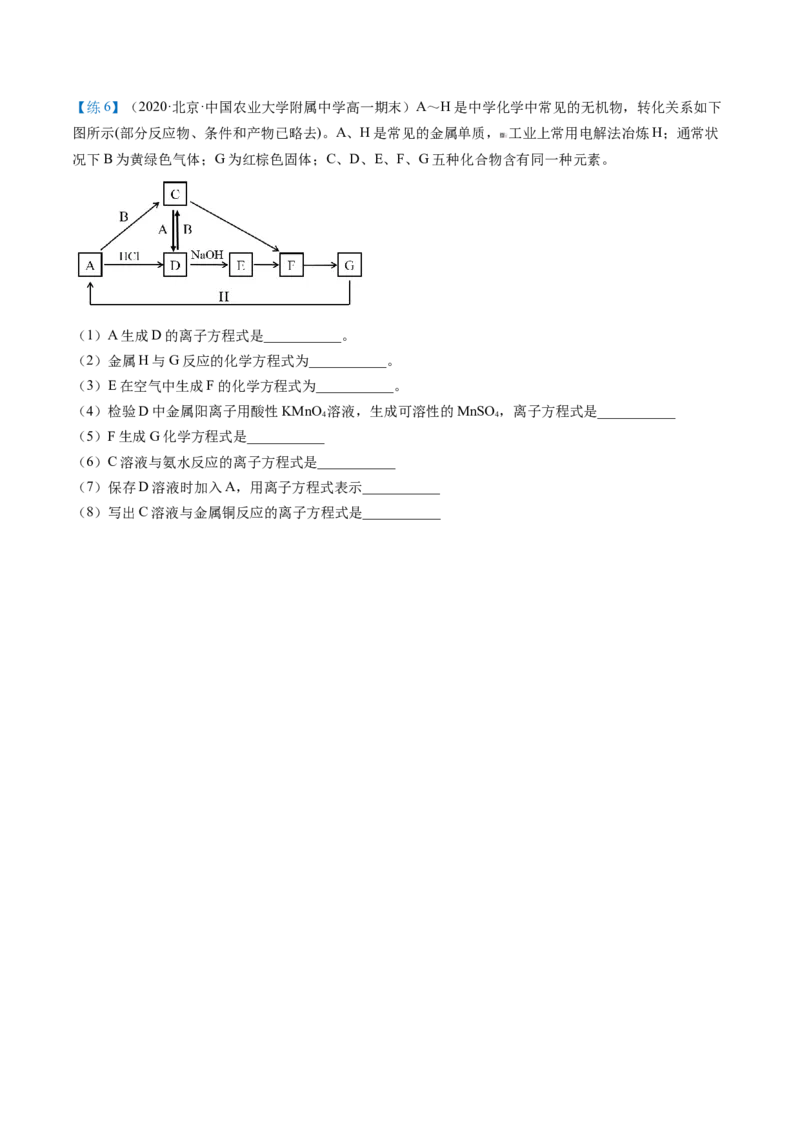
2【练6】(2020·北京·中国农业大学附属中学高一期末)A~H是中学化学中常见的无机物,转化关系如下
图所示(部分反应物、条件和产物已略去)。A、H是常见的金属单质, 工业上常用电解法冶炼H;通常状
况下B为黄绿色气体;G为红棕色固体;C、D、E、F、G五种化合物含有同一种元素。
(1)A生成D的离子方程式是___________。
(2)金属H与G反应的化学方程式为___________。
(3)E在空气中生成F的化学方程式为___________。
(4)检验D中金属阳离子用酸性KMnO 溶液,生成可溶性的MnSO ,离子方程式是___________
4 4
(5)F生成G化学方程式是___________
(6)C溶液与氨水反应的离子方程式是___________
(7)保存D溶液时加入A,用离子方程式表示___________
(8)写出C溶液与金属铜反应的离子方程式是___________关注更新免费领取,淘宝唯一每月更新店铺:知二教育