文档内容
课时素养评价 十二
氯气的实验室制法 氯离子的检验
(30分钟 50分)
一、选择题(本题包括3小题,每小题8分,共24分)
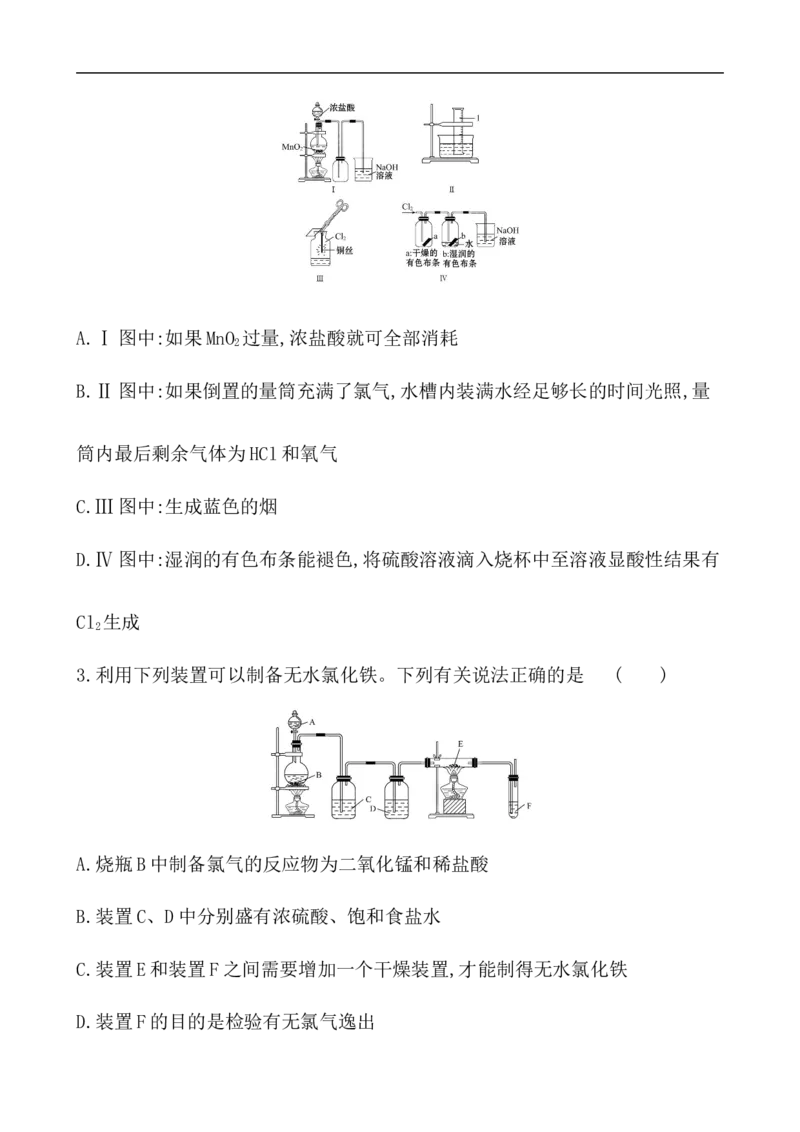
1.在实验室中用浓盐酸与MnO 共热制取Cl 并进行相关实验。下列收集Cl 的正
2 2 2
确装置是 ( )
【互动探究】C装置中倒置的漏斗的作用是什么?
【补偿训练】
1.某实验室的尾气中含有较多的氯气,有毒,要吸收这些尾气,下列试剂最
适合的是 ( )
A.饱和的石灰水 B.饱和的食盐水
C.自来水 D.烧碱溶液
2.检验Cl-时所用试剂HNO 的作用是 ( )
3
A.防止C 的干扰
B.防止Cl-的干扰C.生成Ag CO 沉淀
2 3
D.防止N 的干扰
2.(2019·济南高一检测)下列离子方程式书写正确的是 ( )
A.氯气与水反应
Cl +H O 2H++Cl-+ClO-
2 2
B.二氧化锰与浓盐酸共热制Cl
2
MnO +4H++2Cl- Mn2++Cl ↑+2H O
2 2 2
C.向氯化亚铁溶液中通入氯气
Fe2++Cl Fe3++2Cl-
2
D.向稀漂白粉溶液中通入足量二氧化碳
Ca2++2ClO-+CO +H O CaCO ↓+2HClO
2 2 3
【补偿训练】
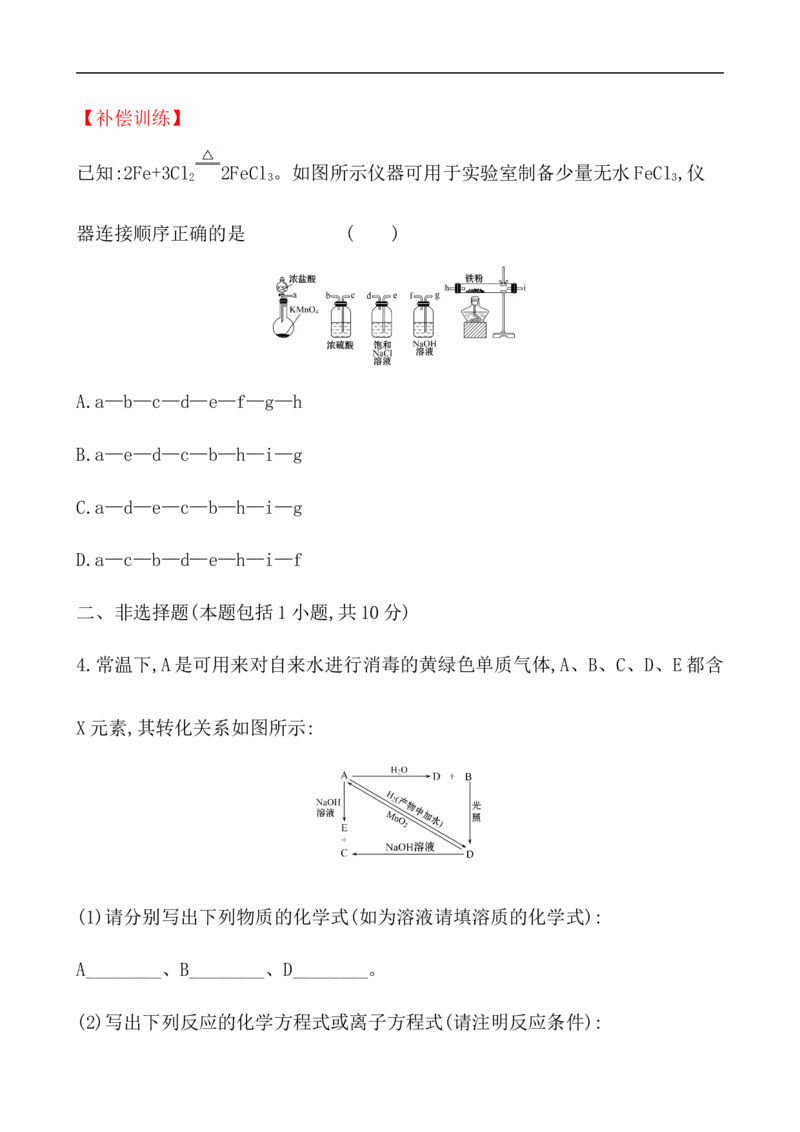
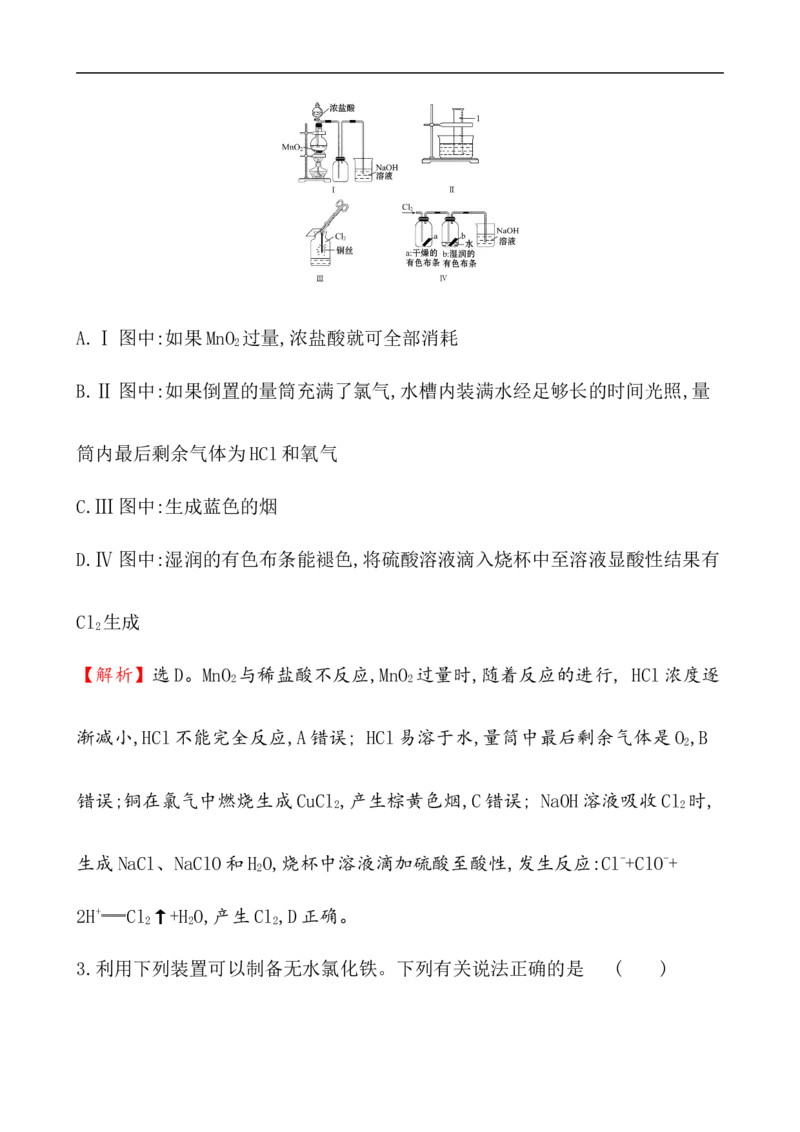
(2019·大同高一检测)某同学用下列装置制备并检验Cl 的性质。下列说
2
法正确的是 ( )A.Ⅰ图中:如果MnO 过量,浓盐酸就可全部消耗
2
B.Ⅱ图中:如果倒置的量筒充满了氯气,水槽内装满水经足够长的时间光照,量
筒内最后剩余气体为HCl和氧气
C.Ⅲ图中:生成蓝色的烟
D.Ⅳ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中至溶液显酸性结果有
Cl 生成
2
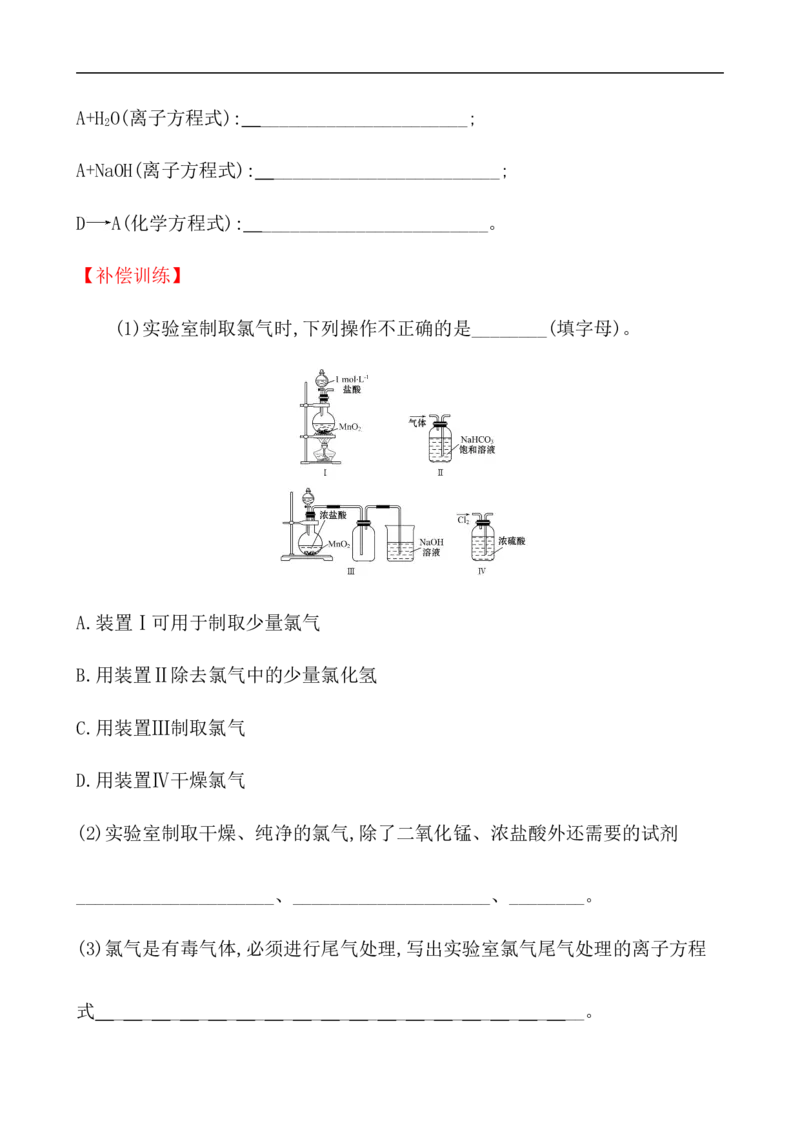
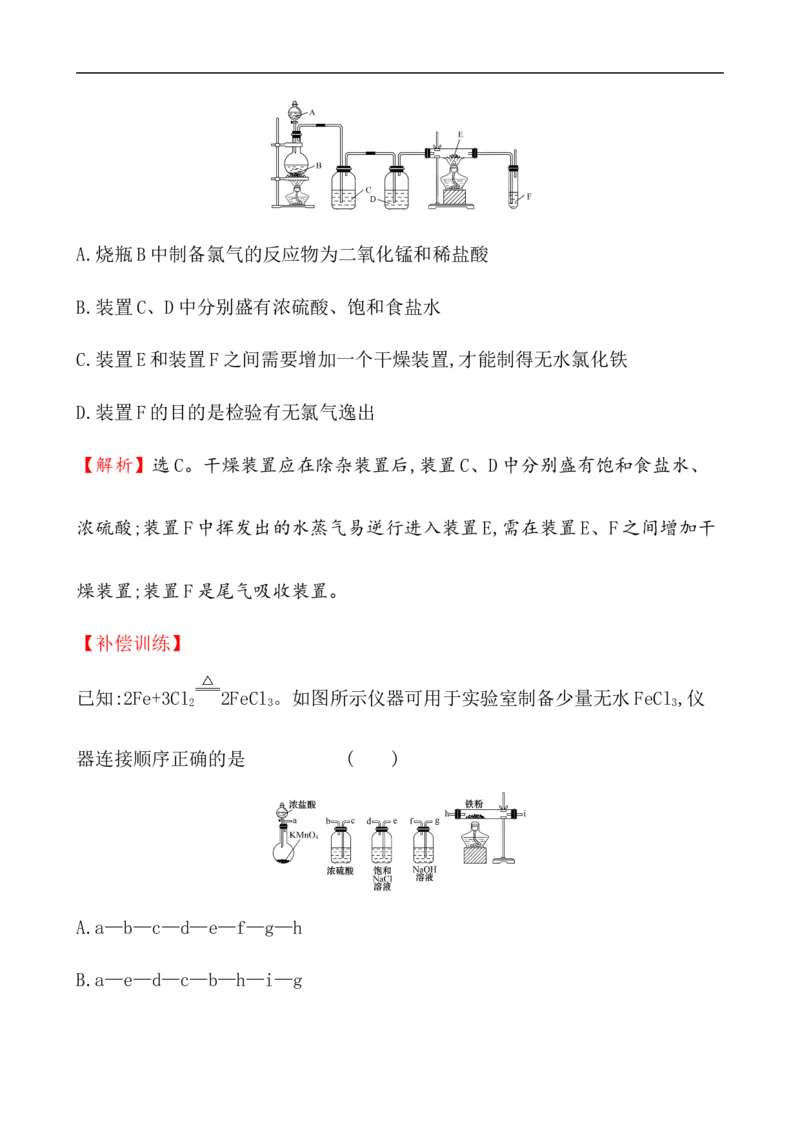
3.利用下列装置可以制备无水氯化铁。下列有关说法正确的是 ( )
A.烧瓶B中制备氯气的反应物为二氧化锰和稀盐酸
B.装置C、D中分别盛有浓硫酸、饱和食盐水
C.装置E和装置F之间需要增加一个干燥装置,才能制得无水氯化铁
D.装置F的目的是检验有无氯气逸出【补偿训练】
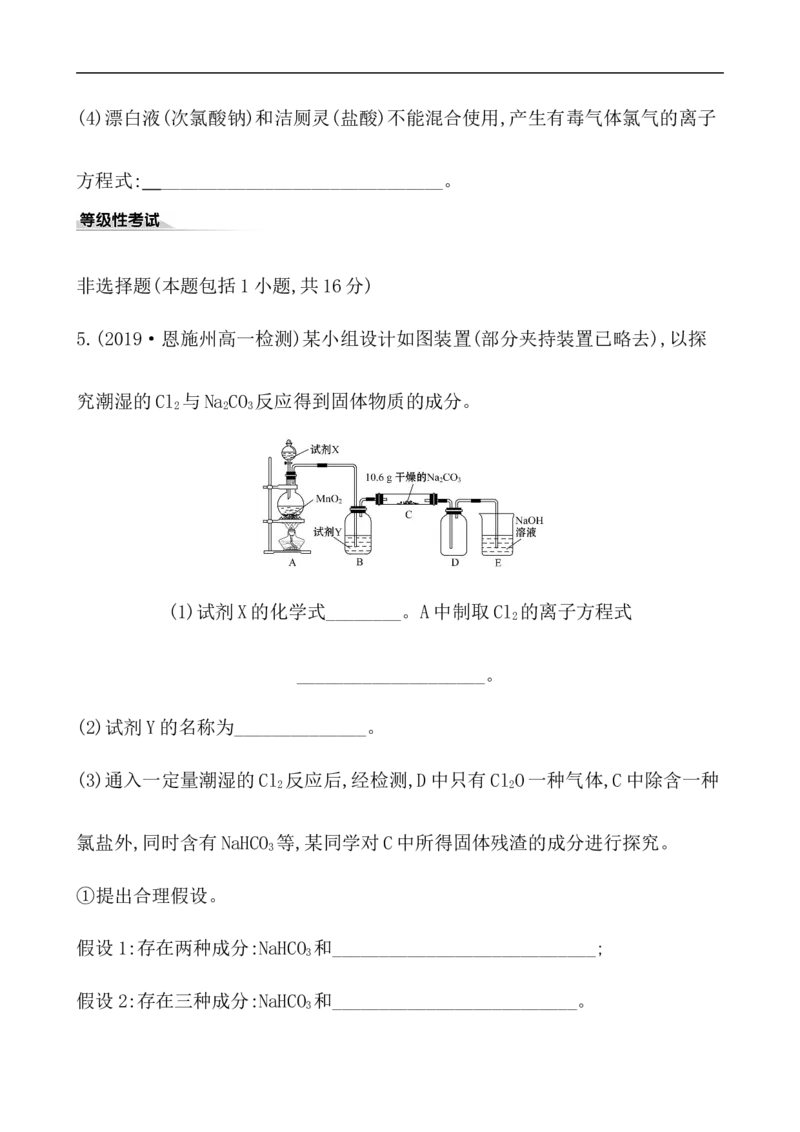
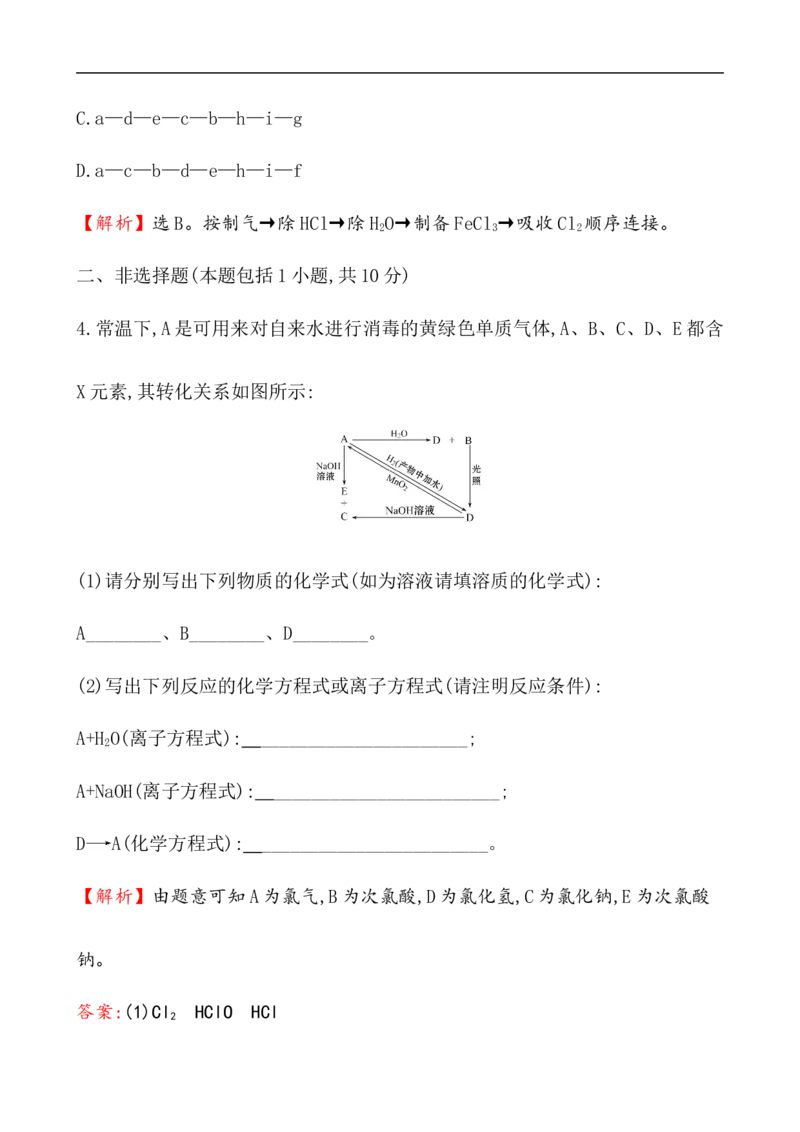
已知:2Fe+3Cl 2FeCl 。如图所示仪器可用于实验室制备少量无水FeCl ,仪
2 3 3
器连接顺序正确的是 ( )
A.a—b—c—d—e—f—g—h
B.a—e—d—c—b—h—i—g
C.a—d—e—c—b—h—i—g
D.a—c—b—d—e—h—i—f
二、非选择题(本题包括1小题,共10分)
4.常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E都含
X元素,其转化关系如图所示:
(1)请分别写出下列物质的化学式(如为溶液请填溶质的化学式):
A________、B________、D________。
(2)写出下列反应的化学方程式或离子方程式(请注明反应条件):A+H O(离子方程式): ______________________;
2
A+NaOH(离子方程式): ________________________;
D A(化学方程式): ________________________。
【补偿训练】
(1)实验室制取氯气时,下列操作不正确的是________(填字母)。
A.装置Ⅰ可用于制取少量氯气
B.用装置Ⅱ除去氯气中的少量氯化氢
C.用装置Ⅲ制取氯气
D.用装置Ⅳ干燥氯气
(2)实验室制取干燥、纯净的氯气,除了二氧化锰、浓盐酸外还需要的试剂
_____________________、_____________________、________。
(3)氯气是有毒气体,必须进行尾气处理,写出实验室氯气尾气处理的离子方程
式 _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ __。(4)漂白液(次氯酸钠)和洁厕灵(盐酸)不能混合使用,产生有毒气体氯气的离子
方程式: ______________________________。
非选择题(本题包括1小题,共16分)
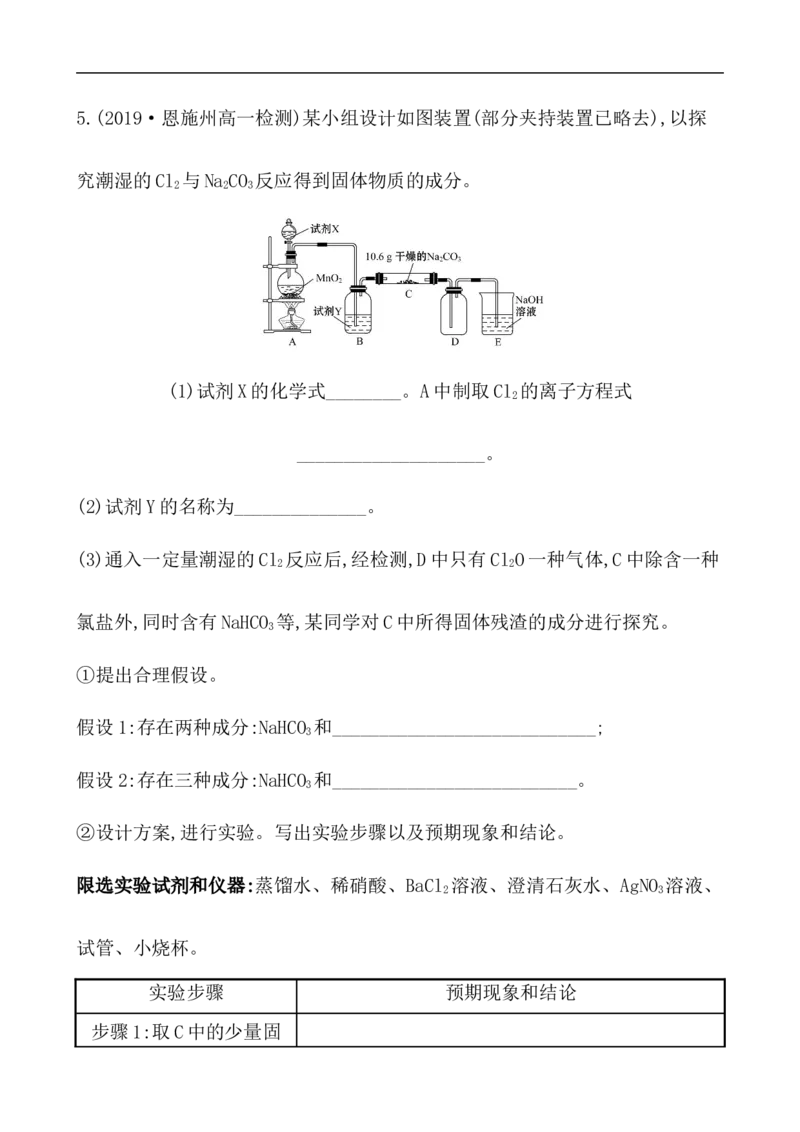
5.(2019·恩施州高一检测)某小组设计如图装置(部分夹持装置已略去),以探
究潮湿的Cl 与Na CO 反应得到固体物质的成分。
2 2 3
(1)试剂X的化学式________。A中制取Cl 的离子方程式
2
____________________。
(2)试剂Y的名称为______________。
(3)通入一定量潮湿的Cl 反应后,经检测,D中只有Cl O一种气体,C中除含一种
2 2
氯盐外,同时含有NaHCO 等,某同学对C中所得固体残渣的成分进行探究。
3
①提出合理假设。
假设1:存在两种成分:NaHCO 和____________________________;
3
假设2:存在三种成分:NaHCO 和__________________________。
3②设计方案,进行实验。写出实验步骤以及预期现象和结论。
限选实验试剂和仪器:蒸馏水、稀硝酸、BaCl 溶液、澄清石灰水、AgNO 溶液、
2 3
试管、小烧杯。
实验步骤 预期现象和结论
步骤1:取C中的少量固
体样品于试管中,滴加足
量蒸馏水至固体溶解,然
后将所得溶液分别置于
A、B试管中
步骤2:向A试管中滴加
BaCl 溶液
2
步骤3:
(4)已知Cl O与水反应生成次氯酸,则D中Cl O进入E反应的化学方程式为
2 2
____________。课时素养评价 十二
氯气的实验室制法 氯离子的检验
(30分钟 50分)
一、选择题(本题包括3小题,每小题8分,共24分)
1.在实验室中用浓盐酸与MnO 共热制取Cl 并进行相关实验。下列收集Cl 的正
2 2 2
确装置是 ( )
【解析】选C。集气瓶中使用单孔橡胶塞塞紧,只能进气,不能排气,则瓶内压强
增大到一定程度,可能将橡胶塞压出,A项错误;因为Cl 比空气的密度大,Cl 应
2 2
短管进,B项错误;该装置既能收集Cl ,又能进行尾气处理且防倒吸,C项正确;由
2
于Cl 和NaOH反应,所以不能收集到Cl ,D项错误。
2 2
【互动探究】C装置中倒置的漏斗的作用是什么?
提示:防止倒吸。
【补偿训练】1.某实验室的尾气中含有较多的氯气,有毒,要吸收这些尾气,下列试剂最
适合的是 ( )
A.饱和的石灰水 B.饱和的食盐水
C.自来水 D.烧碱溶液
【解析】选D。虽然氯气能与饱和石灰水反应,但相同条件下,氢氧化钠的溶解
度大于氢氧化钙的溶解度,吸收效果烧碱溶液更好,A项错误、D项正确;饱和食
盐水中氯离子浓度达到最大,抑制氯气的溶解,则吸收效果最不好,B项错误;自
来水中含有氯离子,将抑制氯气的溶解,且氯气的溶解度较小,用水吸收效果不
好,C项错误。
2.检验Cl-时所用试剂HNO 的作用是 ( )
3
A.防止C 的干扰
B.防止Cl-的干扰
C.生成Ag CO 沉淀
2 3
D.防止N 的干扰【解析】选A。检验Cl-加入的AgNO 溶液,能与C 结合生成Ag CO 白色沉淀,
3 2 3
干扰Cl-的检验。
2.(2019·济南高一检测)下列离子方程式书写正确的是 ( )
A.氯气与水反应
Cl +H O 2H++Cl-+ClO-
2 2
B.二氧化锰与浓盐酸共热制Cl
2
MnO +4H++2Cl- Mn2++Cl ↑+2H O
2 2 2
C.向氯化亚铁溶液中通入氯气
Fe2++Cl Fe3++2Cl-
2
D.向稀漂白粉溶液中通入足量二氧化碳
Ca2++2ClO-+CO +H O CaCO ↓+2HClO
2 2 3
【解析】选B。A中HClO是弱酸,不能改写成ClO-和H+;C中得失电子不守恒;D
中CO 足量,应生成Ca(HCO ) 。
2 3 2
【补偿训练】
(2019·大同高一检测)某同学用下列装置制备并检验Cl 的性质。下列说
2
法正确的是 ( )A.Ⅰ图中:如果MnO 过量,浓盐酸就可全部消耗
2
B.Ⅱ图中:如果倒置的量筒充满了氯气,水槽内装满水经足够长的时间光照,量
筒内最后剩余气体为HCl和氧气
C.Ⅲ图中:生成蓝色的烟
D.Ⅳ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中至溶液显酸性结果有
Cl 生成
2
【解析】选D。MnO 与稀盐酸不反应,MnO 过量时,随着反应的进行, HCl浓度逐
2 2
渐减小,HCl不能完全反应,A错误; HCl易溶于水,量筒中最后剩余气体是O ,B
2
错误;铜在氯气中燃烧生成CuCl ,产生棕黄色烟,C错误; NaOH溶液吸收Cl 时,
2 2
生成NaCl、NaClO和H O,烧杯中溶液滴加硫酸至酸性,发生反应:Cl-+ClO-+
2
2H+ Cl ↑+H O,产生Cl ,D正确。
2 2 2
3.利用下列装置可以制备无水氯化铁。下列有关说法正确的是 ( )A.烧瓶B中制备氯气的反应物为二氧化锰和稀盐酸
B.装置C、D中分别盛有浓硫酸、饱和食盐水
C.装置E和装置F之间需要增加一个干燥装置,才能制得无水氯化铁
D.装置F的目的是检验有无氯气逸出
【解析】选C。干燥装置应在除杂装置后,装置C、D中分别盛有饱和食盐水、
浓硫酸;装置F中挥发出的水蒸气易逆行进入装置E,需在装置E、F之间增加干
燥装置;装置F是尾气吸收装置。
【补偿训练】
已知:2Fe+3Cl 2FeCl 。如图所示仪器可用于实验室制备少量无水FeCl ,仪
2 3 3
器连接顺序正确的是 ( )
A.a—b—c—d—e—f—g—h
B.a—e—d—c—b—h—i—gC.a—d—e—c—b—h—i—g
D.a—c—b—d—e—h—i—f
【解析】选B。按制气→除HCl→除H O→制备FeCl →吸收Cl 顺序连接。
2 3 2
二、非选择题(本题包括1小题,共10分)
4.常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E都含
X元素,其转化关系如图所示:
(1)请分别写出下列物质的化学式(如为溶液请填溶质的化学式):
A________、B________、D________。
(2)写出下列反应的化学方程式或离子方程式(请注明反应条件):
A+H O(离子方程式): ______________________;
2
A+NaOH(离子方程式): ________________________;
D A(化学方程式): ________________________。
【解析】由题意可知A为氯气,B为次氯酸,D为氯化氢,C为氯化钠,E为次氯酸
钠。
答案:(1)Cl HClO HCl
2(2)Cl +H O H++Cl-+HClO
2 2
Cl +2OH- Cl-+ClO-+H O
2 2
4HCl(浓)+MnO MnCl +Cl ↑+2H O
2 2 2 2
【补偿训练】
(1)实验室制取氯气时,下列操作不正确的是________(填字母)。
A.装置Ⅰ可用于制取少量氯气
B.用装置Ⅱ除去氯气中的少量氯化氢
C.用装置Ⅲ制取氯气
D.用装置Ⅳ干燥氯气
(2)实验室制取干燥、纯净的氯气,除了二氧化锰、浓盐酸外还需要的试剂
_____________________、_____________________、________。
(3)氯气是有毒气体,必须进行尾气处理,写出实验室氯气尾气处理的离子方程
式 _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ __。(4)漂白液(次氯酸钠)和洁厕灵(盐酸)不能混合使用,产生有毒气体氯气的离子
方程式: ______________________________。
【解析】(1)实验室利用浓盐酸和二氧化锰混合加热制备氯气,装置Ⅰ的盐酸是
稀盐酸,不能用于制取少量氯气,A错误;氯气也能与碳酸氢钠反应,应该用饱和
食盐水除去氯气中的少量氯化氢,且应该是长口进短口出,B错误;实验室利用浓
盐酸和二氧化锰混合加热制备氯气,装置Ⅲ中缺少加热装置,不能制取氯气,C错
误;用装置Ⅳ干燥氯气时应该是长口进短口出,D错误;(2)实验室制取干燥、纯
净的氯气,需要的试剂有除去氯化氢的饱和食盐水,干燥氯气的浓硫酸以及吸收
尾气的氢氧化钠溶液;(3)氯气是有毒气体,必须进行尾气处理,实验室氯气尾气
处理一般用氢氧化钠溶液;(4)次氯酸钠具有强氧化性,能氧化盐酸产生氯气。
答案:(1)ABCD
(2) 饱和食盐水 浓硫酸 氢氧化钠溶液(此三空顺序可颠倒)
(3) Cl +2OH- Cl-+ClO-+H O
2 2
(4) Cl-+ClO-+2H+ Cl ↑+H O
2 2
非选择题(本题包括1小题,共16分)5.(2019·恩施州高一检测)某小组设计如图装置(部分夹持装置已略去),以探
究潮湿的Cl 与Na CO 反应得到固体物质的成分。
2 2 3
(1)试剂X的化学式________。A中制取Cl 的离子方程式
2
____________________。
(2)试剂Y的名称为______________。
(3)通入一定量潮湿的Cl 反应后,经检测,D中只有Cl O一种气体,C中除含一种
2 2
氯盐外,同时含有NaHCO 等,某同学对C中所得固体残渣的成分进行探究。
3
①提出合理假设。
假设1:存在两种成分:NaHCO 和____________________________;
3
假设2:存在三种成分:NaHCO 和__________________________。
3
②设计方案,进行实验。写出实验步骤以及预期现象和结论。
限选实验试剂和仪器:蒸馏水、稀硝酸、BaCl 溶液、澄清石灰水、AgNO 溶液、
2 3
试管、小烧杯。
实验步骤 预期现象和结论
步骤1:取C中的少量固体样品于试管中,滴加足
量蒸馏水至固体溶解,然
后将所得溶液分别置于
A、B试管中
步骤2:向A试管中滴加
BaCl 溶液
2
步骤3:
(4)已知Cl O与水反应生成次氯酸,则D中Cl O进入E反应的化学方程式为
2 2
____________。
【解析】(1)实验室利用MnO 和浓盐酸在加热条件下发生反应制取Cl ,化学方
2 2
程式为MnO +4HCl(浓) MnCl +Cl ↑+2H O,其中HCl、MnCl 是易溶于水的强电
2 2 2 2 2
解质,改写成离子形式,据此写出离子方程式。
(2)由于浓盐酸具有较强的挥发性,因此A中制取的Cl 中混有HCl、H O(g)。该
2 2
实验的目的是探究潮湿的Cl 与Na CO 反应得到固体物质的成分,故应除去Cl
2 2 3 2
中的HCl气体,试剂Y要求既能除去HCl,又不能吸收Cl ,这里可选用饱和食盐
2
水。
(3)①Cl 与Na CO 反应生成Cl O的过程中,氯元素由0价升高到+1价,根据氧化
2 2 3 2
还原反应中元素化合价有升必有降的规律可知,生成的氯盐为NaCl。潮湿的Cl
2与Na CO 在固体表面发生反应,Na CO 可能反应不完全,据此推测固体残渣中有
2 3 2 3
NaHCO 和NaCl,可能有未反应的Na CO 。
3 2 3
②将C中固体残渣溶于水配成溶液,步骤2利用BaCl 溶液检验是否存在Na CO ;
2 2 3
步骤3检验NaCl,先向B中加入过量稀硝酸,排除干扰,再加入AgNO 溶液进行检
3
验。
(4)Cl O与水反应生成HClO,化学方程式为Cl O+H O 2HClO。HClO与NaOH溶
2 2 2
液发生中和反应生成NaClO和H O,化学方程式为HClO+NaOH NaClO+H O。
2 2
答案:(1)HCl MnO +4H++2Cl- Mn2++Cl ↑+2H O (2)饱和食盐水
2 2 2
(3)①假设1:NaCl 假设2:NaCl、Na CO
2 3
②
实验步骤 预期现象和结论
步骤1:取C中的少
量固体样品于试管
中,滴加足量蒸馏水
至固体溶解,然后将
所得溶液分别置于
A、B试管中
① 若无明显现象 , 证明固体不含碳酸钠
步骤2:向A试管中
滴加BaCl 溶液
2 ② 若溶液变浑浊 , 证明固体中含碳酸钠
步骤3: 向 B 试管中
滴加过量的稀硝酸溶 若溶液变浑浊 , 结合步骤 2 中 ① , 则假设 1 成
液 , 再滴加 AgN O 溶 立 ; 结合步骤 2 中 ② , 则假设 2 成立
3
液
(4)Cl O+2NaOH 2NaClO+H O
2 2