文档内容
晶体结构与性质
重难点 题型 分值
重点 1. 四种晶体类型的性质比较
2. 四种常见晶体类型的判断方法
3. 晶体熔沸点的比较
4. 均摊法判断晶胞中微粒个数 选择题、填空题 4~6
难点 1. 晶体熔沸点的比较
2. 均摊法判断晶胞中微粒个数
一、四种晶体类型的性质比较
晶体 分子晶体 离子晶体 金属晶体 共价晶体
组成晶体微粒 分子 阴、阳离子 金属离子、自由电 原子
第1页子
范德华力(某
粒子间作用 离子键 金属键 共价键
些含氢键)
熔、沸点 较低 很高 一般较高 很高
性 硬度 较小 略硬而脆 较大 较大
质 大多数易溶于 难溶于任何
溶解性 相似相溶 难溶于常见溶剂
水等溶剂 溶剂
共 价 键 短
组成和结构相 金属原子的价电子
离 子 的 电 荷 (电子云重
作用力大小规 似的分子,相 数多、半径小,金
多、半径小, 叠多)、原
律 对分子质量大 属离子与自由电子
离子键强 子半径小,
的范德华力大 间的作用力强
键牢固
多数非金属单 金属单质与合金 金 刚 石 、
典型实例 质 及 其 氧 化 离子化合物 (Na、Al、Fe、青 SiO 、晶体
2
物、氢化物等 铜) 硅、SiC等
【易错辨析】
①分子晶体中都存在共价键(×)
②在晶体中只要有阳离子就一定有阴离子(×)
③金刚石、SiC、NaF、NaCl、HO、HS晶体的熔点依次降低(√)
2 2
④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键(×)
⑤CaTiO 晶体中(晶胞结构如图所示)每个Ti4+和12个O2-相紧邻
3
(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶点)(√)
⑥SiO 晶体中每个硅原子与两个氧原子以共价键相结合(×)
2
⑦晶体中分子间作用力越大,分子越稳定(×)
⑧氯化钠熔化时离子键被破坏(√)
【典例分析1】金属晶体和离子晶体是重要晶体类型。下列关于它们的说法中正确的
是( )
第2页A. 金属晶体和离子晶体都能导电
B. 在镁晶体中,1个Mg2+只与2个价电子存在强烈的相互作用
C. 离子晶体的硬度大、难于被压缩
D. 金属晶体和离子晶体中分别存在金属键和离子键等相互作用,很难断裂,因而都具
有延展性
【答案】C
【解析】离子晶体中的离子不是自由移动的离子,不能导电,A错误;镁晶体中的自
由电子被整个晶体所共有,不属于某个Mg2+,B错误;离子晶体中,离子间存在较强的离
子键,使离子晶体的硬度大、难于被压缩,C正确;离子晶体不具有延展性,D错误。
二、晶体类型判断
1. 依据物质的分类判断
(1)金属氧化物(如KO等)、强碱(如NaOH、KOH等)和绝大多数的盐类是离
2
子晶体。
(2)金属单质(除汞外)与合金是金属晶体。
(3)常见的共价晶体单质有金刚石、晶体硅、晶体硼等;常见的共价晶体化合物有碳
化硅、二氧化硅等。
(4)大多数非金属单质(除金刚石、石墨、晶体硅、晶体硼外)、气态氢化物、非金
属氧化物(除SiO 外)、酸、绝大多数有机物(除有机盐外)都是分子晶体。
2
2. 根据物质的物理性质判断晶体的类型
(1)在常温下呈气态或液态的物质,其晶体应属于分子晶体(Hg除外),如HO、
2
H 等。对于稀有气体,虽然构成物质的微粒为原子,但应看作单原子分子,因为微粒间的
2
相互作用力是范德华力,而非共价键。
(2)在熔融状态下能导电的晶体(化合物)是离子晶体。如:NaCl熔融后电离出Na
+和Cl-,能自由移动,所以能导电。
(3)有较高的熔点,硬度大,并且难溶于水的物质大多为共价晶体,如晶体硅、二氧
化硅、金刚石等。
(4)易升华的物质大多为分子晶体。
【即时练】分析下列物质的物理性质,判断其晶体类型:
(1)碳化铝,黄色晶体,熔点2 200 ℃,熔融状态下不导电________。
(2)溴化铝,无色晶体,熔点98 ℃,熔融状态下不导电________。
(3)五氟化钒,无色晶体,熔点19. 5 ℃,易溶于乙醇、氯仿、丙酮等________。
(4)溴化钾,无色晶体,熔融时或溶于水中能导电________。
第3页【答案】(1)共价晶体 (2)分子晶体 (3)分子晶体 (4)离子晶体
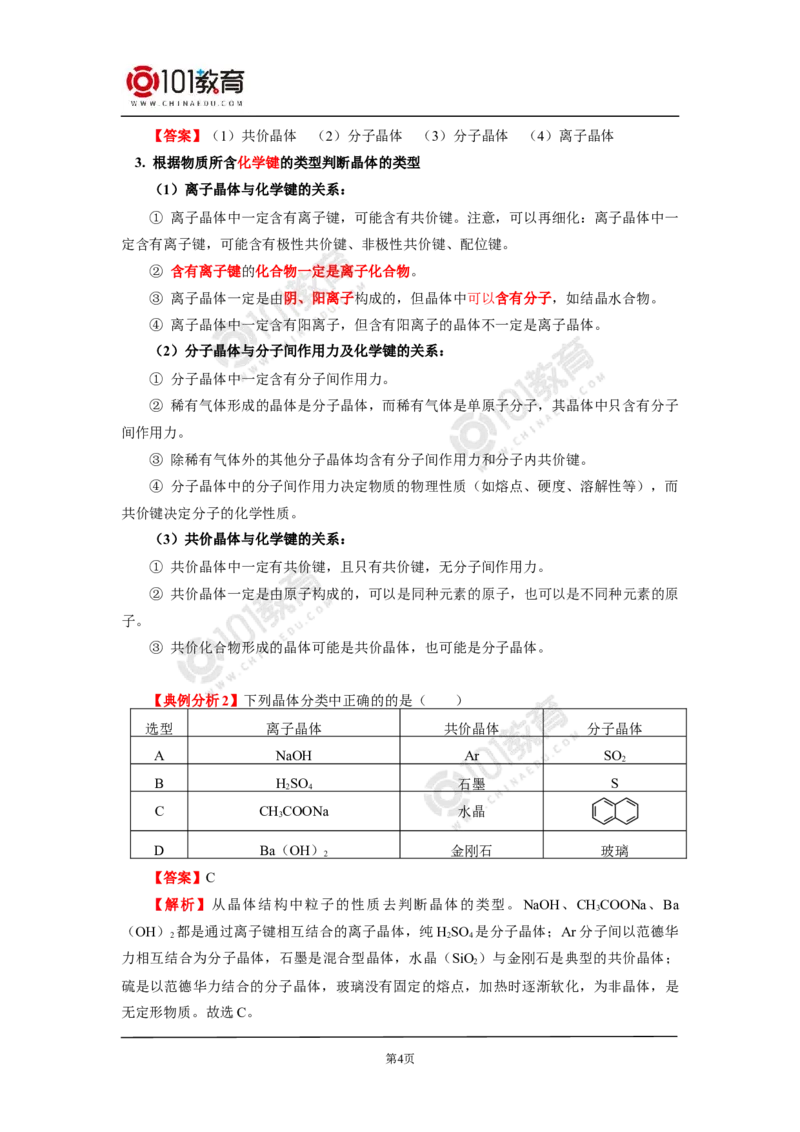
3. 根据物质所含化学键的类型判断晶体的类型
(1)离子晶体与化学键的关系:
① 离子晶体中一定含有离子键,可能含有共价键。注意,可以再细化:离子晶体中一
定含有离子键,可能含有极性共价键、非极性共价键、配位键。
② 含有离子键的化合物一定是离子化合物。
③ 离子晶体一定是由阴、阳离子构成的,但晶体中可以含有分子,如结晶水合物。
④ 离子晶体中一定含有阳离子,但含有阳离子的晶体不一定是离子晶体。
(2)分子晶体与分子间作用力及化学键的关系:
① 分子晶体中一定含有分子间作用力。
② 稀有气体形成的晶体是分子晶体,而稀有气体是单原子分子,其晶体中只含有分子
间作用力。
③ 除稀有气体外的其他分子晶体均含有分子间作用力和分子内共价键。
④ 分子晶体中的分子间作用力决定物质的物理性质(如熔点、硬度、溶解性等),而
共价键决定分子的化学性质。
(3)共价晶体与化学键的关系:
① 共价晶体中一定有共价键,且只有共价键,无分子间作用力。
② 共价晶体一定是由原子构成的,可以是同种元素的原子,也可以是不同种元素的原
子。
③ 共价化合物形成的晶体可能是共价晶体,也可能是分子晶体。
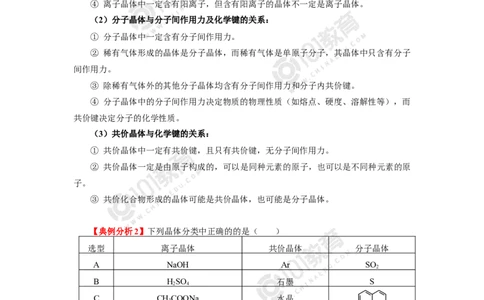
【典例分析2】下列晶体分类中正确的的是( )
选型 离子晶体 共价晶体 分子晶体
A NaOH Ar SO
2
B HSO 石墨 S
2 4
C CHCOONa 水晶
3
D Ba(OH) 金刚石 玻璃
2
【答案】C
【解析】从晶体结构中粒子的性质去判断晶体的类型。NaOH、CHCOONa、Ba
3
(OH) 都是通过离子键相互结合的离子晶体,纯HSO 是分子晶体;Ar分子间以范德华
2 2 4
力相互结合为分子晶体,石墨是混合型晶体,水晶(SiO )与金刚石是典型的共价晶体;
2
硫是以范德华力结合的分子晶体,玻璃没有固定的熔点,加热时逐渐软化,为非晶体,是
无定形物质。故选C。
第4页三、晶体的熔、沸点比较
首先判断物质的状态:固体 > 液体 > 气体,如I > Hg > O 。
2 2
1. 不同晶型的物质的熔、沸点高低顺序一般是:共价晶体 > 离子晶体 > 分子晶体。
金属晶体的熔、沸点差别很大,如钨、铂等沸点很高,汞、铯等沸点很低。
同一晶型的物质,则晶体内部结构微粒间的作用越强,熔、沸点越高。
2. 分子晶体熔、沸点高低的比较规律
(1)组成和结构相似的物质,相对分子质量越大,分子间作用力越大,熔、沸点越高,
如熔、沸点:O > N ,HI > HBr > HCl,I > Br > Cl > F 。
2 2 2 2 2 2
(2)组成和结构不相似的物质,分子极性越大,其熔、沸点就越高,如熔、沸点:
CO>N。
2
(3)在同分异构体中,在烷烃的同分异构体中,一般来说,支链数越多,熔、沸点越
低,如熔、沸点:正戊烷>异戊烷>新戊烷;同分异构体的芳香烃及其衍生物,其熔、沸点
高低顺序是邻>间>对位化合物。
(4)含有氢键的晶体,熔、沸点较高。
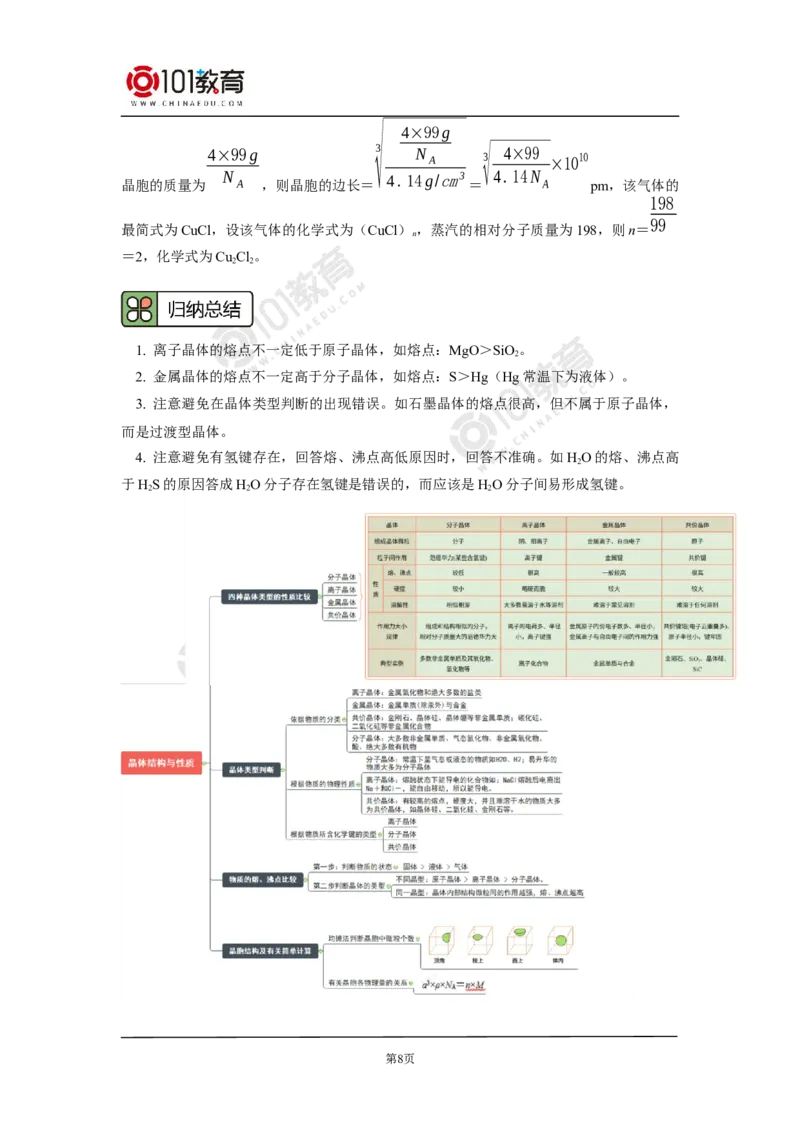
如一些氢化物的沸点如图所示:
从图中看出,从第三周期到第五周期,同主族元素简单氢化物的沸点都依次升高。但
是第VA~ⅦA族元素的氢化物中,NH 、HO和HF的熔、沸点比同主族相邻元素的氢化
3 2
物的熔、沸点高,这种反常现象就是由于它们各自的分子间形成了氢键。
3. 离子晶体要比较离子键的强弱。一般地说,阴、阳离子的电荷数越多,离子半径越小,
则 离 子 间 的 作 用 就 越 强 , 其 离 子 晶 体 的 熔 、 沸 点 就 越 高 , 如 熔 点 :
第5页MgO>MgCl >NaCl>CsCl。
2
4. 共价晶体要比较共价键的强弱,一般地说,原子半径越小,形成的共价键的键长越短,
键能越大,其晶体熔、沸点越高。
如熔点:金刚石>碳化硅>晶体硅。
解释:键长:C—CC—Si>Si—Si
5. 金属晶体中金属离子半径越小,离子电荷数越多,其金属阳离子与自由电子间的作用
越强,金属熔、沸点就越高。如熔、沸点: 。
【典型例题3】下列各组物质中,按熔、沸点由低到高顺序排列正确的是 (填
序号)。
A. KCl、NaCl、MgCl 、MgO
2
B. 金刚石、SiC、SiO、硅
2
C. HO、HS、HSe、HTe
2 2 2 2
D. Na、K、Rb、Al
E. CO 、Na、KCl、SiO
2 2
F. O 、I、Hg、MgCl
2 2 2
G. 钠、钾、钠钾合金
H. CH 、HO、HF、NH
4 2 3
I. CH、C H、C H 、C H。
4 2 6 4 10 3 8
J. CH CHCHCHCH、(CH)CHCH CH、C(CH)
3 2 2 2 3 3 2 2 3 3 4
【答案】AE
【解析】A 中离子半径:K>Na+>Mg2+,O2-Cl-,离子所带电荷数越少,离子半径越大,熔、沸点越低,正确;B中键长:C-C <
Si-O < C-Si < Si-Si,键长越长,熔、沸点越低,错误;C中相对分子质量逐渐增大,熔、
沸点应该逐渐升高,但水分子间形成氢键,导致其熔、沸点较高,错误:D中原子半径:
A1P>As
(2)NH 能形成分子间氢键
3
(3)①共价 sp3杂化 4 ②3∶1
(4)
【解析】(1)氮原子的原子序数为7,价层电子排布式为2s22p3;N、P、As位于同一
主族,随着原子序数逐渐增大,原子半径逐渐增大,原子失去电子的能力逐渐增强,原子
的第一电离能逐渐减小,所以N、P、As原子的第一电离能由大到小的顺序为N>P>As。
(2)NH 的沸点比AsH 的沸点高,是因为氨分子间除存在分子间作用力外,还有氢
3 3
键。
(3)①立方氮化硼晶体超硬,具有优异的耐磨性,推测立方氮化硼晶体为共价晶体;
立方氮化硼晶体中氮原子与周围的4个硼原子形成四面体结构,硼原子与周围的4个氮原
子形成四面体结构,因此晶体中N原子的杂化轨道类型为sp3杂化;B原子的配位数为4。
②B原子最外层有3个电子,形成4个共价键,所以含有1个配位键,故B原子与N原子
之间“一般共价键”与配位键的数目之比为3∶1。
第9页(4)立方氮化硼晶胞中N原子数为4,B原子数为 ,晶胞的质量m =
, 晶 胞 的 体 积 V= ( 362×10-10cm ) 3 , 因 此 立 方 氮 化 硼 的 密 度
。
(答题时间:45分钟)
一、选择题
1. 下列说法正确的是( )
A. 晶体在受热熔化过程中一定存在化学键的断裂
B. 原子晶体的原子间只存在共价键,而分子晶体内只存在范德华力
C. 区分晶体和非晶体最科学的方法是对固体进行X射线衍射实验
D. 非金属元素的原子间只形成共价键,金属元素的原子与非金属元素的原子间只形成
离子键
2. 共价键、金属键、离子键和分子间作用力都是构成物质微粒间的不同相互作用力,下
列含有上述两种相互作用力的晶体是( )
A. SiC晶体 B. Ar晶体 C. NaCl晶体 D. NaOH晶体
3. 仅由下列各组元素所组成的化合物的晶体,不可能属于离子晶体的是( )
A. H、O、S B. Na、H、O C. K、Cl、O D. Na、O、S
4. 下列叙述中正确的是( )
A. 原子晶体、离子晶体、金属晶体、分子晶体中都一定存在化学键
B. 同素异形体之间的转化都是物理变化
C. 原子晶体的熔点不一定比金属晶体的高,分子晶体的熔点不一定比金属晶体的低
D. 已知12 g金刚石中含有2N 个C—C键,则60 g SiO 中也含有2N 个Si—O键
A 2 A
5. 下列物质所属晶体类型分类正确的是( )
A B C D
原子晶体 石墨 生石灰 碳化硅 金刚石
分子晶体 冰 固态氨 氯化铯 干冰
离子晶体 氮化铝 食盐 明矾 芒硝
金属晶体 铜 汞 铝 铁
第10页6. 用烧热的钢针去接触涂有薄薄一层石蜡的云母片的反面,熔化了的石蜡成椭圆形,这
是因为( )
A. 云母是热的不良导体,传热不均匀
B. 石蜡是热的不良导体,传热不均匀
C. 石蜡具有各向异性,不同方向导热性能不同
D. 云母具有各向异性,不同方向导热性能不同
7. 下列有关冰和干冰的叙述不正确的是( )
A. 干冰和冰都是由分子密堆积形成的晶体
B. 冰是由氢键形成的晶体,每个水分子周围有4个紧邻的水分子
C. 干冰比冰的熔点低得多,常压下易升华
D. 干冰中只存在范德华力不存在氢键,一个分子周围有12个紧邻的分子
8. 下列叙述正确的是( )
A. 金属晶体的一个晶胞中所含的原子数:钾型=镁型<铜型
B. 在卤族元素(F、Cl、Br、I)的氢化物中,HF的沸点最低
C. CaH 、NaO 晶体的阴、阳离子个数比分别为2∶1、1∶1
2 2 2
D. 晶体熔点:金刚石>食盐>干冰>冰
9. 对于钠的卤化物(NaX)和硅的卤化物分子(SiX),下列叙述正确的是( )
4
A. SiX 呈空间网状结构,硬度大
4
B. NaX的熔点一般高于SiX
4
C. NaX易水解
D. SiX 由原子构成,熔化时破坏共价键
4
二、非选择题
10. 铜及其合金是人类最早使用的金属材料,铜的化合物在现代生活和生产中有着广泛
的应用。
(1)铜的熔点比钙的高,其原因是______________________________。
(2)科学家通过 X 射线推测,胆矾的结构如下图所示。
胆矾的阳离子中心原子的配位数为________,阴离子的空间构型为________。胆矾中
所含元素的电负性从大到小的顺序为________(用元素符号作答)。
第11页第12页1.【答案】C
【解析】A项,分子晶体受热熔化时破坏的是分子间作用力而不是化学键,错误;B
项,有的分子晶体中存在氢键,错误;D项,金属元素原子与非金属元素原子间也可形成
共价键,如AlCl 错误。
3
2.【答案】D
【解析】SiC晶体、Ar晶体、NaCl晶体中都只含有一种作用力,分别是共价键、范德
华力、离子键。
3.【答案】A
【解析】A 项不可能形成离子化合物,B、C、D 三项形成的离子化合物可能为
NaOH、KClO、NaSO 等。
3 2 3
4.【答案】C
【解析】稀有气体的晶体中不含有化学键,A项错;3O 2O 是化学变化,B项错;
2 3
晶体硅的熔点比金属钨的熔点低,蔗糖的熔点比汞高,C项正确;60 g SiO 中有4N 个Si
2 A
—O键,D项错。
5.【答案】D
【解析】石墨为混合型晶体,生石灰、氯化铯为离子晶体,氮化铝为 原子晶体。
6.【答案】D
【解析】云母是晶体,具有各向异性,在不同方向的导热性能不同,使得熔化的石蜡
成椭圆形。
7.【答案】A
【解析】干冰晶体中CO 分子间作用力只有范德华力,分子采用紧密堆积,一个分子
2
周围有12个紧邻的分子;冰晶体中水分子间除了范德华力还存在氢键,由于氢键具有方向
性,每个水分子周围有4个紧邻的水分子,采用非紧密堆积的方式,空间利用率小,因而
密度小。干冰融化只需克服范德华力,冰融化还需要克服氢键,由于氢键比范德华力大,
所以干冰比冰的熔点低得多,而且常压下易升华。
8.【答案】A
【解析】A项中1个晶胞内的原子数分别是2、2、4,正确;B项因HF分子间存在氢
2−
键,故HF沸点最高;D项熔点:冰>干冰;C项NaO 中阴离子(O2 )与阳离子(Na
2 2
+)个数比为1∶2。
9.【答案】B
【解析】硅的卤化物(SiX )属于分子晶体,不是空间网状结构,其硬度较小,A错
4
误;钠的卤化物(NaX)为离子化合物,属于离子晶体,硅的卤化物(SiX )为共价化合
4
第13页物,属于分子晶体,离子晶体的熔点大于分子晶体的熔点,即NaX的熔点一般高于SiX ,
4
故 B 正确;钠的强酸盐不水解,NaX(NaF 除外)不易水解,C 错误;硅的卤化物
(SiX)是由分子构成的,属于分子晶体,熔化时破坏分子间作用力,故D错误。
4
二、非选择题
10.【答案】(1)铜的金属键强度大于钙 (2)4 正四面体 O>S>H>Cu
【解析】(1)铜的原子半径比钙小,金属键比钙强,因此铜的熔点比钙的高;
(2)根据图示,胆矾晶体中铜离子周围有4个水分子,配位数=4,阴离子为硫酸根
离子,S的价层电子对数=4,采用sp3杂化,空间构型为正四面体;元素的非金属性越强,
电负性数值越大,胆矾中所含元素 O、S、H、Cu 的电负性从大到小的顺序为
O>S>H>Cu;
第14页