文档内容
氯及其化合物(2)
重难点 题型 分值
1. 氯气的实验室制法
重点 2. 氯离子的检验
3. 以氯及其化合物的性质为载体,用来设计实验
填空 12-15分
1. 氯及其化合物的化学性质利用
难点
2. 以氯及其化合物的性质为载体,用来设计实验
核心知识点一
一、氯气的实验室制备
1. 氯气的实验室制备
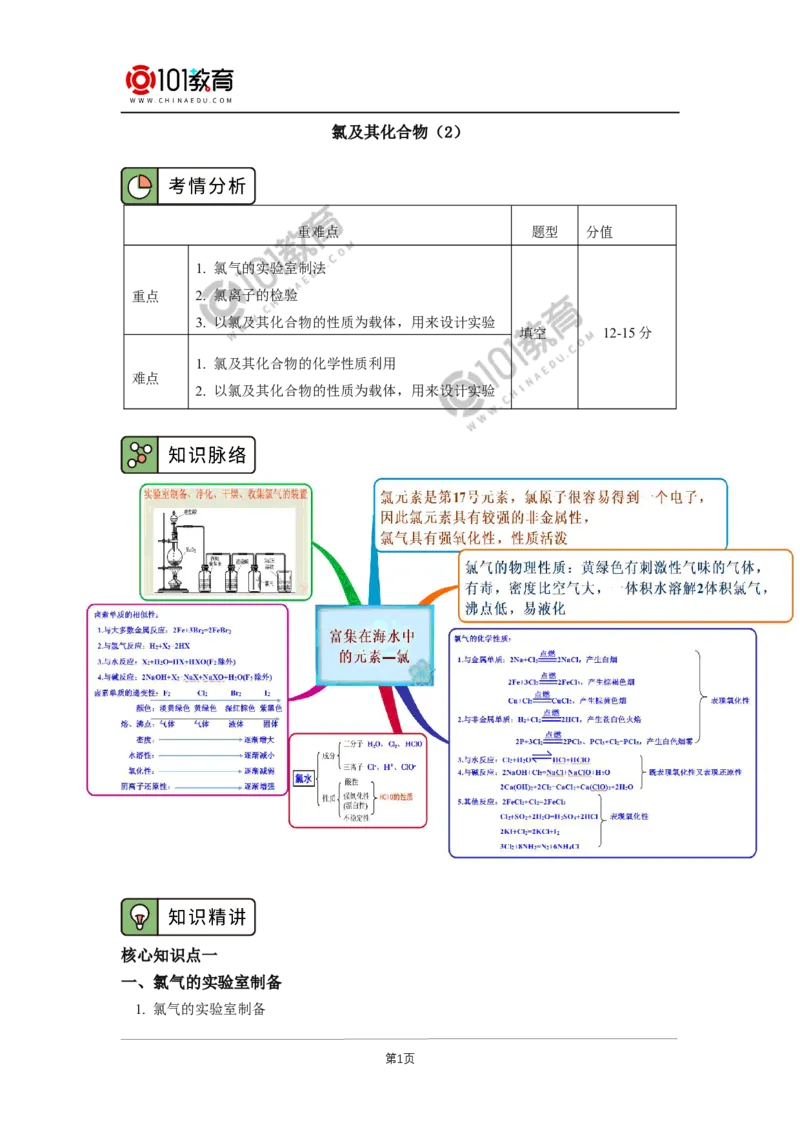
第1页(1)实验室制取、收集干燥纯净氯气的装置
(2)验满方法
①将湿润的淀粉KI试纸靠近盛Cl 的集气瓶口,观察到试纸变蓝,证明已集满。
2
②将湿润的蓝色石蕊试纸靠近盛Cl 的集气瓶口,观察到试纸先变红后褪色的变化,则
2
证明已集满。
③实验室制取Cl 时,常常根据氯气的颜色判断是否收集满。
2
(3)注意事项
①制取Cl 时必须用浓盐酸,稀盐酸不反应;随着反应进行,浓盐酸将逐渐变稀,一定
2
程度时,该反应会自动停止,HCl不可能消耗尽。
②因氧化性强弱不同,MnO 氧化浓盐酸需要加热;KClO 氧化浓盐酸微热即可,
2 3
KMnO 氧化浓盐酸不需要加热。
4
③为了减少制得的Cl 中HCl的含量,应缓缓加热,以减少HCl挥发。
2
④实验结束后,先使反应停止并排出残留的Cl,再拆卸装置,避免污染空气。
2
⑤尾气吸收时,不能使用澄清的石灰水,因为石灰水中Ca(OH) 浓度太小,吸收不
2
完全。
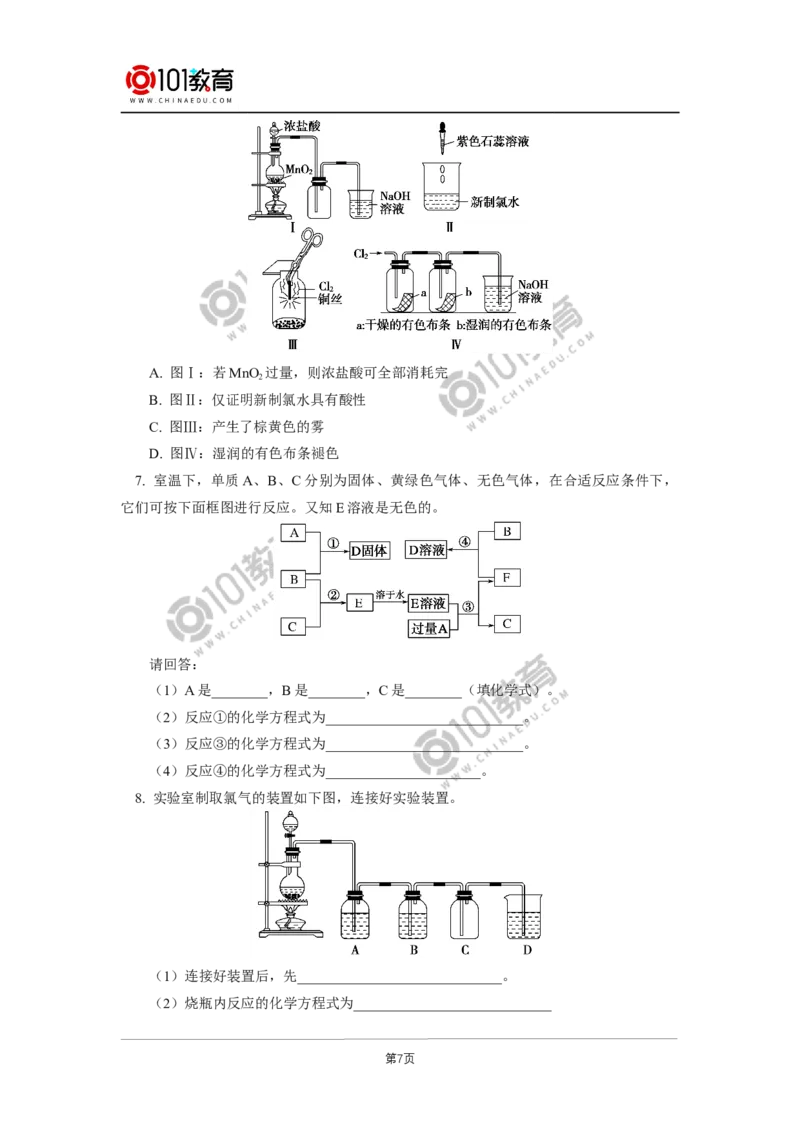
2. 氯气性质的实验探究常见实验形式如图所示:
装置 试剂 实验现象 实验目的
A 浓硫酸 —
验证氯气无漂白作用,湿润的氯气有
B 干燥红布条 无明显变化
漂白作用
C 湿润红布条 红布条褪色
D 淀粉KI溶液 溶液变蓝色 验证氯气具有强氧化性,可与金属及
第2页E 浓硫酸 —
还原性化合物反应
F 铁粉 产生棕色烟
G NaOH溶液 — 吸收多余的氯气
核心知识点二:
二、卤素性质及离子的检验
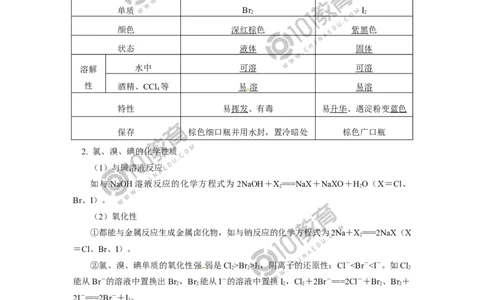
1. 溴、碘单质的物理性质
单质 Br I
2 2
颜色 深红棕色 紫黑色
状态 液体 固体
溶解 水中 可溶 可溶
性 酒精、CCl 等 易溶 易溶
4
特性 易挥发、有毒 易升华、遇淀粉变蓝色
保存 棕色细口瓶并用水封,置冷暗处 棕色广口瓶
2. 氯、溴、碘的化学性质
(1)与碱溶液反应
如与NaOH溶液反应的化学方程式为 2NaOH+X===NaX+NaXO+HO(X=Cl、
2 2
Br、I)。
(2)氧化性
①都能与金属反应生成金属卤化物,如与钠反应的化学方程式为2Na+X===2NaX(X
2
=Cl、Br、I)。
②氯、溴、碘单质的氧化性强 弱是Cl>Br >I ,阴离子的还原性:Cl-