文档内容
氯及其化合物(2)同步练习
(答题时间:25分钟)
一、选择题:本题包括12小题,每小题4分,共48分。
1. 甲、乙、丙三种溶液中各含有一种X−(X−为Cl−、Br−、I−)。向甲溶液中加淀粉溶液
和新制的氯水,溶液变橙色,再加丙溶液,颜色无明显变化。则甲、乙、丙溶液中依次含
有( )
A. Br−、Cl−、I−
B. Br−、I−、Cl−
C. I−、Br−、Cl−
D. Cl−、Br−、I−
2. 溴(Br)与氯同属“卤族”元素,其单质在性质上具有很大的相似性,但Cl 比Br 的
2 2
活泼性强,下面是根据氯的性质对溴的性质的预测,其中不正确的是( )
A. 溴单质常温下为液态,但极容易挥发为溴蒸气
B. 溴单质只具有氧化性
C. 溴原子外层有7个电子,在化学反应中容易得1个电子,表现氧化性
D. 溴离子可以用酸性AgNO 溶液来检验
3
3. 现有盐酸、氯化钠、氢氧化钠和氯水四种溶液,可用来区别它们的一种试剂是(
)
A. AgNO 溶液
3
B. 酚酞试液
C. 紫色石蕊试液
D. 饱和食盐水
4. 自来水可以用氯气消毒。如果实验室中临时没有蒸馏水,可以用自来水配制某些急需
的药品,但有些药品若用自来水配制,则明显会导致药品变质。下列哪些药品不能用自来
水配制( )
A. Na SO B. NaCl C. AgNO D. AlCl
2 4 3 3
5. 只用一种试剂就能把NaSO 、NaCl、(NH ) SO 、NH Cl四种溶液区分开来,这种
2 4 4 2 4 4
试剂( )
A. AgNO B. NaOH C. BaCl D. Ba(OH)
3 2 2
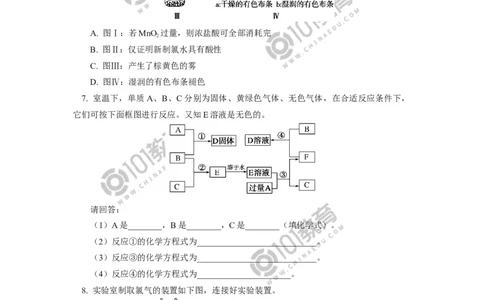
6. 某同学用以下装置制备并检验Cl 的性质。下列说法正确的是( )
2
第1页A. 图Ⅰ:若MnO 过量,则浓盐酸可全部消耗完
2
B. 图Ⅱ:仅证明新制氯水具有酸性
C. 图Ⅲ:产生了棕黄色的雾
D. 图Ⅳ:湿润的有色布条褪色
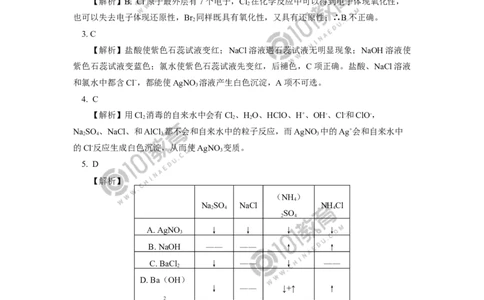
7. 室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适反应条件下,
它们可按下面框图进行反应。又知E溶液是无色的。
请回答:
(1)A是________,B是________,C是________(填化学式)。
(2)反应①的化学方程式为____________________________。
(3)反应③的化学方程式为____________________________。
(4)反应④的化学方程式为______________________。
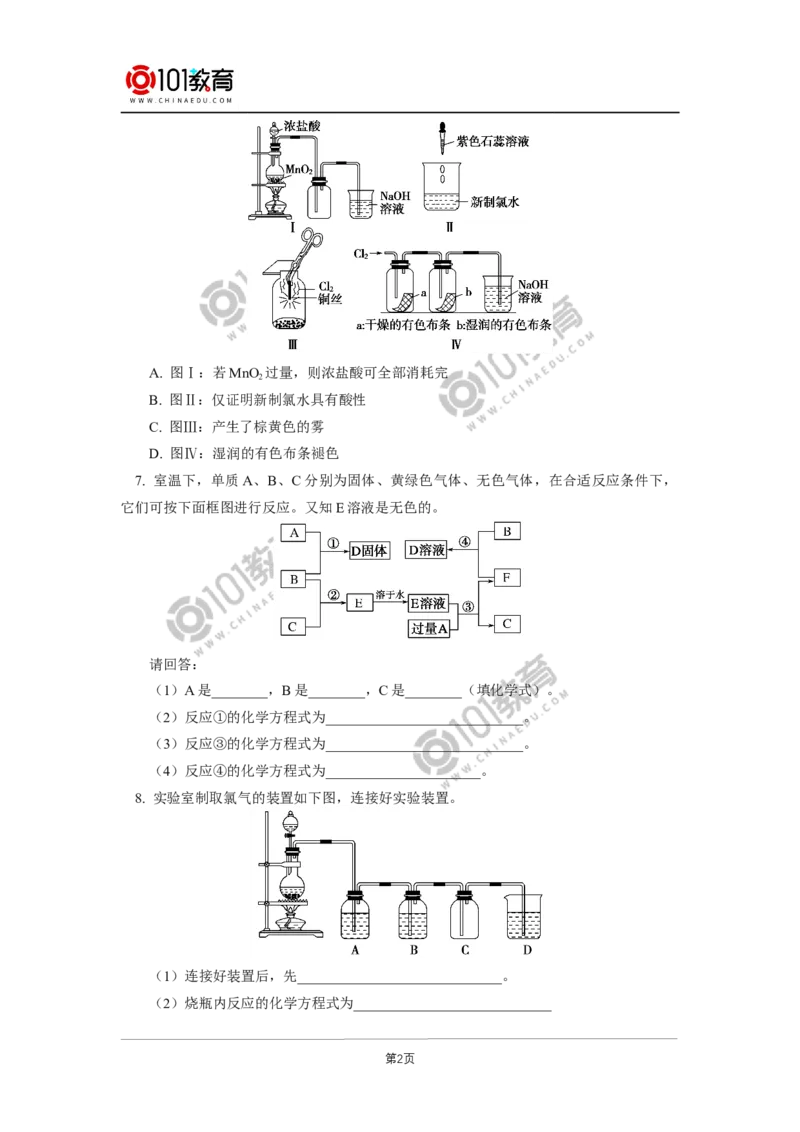
8. 实验室制取氯气的装置如下图,连接好实验装置。
(1)连接好装置后,先_____________________________。
(2)烧瓶内反应的化学方程式为____________________________
第2页(3)以含14.6 g HCl的浓盐酸与足量MnO 充分反应,制得的Cl 在标准状况下总小于
2 2
2.24 L,原因可能是①_______________________②________________________
(4)A中盛放的是________,其作用为_____________________________。
(5)B中盛放的是________,其作用为______________________。
(6)D盛放的是________,其作用为_____________________,该反应的化学方程式
为_________________________
第3页氯及其化合物(2)同步练习参考答案
1. B
【解析】向甲溶液中加入淀粉溶液和新制氯水,溶液不显蓝色,证明甲溶液中不含I,
溶液变橙色,证明甲溶液中含Br−(溴水显橙色);再加丙溶液,颜色无明显变化,表明丙
溶液中不含I−,故丙溶液中含有Cl−,乙溶液中含I−。
2. B
【解析】B. Cl原子最外层有7个电子,Cl 在化学反应中可以得到电子体现氧化性,
2
也可以失去电子体现还原性,Br 同样既具有氧化性,又具有还原性;∴B不正确。
2
3. C
【解析】盐酸使紫色石蕊试液变红;NaCl溶液遇石蕊试液无明显现象;NaOH溶液使
紫色石蕊试液变蓝色;氯水使紫色石蕊试液先变红,后褪色,C项正确。盐酸、NaCl溶液
和氯水中都含Cl−,都能使AgNO 溶液产生白色沉淀,A项不可选。
3
4. C
【解析】用Cl 消毒的自来水中会有Cl、HO、HClO、H+、OH-、Cl-和ClO-,
2 2 2
NaSO 、NaCl、和AlCl 都不会和自来水中的粒子反应,而AgNO 中的Ag+会和自来水中
2 4 3 3
的Cl-反应生成白色沉淀,从而使AgNO 变质。
3
5. D
【解析】
(NH )
4
NaSO NaCl NH Cl
2 4 4
SO
2 4
A. AgNO ↓ ↓ ↓ ↓
3
B. NaOH —— —— ↑ ↑
C. BaCl ↓ —— ↓ ——
2
D. Ba(OH)
↓ —— ↓+↑ ↑
2
由上表可见,只有加入Ba(OH) 后,四种溶液中才出现不同的现象
2
6. D
【解析】A. 实验室制氯气是用MnO 与浓盐酸反应制取的,随着反应的进行,浓盐酸
2
变成了稀盐酸,反应不能进行,所以如果MnO 过量,则浓盐酸也不能全部消耗完。A错。
2
B. 可以证明新制氯水具有酸性,还可以证明新制氯水有漂白性;B错。
C. 产生了棕黄色的烟
D. 氯气能使湿润的有色布条褪色
7. (1)Fe(1分) Cl(1分) H(1分)
2 2
第4页点燃
(2)2Fe+3Cl 2FeCl (2分)
2 3
(3)Fe+2HCl===FeCl +H ↑(2分)
2 2
(4)2FeCl +Cl===2FeCl (2分)
2 2 3
【解析】解答推断题的关键在于寻找“突破口”。由B为黄绿色的气体单质,可知B
为Cl ,C为无色气体且与Cl 能发生反应,则C为H ,E为HCl;由反应③、④可以推出,
2 2 2
A为排在H前面的金属,且A为变价金属,因此A为Fe。
8. (1)检查装置的气密性
(2)MnO +4HCl(浓) MnCl +Cl↑+2HO
2 2 2 2
(3)①随着反应的进行,盐酸浓度变小,MnO 与稀盐酸不反应,该反应停止 ②加
2
热过快,部分HCl挥发
(4)饱和食盐水除去HCl制得纯净的Cl
2
(5)浓硫酸
吸收Cl 中的水蒸气,制得干燥的Cl
2 2
(6)氢氧化钠溶液
吸收剩余Cl,防止Cl 污染空气
2 2
Cl+2NaOH===NaCl+NaClO+HO
2 2
【解析】(1)做实验需要检验装置的气密性。
(2)实验室制取氯气是用二氧化锰与浓盐酸在加热的条件下反应制取的。MnO +
2
4HCl(浓) MnCl +Cl↑+2HO
2 2 2
(3)实验室制取氯气是用二氧化锰与浓盐酸在加热的条件下反应制取;随着反应的进
行,生成水,并且盐酸的量也变少了,所以浓盐酸慢慢变成稀盐酸反应停止。反应是在加
热的条件下进行的,浓盐酸易挥发,也会导致参加反应的盐酸量变少。故答案为:
①随着反应的进行,盐酸浓度变小,MnO 与稀盐酸不反应,该反应停止 ②加热过快,
2
部分HCl挥发
(4)实验室制取氯气是用二氧化锰与浓盐酸在加热的条件下反应制取。浓盐酸易挥发,
故生成的氯气中含有氯化氢。氯化氢极易溶于水,氯气在饱和食盐水中溶解度小。
所以A中盛有饱和食盐水,其作用是除去HCl制得纯净的Cl
2
(5)因为生成的氯气中含有水蒸气,所以用浓硫酸除去氯气中含有的水蒸气。
故B中盛放浓硫酸;其作用是吸收Cl 中的水蒸气,制得干燥的Cl
2 2
(6)氯气有毒,不能排到空气中,所以 D盛放氢氧化钠溶液,其作用为吸收剩余
Cl,防止Cl 污染空气,该反应的化学方程式为Cl+2NaOH===NaCl+NaClO+HO
2 2 2 2
第5页