文档内容
第一章 原子结构与性质
第一节 原子结构
1.1.2 构造原理与电子排布式 电子云与原子轨道
1.了解原子核外电子排布的构造原理。
2.能应用电子排布式表示常见元素(1~36号)原子核外电子的排布。
3.知道电子的运动状态可通过原子轨道和电子云模型来描述。
教学重点:构造原理与电子排布式 电子云与原子轨道
教学难点:电子排布式 原子轨道
[链接课本]
1、构造原理
(1)含义:以 事实为基础,从氢开始,随核电荷数递增,新增电子填入能级的顺序。
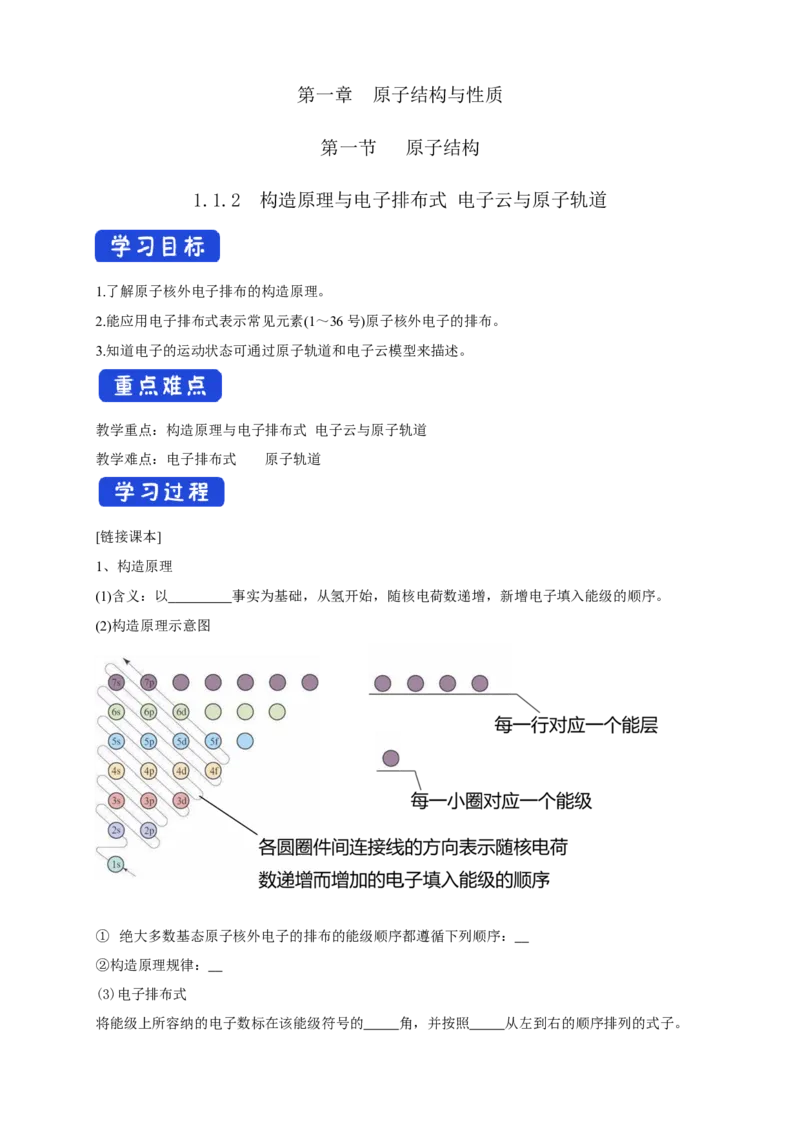
(2)构造原理示意图
① 绝大多数基态原子核外电子的排布的能级顺序都遵循下列顺序:
②构造原理规律:
(3)电子排布式
将能级上所容纳的电子数标在该能级符号的 角,并按照 从左到右的顺序排列的式子。Al原子电子排布式
写出其中2的意义
(4) 能级交错现象(从第3电子层开始):随着电荷数递增,电子并不总是填满一个能层后再开始填
入下一个能层的,电子是按能量由低到高的顺序填充的,这种现象被称为能级交错。
[思考与讨论]
1.书写下列元素基态原子的电子排布式
H C O Na Mg Al Si P S Cl K Ca Mn Fe Co Ni Cu Zn
2.观察K、Ca的核外电子排布式,发现有什么规律?
3.按构造原理写出稀有气体氦、氖、氩、氪、氙、氡的基态原子的最外层电子排布; 除氦外它们
的通式是什么?
4.电子排布式可以简化,如Na的电子排布式可简化为[Ne]3s1,上述方括号的意义是什么?仿照Na
的简化电子排布式,写出O、Si、Cu的简化电子排布式。
5.为突出化合价与电子排布式的关系,将在化学反应中可能发生电子变动的能级称为价电子层。Fe
简化电子排布式为[Ar]3d64s2,价电子排布式为3d64s2 ,通常元素周期表只给出价层电子排布式,
请写出Na、Al、Cl、Mn、Br的价层电子排布。6.阅读课本表1-1,总结电子排布式的书写原则
[答案]
1.(1) 光谱学
(2)1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s……,
ns (n-2)f (n-1)d np
(3)右上 Al原子电子排布式
[学生活动]
1.H 1s1 C 1s22s22p2 O 1s22s22p4
Na 1s22s22p63s1 Mg 1s22s22p63s2 Al 1s22s22p63s23p1
Si 1s22s22p63s23p2 P 1s22s22p63s23p3 S 1s22s22p63s23p4
Cl 1s22s22p63s23p5 K 1s22s22p63s23p64s1 Ca 1s22s22p63s23p64s2
Mn 1s22s22p63s23p63d54s2 Fe 1s22s22p63s23p63d664s2 Co 1s22s22p63s23p63d74s2
Ni 1s22s22p63s23p63d84s2 Cu 1s22s22p63s23p63d104s1 Zn 1s22s22p63s23p63d104s2
2.(1)不同能层的能级有交错现象,如 E(3d)>E(4s)、E(4d)>E(5s)、E(5d)>E(6s)、E(6d)>
E(7s)、E(4f)>E(5p)、E(4f)>E(6s)等。
(2)能级交错现象(从第3电子层开始):随着电荷数递增,电子并不总是填满一个能层后再开始填
入下一个能层的,电子是按能量由低到高的顺序填充的,
(3)电子先填最外层的ns,后填次外层的(n-1)d,甚至填入倒数第三层的(n-2)f,最后填
入np 。
3.He 1s2
Ne 2s22p6
Ar 3s23p6
Kr 4s 24p6
Xe 5s 25p6Rn 6s 26p6
通式:ns2np6
4.方括号:内层电子达到稀有气体元素原子结构的部分以相应稀有气体的元素符号外加方括号的形
式表示
O [He] 2s22p4
Si [Ne]3s23p2
Cu [Ar] 3d10 4s1
5.Na 3s1 Al 3s23p1 Cl 3s23p5 Mn 3d5 4s Br 4s24p5
6. 原子的电子排布式的书写方法
(1) 按照构造原理将电子依次填充到能量逐渐升高的能级中
(2) 一般情况下,能层低的能级要写在左边,而不是按照构造原理顺序写
(3) 为了避免电子排布式过于繁琐,我们可以把内层电子达到稀有气体结构的部分,以相应稀有气
体元素符号外加方括号来表示。
(4) 当p、d、f能级处于全空、全充满或半充满状态时,能量相对较低,原子结构较稳定。
[链接课本]
二、电子云
1.概率密度
用P表示电子在某处出现的概率,V表示该处的体积,则 称为概率密度,用ρ表示。
2.电子云
由于核外电子的 分布看起来像一片云雾,因而被形象地称作电子云。换句话说,电子云
是处于一定空间运动状态的电子在原子核外空间的概率密度分布的形象化描述。
3.电子云轮廓图
①含义:绘制电子云轮廓图的目的是表示 轮廓的形状,对核外电子的空间状态有一个形象
化的简便描述。如1s电子云轮廓图的绘制:
② s电子、p电子的电子云轮廓图
s能级的电子云轮廓是 ,只有一种空间伸展方向。能层序数越大,原子轨道的半径越 。
p能级的电子云轮廓是 ,有三种空间伸展方向。能层序数越大,原子轨道的半径越 。同一原子的s电子的电子云轮廓图 P、P、P 上的电子云轮廓图
x y x
[答案]1.
2.概率密度
3.①电子云轮廓
② 球形 大 哑铃状 大
[链接课本]
三、原子轨道
1.定义:量子力学把电子在原子核外的 称为一个原子轨道。
2.各能级所含有原子轨道数目
能级符号 ns np nd nf
轨道数目
3.各能级的一个伸展方向的电子云轮廓图即表示一个原子轨道。
[总结归纳]
原子轨道与能层序数的关系
(1)不同能层的同种能级的原子轨道形状 ,只是半径 。能层序数n越大,原子轨道的半径
。如:(2)s能级只有 个原子轨道。p能级有 个原子轨道,它们互相垂直,分别以p、p、p 表示。
x y z
在同一能层中p、p、p 的能量 。
x y z
(3)原子轨道数与能层序数(n)的关系是原子轨道为
[答案]
1.一种空间运动状态
2.1 3 5 7
[总结归纳]
(1)相同 不同 越大
(2)1 3 相同
(3)n2
1.构造原理揭示的电子排布能级顺序,实质是各能级能量高低。若以 E(nl)表示某能级的能量,以
下各式中正确的是( )
A.E(5s)>E(4f)>E(4s)>E(3d) B.E(3d)>E(4s)>E(3p)>E(3s)
C.E(4s)E(4s)>E(4f)>E(3d)
【答案】B
【解析】根据构造原理,各能级能量由低到高的顺序为 1s、2s、2p、3s、3p、4s、3d、4p、
5s……,A项和D项正确顺序为E(4f)>E(5s)>E(3d)>E(4s);对于不同能层的相同能级,能层序数越
大,能量越高,所以C项错误。
2.已知Na的核外电子排布式为1s22s22p63s1,通常可把内层已达稀有气体原子的电子层结构的部分
写成“原子实”,如Na的核外电子排布式可写成[Ne]3s1。用“原子实”表示的30号元素锌的原子
核外电子排布式正确的是( )
A. [Ne]3d104s2 B. [Ar]3d104s24p2 C. [Ar]3d84s24p2 D. [Ar]3d104s2
【答案】D
【解析】根据构造原理可知,锌元素原子的核外电子排布式为1s22s22p63s23p63d104s2,除3d104s2外,
锌原子内层电子的排布与稀有气体原子 Ar的电子排布相同,因此锌的核外电子排布式可写为
[Ar]3d104s2。
3.下列有关电子云的叙述中,正确的是( )
A. 电子云形象地表示了电子在核外某处单位体积内出现的概率
B. 电子云直观地表示了核外电子的数目
C. 1s电子云轮廓图是一个球面,表示在这个球面以外,电子出现的概率为零
D. 电子云是电子绕核运动形成了一团带负电荷的云雾【答案】A
【解析】电子云表示电子在核外单位体积内出现的概率大小,小黑点的疏密表示出现概率密度的多
少,密则概率密度大,疏则概率密度小,故A正确。
4.主族元素原子失去最外层电子形成阳离子,主族元素原子得到电子填充在最外层形成阴离子。下
列各原子或离子的电子排布式错误的是( )
A. Ca2+ 1s22s22p63s23p6
B. O2- 1s22s23p4
C. Fe 1s22s22p63s23p63d64s2
D. Fe2+ 1s22s22p63s23p63d6
【答案】B
【解析】氧原子的电子排布式为1s22s22p4,因此O2-的电子排布式为1s22s22p6,B错;原子失去电
子形成离子时,应先失去最外层上的电子。Fe的电子排布式为1s22s22p63s23p63d64s2,铁元素生成
Fe2+时,应先失去4s上的电子,故Fe2+的电子排布式为1s22s22p63s23p63d6。
5.某元素原子的电子排布式为1s22s22p63s23p1,该元素最可能的化合价为( )
A. +1 B. +3 C. +5 D. -5
【答案】B
【解析】根据该元素原子的电子排布式可知,该原子的最外能层上有 3个电子,故该元素容易失去
3个电子,表现为+3价。
6.已知三种微粒(原子或离子)的电子排布式如下:
X:1s22s22p6 Y:1s22s22p63s23p6
11 19
Z:1s22s22p63s23p6
20
若将上述三种微粒归为同一类,下列微粒中也可归为此类的是( )
A. B. C. D.
【答案】C
【解析】 X、 Y、 Z均为金属阳离子,A、D为原子,C为Mg2+,B为S2-。
11 19 20
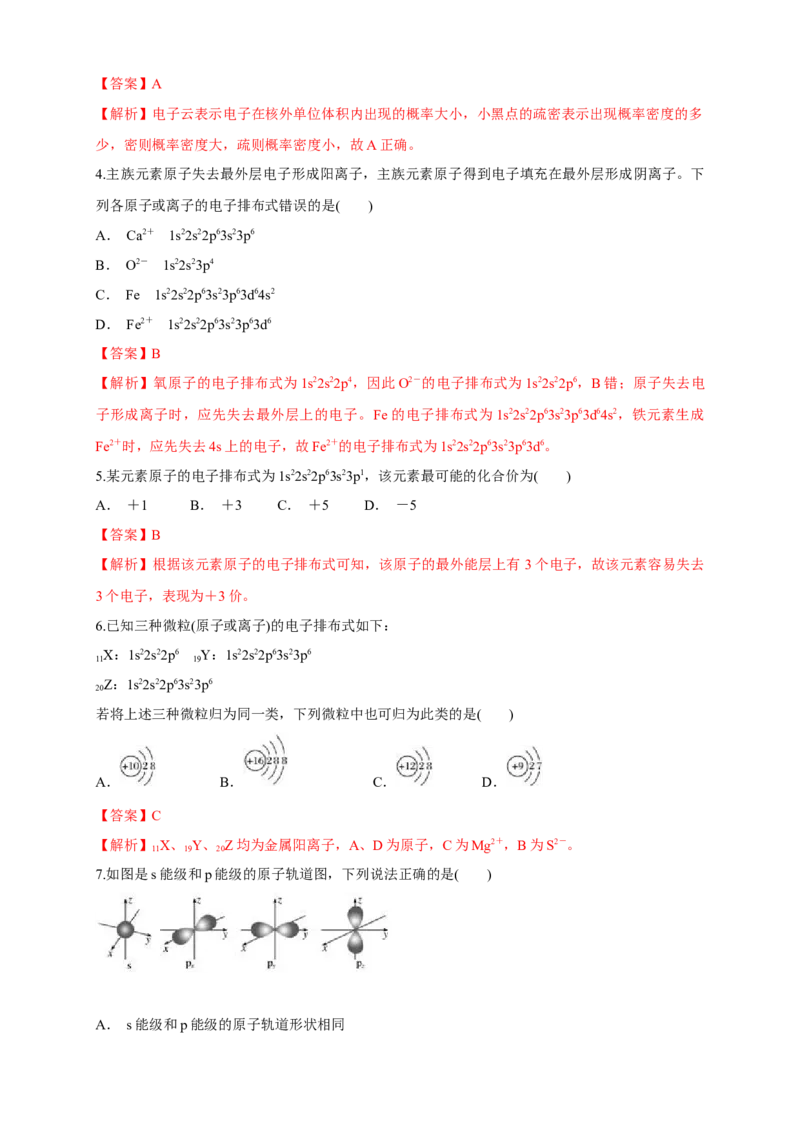
7.如图是s能级和p能级的原子轨道图,下列说法正确的是( )
A. s能级和p能级的原子轨道形状相同B. 每个p能级都有6个原子轨道
C. s能级的原子轨道半径与能层序数有关
D. 钠原子的电子在11个原子轨道上高速运动
【答案】C
【解析】s轨道为球形,p轨道为哑铃形,A项错误;每个p能级只有3个原子轨道,B项错误;能
层序数越小,s能级的原子轨道半径越小,C项正确;钠原子的电子在6个原子轨道上高速运动,D
项错误。