文档内容
第2讲 热化学方程式
【学习目标】
1、理解热化学方程式的意义
2、 学会书写热化学方程式
3、比较反应热的大小关系
【学习重难点】
重点:热化学方程式的书写
难点:热化学方程式的书写、反应热的大小比较
【自主预习】
1.热化学方程式
(1)概念:表示反应所 和 的热量的化学方程式。
(2)意义:既表明化学反应中的 变化,也表明了化学反应中的 变化。
(3)实例:H(g)+O(g)===HO(l) ΔH=-285.8 kJ·mol-1表示的意义是在25 ℃、101 kPa下 气
2 2 2
态H 与 mol气态O 反应生成 时, 的热量是285.8 kJ。
2 2
【合作探究】
一.理解热化学方程式的意义
【思考讨论1】热化学方程式与普通的化学方程式有什么不同?
1、热反应方程式化学计量数的意义:
热反应方程式化学计量数表示 ,因此可以是 ,也可以是 。 化学计量数改变,
要相应改变;逆反应的ΔH 数值与正反应的ΔH 数值 ,符号
2、ΔH 的单位中“mol-1”的含义:
【写一写】
写出2H(g) + O(g) = 2HO(l) ΔH =﹣571.6 kJ/mol 这个热化学方程式表示的意义
2 2 2
3.反应热(ΔH)与热化学方程式的数量关系
观察下列四个热化学方程式,反应热(ΔH)与热化学方程式的计量数有何关系?
(1)H(g) + O(g) =HO(l) ΔH =﹣285.8 kJ/mol
2 2 2
(2)2H(g) + O(g) = 2HO(l) ΔH =﹣571.6 kJ/mol
2 2 2
(3)N(g)+3H(g) 2NH3(g) ΔH =﹣92.4kJ/mol
2 2
(4)2NH(g) N(g)+3H(g) ΔH = + 92.4kJ/mol
3 2 2
【结论】
对于同一化学反应,如果化学计量数扩大或缩小,那么ΔH的数值也同时_________________。
当反应逆向进行时,其反应热与正反应的反应热数值________,符号_______
【知识检测】
【典例1】下列说法不正确的是( )A.热化学方程式中各物质的化学计量数只表示物质的量,不表示分子的个数
B.物质发生化学反应的反应热仅指反应放出的热量
C.所有的燃烧反应都是放热的
D.热化学方程式中,化学式前面的化学计量数可以是分数
【变式1】热化学方程式:C(s)+HO(g) CO(g)+H(g) ΔH=+131.3 kJ/mol
2 2
和H(g)+H(g)=H(g) ΔH=-435.7 kJ/mol 表示 ( )
2
A.氢原子的能量比氢分子的能量低
B.一个氢原子与一个氢原子结合生成1个氢分子且放出435.7 kJ的能量
C.1 mol固态碳和1 mol水蒸气反应生成一氧化碳气体和氢气,并吸热131.3 kJ
D.固态碳和液态水反应生成一氧化碳气体和氢气吸收131.3 kJ能量
【变式2】已知,H
2
(g)+Cl
2
(g)=2HCl(g)ΔH=−184.6kJ⋅mol−1,则反应HCl(g)=1/2H
2
(g)+1/2Cl
2
(g) ΔH为
__________________
【合作探究】
二.学会书写热化学方程式
【思考讨论2】说一说为什么热化学方程式的书写需注明反应物和生成物的聚集状态?
1、书写热化学方程式应注意事项
(1)条件:指明反应时的 和 ;若在 25℃、101kPa 时进行的反应,可以不注明。
(2)状态:要注明反应物和生成物的 ,固体: 液体: 气体: 溶液:
(3)标注ΔH的正负。化学方程式后面空一格标注ΔH,若为放热反应,ΔH为“____”;若为吸热反
应,ΔH为“______”。
(4)反应条件区:别于普通方程式,一般不注“↑”“↓”以及“点燃”“加热”等
(5)同素异形体转化的热化学方程式除了注明状态外,还要注明名称。
2、“五查”法判断热化学方程式书写正误
①看方程式是否配平;
②看各物质的聚集状态是否正确;
③看ΔH 变化的“+”、“-”是否正确;
④看反应热的单位是否为 kJ·mol-1;
⑤看反应热的数值与化学计量数是否相对应
【思考讨论3】
(1)已知 N(g)+3H(g) =2NH(g) ΔH =﹣92.4kJ/mol,那么,1 mol N 与3 mol H 充分反应,放出
2 2 3 2 2
92.4kJ的能量。这种说法是否正确?
(2)已知H(g)+I(g) 2HI(g) ΔH=-14.9 kJ·mol-1,把1 mol的H 和1 mol I 在该温度和压强下
2 2 2 2
放入密闭容器中充分反应,最终放出的热量是14.9 kJ吗?
【知识检测】
【典例2】实验测得:101kPa时,1mol H 完全燃烧生成液态水,放出285.8kJ的热量。1mol CH 完全燃烧
2 4生成液态水和CO,放出890.3kJ的热量。下列热化学方程式的书写正确的是( )
2
①CH(g)+2O(g)═CO(g)+2HO(l)△H=890.3kJ•mol﹣1
4 2 2 2
②CH(g)+2O(g)═CO(g)+2HO(l)△H=﹣890.3kJ
4 2 2 2
③CH(g)+2O(g)═CO(g)+2HO(g)△H=﹣890.3kJ•mol﹣1
4 2 2 2
④2H(g)+O(g)═2HO(l) △H=﹣571.6kJ•mol﹣1
2 2 2
A.仅有②④ B.仅有④
C.仅有②③④ D.全部符合要求
【变式1】氢气是人类最理想的能源。已知在25℃、101kPa下,1g氢气完全燃烧生成液态水时放出热量
142.9kJ,则下列热化学方程式书写正确的是( )
A.2H+O═2HO△H=﹣142.9kJ•mol﹣1
2 2 2
B.2H(g)+O(g)═2HO(l)△H=﹣142.9kJ•mol﹣1
2 2 2
C.2H(g)+O(g)═2HO(l)△H=﹣571.6kJ•mol﹣1
2 2 2
D.2H(g)+O(g)═2HO(l)△H=﹣142.9kJ
2 2 2
【变式2】根据信息书写热化学方程式
(1)化合物AX 和单质X 在一定条件下反应可生成化合物AX 回答下列问题:已知AX 的熔点和沸点分别
3 2 5. 3
为-93.6 ℃和76 ℃,AX 的熔点为167 ℃。室温时AX 与气体X 反应生成1 mol AX,放出热量123.8
5 3 2 5
kJ。该反应的热化学方程式为___________。
(2)在25 ℃、101 kPa下,一定质量的无水乙醇完全燃烧时放出热量Q kJ,其燃烧生成的CO 用过量饱和
2
石灰水吸收可得100 g CaCO 沉淀,则乙醇燃烧的热化学方程式为___________。
3
(3)在一定条件下,将1 mol N 和3 mol H 充入一密闭容器中发生反应生成氨气,达到平衡时N 的转化率
2 2 2
为25%,放出Q kJ的热量,写出N 与H 反应的热化学方程式为___________。
2 2
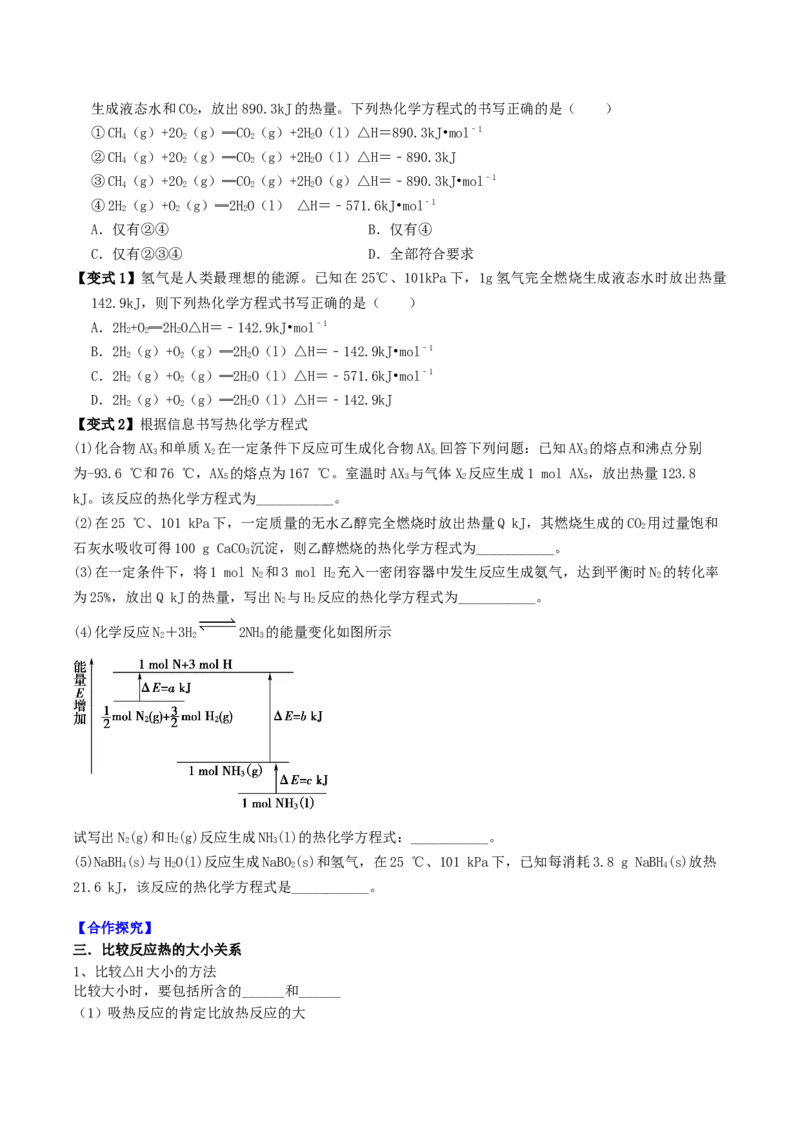
(4)化学反应N+3H 2NH 的能量变化如图所示
2 2 3
试写出N(g)和H(g)反应生成NH(l)的热化学方程式:___________。
2 2 3
(5)NaBH(s)与HO(l)反应生成NaBO(s)和氢气,在25 ℃、101 kPa下,已知每消耗3.8 g NaBH(s)放热
4 2 2 4
21.6 kJ,该反应的热化学方程式是___________。
【合作探究】
三.比较反应热的大小关系
1、比较△H大小的方法
比较大小时,要包括所含的______和______
(1)吸热反应的肯定比放热反应的大(2)同一放热(吸热)反应,其他条件相同时,参加反应的反应物的物质的量越大,放出(吸收)的热
量越多,△H的值越小(越大)
(3)燃料的燃烧,其他条件相同时
①燃烧产物越稳定,放出热量越多,则△H越小
②燃料状态为气、液、固,放出的热量依次减少,则△H依次增大
【典例3】已知①H (g) + 1/2 O (g) = HO (g) ΔH=akJ/mol
2 2 2 1
② 2H (g) + O (g) = 2HO (g) ΔH= b kJ/mol
2 2 2 2
③ H (g) + 1/2 O (g) = HO (l) ΔH= c kJ/mol
2 2 2 3
④ 2H (g) + O (g) = 2HO (l) ΔH= d kJ/mol
2 2 2 4
下列关系中正确的是( )
A.a<c<0 B.b>d>0 C.2a=b<0 D.2c=d>0
【变式1】下列各组热化学方程式中,化学反应的△H前者大于后者的是___________ 。
① C(s)+O(g)=CO(g);△H1
2 2
C(s)+O(g)=CO(g);△H2
2
② S(s)+O(g)=SO(g);△H3
2 2
S(g)+O(g)=SO(g);△H4
2 2
③ H(g)+O(g)=HO(l);△H5
2 2 2
2H(g)+O(g)=2HO(l);△H6
2 2 2
④ CaCO(s)=CaO(s)+CO(g);△H7
3 2
CaO(s)+HO(l)=Ca(OH)(s);△H8
2 2
【巩固练习】
1.已知:H(g)+Cl(g)===2HCl(g) ΔH=-183 kJ/mol ,下列说法正确的是( )
2 2
A.2L氯化氢气体分解成1L的氢气和1L的氯气,吸收183kJ热量
B.1mol氢气与1mol氯气反应生成2mol液态氯化氢放出的热量小于183kJ
C.在相同条件下,1mol氢气与1mol氯气的能量总和大于2mol氯化氢气体的能量
D.1个氢气分子与1个氯气分子反应生成2个氯化氢分子放出183kJ热量
2.2g碳与水蒸气反应生成CO和H,需吸收21.88kJ热量,此反应的热化学方程式为( )
2
A.C + HO ==CO + H ΔH =+131.3kJ·mol—1
2 2
B.C(s)+ HO(g) ==CO(g) + H(g)ΔH =+10.94kJ·mol—1
2 2
C.C(s)+ HO(g) ==CO(g) + H(g)ΔH = -131.3kJ·mol—1
2 2
D.C(s)+ HO(g) ==CO(g) + H(g)ΔH = +131.3kJ·mol—1
2 2
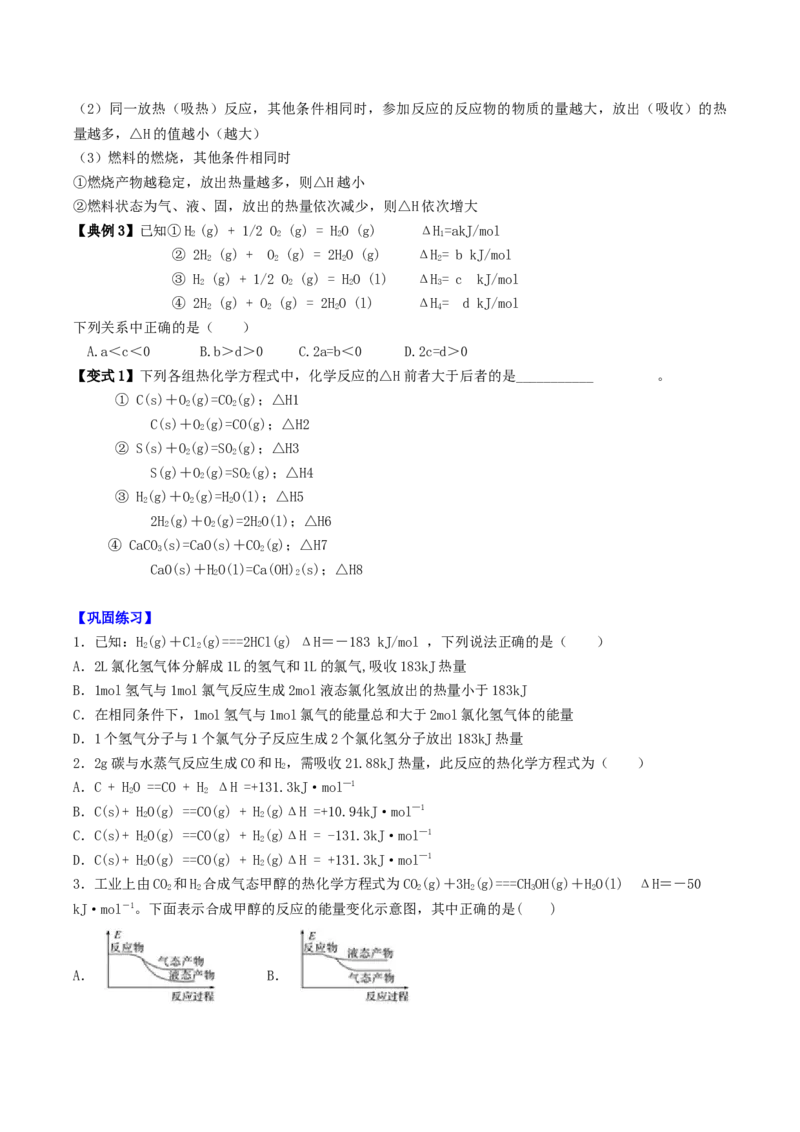
3.工业上由CO 和H 合成气态甲醇的热化学方程式为CO(g)+3H(g)===CHOH(g)+HO(l) ΔH=-50
2 2 2 2 3 2
kJ·mol-1。下面表示合成甲醇的反应的能量变化示意图,其中正确的是( )
A. B.C. D.
4.锡是大名鼎鼎的“五金”——金、银、铜、铁、锡之一。早在远古时代,人们便发现并使用锡了。灰
锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
①Sn(s,白)+2HCl(aq)=SnCl(aq)+H(g) ΔH
2 2 1
②Sn(s,灰)+2HCl(aq)=SnCl(aq)+H(g) ΔH
2 2 2
③Sn(s,灰) Sn(s,白) ΔH=2.1 kJ·mol-1
3
下列说法正确的是( )
A.ΔH>ΔH
1 2
B.锡在常温下以灰锡状态存在
C.灰锡转化为白锡的反应是放热反应
D.锡制器皿长期处在低于13.2 ℃的环境中,会自行毁坏
5、写出下列反应的热化学方程式:
(1)NH(气态)在高温高压催化剂下分解生成 1mol N(气态)与 H(气态),吸收 92.2kJ 的热量
3 2 2
___________________________________________________
( 2 ) 1mol H( 气 态 ) 与 适 量 O( 气 态 ) 起 反 应 , 生 成 HO( 液 态 ) 能 放 出 285.8kJ 的 热 量
2 2 2
__________________________________________________
( 3 ) 32g Cu( 固 态 ) 与 适 量 O( 气 态 ) 起 反 应 , 生 成 CuO( 固 态 ) 放 出 78.5kJ 的 热 量
2
_________________________________________________________