文档内容
1.2.2 反应热的计算(学案)
1.能用盖斯定律进行有关反应热的简单计算。
1.用盖斯定律进行有关反应热的计算。
盖斯定律的内容:不论化学反应是一步完成还是分几步完成,其反应热是___________的(填
“相同”或“不同”)。
一、反应热的计算
1.主要依据:热化学方程式、键能、____________及燃烧热等数据。
2.主要方法
(1)依据热化学方程式:反应热的绝对值与各物质的物质的量成________比,依据热化学方程式
中的______求反应热。
(2)依据盖斯定律:根据盖斯定律,可以将两个或两个以上的热化学方程式包括其ΔH相加或相
减,得到一个新的热化学方程式,同时反应热也作相应的改变。
【练习】1.LiH可作飞船的燃料,已知下列反应:
2Li(s)+H (g)═2LiH(s)△H=﹣182kJ•mol﹣1
2
①2H (g)+O (g)═2H O(1)△H=﹣572 kJ•mol﹣1
2 2 2
②4Li(s)+O (g)═2Li O(s)△H=﹣1196 kJ•mol﹣1
2 2
③则反应2LiH(s)+O
2
(g)═Li
2
O(s)+H
2
O(l)的焓变为( )
A.+351 kJ•mol﹣1 B.﹣351 kJ•mol﹣1
C.+702 kJ•mol﹣1 D.﹣702 kJ•mol﹣1
【练习】2.已知: CH COOH(l)+2O (g)═2CO (g)+2H O(l)△H
3 2 2 2 1
C(s)+O
2
(g①)═CO
2
(g)△H
2
②2H
2
(g)+O
2
(g)═2H
2
O(l)△H
3
③2CO
2
(g)+4H
2
(g)═CH
3
COOH(1)+2H
2
O(l)△H
4
④2C(s)+2H
2
(g)+O
2
(g)═CH
3
COOH(l)△H
5
⑤下列关于上述反应的焓变的判断正确的是( )
A.△H >0,△H <0 B.△H =2△H +△H ﹣△H
1 2 5 2 3 1C.△H >0 D.△H =△H ﹣2△H
2 4 1 3
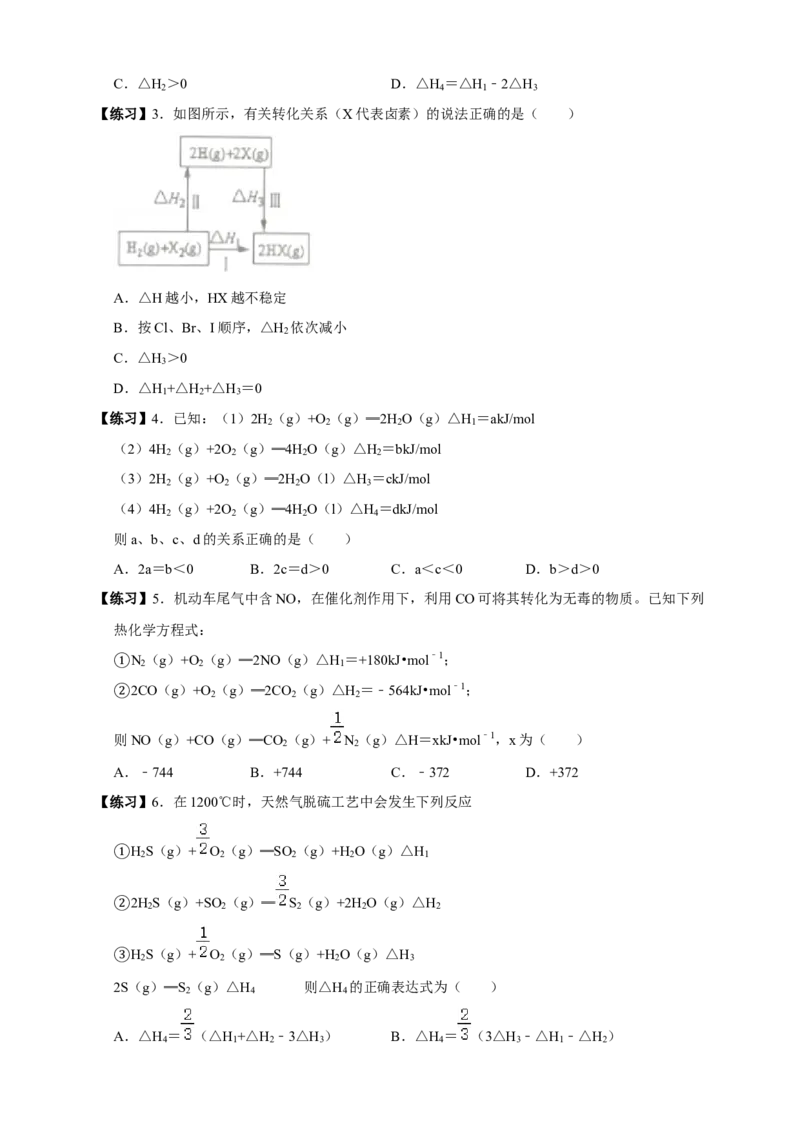
【练习】3.如图所示,有关转化关系(X代表卤素)的说法正确的是( )
A.△H越小,HX越不稳定
B.按Cl、Br、I顺序,△H 依次减小
2
C.△H >0
3
D.△H +△H +△H =0
1 2 3
【练习】4.已知:(1)2H (g)+O (g)═2H O(g)△H =akJ/mol
2 2 2 1
(2)4H (g)+2O (g)═4H O(g)△H =bkJ/mol
2 2 2 2
(3)2H (g)+O (g)═2H O(l)△H =ckJ/mol
2 2 2 3
(4)4H (g)+2O (g)═4H O(l)△H =dkJ/mol
2 2 2 4
则a、b、c、d的关系正确的是( )
A.2a=b<0 B.2c=d>0 C.a<c<0 D.b>d>0
【练习】5.机动车尾气中含NO,在催化剂作用下,利用CO可将其转化为无毒的物质。已知下列
热化学方程式:
N (g)+O (g)═2NO(g)△H =+180kJ•mol﹣1;
2 2 1
①2CO(g)+O (g)═2CO (g)△H =﹣564kJ•mol﹣1;
2 2 2
②
则NO(g)+CO(g)═CO (g)+ N (g)△H=xkJ•mol﹣1,x为( )
2 2
A.﹣744 B.+744 C.﹣372 D.+372
【练习】6.在1200℃时,天然气脱硫工艺中会发生下列反应
H
2
S(g)+ O
2
(g)═SO
2
(g)+H
2
O(g)△H
1
①
2H
2
S(g)+SO
2
(g)═ S
2
(g)+2H
2
O(g)△H
2
②
H
2
S(g)+ O
2
(g)═S(g)+H
2
O(g)△H
3
③2S(g)═S (g)△H 则△H 的正确表达式为( )
2 4 4
A.△H = (△H +△H ﹣3△H ) B.△H = (3△H ﹣△H ﹣△H )
4 1 2 3 4 3 1 2C.△H = (△H +△H ﹣2△H ) D.△H = (△H ﹣△H ﹣3△H )
4 1 2 3 4 1 2 3
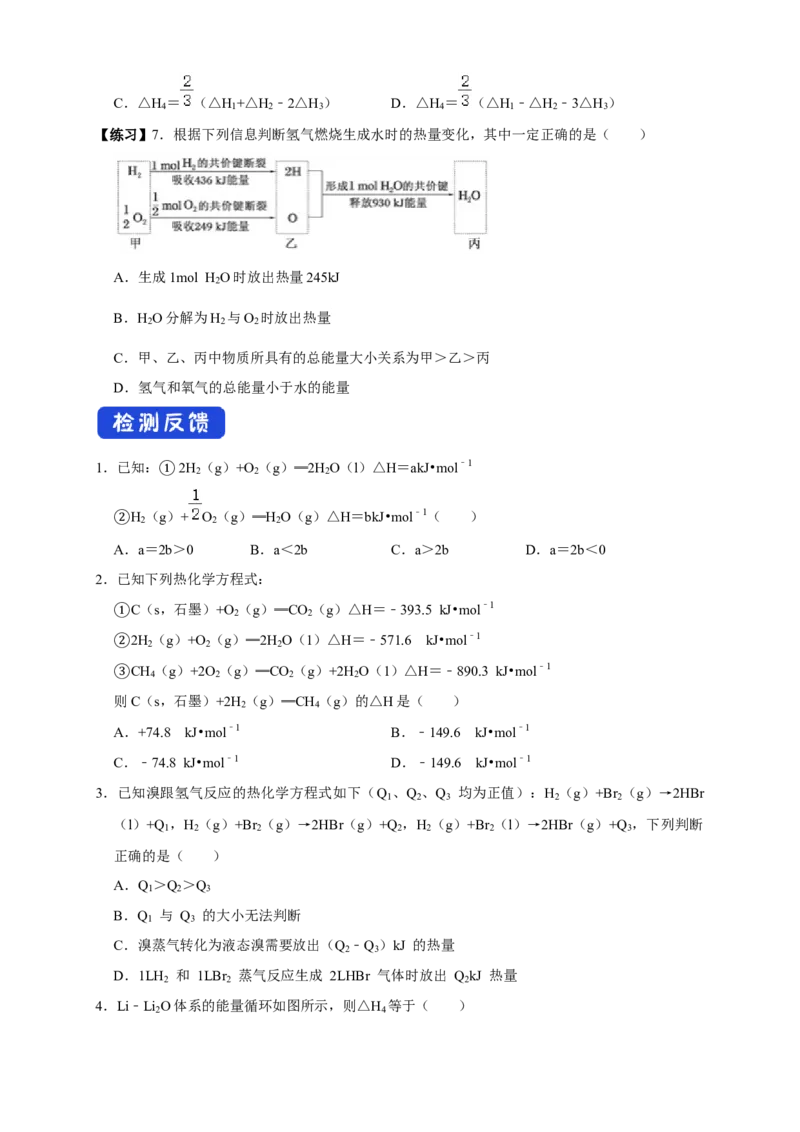
【练习】7.根据下列信息判断氢气燃烧生成水时的热量变化,其中一定正确的是( )
A.生成1mol H O时放出热量245kJ
2
B.H O分解为H 与O 时放出热量
2 2 2
C.甲、乙、丙中物质所具有的总能量大小关系为甲>乙>丙
D.氢气和氧气的总能量小于水的能量
1.已知: 2H (g)+O (g)═2H O(l)△H=akJ•mol﹣1
2 2 2
①
H (g)+ O (g)═H O(g)△H=bkJ•mol﹣1( )
2 2 2
②A.a=2b>0 B.a<2b C.a>2b D.a=2b<0
2.已知下列热化学方程式:
C(s,石墨)+O (g)═CO (g)△H=﹣393.5 kJ•mol﹣1
2 2
①2H (g)+O (g)═2H O(1)△H=﹣571.6 kJ•mol﹣1
2 2 2
②CH (g)+2O (g)═CO (g)+2H O(1)△H=﹣890.3 kJ•mol﹣1
4 2 2 2
③则C(s,石墨)+2H
2
(g)═CH
4
(g)的△H是( )
A.+74.8 kJ•mol﹣1 B.﹣149.6 kJ•mol﹣1
C.﹣74.8 kJ•mol﹣1 D.﹣149.6 kJ•mol﹣1
3.已知溴跟氢气反应的热化学方程式如下(Q 、Q 、Q 均为正值):H (g)+Br (g)→2HBr
1 2 3 2 2
(l)+Q ,H (g)+Br (g)→2HBr(g)+Q ,H (g)+Br (l)→2HBr(g)+Q ,下列判断
1 2 2 2 2 2 3
正确的是( )
A.Q >Q >Q
1 2 3
B.Q 与 Q 的大小无法判断
1 3
C.溴蒸气转化为液态溴需要放出(Q ﹣Q )kJ 的热量
2 3
D.1LH 和 1LBr 蒸气反应生成 2LHBr 气体时放出 Q kJ 热量
2 2 2
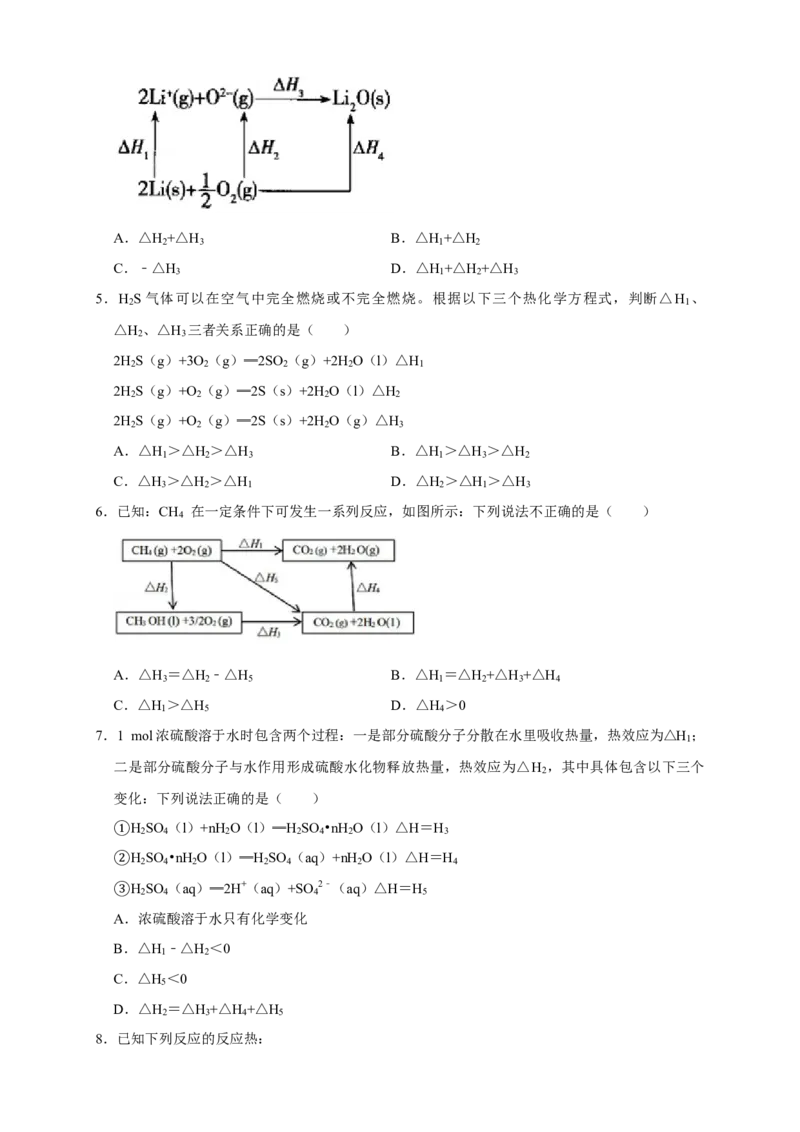
4.Li﹣Li O体系的能量循环如图所示,则△H 等于( )
2 4A.△H +△H B.△H +△H
2 3 1 2
C.﹣△H D.△H +△H +△H
3 1 2 3
5.H S气体可以在空气中完全燃烧或不完全燃烧。根据以下三个热化学方程式,判断△H 、
2 1
△H 、△H 三者关系正确的是( )
2 3
2H S(g)+3O (g)═2SO (g)+2H O(l)△H
2 2 2 2 1
2H S(g)+O (g)═2S(s)+2H O(l)△H
2 2 2 2
2H S(g)+O (g)═2S(s)+2H O(g)△H
2 2 2 3
A.△H >△H >△H B.△H >△H >△H
1 2 3 1 3 2
C.△H >△H >△H D.△H >△H >△H
3 2 1 2 1 3
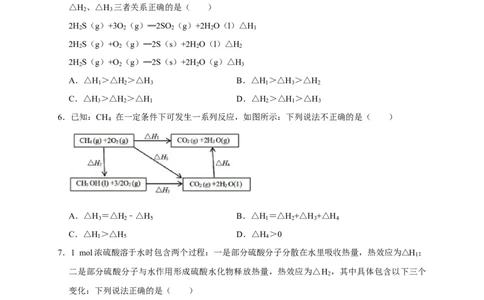
6.已知:CH 在一定条件下可发生一系列反应,如图所示:下列说法不正确的是( )
4
A.△H =△H ﹣△H B.△H =△H +△H +△H
3 2 5 1 2 3 4
C.△H >△H D.△H >0
1 5 4
7.1 mol浓硫酸溶于水时包含两个过程:一是部分硫酸分子分散在水里吸收热量,热效应为△H ;
1
二是部分硫酸分子与水作用形成硫酸水化物释放热量,热效应为△H ,其中具体包含以下三个
2
变化:下列说法正确的是( )
H SO (l)+nH O(l)═H SO •nH O(l)△H=H
2 4 2 2 4 2 3
①H
2
SO
4
•nH
2
O(l)═H
2
SO
4
(aq)+nH
2
O(l)△H=H
4
②H SO (aq)═2H+(aq)+SO 2﹣(aq)△H=H
2 4 4 5
③A.浓硫酸溶于水只有化学变化
B.△H ﹣△H <0
1 2
C.△H <0
5
D.△H =△H +△H +△H
2 3 4 5
8.已知下列反应的反应热:(1)CH COOH(l)+2O (g)=2CO (g)+2H O(l)△H =﹣870.3kJ•mol﹣1
3 2 2 2 1
(2)C (s)+O (g)=CO (g)△H =﹣393.5kJ•mol﹣1
2 2 2
(3)H (g)+ O (g)=H O(l)△H ═﹣285.8kJ/mol﹣1
2 2 2 3
则以下反应的反应热为( )
2C(s)+2 H (g)+O (g)=CH COOH(l)
2 2 3
A.△H=+488.3kJ•mol﹣1 B.△H=﹣244.15kJ•mol﹣1
C.△H=﹣977.6kJ•mol﹣1 D.△H=﹣488.3kJ•mol﹣1
【课前复习】相同
【知识点填空答案】盖斯定律;正;△H
【练习答案】DBBACAA
【检测反馈答案】BCADCADD