文档内容
1.2.2 反应热的计算(导学案)
【学习目标】
1、用盖斯定律计算反应热
2、用键能计算反应热
3、用反应物和生成物的总能量计算反应热
【学习重难点】
重点:反应热的计算
难点:反应热的计算
【温故知新】
1.盖斯定律内容:一个化学反应,不管是一步完成的还是分几步完成的,其反应热是相同的。也就是说,化学
反应的反应热与体系的始态和终态有关,而与反应的途径无关,这就是盖斯定律。
【做一做】已知下列热化学方程式:
反应Ⅰ.Hg(l)+O(g)=HgO(s) ΔH;
2 1
反应Ⅱ.Zn(s)+O(g)=ZnO(s) ΔH;
2 2
反应ⅢZn(s)+HgO(s)= Hg(l)+ZnO(s) ΔH 值为( )
3
A.ΔH-ΔH B.ΔH+ΔH C.ΔH-ΔH D.-ΔH-ΔH
2 1 2 1 1 2 1 2
【答案】A
【解析】根据盖斯定律:Ⅲ=Ⅱ-Ⅰ,则ΔH=ΔH-ΔH,故选A。
3 2 1
【想一想】用盖斯定律解题的技巧
①目标方程中找唯一
目标方程式中的物质:在给出的各个已知方程式中只出现一次的物质
②化系数
把已知方程式中的系数化成与目标方程式中物质的系数一致。
③同加异减
目标方程式中的物质:与已知方程式中物质在方程式的同侧,则相加;
与已知方程式中物质在方程式的异侧,则相减;
【合作探究】
一.用盖斯定律计算反应热
【典例1】已知下列热化学方程式:
①Fe O(s)+3CO(g)===2Fe(s)+3CO(g) ΔH=-26.7 kJ·mol-1
2 3 2 1
②3Fe O(s)+CO(g)===2Fe O(s)+CO(g) ΔH=-50.75 kJ·mol-1
2 3 3 4 2 2
③Fe O(s)+CO(g)===3FeO(s)+CO(g) ΔH=-36.5 kJ·mol-1
3 4 2 3
则反应FeO(s)+CO(g)===Fe(s)+CO(g)的焓变为( )
2
A.+7.28 kJ·mol-1 B.-7.28 kJ·mol-1
C.+43.68 kJ·mol-1 D.-43.68 kJ·mol-1
【答案】A
【解析】根据盖斯定律,首先考虑目标反应与三个已知反应的关系,三个反应中,FeO、CO、Fe、CO 是要保留
2
的,而与这四种物质无关的FeO 、FeO 要通过热化学方程式的叠加处理予以消去,因此将①×3-②-③×2
2 3 3 4
得到:6FeO(s)+6CO(g)===6Fe(s)+6CO(g)ΔH=+43.65 kJ·mol-1
2
化简后得FeO(s)+CO(g)===Fe(s)+CO(g) ΔH=+7.28 kJ·mol-1。
2
【变式1】甲烷和水蒸气催化制氢主要有如下两个反应:
①CH(g)+HO(g)=CO(g)+3H(g) ΔH=+206 kJ/mol
4 2 2
②CO(g)+HO(g)=CO(g)+H(g) ΔH=-41 kJ/mol
2 2 2
写出CH 与 CO 生成H 和CO的热化学方程式:
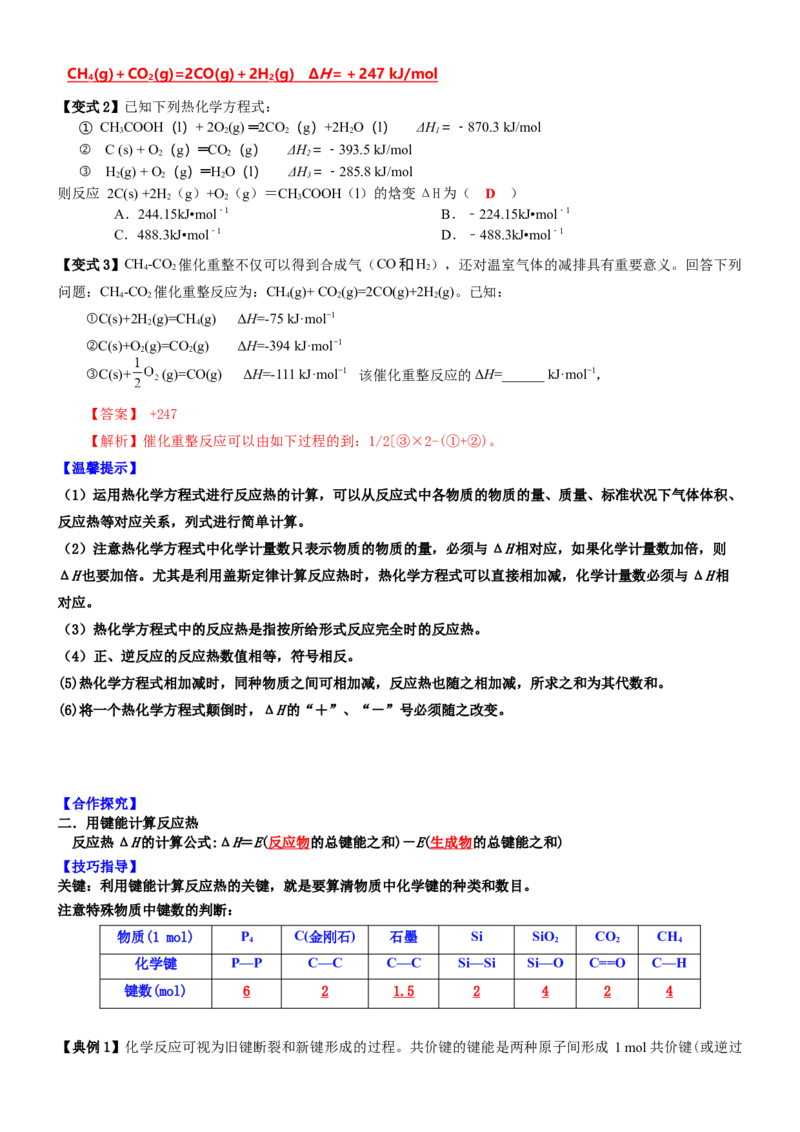
4 2 2CH (g) + CO (g)=2CO(g) + 2H (g) Δ H =+ 247 kJ/mo l
4 2 2
【变式2】已知下列热化学方程式:
① CHCOOH(l)+ 2O (g) ═2CO(g)+2H O(l) ΔH=﹣870.3 kJ/mol
3 2 2 2 1
② C (s) + O (g)═CO(g) ΔH=﹣393.5 kJ/mol
2 2 2
③ H (g) + O(g)═HO(l) ΔH=﹣285.8 kJ/mol
2 2 2 3
则反应 2C(s) +2H (g)+O (g)=CHCOOH(l)的焓变ΔH为( D )
2 2 3
A.244.15kJ•mol﹣1 B.﹣224.15kJ•mol﹣1
C.488.3kJ•mol﹣1 D.﹣488.3kJ•mol﹣1
【变式3】CH-CO 催化重整不仅可以得到合成气(CO和H ),还对温室气体的减排具有重要意义。回答下列
4 2 2
问题:CH-CO 催化重整反应为:CH(g)+ CO (g)=2CO(g)+2H(g)。已知:
4 2 4 2 2
①C(s)+2H(g)=CH (g) ΔH=-75 kJ·mol−1
2 4
②C(s)+O (g)=CO (g) ΔH=-394 kJ·mol−1
2 2
③C(s)+ (g)=CO(g) ΔH=-111 kJ·mol−1 该催化重整反应的ΔH=______ kJ·mol−1,
【答案】 +247
【解析】催化重整反应可以由如下过程的到:1/2[③×2-(①+②)。
【温馨提示】
(1)运用热化学方程式进行反应热的计算,可以从反应式中各物质的物质的量、质量、标准状况下气体体积、
反应热等对应关系,列式进行简单计算。
(2)注意热化学方程式中化学计量数只表示物质的物质的量,必须与ΔH相对应,如果化学计量数加倍,则
ΔH也要加倍。尤其是利用盖斯定律计算反应热时,热化学方程式可以直接相加减,化学计量数必须与ΔH相
对应。
(3)热化学方程式中的反应热是指按所给形式反应完全时的反应热。
(4)正、逆反应的反应热数值相等,符号相反。
(5)热化学方程式相加减时,同种物质之间可相加减,反应热也随之相加减,所求之和为其代数和。
(6)将一个热化学方程式颠倒时,ΔH的“+”、“-”号必须随之改变。
【合作探究】
二.用键能计算反应热
反应热ΔH的计算公式:ΔH=E(反应物的总键能之和)-E(生成物的总键能之和)
【技巧指导】
关键:利用键能计算反应热的关键,就是要算清物质中化学键的种类和数目。
注意特殊物质中键数的判断:
物质(1 mol) P C(金刚石) 石墨 Si SiO CO CH
4 2 2 4
化学键 P—P C—C C—C Si—Si Si—O C==O C—H
键数(mol) 6 2 1.5 2 4 2 4
【典例1】化学反应可视为旧键断裂和新键形成的过程。共价键的键能是两种原子间形成 1 mol共价键(或逆过程)时释放(或吸收)的能量。已知H—H键的键能为436 kJ·mol-1,Cl—Cl键的键能为243 kJ·mol-1,H—Cl键的
键能为431 kJ·mol-1,则H(g)+Cl(g)===2HCl(g)的反应热(ΔH)等于( )
2 2
A.183 kJ·mol-1 B.-183 kJ·mol-1
C.-862 kJ·mol-1 D.862 kJ·mol-1
【答案】B
【解析】ΔH=436 kJ·mol-1+243 kJ·mol-1-2×431 kJ·mol-1=-183 kJ·mol-1。
【变式1】已知几种化学键的键能如表所示:
化学键
键能 a 436 463 750
根据热化学方程式: ,计算表中的a为
A.484.5 B.969 C.872 D.1938
【答案】B
【详解】 反应物总键能-生成物总键能 ,可求得 ,B项正确。
【变式2】甲醇是重要的化工原料,工业上由CO、 和 合成甲醇的主要反应如下:
I.
II.
III.
已知:反应Ⅲ中相关化学键的数据如下表
化学键
键能/ 436 343 a 465 413
则 键的键能a为
A.1076 B.826 C.779 D.538
【答案】A
【详解】反应Ⅱ-Ⅰ得: ,根据H=反应物的总键能-生
成物的总键能= ,解得 。
【变式3】科学家已获得了气态N 分子,其结构为正四面体形(如图所示)。已知键能是指断开1mol化学键变为
4
气态原子所需要的能量,或形成1mol化学键所释放的能量。下列说法正确的是
化学键 N≡N N−N
键能/ kJ∙mol−1 946 193
A.N 属于一种新型的化合物
4B.N(g)比N (g)稳定
4 2
C.56 g N (g)转化为N (g)时要释放734 kJ能量
4 2
D.N (g)和N (g)互为同位素,N 转化为N 属于化学变化
4 2 4 2
【答案】C
【详解】A.N 是单质,不是化合物,故A错误;
4
B.N 分子中是N-N,N 分子中是N N,N-N键能小于N N,所以N 没有N 稳定,故B错误;
4 2 4 2
C.56gN 的物质的量为1mol,1molN 分子中有6molN-N,1molN 转化为2molN,则断开1molN 分子中的化学键
4 4 4 2 4
吸收的能量为193kJ×6=1158kJ,形成2molN 放出的能量为946kJ×2=1892kJ,故56 g N (g)转化为N (g)时
2 4 2
要释放1892kJ-1158kJ=734 kJ能量,故C正确;
D.同位素是质子数相同中子数不同的原子,N(g)和N((g)不互为同位素,N (g)和N (g)互为同素异形体,N
4 2 4 2 4
转化为N 属于化学变化,故D错误;
2
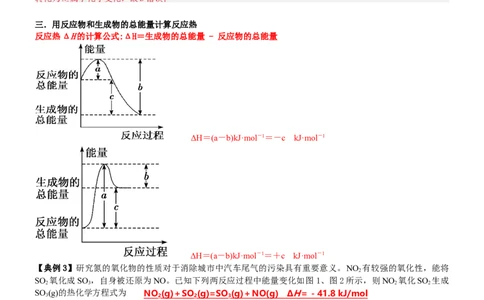
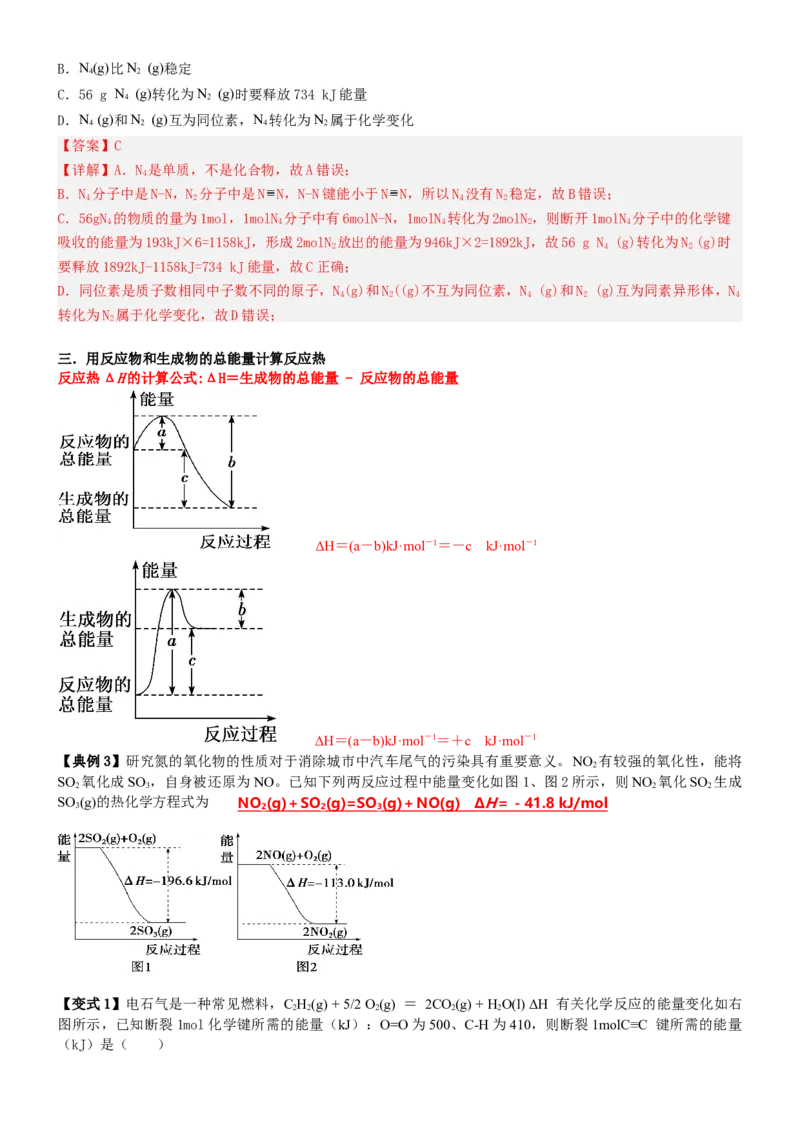
三.用反应物和生成物的总能量计算反应热
反应热ΔH的计算公式:ΔH=生成物的总能量 - 反应物的总能量
ΔH=(a-b)kJ·mol-1=-c kJ·mol-1
ΔH=(a-b)kJ·mol-1=+c kJ·mol-1
【典例3】研究氮的氧化物的性质对于消除城市中汽车尾气的污染具有重要意义。NO 有较强的氧化性,能将
2
SO 氧化成SO ,自身被还原为NO。已知下列两反应过程中能量变化如图1、图2所示,则NO 氧化SO 生成
2 3 2 2
SO (g)的热化学方程式为 NO (g) + SO (g)=SO (g) + NO(g) Δ H =- 41.8 kJ/mo l
3 2 2 3
【变式1】电石气是一种常见燃料,C H(g) + 5/2 O (g) = 2CO(g) + H O(l) ΔH 有关化学反应的能量变化如右
2 2 2 2 2
图所示,已知断裂1mol化学键所需的能量(kJ):O=O为500、C-H为410,则断裂1molC≡C 键所需的能量
(kJ)是( )【答案】A
A.840 B.1590 C.900 D.1250
【变式2】肼( )是一种高能燃料,有关化学反应的能量变化如图所示。已知断裂1mol化学键所需的能
量(kJ):N=N键为942、O=O键为500、N-N键为154,则断裂1molN-H键所需的能量是
A.194kJ B.391kJ C.516kJ D.658kJ
【答案】B
【详解】根据图中内容可知, ,化学反应的焓变等于产物的能量与反应物能
量的差值,旧键断裂吸收能量,新建形成释放能量,设断裂1molN-H键所需的能量为K,所以有
154+4K+500=2218;解得K=391;
【变式3】化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1mol化学键时释放(或吸
收)的能量。一定条件下,氢气与氧气反应的能量变化如图所示,下列说法中正确的是
A.该反应的反应热
B.该反应为吸热反应
C.断裂 和 放出 的能量D. 燃烧热的热化学方程式为:
【答案】A
【详解】A.由题干图示信息可知,该反应的反应热 ,A正确;
B.由题干图示信息可知,该反应中反应物总能量高于生成物总能量,故为放热反应,B错误;
C.化学键断裂需要吸收能量,化学键形成才能释放能量,故断裂 和 吸收 的能量,
C错误;
D.燃烧热是指1mol纯物质燃料完全燃烧生成指定稳定的物质是释放的热量,H2燃烧需生成液态水,故H 燃烧
2
热的热化学方程式为: ,D错误;
【技巧指导】
计算依据 计算反应热方法
热化学方程式与数学上的方程式相似,可以左右颠倒同时改
热化学方程式 变正负号,各项的化学计量数包括ΔH的数值可以同时扩大
或缩小相同的倍数
根据盖斯定律,可以将两个或两个以上的热化学方程式包括
根据盖斯定律
其ΔH相加或相减,得到一个新的热化学方程式
根据燃烧热 可燃物完全燃烧产生的热量=可燃物的物质的量×其燃烧热
根据化学键的变 ΔH=反应物的化学键断裂所吸收的能量和-生成物的化学键
化 形成所放出的能量和
根据反应物和生
ΔH=E(生成物)-E(反应物)
成物的总能量
【巩固练习】
1.(1)已知拆开1 mol H—H、1 mol N—H、1 mol N≡N需要的能量分别是436 kJ、391 kJ、946 kJ,则N 与H
2 2
反应生成NH 的热化学方程式为_________________________________。
3
(2)已知化学反应A(g)+B (g)===2AB(g)的能量变化如图所示,回答下列问题:
2 2
①该反应的ΔH____________________________(填“>”“<”或“=”)0。
②反应物的总键能为________。
③写出该反应的热化学方程式:__________________________________。
(3)联氨(又称肼,NH,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
2 4
①2O(g)+N(g)===N O(l) ΔH
2 2 2 4 1
②N (g)+2H(g)===N H(l) ΔH
2 2 2 4 2③O(g)+2H(g)===2H O(g) ΔH
2 2 2 3
④2N H(l)+NO(l)===3N (g)+4HO(g) ΔH=-1048.9 kJ·mol-1
2 4 2 4 2 2 4
上述反应热之间的关系式为ΔH=__________________________,联氨和NO 可作为火箭推进剂的主要原因为
4 2 4
_________________________________。
【解析】(1)N 与H 反应生成NH 的化学方程式为N(g)+3H(g)2NH(g),该反应的ΔH=反应物的键能总和
2 2 3 2 2 3
-生成物的键能总和=E(N≡N)+3E(H—H)-6E(N—H)=946 kJ·mol-1+3×436 kJ·mol-1-6×391 kJ·mol-
1=-92 kJ·mol-1;N 与H 反应生成NH 的热化学方程式为N(g)+3H(g)=2NH(g) ΔH=-92 kJ·mol-1。
2 2 3 2 2 3
(2)①1 mol A(g)和1 mol B(g)具有的总能量小于2 mol AB(g)具有的总能量,反应A(g)+B(g)===2AB(g)为
2 2 2 2
吸热反应,ΔH>0。②根据题图可知反应物的总键能为a kJ·mol-1。③根据题图可知该反应的 ΔH=+(a-
b)kJ·mol-1,该反应的热化学方程式为A(g)+B(g)===2AB(g) ΔH=+(a-b)kJ·mol-1。
2 2
(3)根据盖斯定律可知,③×2-②×2-①得④,则ΔH=2ΔH-2ΔH-ΔH。根据反应④知,联氨和NO 可
4 3 2 1 2 4
作为火箭推进剂的主要原因为反应放热量大、产生大量气体、无污染。
答案:(1)N(g)+3H(g)2NH(g) ΔH=-92 kJ·mol-1
2 2 3
(2)①> ②a kJ·mol-1 ③A(g)+B(g)===2AB(g) ΔH=+(a-b)kJ·mol-1
2 2
(3)2ΔH-2ΔH-ΔH 反应放热量大、产生大量气体、无污染
3 2 1
2.(1)环戊二烯 是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
ΔH=+100.3 kJ·mol-1 ①
1
H(g)+I(g)===2HI(g) ΔH=-11.0 kJ·mol-1 ②
2 2 2
对于反应: +2HI(g) ΔH=_______ kJ·mol-1 ③。
3
(2)近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长。因此,将氯化氢转化
为氯气的技术成为科学研究的热点。Deacon直接氧化法可按下列催化过程进行:
CuCl (s)===CuCl(s)+Cl(g) ΔH=+83 kJ·mol-1
2 2 1
CuCl(s)+O(g)===CuO(s)+Cl(g) ΔH=-20 kJ·mol-1
2 2 2
CuO(s)+2HCl(g)===CuCl (s)+HO(g) ΔH=-121 kJ·mol-1
2 2 3
则4HCl(g)+O(g)===2Cl(g)+2HO(g)的ΔH=________ kJ·mol-1。
2 2 2
(3)多晶硅是制作光伏电池的关键材料。回答下列问题:
Ⅰ.硅粉与HCl在300 ℃时反应生成1 mol SiHCl 气体和H ,放出225 kJ热量,该反应的热化学方程式为
3 2
_________________________________。
Ⅱ.将SiCl 氢化为SiHCl 有三种方法,对应的反应依次为:
4 3
①SiCl (g)+H(g)=SiHCl (g)+HCl(g) ΔH>0
4 2 3 1
②3SiCl (g)+2H(g)+Si(s)=4SiHCl (g) ΔH<0
4 2 3 2
③2SiCl (g)+H(g)+Si(s)+HCl(g)=3SiHCl (g) ΔH
4 2 3 3
反应③的ΔH=________(用ΔH、ΔH表示)。
3 1 2
【解析】(1)根据盖斯定律,将反应①和②叠加可得反应③,故 ΔH=ΔH+ΔH=+100.3 kJ·mol-1+(-
3 1 2
11.0 kJ·mol-1)=+89.3 kJ·mol-1。
(2)由盖斯定律可知,将题给催化过程的三个反应直接相加可得:
2HCl(g)+O(g)===Cl(g)+HO(g) ΔH′=(+83-20-121)kJ·mol-1=-58 kJ·mol-1,则 ΔH=2ΔH′=-116
2 2 2kJ·mol-1。
(3)Ⅰ.首先书写反应的化学方程式:Si+3HCl=====SiHCl+H,然后加上状态和焓变得热化学方程式:
3 2
Si(s)+3HCl(g)=====SiHCl (g)+H(g) ΔH=-225 kJ·mol-1。
3 2
Ⅱ.根据盖斯定律:反应②-反应①可得反应③,则ΔH=ΔH-ΔH。
3 2 1
【答案】(1)+89.3 (2)-116
(3)Ⅰ.Si(s)+3HCl(g)=====SiHCl (g)+H(g) ΔH=-225 kJ·mol-1
3 2
Ⅱ.ΔH-ΔH
2 1